Роль коррекции состояния эндотелия и базальной мембраны сосудистой стенки при диабетической ретинопатии
- Аннотация
- Статья
- Ссылки
- English

Введение
Актуальность проблемы сахарного диабета (СД) и его осложнений не подвергается сомнению. Заболеванием страдает около 3–5% населения Земли, и число больных, несмотря на усилия медицинского сообщества, ежегодно увеличивается на 5–7% [1–3].
Диабетическая ретинопатия (ДР) выявляется у 40–85% пациентов с СД. Заболевание характеризуется тяжелым прогрессирующим течением и часто приводит к инвалидизации [3, 4].
Согласно данным Всемирной организации здравоохранения (ВОЗ), ДР – одна из основных причин снижения зрения и слепоты среди взрослого населения [4, 5].
Медицинская и социальная значимость ДР определяется высокой распространенностью, ежегодным приростом числа больных, прогрессирующим снижением зрения, неудовлетворительными результатами проводимого лечения и неблагоприятным прогнозом.
Современное представление о патогенезе
В основе патогенеза ДР лежат различные механизмы. При этом большинство авторов выделяют широкий спектр обменных нарушений, обусловленных гипергликемией.
Повышение уровня глюкозы в крови приводит к глюкозотоксичности, проявляющейся как гликозилирование белков и клеточных мембран различных органов и тканей. Это ведет к нарушению их функции, а при длительном повышении глюкозы в крови – к развитию таких осложнений, как ретинопатия, полинейропатия, атеросклероз, нефропатия [5–8].
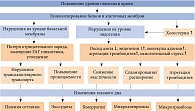
На сегодняшний день патогенез ранних проявлений ДР с позиции повреждения эндотелия описан достаточно подробно (рис. 1). Именно клетки эндотелия первыми принимают метаболический и гидравлический «удар» гипергликемии и дислипидемии [9]. Подвергаясь длительному воздействию гипергликемии и дислипидемии, они начинают продуцировать факторы, ускоряющие процессы атерогенеза. Речь, в частности, идет о снижении синтеза эндотелиального фактора релаксации сосудов – оксида азота, повышении секреции сосудосуживающего фактора – эндотелина 1, активации экспрессии молекул адгезии, усилении агрегации тромбоцитов, окислительного стресса, пролиферации гладкомышечных клеток.
Одновременно происходит неферментативное гликозилирование белков, что приводит к утолщению сосудистой стенки, ее деформации, снижению эластичности и повышению проницаемости [7, 9].
Нарушение функции эндотелия и базальной мембраны сосудов обусловливает основные патологические эффекты, определяющие изменения глазного дна при ДР [5, 9, 10].
Одним из первых проявляется нарушение транскапиллярного транспорта. Как следствие, развивается ишемия сетчатки.
Наблюдается также повышение проницаемости сосудистой стенки, что приводит к появлению экссудатов и геморрагиям.
Снижение эластичности сосудистой стенки способствует микроаневризму и, как следствие, геморрагиям.
В результате спазмирования или расширения сосудов происходит их деформация и усугубляется ишемия. Повышенная адгезия тромбоцитов приводит к тромбозам.
При непролиферативной стадии ДР на глазном дне выявляются микроаневризмы, микрогеморрагии, экссудативные очаги, препролиферативной – сосудистые аномалии, множественные геморрагии и экссудаты, ишемические зоны сетчатки.
Лечение
В настоящее время выделяют три основных направления в лечении ДР:
-
коррекция системных нарушений, обусловленных СД (гликемии, липидного профиля, артериального давления);
-
хирургическое (в первую очередь лазерная коагуляция), направленное на профилактику и устранение проявлений ДР;
-
медикаментозное, направленное на коррекцию метаболических и гемоциркуляторных нарушений сетчатки.
Согласно рекомендациям ВОЗ единственный эффективный способ предотвращения слепоты, обусловленной СД, – лазерная коагуляция сетчатки [4, 5].
Вессел Дуэ Ф
Коррекция состояния эндотелия и базальной мембраны сосудистой стенки представляется одним из наиболее перспективных направлений профилактики и терапии ДР на ранней стадии.
В патогенезе ранних стадий ДР важное значение отводится нарушению синтеза гепарансульфата – гликозаминогликана (ГАГ), входящего в состав базальной мембраны и образующего активный поверхностный слой клеток эндотелия сетчатки. Снижение синтеза ГАГ приводит к дисфункции эндотелия и базальной мембраны сосудов сетчатки, что и обусловливает изменения глазного дна.
При восполнении дефицита ГАГ на ранних стадиях заболевания возможно восстановление нормальной проницаемости сосудистой стенки и предотвращение развития ее структурно-функциональных нарушений [1, 9].
В последние годы появились данные о применении при ДР одного из препаратов группы ГАГ – сулодексида (Вессел Дуэ Ф, компания «Альфа Вассерманн»). Препарат состоит из двух компонентов: гепариноподобной фракции (80%) и дерматановой (20%) [9, 11–14].
Сулодексид оказывает комплексное воздействие:
-
ангиопротективное – восстанавливает электрический заряд базальной мембраны и целостность сосудистой стенки;
-
антитромботическое – подавляет активированный фактор Ха, тромбин, стимулирует синтез и секрецию простагландина I2, снижает уровень фибриногена;
-
профибринолитическое – активирует секрецию тканевого активатора плазминогена и уменьшает уровень ингибитора тканевого активатора плазминогена 1;
-
антикоагуляционное.
Фармакологические эффекты сулодексида и наличие успешного опыта применения у пациентов с диабетической нефропатией (значительное снижение альбуминурии за счет восстановления целостности сосудов клубочкового аппарата почек) [8, 15, 16] позволили предположить целесообразность использования препарата при ДР (см. таблицу).
Впервые для лечения ДР сулодексид был применен в 2000 г. [11]. F. Rubbi и соавт. в многоцентровом исследовании с участием больных СД типов 1 и 2 и непролиферативной ДР показали достоверное уменьшение количества твердых экссудатов (p = 0,0004), интраретинальных микрососудистых аномалий (p = 0,007) и микрогеморрагий (p = 0,02) после курса лечения сулодексидом. Полученные результаты авторы объясняли положительным влиянием сулодексида на состояние базальной мембраны и эндотелия ретинальных микрососудов.
В исследовании И.М. Ищенко и Т.М. Миленькой оценивалась клиническая эффективность сулодексида в сочетании с лазерной коагуляцией сетчатки на начальных стадиях ДР [12].
Под наблюдением находился 191 пациент с непролиферативной и препролиферативной ДР. Сулодексид в виде монотерапии применяли при непролиферативной ДР, в комбинации с лазерной коагуляцией – при непролиферативной и препролиферативной ДР. Курс лечения начинали с внутримышечных инъекций Вессел Дуэ Ф (ежедневно в течение 14 дней), затем пациентов переводили на пероральный прием препарата (два раза в день в течение 30 дней). Длительность наблюдения – два года.
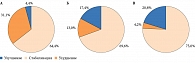
В группе Вессел Дуэ Ф количество пациентов с улучшением состояния сосудов сетчатки было почти в четыре раза больше, чем в контрольной группе (17,4 против 4,4%) (рис. 2). Еще более выраженный эффект получен при применении Вессел Дуэ Ф в комплексе с лазерной коагуляцией: количество пациентов с улучшением состояния сосудов сетчатки в этой группе было почти в пять раз больше, чем в контрольной (рис. 2).
Авторы сделали вывод: терапия сулодексидом оказывает стойкий (при повторении курса лечения) положительный эффект при ДР.
Еще одно исследование в отношении пациентов с пролиферативной ДР, которым планировались проведение панретинальной лазерной коагуляции сетчатки и лечение сулодексидом по поводу диабетической нефропатии, было проведено Ф.Е. Шадричевым [13].
Препарат применяли по следующей схеме: 600 липопротеинлипазных единиц (ЛЕ) внутримышечно один раз в сутки в течение десяти дней, затем по 500 ЛЕ перорально (две капсулы) один раз в сутки в течение 90 дней.
Установлено, что использование сулодексида в комплексном лечении диабетической нефропатии достоверно не увеличивало риск внутриглазных (преретинальных и витреальных) кровоизлияний при выполнении панретинальной лазерной коагуляции сетчатки даже у пациентов с пролиферативной ДР.
Н.А. Гаврилова и О.Е. Тищенко изучали влияние сулодексида на функциональное состояние эндотелия у 37 пациентов с непролиферативной и препролиферативной ДР [9].
Для оценки функционального состояния эндотелия определяли уровни эндотелиальных факторов (sVCAM, эндотелина, оксида азота, фибринолитической активности сосудистой стенки, гликопротеина) в сыворотке или плазме крови до и после лечения. Режим применения сулодексида (Вессел Дуэ Ф): первые 14 дней внутримышечно по 2 мл (600 ЛЕ), далее – по две капсулы (500 ЛЕ) в сутки в течение 30 дней.
Исходный уровень эндотелиальных факторов у всех пациентов был достоверно изменен, что подтверждало дисфункцию эндотелия, связанную с его альтерацией при ДР. Анализ результатов исследования эндотелиальных факторов после курса терапии Вессел Дуэ Ф свидетельствовал о нормализации функции эндотелия при всех стадиях ДР вследствие коррекции выработки вазоактивных факторов (эндотелина, оксида азота) и стимуляции фибринолитической активности сосудистой стенки.
Отсутствие достоверных изменений коагуляционного звена системного гемостатического потенциала подтвердило минимальный риск осложнений со стороны системы гемостаза.
Через месяц после лечения оценка функционального состояния сетчатки с помощью регистрации электроретинограммы показала повышение биоэлектрической активности процессов в наружных слоях сетчатки у всех пациентов. Полученный результат сохранялся в течение четырех – шести месяцев, что свидетельствовало об улучшении функциональной активности сетчатки. Цифровой анализ состояния сосудов глазного дна через два-три месяца после лечения показал уменьшение амплитуды, частоты и извилистости толщины артериол. Это подтвердило регресс сосудистой патологии. Авторами был сделан вывод о целесообразности применения сулодексида (Вессел Дуэ Ф) у пациентов с непролиферативной и препролиферативной ДР.
Интерес представляют результаты исследования DRESS, завершенного в 2014 г. [17]. DRESS – рандомизированное плацебоконтролируемое многоцентровое исследование, целью которого стала оценка влияния сулодексида на состояние глазного дна у пациентов с непролиферативной ДР. В исследовании участвовало 130 пациентов.
В течение 12 месяцев больные перорально получали сулодексид (500 ЛЕ в сутки) или плацебо.
Основная контрольная точка исследования – регресс твердых экссудатов, оцениваемый как снижение степени твердых экссудатов по крайней мере на две ступени по шкале ETDRS (Early Treatment of Diabetic Retinopathy Study) при фотографировании глазного дна.
Результаты показали, что по окончании 12 месяцев лечения регресс твердых экссудатов сетчатки в группе пациентов, получавших сулодексид, был достоверно выше, чем в группе плацебо (39,0 против 19,3%, p = 0,005). Был сделан вывод: терапия сулодексидом улучшает состояние глазного дна при непролиферативной ДР. Было также отмечено, что количество и степень выраженности побочных эффектов в группе сулодексида были сравнимы с таковыми в группе плацебо, что подтверждает высокий профиль безопасности препарата.
Заключение
Успешное лечение ДР – сложная задача. Для ее решения требуется воздействие на различные звенья патогенеза. Одним из важных направлений терапии ДР на ранних стадиях должна стать коррекция состояния эндотелия и базальной мембраны сосудистой стенки.
Отечественные и зарубежные исследования свидетельствуют о том, что применение Вессел Дуэ Ф открывает новые возможности в лечении ДР и позволяет улучшить прогноз заболевания.
M.N. Koledintsev, R.A. Verzin
Moscow State University of Medicine and Dentistry named after A.I. Evdokimov
Contact person: Mikhail Nikolayevich Koledintsev, 1mnk@mail.ru
Here we discuss epidemiology, pathogenesis and main therapeutic directions of diabetic retinopathy. The data on efficacy and safety of sulodexide (Vessel Due F) at early stage of disease.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.