Сравнительная гиполипидемическая эффективность препаратов аторвастатина Атомакс® и Липримар у пациентов с гиперхолестеринемией
- Аннотация
- Статья
- Ссылки



Для достижения так называемых целевых уровней липидов крови, согласно современным рекомендациям, требуются как изменения образа жизни, включая диету, так и медикаментозная терапия (1, 2). Для ингибиторов ГМГ-КоА-редуктазы (статинов) получено наибольшее число веских доказательств, указывающих и на благоприятные изменения липидного профиля, и на снижение риска развития сердечно-сосудистых осложнений. Увеличение использования статинов для первичной и вторичной профилактики ССЗ в соответствии с новыми рекомендациями NCEP ежегодно сможет предотвращать десятки тысяч случаев преждевременной смерти (2). Более широкое внедрение статинов в клиническую практику возможно с помощью генериков, имеющих более низкую стоимость по сравнению с оригинальными препаратами. Тем не менее, по клиническому эффекту и профилю безопасности генерические продукты должны соответствовать оригинальному препарату. В настоящей работе мы представляем результаты сравнительного рандомизированного перекрестного исследования гиполипидемической эффективности, безопасности и переносимости препарата АТОМАКС® (генерический аторвастатин, ЗАО «МАКИЗ-Фарма», Россия) по сравнению с оригинальным препаратом ЛИПРИМАР (Pfizer, США) у пациентов с повышенным уровнем холестерина (ХС) крови.
Материалы и методы
Исследование проводилось на базе лаборатории гемодиализа и плазмафереза Института клинической кардиологии им. А.Л. Мясникова. Все лабораторные анализы выполнены в лаборатории клинической биохимии этого же учреждения. Уровни общего ХС, триглицеридов (ТГ) и ХС липопротеинов высокой плотности (ЛПВП) определяли стандартными ферментативными методами. Уровень ХС липопротеинов низкой плотности (ЛПНП) рассчитывали по формуле Friedewald.
Препараты АТОМАКС® и ЛИПРИМАР назначали в дозе 10 мг в сутки. На каждом визите, кроме заключительного, больному выдавали тестируемый препарат из расчета на 6 недель терапии. Всех пациентов инструктировали принимать препарат по одной таблетке вечером после ужина.
Дизайн и протокол исследования
Критериями включения пациентов в исследование были: 1) возраст от 18 до 80 лет; 2) документированная ишемическая болезнь сердца (ИБС) или другие клинические формы атеросклероза (ишемический инсульт в анамнезе, симптомы каротидного или периферического атеросклероза, аневризма брюшной аорты); 3) сахарный диабет; 4) наличие 2-х и более факторов риска при 10-летнем риске ИБС 10-20%; 5) уровень ХС ЛПНП в сыворотке крови ≥2,6 ммоль/л после 4-х недельного периода гиполипидемической диеты у больных с ИБС или ее эквивалентами, и ≥3,4 ммоль/л при наличии 2-х и более факторов риска с 10-летним риском ИБС 10-20%; 6) подписание информированного согласия на участие в исследовании. Пациентов с сердечно-сосудистыми осложнениями или после оперативных вмешательств включали в исследование не ранее 3-х месяцев с момента этих событий.
Критериями, исключающими участие в исследование, были: гиперчувствительность при применении статинов в анамнезе; беременность или лактация; уровень общего ХС в сыворотке крови ≥9,0 ммоль/л или ТГ >4,5 ммоль/л; вторичная дислипидемия (за исключением диабетической); заболевания печени в активной стадии или повышение активности трансаминаз (АЛТ, АСТ) более, чем в 2 раза от верхней границы нормы; превышение уровня КФК более, чем в 5 раз от верхней границы нормы; острые состояния (инфекция, обострение хронических заболеваний, травма, хирургические вмешательства) в течение последних 3 месяцев от начала исследования; злоупотребление алкоголем; одновременный прием препаратов (циклоспорина, эритромицина, кларитромицина, азитромицина, варфарина, кетоконазола или итроконазола – для исключения возможного взаимодействия вышеупомянутых препаратов с тестируемым лекарственным средством); прием гиполипидемических средств в течение 4-х недель, предшествующих началу исследования.
Скрининг
На этом визите проверяли соответствие пациентов критериям включения и исключения, кроме лабораторных показателей. Назначенные ранее этим больным липидоснижающие препараты были отменены. Затем в течение 4-х недель включенные в исследование пациенты соблюдали низкохолестериновую диету и принимали только рекомендованные антиангинальные и гипотензивные препараты (если это было необходимо).
Исследование
После получения письменного информированного согласия и осмотра у всех пациентов были взяты пробы крови для проведения биохимического анализа (определение уровней аспартатаминотрансферазы (АСТ), аланинаминотрансферазы (АЛТ), креатинфосфокиназы (КФК), щелочной фосфатазы (ЩФ), общего ХС, ТГ и ХС ЛПВП). Пациентов, соответствовавших критериям включения и исключения, были распределены в 2 группы путем простой рандомизации для участия в перекрестном исследовании без периода «отмывки». Первая группа получала ЛИПРИМАР в течение первых 6 недель, затем ее переводили на АТОМАКС®, и, наоборот, вторая группа пациентов в течение первых 6 недель получала АТОМАКС®, а следующие 6 недель – ЛИПРИМАР.
В течение 12 недель терапии больных наблюдали с 6-недельными интервалами, таким образом, было запланировано 3 визита. На каждом визите фиксировали жалобы, артериальное давление (АД), частоту сердечных сокращений (ЧСС), вес пациентов, изменения в сопутствующей терапии и брали кровь для биохимического исследования (см. выше). Согласно протоколу, исключение пациентов из исследования в процессе лечения было предусмотрено в следующих случаях: трехкратное превышение верхней границы нормы для печеночных трансаминаз или десятикратное превышение верхней границы нормы для КФК в сыворотке крови; появление симптомов патологии печени или миопатии с повышением уровня соответствующих ферментов в крови; возникновение иных серье зных побочных эффектов; а также низкая (менее 80%) приверженность пациента к назначенному лечению.
Основным показателем при оценке данного исследования был уровень ХС ЛПНП сыворотки крови.
Статистический анализ
При статистической обработке данных применяли программное обеспечение Statistica 6.0, предусматривающее возможность параметрического и непараметрического анализа. Для оценки достоверности межгрупповых различий применяли непарный непараметрический метод анализа по Манн-Уитни. Оценка динамики на фоне лечения проводилась с применением парного непараметрического метода анализа по Вилкоксону. Различия считались достоверными при p<0,05. Результаты представлены как среднее ± стандартное отклонение.
Результаты
В исследование было включено 27 пациентов, которые удовлетворяли критериям включения. 14 больных случайным способом были распределены в первую группу, получавшую ЛИПРИМАР, 13 – во вторую, получавшую АТОМАКС®. Между группами не было значимых различий по возрасту, полу и исходным параметрам липидов сыворотки крови (таблица 1).
После назначения препаратов в течение первых 6 недель терапии две пациентки второй группы были исключены из исследования в связи с самостоятельным прекращением терапии. Одна больная прекратила прием препарата в связи с обнаружением у нее опухоли молочной железы, у другой пациентки после 8 дней терапии появились боли в икроножных мышцах, которые прекратились после отмены препарата. Поскольку больная сообщила об этом явлении только накануне очередного визита, т. е. через месяц, данными об уровне КФК в крови во время развития симптомов мы не располагаем.
Из таблицы 2 видно, что показатели липидов крови в конце первого периода исследования (6 недель терапии) не имели статистически значимых различий между двумя группами.
По окончании первого периода все пациенты первой группы (n=14) были переведены на АТОМАКС,® а пациенты второй группы – на ЛИПРИМАР (n=11). Лечение продолжалось в течение последующих 6 недель. Дальнейшего выбывания пациентов не наблюдалось, таким образом, исследование завершили 25 человек. У этих пациентов отмечалась хорошая переносимость препаратов, вне зависимости от производителя. Данные таблицы 3 демонстрируют отсутствие значимых различий в уровне липидов между сравниваемыми группами по окончании второго периода (и завершения) исследования.
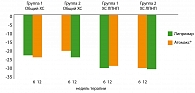
В обеих группах в процессе лечения отмечалось значимое изменение уровней общего ХС и ХС ЛПНП (p<0,05) (рисунок 1). Снижение уровня ХС ЛПНП при приеме ЛИПРИМАРА составляло 30-31% от исходного уровня, АТОМАКСА® – 29-30%. Что касается ТГ и ХС ЛПВП, их динамика в обеих группах была статистически недостоверной (данные не показаны).
Обсуждение
Одним из способов повышения доступности лекарственных средств на фоне возрастающей в них потребности является организация местного производства качественных генерических препаратов. Такая стратегия популярна во многих странах, особенно с развивающейся экономикой. Оценка безопасности и эффективности этих лекарственных средств является существенным моментом, влияющим на их применение в клинической практике. В данной статье мы представили результаты рандомизированного перекрестного исследования клинической эффективности отечественного генерического аторвастатина АТОМАКС® по сравнению с оригинальным импортным продуктом ЛИПРИМАР у 27 пациентов с гиперхолестеринемией.
Согласно результатам нашей работы, между двумя исследованными препаратами аторвастатина не отмечалось значимых статистических отличий (p>0,05) в динамике уровня ХС ЛПНП как на 6-й (-1,51 и –1,43 ммоль/л), так и на 12-й неделе (+0,05 и –0,02 ммоль/л). Полученные данные свидетельствуют о том, что с точки зрения клинической эффективности продукты АТОМАКС® и ЛИПРИМАР были эквивалентны.
Снижение содержания ХС ЛПНП сыворотки крови при лечении как оригинальным препаратом (30-31%), так и генериком (29-30%) аторвастатина, достигнутое в этой работе, аналогично результатам, полученным на большом количестве пациентов, принимавших аторвастатин в дозе 10 мг в сут. в исследовании ASCOT-LLA (-29%) (3).
В нашем исследовании был зарегистрирован только один случай побочного действия, связанный с приемом генерического препарата – появление боли в икроножных мышцах, прекратившейся после отмены препарата. Вследствие несвоевременного сообщения пациенткой об этом явлении, исследования уровня КФК в крови во время развития симптомов не проводилось. Таким образом, мы не можем исключить эффект статина, хотя симптомы могли носить и неспецифический характер.
Другим проявлением побочного эффекта у больных, получающих статины, может быть повышение ферментов печени, которое обычно наблюдается в 0,5-2% случаев (4). В нашем исследовании трехкратное превышение верхней границы нормы для печеночных трансаминаз не отмечалось ни у одного из 25 пациентов, принимавших исследуемые препараты аторвастатина.
Результаты данного исследования показали, что препараты АТОМАКС® (ЗАО «МАКИЗ-Фарма», Россия) и ЛИПРИМАР (Pfizer, США) в дозе 10 мг в сутки были эквивалентны по клинической эффективности и обладали схожей переносимостью.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.