Связь факторов патогенности Helicobacter pylori с развитием пренеопластических изменений и рака желудка
- Аннотация
- Статья
- Ссылки
- English

Введение
В 1982 г. австралийскими учеными Барри Маршалом и Робином Уорреном была доказана ведущая роль бактерии Нelicobacter pylori в развитии хронического гастрита и язвенной болезни [1]. Ранее имевшиеся представления о роли стресса и питания, как ключевых причин развития язвенной болезни и гастрита, были опровергнуты новыми данными. Открытие роли H. pylori стало пусковым механизмом для новой эры как в научных исследованиях в этой области, так и в лечении заболеваний верхних отделов пищеварительного тракта. Дальнейшие работы показали, что инфекция H. pylori играет ведущую роль в развитии также рака желудка и MALT-лимфомы. Всемирная организация здравоохранения признала H. pylori канцерогеном I класса. Согласно обобщенным данным, до 89% случаев дистального рака желудка связаны с инфекцией H. pylori [2]. Данные положения отражены как в консенсусе Маастрихт VI, так и в рекомендациях Российской гастроэнтерологической ассоциации [3, 4].
Инфекция H. pylori широко распространена в мире, она встречается примерно у 50% населения, при этом за последние десятилетия отмечается общемировая тенденция к снижению ее распространенности, что сопровождается статистически значимым снижением и распространенности рака желудка в мире [5]. Этот же тренд в снижении распространенности инфекции H. pylori отмечается и на территории нашей страны с 1990 по 2023 г. [6]. По данным систематического обзора и метаанализа 2025 г., включившего 20 исследований, проведенных в России, было показано статистически значимое снижение распространенности инфекции H. pylori: в период до 2005 г. она составляла 79,334%, в то время как после 2018 г. – 42,949%, коэффициент регрессии в год составил -3,773%, p < 0,001 [7]. В Москве до 2015 г. инфицированность населения H. pylori была 81,294% (95%-ный доверительный интервал (95% ДИ) 67,202–92,109), в 2015–2020 гг. – 68,028% (95% ДИ 29,383–95,895), а после 2020 г. снизилась до 39,860% (95% ДИ 33,993–45,877). Метарегрессионный анализ показал коэффициент регрессии -4,22% в год (95% ДИ -6,27–(-2,17), p < 0,0099) [8].
Важнейшую роль в первичной профилактике рака желудка играет эрадикация H. pylori у взрослого населения как с целью предотвращения прогрессирования предраковых изменений у зараженного индивидуума, так и с целью профилактики передачи этой бактерии другим лицам, в том числе и детям [9, 10]. Немаловажную роль также играет дальнейшее изучение особенностей самой бактерии H. pylori как для лучшего понимания терапевтических мишеней, так и с целью определения групп пациентов особого риска для их дополнительного наблюдения.
За последние десятилетия отмечен значительный прогресс в понимании патофизиологии и патогенетических механизмов бактерии H. pylori. Штаммы H. pylori генетически гетерогенны и отличаются друг от друга, в том числе наличием факторов патогенности [11]. К настоящему времени известно о более чем 15 различных факторах патогенности H. pylori, каждый из которых оказывает влияние на риски заражения и развития инфекции, – прогрессирование воспаления, атрофические и другие предраковые изменения (метаплазия и дисплазия) в слизистой оболочке желудка [12, 13]. Наиболее изученными и доказанными факторами патогенности H. pylori являются CagA (ген, ассоциированный с цитотоксином) и VacA (вакуолирующий цитотоксин).
В представленном обзоре проанализированы международные и отечественные данные о роли факторов патогенности H. pylori на развитие пренеопластических изменений и рака желудка:
- влияние факторов патогенности H. pylori на развитие гастродуоденальной патологии и особенно рака желудка;
- соотношение факторов патогенности H. pylori с серологическими маркерами атрофии слизистой желудка;
- оценка связи факторов патогенности H. pylori с морфологическими изменениями слизистой оболочки желудка.
Факторы патогенности H. pylori
У значимой части инфицированных H. pylori гастрит протекает бессимптомно, в то время как у других больных развиваются тяжелые осложнения, включая язвенную болезнь, атрофический гастрит, рак желудка и MALT-лимфому.
H. pylori – это грамотрицательная спиралевидная бактерия, имеющая жгутики. Вирулентность и патогенность H. pylori являются результатом сложного взаимодействия факторов патогенности самой бактерии, организма хозяина и факторов окружающей среды.
Колонизация бактерии и возникновение заболеваний, вызванных H. pylori, зависят от четырех основных этапов: 1) адаптация патогена к кислой среде слизистой оболочки желудка; 2) движение к эпителиальному клеточному барьеру; 3) прикрепление (адгезия) бактерии к специфическим рецепторам слизистой оболочки; 4) повреждение эпителиальных клеток токсинами. Поэтому для успешной колонизации хозяина и развития патологических изменений бактерия H. pylori должна быть способна выживать в кислой среде желудка, прикрепляться к клеткам хозяина и выделять повреждающие ткани токсины.
Основные эффекторные белки/токсины, выделяемые H. pylori, включают: адгезин, связывающий антиген группы крови (BabA); внешний воспалительный белок (OipA); белки наружной мембраны (OMP) – всего 64 белка; везикулы внешней мембраны (OMV); вакуолизирующий цитотоксин (VacA); продукт гена, ассоциированного с цитотоксином А (CagA); белок A, требующий высокой температуры (HtrA); белок A, активирующий нейтрофилы (NepA); адгезины, связывающие сиаловую кислоту (SabA); DupA (ген, способствующий развитию дуоденальной язвы); IceA (ген, индуцируемый контактом с эпителием). Другие белки наружной мембраны, присутствующие в H. pylori, включают Helicobacter OMPQ (HopQ) и Helicobacter OMPZ (HopZ), белки семейства белков наружной мембраны H. pylori – HomA, HomB, HomC и HomD. Связывание H. pylori с эпителиальными клетками желудка, колонизация и образование биопленки также опосредованы липопротеинами A и B, ассоциированными с адгезией (AlpA/AlpB) [14].
Наиболее изученными и клинически значимыми факторами патогенности H. pylori являются CagA (ген, ассоциированный с цитотоксином) и VacA (вакуолирующий цитотоксин).
CagA – ген H. pylori, ассоциированный с цитотоксином, является ведущим геном островка патогенности (CagPAI). Другие гены островка патогенности (их насчитывают около 30) необходимы как компоненты для формирования T4SS – четырех типов секреторной системы, которая обеспечивает встраивание белка CagA в клетки-мишени.
Ген CagA связан с более высоким риском рака желудка и язвенной болезни двенадцатиперстной кишки (ДПК). При проникновении этого белка в клетки хозяина запускаются патологические процессы, которые и приводят к воспалению, повреждению, а в долгосрочной перспективе и к канцерогенезу [15]. Это происходит через активацию сигнального пути NF-kB и усиление выработки цитокина интерлейкина 8, запускающего воспаление [16, 17].
Фактор патогенности VacA (вакуолирующий цитотоксин) участвует в формировании каналов в мембране клетки хозяина и митохондриях клетки хозяина и таким образом нарушает работу ионных каналов. Это приводит к образованию вакуолей и развитию апоптоза в инфицированных клетках [18]. Также белок VacA нарушает работу сигнальных систем в инфицированных клетках (например, работу митоген-активируемой протеинкиназы (MAPK)). Все эти механизмы гена VacA играют роль в онкогенном потенциале H. pylori [19].
Ген VacA имеет различные аллельные варианты, которые и определяют суммарную его патогенность. Он содержит вариабельные последовательности: s-регион – кодирует сигнальный пептид и m-регион (medium) – кодирует средний участок зрелого вакуолизирующего белка. Описаны различные по размеру и нуклеотидной последовательности аллельные варианты этого гена: s1 или s2 и m1 или m2 соответственно.
Штаммы H. pylori, имеющие аллельные варианты s1m1, проявляют наиболее патогенные свойства. Штаммы с аллельными вариантами s2m2, наоборот, обладают менее патогенными свойствами. Промежуточные аллельные варианты s1m2 и s2m1 имеют промежуточные свойства по патогенности [20].
Влияние факторов патогенности H. pylori на риски развития язвенной болезни и рака желудка
Данные многочисленных наблюдательных работ показали, что среди инфицированных H.pylori у носителей CagA-позитивных штаммов H. pylori и более патогенных вариантов гена VacA выше частота язвенной болезни и рака желудка [21–23]. Так, еще в 1995 г. было показано, что инфекция с CagA-позитивными штаммами H. pylori повышает риски развития рака желудка, особенно кишечного типа (отношение шансов (ОШ) 2,3; 95% ДИ 1,0–5,2), характерного для дистальных отделов желудка [24].
В метаанализе 2024 г., объединившем данные 2848 пациентов из 24 исследований, проведенных в восьми странах Индо-Тихоокеанского региона (Бутан, Индия, Индонезия, Малайзия, Мьянма, Сингапур, Таиланд, Вьетнам), было показано, что риски развития рака желудка достоверно выше у лиц с CagA-позитивными штаммами по сравнению с CagA-негативными (ОШ 2,53; 95% ДИ 1,15–5,55). Диагностику CagA проводили методом полимеразной цепной реакции (ПЦР). Распространенность CagA-позитивных штаммов H. pylori составила: 78% – при гастрите (95% ДИ 67–90%), 86% – при язвенной болезни (95% ДИ 73–96%) и 83% – при раке желудка (95% ДИ 51–100%) [25].
Метаанализ 2022 г. выявил связь между серологическим выявлением антител к факторам патогенности и раком желудка. Было проанализировано девять исследований (всего 3209 случаев рака желудка и 6964 пациента в контрольной группе). Пять факторов вирулентности H. pylori были значимо ассоциированы с риском некардиального рака желудка при p-значении < 0,0033, включая: CagA (ОШ 3,22; 95% ДИ 2,10–4,94), VacA (ОШ 2,05; 95% ДИ 1,67–2,52), а также HP0305 (ОШ = 1,72; 95% ДИ 1,32–2,25), HyuA (ОШ = 1,42; 95% ДИ 1,13–1,79), Omp (ОШ = 1,83; 95% ДИ 1,30–2,58). Однако ни один из 15 исследуемых антигенов не был связан с риском кардиального рака желудка [26].
Более ранний метаанализ 2013 г., в который было включено 44 исследования из 17 стран (всего 17374 пациента), также показал связь факторов патогенности H. pylori – CagA и VacA (различными его аллельными вариантами) с патологией желудка. Позитивный CagA-статус был связан с повышенным риском рака желудка (ОШ 2,09; 95% ДИ 1,48–2,94) и язвенной болезни (ОШ 1,69; 95% ДИ 1,12–2,55). Лица, являющиеся носителями штаммов H. pylori VacA: s1 по сравнению с s2, m1 по сравнению с m2, s1m1 по сравнению с s1m2 и s1m1 по сравнению с s2m2, имели повышенный риск развития рака желудка – ОШ 5,32 (95% ДИ 2,76–10,26); ОШ 2,50 (95% ДИ 1,67–3,750); ОШ 2,58 (95% ДИ 1,24–5,38) и ОШ 4,36 (95% ДИ 2,08–9,10) соответственно. Штаммы s1m1 по сравнению с s2m2 также были связаны с язвенной болезнью – ОШ 2,04 (95%ДИ 1,01–4,13) [27].
Метаанализ 2010 г., который включил 10 исследований из восточно-азиатских стран (всего 4325 пациентов), показал, что в целом отмечается положительная связь между наличием антител к CagA и повышенным риском рака желудка, однако результаты различались в зависимости от условий исследования и, по-видимому, были связаны с использованием разных методик или вариациями в антигенах для обнаружения антител к CagA. В семи исследованиях ОШ составило 1,26 (95% ДИ 1,05–1,52). Показатель ОШ в странах Восточной Азии был ниже, чем в метаанализе, включавшем западные страны (1,26 против 1,49). Также авторы метаанализа обращают внимание, что среди лиц с низким титром антител к CagA имеется более высокий и более значимый риск некардиального рака желудка (относительный риск (ОР) 3,9; p < 0,001), чем среди тех лиц, у кого был CagA-серонегативный статус (ОР 2,2; p = 0,0052) или высокий титр антител CagA (ОР 2,0; p = 0,0022) [28]. Эти данные свидетельствуют о том, что следует уделять внимание не только факту выявления, но и титру антител к CagA. Данные о роли титра антител и риске выявления рака желудка подтверждаются исследованиями из Бразилии [29] и Японии [30]. Видимо, более низкий титр антител к CagA связан с более низкой обсемененностью H. pylori, что является следствием более выраженной атрофии слизистой желудка.
Метаанализ 2003 г., включающий 16 исследований (2284 случая заболевания и 2770 контрольных пациентов), показал, что серопозитивность как по H. pylori, так и по CagA значительно увеличивала риск рака желудка – в 2,28 и 2,87 раза соответственно. При этом выявление СagA-положительных штаммов H. pylori дополнительно увеличивало риск рака желудка в 1,64 раза по сравнению с фактом наличия инфекции H. pylori (95% ДИ 1,21–2,24) [31].
В отечественных исследованиях была проанализирована связь различных факторов патогенности H. pylori и подтверждена их роль в развитии более тяжелых проявлений заболевания – выше риск язвенной болезни и рака желудка [32–34].
Таким образом, наличие факторов патогенности H. pylori играет значимую роль в развитии более тяжелых проявлений ассоциированной патологии. Особое внимание уделяется фактору патогенности CagA.
Связь факторов патогенности H. pylori и серологических маркеров атрофии
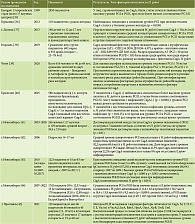
В качестве серологических маркеров атрофии слизистой оболочки желудка активно изучаются уровни сывороточных пепсиногенов I (PGI) и II (PGII), а также их соотношение (PG I/II). Опубликован ряд работ, в которых оценивали связь серологических маркеров атрофии слизистой желудка и статуса пациента по фактору патогенности CagA (табл. 1) [35–45].
Таким образом, анализ результатов исследований выявил общую тенденцию к повышению средних значений уровней пепсиногенов PGI и/или PGII и снижение соотношения PGI/II у CagA-позитивных пациентов в группе хронического гастрита. В ряде работ также показано, что доля пациентов со сниженными пепсиногенами выше среди CagA-позитивных пациентов, а также наблюдается снижение PGI у CagA-позитивных пациентов с раком желудка.
Связь факторов патогенности H. pylori и морфологических характеристик гастрита
В 2024 г. был опубликован метаанализ с оценкой связи серопозитивности по CagA и предраковых поражений желудка (ППЖ) по результатам 13 исследований (2728 пациентов с ППЖ и 17612 пациентов группы контроля). Суммарное ОШ между выявлением антител к CagA и ППЖ составило 2,74 (95% ДИ 2,25–3,32; p = 0,00; I2 = 60,4%), независимо от статуса инфицирования H. pylori. В когорте пациентов, инфицированных H. pylori, ОШ составил 2,25 (95% ДИ 1,99–2,56; p = 0,00; I2 = 0,0%). Напротив, среди неинфицированных лиц ОШ составил 1,63 (95% ДИ 1,04–2,54; p = 0,038; I2 = 0,0%). По итогам метаанализа выявлена более выраженная связь между серопозитивностью по CagA и риском развития ППЖ, чем между серонегативностью и тем же риском, независимо от статуса инфекции H. pylori на тот момент. Кроме того, выраженность этой связи возрастала при наличии активной инфекции H. pylori. Результаты исследования подтверждают целесообразность учета серологического статуса CagA в качестве потенциального биомаркера для скрининга ППЖ [46].
В работе 2025 г. представлены данные о распространенности предраковых изменений слизистой оболочки желудка в районе Нанкин (Китай). При обследовании 15 668 человек с июля 2022 г. по июнь 2023 г. у 259 (1,65%) пациентов были выявлены ППЖ (дисплазия слизистой желудка низкой и высокой степени), а у 218 (1,39%) – рак желудка. Частота инфицирования H. pylori среди всех пациентов составила 5014 (32%) пациентов, среди мужчин – 2684 (34,06% от всех мужчин); среди женщин – 2335 (29,92% от всех женщин). Частота инфицирования H. pylori среди пациентов с доброкачественными образованиями желудка составила 31,45%, при наличии ППЖ – 44,40%, при выявлении рака желудка – 55,50% [47].
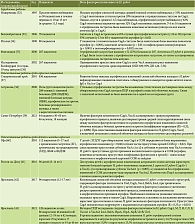
Работы, в которых проводили оценку влияния факторов патогенности Н. pylori на развитие атрофических изменений по системе OLGA (Operative Link on Gastritis Assessment), представлены в табл. 2 [48–51]. Данные работы суммарно показывают, что более высокопатогенные штаммы Н. pylori достоверно повышают риски развития более выраженной стадии атрофии и/или метаплазии по OLGA/OLGIM. Это относится как к CagA-позитивным штаммам, так и к аллельным вариантам генов VacA (s1m1), IceA1.
Опубликованы результаты исследований, в которых были сопоставлены факторы патогенности H. pylori и атрофия слизистой оболочки желудка при оценке по Сиднейской классификации (табл. 3) [52–62]. Как и в работах, где морфологическую оценку проводили по системе OLGA, прослеживается выраженное влияние высокопатогенных штаммов H. pylori на повышение частоты развития атрофического гастрита, более выраженной атрофии и наличия кишечной метаплазии.
Заключение
Представленный анализ демонстрирует связь факторов патогенности H. pylori с риском развития пренеопластических изменений и рака желудка как в опубликованных исследованиях по оценке серологических маркеров атрофии слизистой оболочки желудка, так и непосредственно при ее морфологической оценке. Выявление факторов патогенности H. pylori, таких как CagA и VacA, может быть ценным инструментом при формировании групп риска развития рака желудка с целью последующего наблюдения после эрадикации H. pylori.
E.S. Kuznetsova, K.A. Nikolskaya, PhD, D.S. Bordin, PhD, Prof.
A.S. Loginov Moscow Clinical Scientific Center
Research Institute of Health Organization and Medical Management, Moscow
Russian University of Medicine, Moscow
Tver State Medical University
Contact person: Elena S. Kuznetsova, dietolog.elenakuznetsova@yandex.ru
Helicobacter pylori infection affects approximately half the world's population, always leading to the development of chronic gastritis, which can lead to ulcers and gastric cancer. Although gastric cancer develops in only 1–2% of infected individuals, 90% of cases of adenocarcinoma are caused by long-term H. pylori gastritis. The risk of developing cancer is influenced by host characteristics, environmental factors, and lifestyle, as well as the specific H. pylori strain. A number of H. pylori virulence factors have been described that contribute to a more pronounced inflammatory response of the gastric mucosa, as well as the development and progression of precancerous lesions. Among the most studied and significant H. pylori virulence factors are CagA (a cytotoxin-associated gene) and VacA (vacuolating cytotoxin).
This review presents data from studies evaluating the association between H. pylori virulence factors and the development of preneoplastic lesions and gastric cancer.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.