Влияние фактора патогенности CagA Helicobacter pylori на развитие атрофических изменений слизистой оболочки желудка
- Аннотация
- Статья
- Ссылки
- English

Введение
Результаты более чем 40-летних исследований Helicobacter pylori свидетельствуют о важности диагностики и лечения этой инфекции [1]. H. pylori – это грамотрицательная спиралевидная бактерия, имеющая жгутики, которая является основной причиной развития гастрита, язвенной болезни и рака желудка [2]. По данным метаанализа 2023 г., распространенность этой инфекции в мире составляет 43,1% [3]. При этом распространенность хеликобактерной инфекции снижается как во всем мире [4], так и в нашей стране в частности [5, 6].
H. pylori приводит к развитию хронического гастрита у всех инфицированных, у части из них развивается язвенная болезнь, атрофический гастрит, а также предраковые изменения слизистой желудка, такие как метаплазия и дисплазия; примерно у 1–2% развивается рак желудка. Поэтому своевременное выявление и эрадикация этой инфекции рассматриваются в качестве стратегии первичной профилактики рака желудка [7–9].
В то же время исходы хеликобактерной инфекции зависят как от особенностей макроорганизма (человека), факторов среды, так и от свойств самой бактерии. Было показано, что штаммы H. pylori неоднородны по патогенным свойствам и агрессивному воздействию на слизистую желудка [10]. Выявлено более 15 факторов патогенности H. pylori, среди них белки внешней мембраны (Omp), адгезины, DupA (ген, способствующий развитию дуоденальной язвы), IceA (ген, индуцируемый контактом с эпителием), вакуолизирующий цитотоксин (VacA) и CagA (цитотоксин-ассоциированный ген А) [11].
CagA является одним из наиболее подробно изученных факторов патогенности H. pylori в развитии гастродуоденальной патологии, что отражено в результатах многочисленных работ [12–15]. Так, данные метаанализа 2024 г. [16], объединившего результаты 24 исследований из стран Индо-Тихоокеанского региона (2848 пациентов), показали, что риски развития рака желудка достоверно выше у лиц, инфицированных CagA-позитивными штаммами (диагностика методом полимеразной цепной реакции) по сравнению с CagA-негативными (отношение шансов – 2,53; 95%-ный доверительный интервал – 1,15–5,55).
В Москве ранее уже были проведены исследования частоты выявления антител к фактору патогенности CagA. В 2010 г. среди 264 обследованных 17–69 лет CagA-позитивные штаммы были выявлены у 214 (81%) пациентов [17]. В 2019 г. при обследовании 698 лиц с метаболическим синдромом, инфицированных H. pylori (средний возраст 46 лет), CagA-позитивные штаммы были выявлены у 392 (56,2%) пациентов [18]. В работе 2018 г. среди 267 H. pylori-позитивных пациентов 18–67 лет антитела к CagA были выявлены у 162 (60,67%) пациентов [19]. Опубликованные данные гетерогенны и получены на небольших выборках.
Связь факторов патогенности H. pylori, в частности фактора патогенности CagA, и серологических маркеров атрофии (уровни сывороточных пепсиногенов I (PGI) и II (PGII), а также их соотношение (PGI/PGII)) изучаются с 1999 г. [20]. Полученные данные противоречивы, но в целом отмечена тенденция к повышению средних значений PGII и снижению соотношения PGI/PGII у CagA-позитивных пациентов [21]. В отдельных исследованиях также было показано, что среди CagA-позитивных пациентов доля пациентов с серологическими маркерами атрофии выше [22, 23]. Среди больных раком желудка было выявлено снижение уровня PGI при выявлении CagA-антигена [24].
В пяти зарубежных работах было показано, что высокопатогенные штаммы Н. pylori, в том числе CagA-позитивные, достоверно повышают риск выявления более тяжелых стадий атрофии по OLGA и/или по OLGIM [21].
В настоящей статье представлена частота выявления фактора патогенности CagA в репрезентативной выборке взрослого населения города Москвы, оценена связь статуса CagA с серологическими маркерами атрофии и морфологической стадией по системе OLGA.
Материал и методы
Данные получены в июне 2022 г. – июле 2025 г. при исследовании распространенности инфекции H. pylori у жителей города Москвы. Критерием включения в исследование было отсутствие эрадикационной терапии в анамнезе. Общая когорта была сформирована из возрастно-половых групп, отражающих структуру населения города Москвы. В данную работу были включены пациенты с подтвержденной 13С-уреазным дыхательным тестом (13С-УДТ) инфекцией H. pylori. 13С-УДТ проводили на инфракрасном газовом анализаторе (спектрометре) IR-Fors 200, тест-набор «ХЕЛИКАРБ» (производитель ООО «ИЗОКАРБ», Россия). Положительный результат 13С-УДТ считали при DOB 4‰ и более.
Для определения CagA статуса пациентов было проведено серологическое исследование – иммуноферментный анализ суммарных антител к CagA антигену H. pylori (фирма АО «Вектор-Бест», Россия), норма < 0,41 у.е.
Для оценки серологических маркеров атрофии использовали тест-систему «Гастропанель» (Biohit, Финляндия). Серологическими маркерами атрофии являлись уровень PGI менее 30 мкг/л и/или соотношение PGI/PGII ≤ 3.
При эзофагогастродуоденоскопии (ЭГДС) выполняли забор пяти биоптатов по новому Сиднейскому протоколу (два из антрального отдела, два из тела желудка – по большой и малой кривизне желудка и один биоптат из угла желудка). Была проведена морфологическая оценка атрофии по системе OLGA (от 0 до IV стадии).
Статистическую обработку данных проводили с использованием специализированного программного обеспечения MedCalc 23.2.1 (MedCalcSoftware, Бельгия) в Microsoft Windows 11 (Microsoft Corp., США). Для расчета показателя p использовали тест Манна – Уитни, а также точный тест Фишера для оценки статистической значимости различий в доле CagA-позитивных пациентов среди разных групп по возрасту и полу. Для оценки корреляции использовали коэффициент корреляции Кэнделла.
Результаты
Проведен анализ данных 1871 пациента (901 мужчина и 970 женщин) в возрасте от 18 до 80 лет, средний возраст всех пациентов – 47,45 ± 13,92 года, средний возраст мужчин – 46,25 ± 13,3 года, средний возраст женщин – 48,57 ± 14,39 года. Различия по возрасту между группой мужчин и женщин статически достоверны (p = 0,0005).
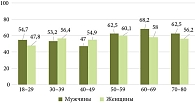
У всех была выявлена инфекция H. pylori при проведении 13С-УДТ. Антитела к фактору патогенности CagA H. pylori были выявлены у 1056 (56,4%) обследованных. Среднее значение уровня антител у CagA-позитивных пациентов составило 1,971 ± 0,84 у.е. У мужчин частота выявления антител к CagA составила 56,6% (510 из 901), у женщин – 56,3% (546 из 970), отличия статически недостоверны (p = 0,92). Средний уровень антител у CagA-позитивных мужчин составил 1,778 ± 0,804 у.е., у женщин – 2,151 ± 0,834 у.е.
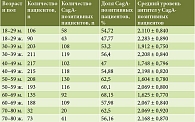
Распределение CagA-позитивных пациентов по возрастно-половым группам представлено в табл. 1 и на рис. 1.
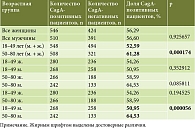
В таблице 2 представлены данные о достоверности различий между половозрастными группами пациентов. Отмечено нарастание доли CagA-позитивных пациентов в более старших возрастных группах – старше 50 лет (50–80 лет) по сравнению с группой до 50 лет (18–49 лет): различия статистически достоверны при сравнении объединенных групп мужчин и женщин (p = 0,000174) и при сравнении мужских групп до и после 50 лет (p = 0,000056). По остальным представленным группам достоверных различий в частоте выявления доли CagA-позитивных пациентов не выявлено.
Связь фактора патогенности CagA H. pylori и серологических маркеров атрофии
Проведено сопоставление статуса CagA и серологических маркеров атрофии у 1860 пациентов (895 мужчин и 965 женщин) со средним возрастом 47,45 ± 13,91 года. CagA-позитивными были 1053 (56,61%) пациента. Средние значения уровней PGI и PGII, а также соотношение PGI/PGII в зависимости от статуса CagA представлены в табл. 3. У CagA-позитивных пациентов были достоверно выше средние уровни PGI и PGII, что отражает бо́льшую выраженность воспалительных изменений слизистой оболочки желудка (СОЖ). При этом соотношение PGI/PGII было значимо ниже, что указывает на тенденцию к развитию атрофических изменений СОЖ.
Серологические маркеры атрофии СОЖ выявлены у 251 (13,49%) пациента: изолированное снижение PGI менее 30 мкг/л выявлено у трех больных, изолированное снижение соотношения PGI/PGII ≤ 3 – у 198 пациентов, а одновременное снижение PGI менее 30 мкг/л и соотношения PGI/PGII ≤ 3 – у 50 пациентов. При анализе группы CagA-позитивных пациентов выявлено 187 из 1053 (17,76%) с серологическими маркерами атрофии; в группе CagA-негативных пациентов – только у 64 из 807 (7,93%). Таким образом, пациенты с серологическими маркерами атрофии достоверно чаще встречаются в группе CagA-позитивных по сравнению с CagA-негативными пациентами и всей когортой обследованных – 17,76 против 7,93% (p < 0,01) и 17,76 против 13,49% (p < 0,01) соответственно, что подтверждает влияние фактора патогенности CagA H. pylori на развитие атрофии СОЖ.
Связь фактора патогенности CagA H. pylori и результатов морфологического исследования по OLGA
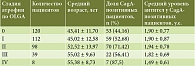
Анализ данных 377 больных (174 мужчины и 203 женщины), которым были проведены ЭГДС и морфологическое исследование по системе OLGA, их распределение в зависимости от стадии атрофии представлены в табл. 4. Средний возраст составил 47,71 ± 13,12 года (от 19 до 73 лет). Антитела к CagA были выявлены у 211 (55,97%) пациентов.
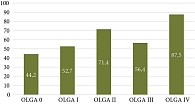
По результатам исследования отмечено нарастание доли CagA-позитивных пациентов по мере повышения стадии атрофии по OLGA (от 44,16% при 0 стадии до 87,5% при IV стадии), коэффициент корреляции Кендалла +0,176 (p < 0,01) – слабая положительная корреляционная связь. Средний возраст пациентов также нарастает по мере увеличения стадии атрофии по OLGA (от 43,41 года при 0 стадии до 55,38 года при IV стадии), коэффициент корреляции Кендалла +0,255 (p < 0,01) – слабая положительная корреляционная связь. Таким образом, выраженность атрофического гастрита определяет как возраст (косвенно отражая длительность течения H. pylori-ассоциированного гастрита), так и наличие у H. pylori фактора патогенности CagA.
Обсуждение
Из репрезентативной выборки взрослого населения города Москвы, принявшего участие в эпидемиологическом исследовании распространенности инфекции H. pylori, была отобрана когорта из 1871 пациента с позитивным результатом 13С-УДТ. В этой группе отмечена высокая частота выявления CagA-позитивных штаммов H. pylori – 56,4%. Среди мужчин CagA-позитивными были 56,6%, среди женщин – 56,3% (p = 0,92). В ранее проведенных исследованиях когорты пациентов были меньше и критерии их формирования были менее строгими. Этим, вероятно, объясняется гетерогенность ранее полученных данных – 81% [17], 56,2% [18], 60,67% [19]. Стоит отметить, что в исследованиях, проведенных в 2018 и 2019 гг., получены результаты, сопоставимые с нашими. При этом в 2010 г. частота выявления CagA- позитивных штаммов H. pylori была выше.
При углубленном анализе влияния позитивного статуса по CagA на серологические маркеры атрофии в выборке из 1860 пациентов мы отметили достоверное повышение средних уровней PGI (p < 0,01) и PGII (p < 0,01) по сравнению с CagA-негативными пациентами. Напротив, соотношение PGI/PGII было статически значимо ниже (p < 0,01) в группе CagA-позитивных лиц. Кроме того, в этой группе была выше частота выявления серологических маркеров атрофии по сравнению с CagA-негативными пациентами: 17,76 против 7,93% (p < 0,01). Таким образом, фактор патогенности CagA стимулирует более выраженное воспаление в СОЖ (повышение PGI и PGII), что закономерно приводит к более частому развитию атрофии. Эти результаты, полученные на большой выборке больных, подтверждают опубликованные ранее данные [21].
Нами впервые в России был проведен анализ влияния фактора патогенности CagA на развитие атрофических изменений слизистой желудка, оцененных по системе OLGA. Была выявлена слабая положительная корреляционная связь наличия CagA и атрофических изменений (коэффициент корреляции Кендалла +0,176; p < 0,01). Кроме того, показано, что фактор патогенности CagA наряду с длительностью течения хронического гастрита, ассоциированного с H. pylori, повышают риск развития атрофии.
Заключение
Высокая распространенность CagA-позитивных штаммов H. pylori в городе Москве и влияние этого фактора патогенности на развитие атрофических изменений слизистой желудка обусловливают необходимость системной работы, направленной на своевременную диагностику и эрадикацию инфекции H. pylori с целью предотвращения развития пренеоплаcтических изменений и первичной профилактики рака желудка.
E.S. Kuznetsova, K.A. Nikolskaya, PhD, S.G. Khomeriki, PhD, Prof., E.V. Parfenchikova, PhD, A.S. Dorofeev, D.N. Andreev, PhD, M.V. Chebotareva, I.N. Voinovan, PhD, K.K. Noskova, PhD, N.A. Neyasova, V.V. Lomova, N.A. Gulieva, D.S. Bordin, PhD, Prof.
A.S. Loginov Moscow Clinical Scientific Center
Russian University of Medicine, Moscow
Tver State Medical University
Research Institute of Health Organization and Medical Management, Moscow
Contact person: Elena S. Kuznetsova, dietolog.elenakuznetsova@yandex.ru
Helicobacter pylori is the most significant cause of gastric cancer. Carcinogenesis is influenced by the characteristics of the host (human) and H. pylori, of which the CagA virulence factor has been the most studied. In an epidemiological study conducted between 2022 and 2025, a cohort of 1,871 Moscow residents (901 men and 970 women, average age 47.45 ± 13.92 years) was formed. They were infected with H. pylori based on the 13C-urea breath test. Serological testing for total antibodies to the CagA virulence factor and analysis of serological markers of atrophy were conducted. 377 patients underwent endoscopy with biopsy according to the new Sydney protocol and assessment using the OLGA system. Antibodies to H. pylori CagA were detected in 1056 patients (56.44%), with equal frequency among men (56.6%) and women (56.3%). In the group of CagA-positive patients, the proportion of individuals with detection of serological markers of atrophy was significantly higher compared to the group of CagA-negative patients (17.76 versus 7.93%, p < 0.001). A weak positive correlation was noted between the presence of antibodies to the CagA virulence factor and a more severe stage of atrophy according to OLGA: Kendall's correlation coefficient was 0.176 (p < 0.01).
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.