Тиазолидиндионы – клиническая эффективность, безопасность, роль и варианты применения в клинической практике
- Аннотация
- Статья
- Ссылки
Акцентируя внимание на актуальности проблемы сахарного диабета 2 типа, приведем высказывание Пола Зиммета, директора Центра диабета при ВОЗ и Международного института по исследованию диабета в Австрии: «Грядет глобальный цунами диабета, катастрофа, которая станет кризисом здравоохранения XXI столетия. Это может впервые за 200 лет снизить продолжительности жизни в глобальном масштабе». Все вышеприведенное диктует необходимость активного поиска и внедрения в клиническую практику новых подходов к управлению этим заболеванием и предотвращению его осложнений (1).
В основе сахарного диабета 2 типа лежат два основных фактора: инсулинорезистентность и недостаточная функция β-клеток. Особенности течения заболевания и эффективность применяемой терапии определяются индивидуальным сочетанием этих двух основных причин. Единого мнения о том, какой из перечисленных факторов является первичным в патогенезе сахарного диабета 2 типа, нет. Тем не менее, исследования последних лет подтверждают первичность инсулинорезистентности (2).
В настоящее время существуют немедикаментозные и фармакологические методы коррекции инсулинорезистентности. К первым относятся низкокалорийная диета и физические нагрузки – опора, на которой базируется лечение всех больных с сахарным диабетом 2 типа. Следование указанным предписаниям – постепенное снижение массы тела и повышение физической активности – у мотивированных пациентов может резко повысить чувствительность к инсулину. Тем не менее, у тучных больных в силу значительной выраженности инсулинорезистентности указанных мер чаще оказывается недостаточно. Тогда возникает необходимость применения фармакологических методов. С середины XX века фармацевтическая промышленность работает над созданием препаратов, устраняющих инсулинорезистентность. Первым лекарственным средством, доказавшим свою эффективность и безопасность и заслужившим признание специалистов, стал метформин из группы бигуанидов. Однако он лишь отчасти позволял решить поставленную задачу, снижая инсулинорезистентность ткани печени, тем самым, уменьшая активность протекающих там процессов гликогенолиза и глюконеогенеза, и в меньшей степени влияя на инсулинорезистентность мышечной и жировой ткани. Только в конце 90-х гг. прошлого века появилась принципиально новая группа лекарственных препаратов, способствующая решению этой проблемы (3).
Такой группой стали тиазолидиндионы, или глитазоны. Они являются синтетическими агонистами гамма-рецепторов, активируемых пероксизмальным пролифератором (PPAR-гамма). Активирование PPAR-γ сопровождается многочисленными метаболическими и сосудистыми эффектами как следствие ингибирования или повышения экспрессии значительного количества генов, включая гены, участвующие в контроле углеводного и жирового обмена, микроциркуляции, свертывающей системы и воспалительного ответа организма. В результате увеличивается активность транспортеров глюкозы (ГЛЮТ-1 и ГЛЮТ-4), глюкокиназы, липопротеинлипазы и других ферментов, активируется липогенез в жировых клетках, уменьшается поступление свободных жирных кислот в другие ткани, снижается возможность развития инсулинорезистентности в мышцах и печени. Тиазолидиндионы, устраняя инсулинорезистентность, усиливают физиологическое действие собственного эндогенного инсулина и при этом снижают его концентрацию в крови. Кроме того, глитазоны обладают способностью сохранять функциональную активность β-клеток поджелудочной железы, т. е. способностью осуществлять профилактику сахарного диабета 2 типа, что ставит их на ступень выше других сахароснижающих препаратов.
В России зарегистрировано два препарата из рассматриваемой группы – росиглитазон и пиоглитазон. Наибольшее распространение получил росиглитазон, который используется во всем мире уже на протяжении многих лет. Многочисленные клинические исследования, в том числе такие масштабные, как ADOPT, DREAM, RECORD, оценивали клиническую эффективность данного препарата, определяемую на основании влияния на гликемический контроль. Результаты многих исследований продемонстрировали достоверное улучшение параметров углеводного обмена, снижение уровня гликированного гемоглобина. Более того, выявлены значительное улучшение чувствительности к инсулину по сравнению с другими ПССП и даже способность тиазолидиндионов играть позитивную роль в сохранении функции β-клеток. Однако известно, что, способность лекарственного препарата улучшать гликемический контроль совершенно не обязательно определяет также и его способность существенно снижать риск осложнений сахарного диабета, во всяком случае, макроваскулярных (4). Тем не менее, именно исходя из подобных показателей (изменение гликемического контроля, липидного профиля сыворотки, уровня антиоксидантов и др.) проистекали выводы об эффективности, безопасности применения росиглитазона и благоприятном его влиянии на сердечно-сосудистые исходы. В этой связи данные мета-анализа «Влияние росиглитазона на риск развития инфаркта миокарда и смерти от сердечно-сосудистых причин», представленные Nissen и Wolski в мае 2007 г (5), всколыхнули медицинскую общественность и вызвали подъем научного интереса к рассматриваемой проблеме.
В своей работе Nissen и Wolski (5) проанализировали 42 исследования, соответствовавших следующим критериям включения – продолжительность более 24 недель, наличие контрольной группы лиц, не получавших росиглитазон, и, регистрация за время испытания, по крайней мере, одного инфаркта миокарда или смерти от сердечно-сосудистых причин.
В мета-анализ вошли и такие крупные исследования, как ADOPT и DREAM. Все пациенты, принимавшие росиглитазон, были объединены в одну группу, контрольная же группа была представлена больными, получавшими любой другой сахароснижающий препарат (метформин, препарат сульфонилмочевины, инсулин) или плацебо. Средний возраст пациентов обеих групп был менее 57 лет, по численности умеренно преобладали мужчины, исходный уровень гликированного гемоглобина составлял около 8,2%. Поскольку количество кардиоваскулярных событий, зарегистрированных во многих исследованиях, было крайне небольшим, относительный риск и 95% доверительный интервал оценивался путем применения метода Пето. Данные мета-анализа показали, что применение росиглитазона ассоциируется с достоверным увеличением риска развития инфаркта миокарда (коэффициент вероятности – 1,43; 95% доверительный интервал – 1,03-1,98; Р=0,03) и риска смерти от сердечно-сосудистых причин (коэффициент вероятности 1,64; 95% доверительный интервал 0,98-2,74), не достигшего, однако, уровня статистической значимости (P=0,06). Сопоставление полученных коэффициентов вероятности с плацебо подтверждает, что выявленное повышение риска на фоне приема росиглитазона не является следствием протективных эффектов активных препаратов из группы сравнения. Механизм, лежащий в основе увеличения частоты развития инфаркта миокарда и смерти от кардиоваскулярных причин, остается неясным. Возможной причиной этого может служить тот факт, что тиазолидиндионы учащают и ускоряют развитие застойной сердечной недостаточности, обусловленной задержкой жидкости и увеличением ОЦК. Вероятно, перегрузка объемом левого желудочка повышает потребность миокарда в кислороде, что у предрасположенных лиц может провоцировать ишемию (5). Однако все вышеперечисленное является лишь логическим предположением, поскольку знание механизма действия лекарственного препарата отнюдь не позволяет составить представление обо всех его благоприятных и неблагоприятных эффектах и напротив.
Отдельного внимания заслуживают исследования, оценивающие роль тиазолидиндионов в развитии и прогрессировании сердечной недостаточности.
Ретроспективное когортное исследование, представленное Thomas E. Delea, John S. Edelsberg, May Hagiwara at al. (6), сообщает о том, что применение тиазолидиндионов ассоциируется с 60%-ным относительным увеличением риска развития новых случаев сердечной недостаточности (уровень риска – 1,76; доверительный интервал – 1,43-2,18; Р<0,001) по сравнению с использованием других сахароснижающих препаратов, особенно у пациентов пожилого возраста, с отягощенным анамнезом по осложнениям сахарного диабета, кардиоваскулярной патологии (артериальная гипертензия, ОНМК, транзиторные ишемические атаки и др.), принимающих ингибиторы АПФ, β-адреноблокаторы. Однако исследователи акцентируют внимание на том, что результатов одного ретроспективного исследования недостаточно для установления точной причинно-следственной связи, но, полученные данные свидетельствуют о необходимости осторожно использовать тиазолидиндионы у пациентов с сердечно-сосудистой патологией, сердечной недостаточностью и быть предельно внимательными к малейшим начальным проявлениям недостаточности кровообращения на фоне терапии препаратами данной группы.
Сходные данные были получены в проспективном, наблюдательном, когортном исследовании Karter and al. (8), изучавшем частоту впервые развившейся сердечной недостаточности на фоне терапии пиоглитазоном у пациентов с сахарным диабетом 2 типа, не получавших до этого момента никаких сахароснижающих препаратов. По результатам исследования у 74 (0,2%) из 24973 пациентов без предшествующих проявлений сердечной недостаточности, принимавших пиоглитазон, был зарегистрирован первый подобный эпизод, а у 69 (3,5%) из 1964 больных с отягощенным анамнезом по указанному патологическому состоянию на фоне пиоглитазона оно развилось повторно. По сравнению с контрольной группой, уровень риска составил 1,8.
Обращаясь ко второму препарату из группы тиазолидиндионов – пиоглитазону, приведем результаты недавно завершенного крупного многоцентрового двойного слепого рандомизированного плацебо-контролированного исследования PROactive (11). В исследовании приняли участие 5238 пациентов с сахарным диабетом 2 типа и сердечно-сосудистым заболеваниями, получавшие пиоглитазон или плацебо в дополнение к своей исходной сахароснижающей терапии. Пациенты, перенесшие в анамнезе инфаркт миокарда (n=2445), были дополнительно объединены в подгруппу, для которой исследователи предварительно задали и определили несколько составных конечных точек. По результатам исследования не зарегистрирована достоверная разница в скорости развития кардиоваскулярных событий или смерти (первичные конечные точки) между двумя группами, однако при анализе дополнительных точек в обозначенной подгруппе выявлено достоверное снижение риска повторного инфаркта миокарда (5,3% в сравнении с 7,2%; р = 0,0453) и в целом острого коронарного синдрома (уровень риска 0,63; р=0,035) среди пациентов, получавших терапию пиоглитазоном. И хотя в упоминавшейся подгруппе достоверно чаще регистрировалось развитие сердечной недостаточности на фоне лечения пиоглитазоном (13,5% в сравнении с 9,6%; р=0,003), увеличение смертности по причине возникшей недостаточности кровообращения при этом не обладало достаточным уровнем доказательности (1,4% по сравнению с 0,9%; р=0,283). Полученные результаты в целом выглядят довольно обнадеживающе, пока не возникает вопрос: «Насколько необходимо клиницисту, планируя коррекцию сахароснижающей терапии у пациента с сахарным диабетом 2 типа и перенесенным инфарктом миокарда, а, вероятно, и другими сопутствующими кардиологическими проблемами, назначать препарат, не имеющий преимуществ по антигипергликемическому действию и достоверно увеличивающий риск развития, пусть и нефатальной, но недостаточности кровообращения, при наличии более безопасных альтернатив?». Вместе с этим, по данным литературных источников и материалам клинических исследований препарат демонстрирует способность отдалять развитие сахарного диабета и замедлять его прогрессирование до формирования сердечно-сосудистых осложнений (18, 19.) благодаря уменьшению инсулинорезистентности, снижению секреции инсулина, протекции β-клеток поджелудочной железы, благотворному влиянию на липидный обмен – повышение ЛПВП-ХС, снижение триглицеридов, индекса атерогенности (20).
Имеющиеся эффекты препаратов из группы глитазонов позволяют с оптимизмом смотреть на возможное их использования за рамками СД 2 типа. Так в 2006 г опубликованы результаты плацебо-контролируемого исследования применения пиоглитазона у пациентов с неалкогольным стеатогепатозом. На фоне терапии и соблюдения диеты в сравнении с режимом «плацебо+диета» отмечено достоверное улучшение гликемического контроля (р<0,001), нормализация уровней печеночных трансаминаз – АСТ (на 40% в сравнении с 21%; р = 0,04), АЛТ (на 58% в сравнении с 34%; р < 0,001), уменьшение жировых отложений в печени (на 54% в сравнении с 0%; р < 0,001), а также повышение чувствительности ткани печени к инсулину (на 54% в сравнении с 14%) (21).
Интересными, на наш взгляд, представляются попытки применения глитазонов в неврологии. В настоящее время имеются немногочисленные данные об эффективном их использовании для лечения болезни Альцгеймера (22). В рамках небольшого когортного исследования (23) проводилось изучение влияния приема пиоглитазона 30-60 мгв сутки в течение 3-4 месяцев на ряд поведенческих категорий у 25 детей (средний возраст 7,9 +/- 0,7 лет), страдающих аутизмом. По итогам работы побочных эффектов действия препарата отмечено не было, кроме того, зарегистрировано значительное улучшение по четырем из пяти изучавшихся поведенческих категорий – раздражительность, гиперактивность, стереотипия и летаргия. Полученный результат дает хороший потенциал для дальнейших клинических и научных разработок в этой области.
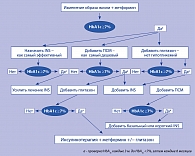
Подводя итог изложенному материалу, хочется расставить основные акценты. Тиазолидиндионы – «принципиально новая, перспективная, высокоэффективная группа сахароснижающих препаратов», как говорили о ней с момента ее появления на мировом фармацевтическом рынке в 1999 г. Постепенно появлялась и накапливалась новая информация относительно эффективности и безопасности данных лекарственных средств. Несомненным является доказанный антигипергликемический эффект данных препаратов и прямое влияние на снижение инсулинорезистентности, принципиальным участником патогенеза СД 2 типа. Эти особенности группы позволили включить глитазоны в качестве препаратов второй линии в лечении СД 2 типа в совместный консенсус (рисунок 1) Американской Диабетической Ассоциации (АDА) и Европейской ассоциации по изучению диабета (EASD) в 2006 году (23). Однако результаты проведенных многочисленных клинических исследований и мета-анализов в настоящее время заставляют иначе взглянуть на препараты рассматриваемой группы в определенных ситуациях. В частности, в группах с высоким риском развития ИМ или сердечной недостаточности, у лиц с выраженной остеопенией, данные препараты следует применять с осторожностью.
В то же время, изучение использования глитазонов в других областях медицины с учетом уже установленных благоприятных воздействий на организм, может дать новую жизнь данному классу, возможно, в совершенно ином качестве.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.