Вирусные генитальные инфекции: новые подходы к лечению
- Аннотация
- Статья
- Ссылки






Терапия ВПЧ-ассоциированных заболеваний: анализ клинициста
Тактика лечения клинической и субклинической форм папилломавирусной инфекции определяется прежде всего исходя из состояния иммунитета пациента. Имеют значение наличие сопутствующей соматической болезни, урогенитальная патология; локализация и характер патологического процесса на шейке матки, на вульве или влагалище; наличие рецидивов.
Принципы комплексного лечения как клинической, так и субклинической форм ВПЧ-инфекции заключаются, в первую очередь, в деструкции кондилом; стимуляции противовирусного иммунитета; устранении факторов риска, которые способствуют рецидивам заболевания.
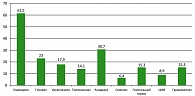
На практике мы начинаем именно с устранения факторов, которые способствуют рецидивам заболевания. Следует обратить внимание на то, что очень часто в 67-93% случаев папилломавирусная инфекция сочетается с другими урогенитальными инфекциями (рисунок 1). И поэтому при наличии сопутствующей инфекции обязательно следует провести противовоспалительное лечение.
Прежде чем применять хирургические методы лечения, как показывает практика, следует провести противовирусную терапию – об этом говорят результаты исследований: иммунограмма у больных с ВПЧ-инфекцией снижена.
Существующие хирургические методы лечения: электро-, крио-, лазерное, хирургическое иссечение, аргоноплазменная коагуляция. Нет исследований, которые показали бы преимущество того или иного хирургического метода. Результаты исследований говорят о правильной тактике использования комбинированного лечения (медикаментозного + хирургического), это повышает эффективность лечения.
Все противовирусные средства по происхождению можно разделить на синтетические и на средства природного происхождения, к последним и относится Панавир.
Препарат состоит из очищенного экстракта побегов растения Solanum tuberosum. Субстанцию препарата Панавир составляют растительные полисахариды, относящиеся к классу высокомолекулярных гексозных гликозидов сложного строения и состоящие из глюкозы, рамнозы, арабинозы, маннозы, ксилозы, галактозы и уроновых кислот. Полисахариды Панавира воздействуют на Т-лимфоциты, то есть на их количественную и функциональную активность. Кроме того, они повышают продукцию интерферона, повышают активность макрофагов и снижают проницаемость мембран для вирусов и бактерий.
Было проведено много как экспериментальных, так и клинических исследований институтами вирусологии, фармакологии, физико-химической медицины и была показана эффективность и безопасность препарата Панавир.
Было доказано, что препарат обладает цитопротективным действием, то есть защищает клетку от воздействия вирусов. Кроме того, Панавир способен тормозить репликацию вируса в инфицированных культурах клеток и приводить к существенному снижению инфекционной активности вирусов. Он также индуцирует синтез интерферона в организме.
Схематически механизм действия Панавира можно представить так: происходит препятствие адгезии; ингибиция пенетрации; препятствие раскрытию вирусного капсида; нарушение репликации вирусной ДНК (синтетические нуклеозиды); нарушение сборки вирусных частиц.
Руководствуясь инструкцией, в гинекологии Панавир применяют при следующих вирусных инфекциях: генитальный герпес, цитомегаловирус, аногенитальные папилломы.
Методика комплексного лечения остроконечных кондилом: начинают с лечения сопутствующих бактериальных инфекций, которое проводится до назначения Панавира, в соответствии с существующими стандартами без использования иммунотропных препаратов. Далее проводится деструкция остроконечных кондилом на фоне системного и местного применения Панавира. До деструкции назначают один раз в день наружно гель Панавир и после деструкции дважды в день утром и вечером. Системная терапия по схеме: 0,004% раствор Панавир внутривенно 5,0 мл – 3 инъекции с интервалом 48 часов, две последующие с интервалом 72 часа, курс – 5 инъекций.
Лечение поражений шейки матки (плоская кондилома, CINI): 0,004% раствор Панавир внутривенно 5,0 мл: 3 инъекции с интервалом 48 часов, две последующие с интервалом 72 часа, курс – 5 инъекций, или Панавир ректальные свечи через день вводят на ночь, курс 10 суппозиториев, в качестве метода деструкции кондилом рекомендуется радиоволновая хирургия.
Лечение эндоуретральных кондилом: Панавир системно № 5-6 раствор внутривенно или суппозитории Панавир на курс – 10; эндоуретральное облучение низкоинтенсивными лазером № 10-15.
Результаты исследований показали высокую эффективность препарата Панавир: отсутствие рецидивов через 6-12 месяцев наблюдения у большинства больных (93%), а эффективность определяется только отсутствием рецидивов.
Была отмечена хорошая переносимость препарата и отсутствие побочных эффектов и осложнений. Кроме того, препарат применялся у беременных женщин после получения их согласия и после оценки состояния беременной и характера патологического процесса, у женщин с остроконечными кондиломами, с вирусоносительством ВПЧ, включая 16 и 18 тип, и с субклиническими формами папилломавирусной инфекции. Результаты исследований: отсутствие ВПЧ по результатам ПЦР-диагностики после внутривенного введения раствора Панавира – 97%, после ректальных свечей Панавир – 93%. Таким образом, на основании этого можно сказать, что препарат Панавир высокоэффективен при бессимптомном носительстве ВПЧ (частота элиминации ВПЧ – 93-97%). Препарат является эффективным средством в лечении клинически выраженной формы папилломавирусной инфекции. Панавир позволяет добиваться стойкой ремиссии папилломавирусной инфекции на протяжении беременности.
Конечно, этих исследований еще не достаточно и проводятся новые клинические исследования. Но, тем не менее, 10-летняя практика показывает, что препарат Панавир обладает высокой эффективностью лечения.
Диагностика и лечение генитального герпеса
Герпесвирусная инфекция занимает одно из ведущих мест по распространенности среди заболеваний, передающихся половым путем. Заболевания, вызванные вирусом простого герпеса (ВПГ), занимают второе место после гриппа в качестве причин смерти от вирусных инфекций (не считая СПИДа). Генитальный герпес поражает все популяционные группы, 98% взрослого населения во всем мире имеют антитела к ВПГ I или II типа.
Инкубационный период составляет от 3 до 12 дней. Инфицирование возможно от партнера, являющегося источником инфекции и имеющего типичные герпетические высыпания на половых органах. И также от партнера, выделяющего вирус при отсутствии клинических симптомов, то есть при атипичной форме или при бессимптомном вирусоносительстве. Основные пути передачи – это контактный, воздушно-капельный, половой. Существует также риск передачи инфекции при переливании крови и при трансплантации органов.
Клинические формы генитального герпеса – это первичный генитальный герпес и рецидивирующий генитальный герпес, который может протекать типично, атипично и бессимптомно. До 60% случаев рецидивирующий генитальный герпес протекает атипично, и именно эти формы являются наиболее опасными.
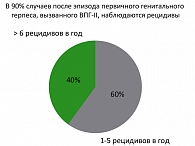
В 90% случаев после эпизода первичного генитального герпеса, вызванного ВПГ II типа, наблюдаются рецидивы. Причем в 60% случаев наблюдается от 1 до 5 рецидивов в год. Более 6 рецидивов наблюдаются у 40% пациентов (рисунок 2).
Большое значение для диагностики имеет правильный забор материала. Материалом для исследования являются содержимое везикул, соскоб со дна эрозий, слизистой оболочки уретры, влагалища, цервикального канала, пробы крови. Для диагностики генитального герпеса используются вирусологические методы обнаружения и идентификации ВПГ; молекулярно-биологические методы (ПЦР, дот-гибридизация); цитоморфологический метод (выявление внутриклеточных включений); иммунологические (выявление антигенов ВПГ: реакции прямой и непрямой иммунофлуоресценции, иммуноферментный анализ), выявление антител иммуноглобулинов M и G в сыворотке крови методом ИФА. IgG можно определить на 21-28 день после заражения. IgM определяется на 9-10 сутки с момента заражения в течение 7-14 дней. И только определение типоспецифических антител к гликопротеину G обеспечивает адекватную точную диагностику.
Дифференциальную диагностику проводят с сифилисом, красным плоским лишаем, болезнью Бехчета, редицивирующим кандидозом, болезнью Крона, чесоткой, пузырчаткой, стрептококковым импетиго.
Каковы основные подходы к терапии генитального герпеса? В первую очередь, это противовирусная химиотерапия. Также могут быть использованы иммуномодулирующая терапия или комбинация этих методов. Длительность, интенсивность и требуемый объем лечения генитального герпеса определяется тяжестью клинического течения, частотой рецидивов, состоянием иммунной системы, психо-эмоциональными последствиями, наличием риска передачи инфекции половому партнеру или новорожденному.
Для лечения первого эпизода генитального герпеса используются препараты Ацикловир, Фамцикловир и Валацикловир. Цель терапии заключается, в первую очередь, в уменьшении тяжести и длительности эпизода герпетической инфекции.
Для рецидивирующего генитального герпеса существует два варианта терапии: эпизодическая и супрессивная. Эпизодическая терапия используется для снижения тяжести и продолжительности текущего рецидива. Супрессивную терапию мы можем использовать для снижения частоты последующих рецидивов и предотвращения передачи вируса партнеру.
Однако существует проблема увеличения случаев резистентности к синтетическим нуклеозидам при длительной терапии и токсическое воздействие препаратов. На этом основании в практике врачей появляются новые схемы лечения с применением противовирусных препаратов растительного происхождения.
Мне бы хотелось представить российский противовирусный препарат растительного происхождения Панавир, который отличается своей химической структурой и механизмом действия. Особенностями противовирусного действия препарата Панавир является то, что препарат обладает цитопротективным действием; ингибирует синтез вирусных белков, тормозит репликацию вирусов в инфицированных культурах клеток и приводит к существенному снижению инфекционной активности вирусов; модулирует уровень интерферона γ и α; повышает жизнеспособность инфицированных клеток.
Безопасность Панавира была доказана в многочисленных доклинических и клинических исследованиях. Было показано отсутствие мутагенного, тератогенного, канцерогенного, аллергизирующего и эмбриотоксического действия.
В период рецидива заболевания применяются 2 внутривенные инъекции 0,004% раствора Панавир по 5,0 мл с интервалом 48 ч. Еще одна форма терапии, которая может быть использована при генитальном герпесе – суппозитории ректальные. Схема применения: по 1 суппозиторию Панавир на ночь на курс 5-10 свечей. В качестве местной терапии гель Панавир – наружно 3-4 раза в сутки. Курс при необходимости можно повторить через месяц.
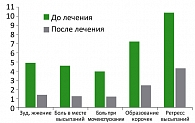
Данные о клинической эффективности препарата Панавир при рецидивирующей герпетической инфекции таковы (при лечении 0,004% раствором Панавира по 5,0 мл на курс 2 или 5 инъекций по схеме): значительное улучшение и сокращение длительности рецидива и/или увеличение длительности ремиссии более чем в 2 раза отметили 20% пациентов; улучшение и сокращение длительности рецидива и/или увеличение длительности ремиссии менее чем в 2 раза отметили 62% пациентов; отсутствие эффекта отметили 18%. Таким образом, клиническая эффективность препарата составила 82%. Также было показано, что при применении препарата уже на второй день произошло значительное уменьшение таких явлений, как зуд, жжение, боль в месте высыпаний, боль при мочеиспускании и т.д. (рисунок 3).
Постмаркетинговое исследование эффективности, безопасности и переносимости Панавира при лечении генитального герпеса и его влияние на показания ИНФ-статуса (при лечении 0,004% раствором Панавира по 5,0 мл – от 2 до 5 инъекций) показало, что ремиссия 6 и более месяцев отмечалась у 58,1% пациентов. Увеличение межрецидивного промежутка в 2 раза произошло у 27,1% пациентов. И у 14,8% изменений не произошло. Также 59,5% пациентов отмечали значительное улучшение; улучшение – 21,6%; отсутствие эффекта – 18,9%.
Было проведено еще исследование по эффективности препарата Панавир ректальные суппозитории у пациентов с рецидивирующим генитальным герпесом. Использование ректальных суппозиториев Панавир на курс 10 суппозиториев в период продромальных явлений у пациентов с генитальным герпесом способствовало абортированию рецидива у 60% больных. Сокращалась длительность рецидива герпеса у 90% больных. При наблюдении за больными в течение 3 месяцев после лечения ремиссия отмечалась у 29 из 30 человек. Ни в одном случае в процессе применения не зарегистрировано нежелательных побочных явлений или аллергических реакций.
Высокая клиническая эффективность и безопасность, хорошая переносимость и комфортность использования суппозиториев Панавир, отмеченные у абсолютного числа пролеченных пациентов, позволяет рекомендовать эти суппозитории к широкому применению в терапии рецидивирующего генитального герпеса.
Возможности лечения и профилактики цитомегаловирусной инфекции
Цитомегаловирус (ЦМВ) – крупных размеров вирус, условно-патогенный микроорганизм семейства герпесвирусов. Это очень широко распространенная инфекция. Ее распространенность у детей первого года жизни уже достигает 20%. В детских садах в процессе оборота инфекций до 60-80% детей инфицируются ЦМВ или имеют антитела к нему. А увзрослых к 50-60 годам эта цифра достигает 90-95%. Женщины детородного возрастав 60%, а по некоторым данным в 80% случаев являются носителями ЦМВ.
Источником цитомегаловирусной инфекции являемся мы с вами. Кроме вирусоносителей, источником инфекции является больной острой формой ЦМВ и больной в период обострения инфекции. Пути передачи вируса – все, какие существуют на свете: воздушно-капельный, половой, контактный, пероральный, парентеральный, энтеральный, вертикальный. Инфекция передается через все биологические жидкости и выделения организма.
Как протекает инфекция у иммунокомпетентных лиц? После первичного инфицирования вирус находится в организме пожизненно. Вирус надежно защищен лимфоцитами от воздействия антител и интерферона. Инфекция протекает бессимптомно в виде вирусоносительства. Клинически выраженное заболевание развивается при активации латентной инфекции на фоне снижения резистентности организма (детский возраст, беременность, воздействие неблагоприятных экологических факторов, ятрогенные вмешательства, прием цитостатиков и иммунодепрессантов, химиотерапия).
Клиническая картина неспецифична и протекает цитомегаловирусная инфекциякак гриппоподобная инфекция. Дело в том, что клиническое проявление цитомегаловирусной инфекции протекает как гриппоподобная инфекция. Период первичного инфицирования длится 2-3 недели. При достаточном иммунном ответе происходит самоизлечение – это те самые 90-95% взрослого населения, о которых я говорила. Если у человека нет иммунного ответа, инфекция переходит в генерализованную форму. Проявляется ЦМВИ воспалением околоушных и подчелюстных слюнных желез, печеночной ткани, надпочечников, селезенки, суставов и др. Если иммунный ответ недостаточный, вирус переходит в локализованную форму. Проявляется в виде цервицита, эндометрита, сальпингоофорита, поражения околоушных и подчелюстных слюнных желез. У мужчин протекает бессимптомно или в виде вялотекущего уретрита.
Одним из средств для этиотропного лечения цитомегаловирусной инфекции является отечественный противовирусный препарат Панавир. Обладает выраженным противовирусным, вирусостатическим, иммуномодулирующим действием, активен в отношении многих ДНК- и РНК-содержащих вирусов, в частности ЦМВ. Препарат Панавир выпускается для внутривенного введения – в ампулах, для введения ректально в виде суппозиториев и для наружного применения в виде геля. Препарат вводится внутривенно 3 раза в течение первой недели лечения с интервалом 48 или 72 часа через 2 дня. И 2 раза в течение второй недели с интервалом в 72 часа. То есть на 1-й, 3-й, 5-й, 7-й, 11-й дни лечения. Через 3 месяца после проведенного лечения Панавиром в группе из 30 женщин с экзо-эндоцервицитами на фоне зоны трансформации контрольное обследование показало: отсутствие патологии шейки матки, ПЦР на ЦMB не выявило ни у одной пациентки наличия инфекции. Полученные результаты свидетельствуют об отсутствии характерной клинической картины для ЦМВ. Таким образом, положительные результаты применения препарата Панавир свидетельствуют о возможности его использования в целях подготовки женщин с ЦМВ к беременности.
Комплекс профилактических мероприятий показан женщинам высокой группы риска – с отрицательными результатами обследования на иммуноглобулины G и M к ЦМВ. Нужно соблюдать правила личной гигиены, что позволяет снизить вероятность заболевания во время беременности. Необходимо мыть руки, особенно после посещения улицы и общественного транспорта; избегать поцелуев в губы, особенно с детьми младше 5 лет (они, как правило, в этом возрасте впервые болеют ЦМВИ и являются самыми частыми распространителями острой инфекции); пользоваться отдельной косметикой, особенно губной помадой.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.