Сателлитный симпозиум компании HiРР «Вскармливание детей первого года жизни. Новые возможности» состоялся 25 февраля 2012 г. в рамках ХVI Конгресса педиатров с международным участием. Профессор Т.Н. СОРВАЧЕВА (Москва) рассказала об истории применения пробиотиков и пребиотиков, а также о молочных смесях нового поколения, содержащих в своем составе как пре-, так и пробиотики. Она отметила появление на российском рынке новой перспективной синбиотической молочной смеси для детского питания HiРР Combiotic, включающей пробиотик Lactobacillus fermentum hereditum и пребиотик галактоолигосахарид.
Доктор Э. ЛОПЕС (Гранада, Испания) рассказал о результатах новаторских исследований испанских ученых, которые доказали наличие в грудном молоке многих видов и штаммов бактерий и изучили свойства этих бактерий в опытах in vitro и на животных. Отобранный в результате лабораторных исследований штамм Lactobacillus fermentum hereditum включен в состав синбиотической смеси, которая в ходе клинических исследований существенно снижала заболеваемость гастроинтестинальными инфекциями у младенцев 1–6 месяцев и гастроинтестинальными и респираторными инфекциями у детей 6–12 месяцев.

Профессор Т.Н. Сорвачева
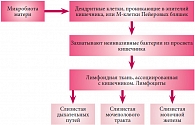
Рис. 1. Предполагаемый путь проникновения лактобактерий в грудное молоко

Доктор Эдуардо Лопес
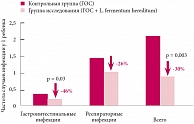
Рис. 2. Снижение заболеваемости у детей 6–12 месяцев на фоне применения молочной смеси с пребиотиком (ГОС) и пробиотиком (L. fermentum hereditum)
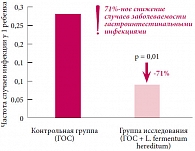
Рис. 3. Снижение частоты гастроинтестинальных инфекций у младенцев до 6 месяцев на фоне кормления молочной смесью с пребиотиком (ГОС) и пробиотиком (L. fermentum hereditum)
Пробиотики. Что нового?
В начале своего выступления профессор кафедры питания детей и подростков РМАПО, д.м.н. Т.Н. СОРВАЧЕВА напомнила аудитории, что использование кисломолочных смесей в питании младенцев является давней отечественной традицией. Татьяна Николаевна перечислила этапы истории применения смесей в нашей стране: сначала использовали неадаптированные смеси, затем перешли на адаптированные. Смеси, содержащие ацидофильную палочку, имели высокую кислотность и осмолярность, поэтому использовали сочетание пресных и кисломолочных смесей в соотношении 50:50. Кисломолочные смеси не применялись для вскармливания детей в неонатальном периоде. На смену смесям с ацидофильной палочкой пришли продукты, содержащие бифидобактерии. Однако технологические возможности того времени не обеспечивали адекватную сохранность бифидобактерий в смесях. Эффективность кисломолочных смесей в исследованиях 1970–80-х гг. оценивали по следующим показателям:
- переносимость;
- динамика массо-ростовых показателей у младенцев;
- влияние на микробиоценоз кишечника;
- уровень заболеваемости у детей.
Еще полвека назад было показано, что применение кисломолочных смесей приводит к снижению роста условно-патогенной флоры и стимулирует рост комменсалов; предпринимались попытки использовать кисломолочные смеси как иммуностимулирующее средство.
«Сегодня наступила эра про- и пребиотиков, – так охарактеризовала современный этап развития смесей для искусственного вскармливания профессор Т.Н. Сорвачева и дала определение пробиотиков: – Это живые микроорганизмы (или содержащие их продукты), которые являются нормальным компонентом микрофлоры». Первыми микроорганизмами, которые использовались в России в качестве пробиотиков, были бифидобактерии. Вначале изучались отдельные виды бифидобактерий, затем в кисломолочные смеси стали включать бифидобактерии с доказанными свойствами. Далее настал черед детального исследования состояния микробиоты при естественном и искусственном вскармливании у детей 1-го года жизни, что позволило дифференцированно применять пробиотики в зависимости от изменения состояния микробиоты.
Основным источником бактерий для новорожденного является вагинальная, кишечная и кожная микрофлора матери, а также окружающая среда. Имеет значение и способ родоразрешения: при кесаревом сечении выше уровень колонизации Escherichia coli, Klebsiella, Staphylococcus aureus. Грудное молоко – важнейший фактор становления нормальной здоровой микрофлоры. Для него характерно низкое содержание белка и альфа-лактоальбумина, белок не достигает толстой кишки, благодаря чему снижается концентрация протеолитических бактерий. Другими особенностями грудного молока являются низкое содержание фосфора (160 мг/л по сравнению с 290–350 мг/л в смесях) и более низкий pH, что способствует росту бифидобактерий и ослабляет рост условно-патогенной микрофлоры.
В последнее время активно изучалось влияние пробиотиков на состояние микробиоты, иммунные функции, формирование пищевой толерантности, профилактику аллергии, экспрессию генов. Изменились методы оценки состояния микробиоты: стали применять ПЦР-анализ, флуоресцентную гибридизацию и др. Меняется определение пробиотиков, теперь их определяют как «живые организмы, которые, попадая в ЖКТ в адекватном количестве, оказывают благоприятное влияние на здоровье человека». В 2001–2002 гг. пробиотики были официально разрешены для использования в продуктах детского питания. Проведенные в последнее десятилетие исследования продемонстрировали положительное влияние молочных смесей с пробиотическими культурами на рост ребенка, снижение частоты гастроинтестинальных нарушений, снижение частоты колик. Правда, не во всех исследованиях эффекты пробиотиков оказались статистически значимыми, что, по мнению профессора Т.Н. Сорвачевой, объясняется использованием в исследованиях разных штаммов одного вида, свойства которых могут заметно отличаться.
Следующим этапом в истории применения смесей для искусственного вскармливания стало появление молочных смесей, содержащих пребиотики – пищевые ингредиенты, необходимые для стимуляции роста и жизнедеятельности полезной микрофлоры в кишечнике. «В нашей стране, как и во всем мире, развернулась борьба между сторонниками пробиотиков и пребиотиков. Апологеты пребиотиков обвиняли оппонентов в том, что пробиотические бактерии вызывают антигенную стимуляцию иммунной системы. Сторонники пробиотиков парировали: пребиотики оказывают влияние только на pH, характер стула, и функции их не столь значимы, как у пробиотических культур», – комментирует докладчик.
Пребиотическими свойствами обладает грудное молоко. Входящая в его состав бета-лактоза, достигая толстой кишки, создает там питательную среду для бифидо- и лактобактерий, что способствует подавлению патогенных и условно-патогенных микроорганизмов. В грудном молоке содержится в общей сложности около 900 различных олигосахаридов, из которых изучены только 200. Содержание олигосахаридов составляет 20–30 г/л в молозиве и 12–15 г/л в зрелом молоке. Все эти вещества не расщепляются, не всасываются в тонкой кишке, достигают толстой кишки, где происходит их ферментация представителями интестинальной микрофлоры. Следствием является, с одной стороны, избирательная стимуляция комменсалов, а с другой стороны, благодаря сродству некоторых олигосахаридов с рецепторами клеточной стенки осуществляется связывание патогенных микроорганизмов и их токсинов и профилактика диарейных заболеваний. Олигосахариды грудного молока также воздействуют на пролиферацию и созревание эпителия кишечника у младенца. Установлено их влияние на выработку цитокинов и формирование нервной системы.
Научно доказаны пребиотические свойства двух групп химических веществ. Одну из них составляют фруктаны – инулин, олигофруктоза, длинноцепочечные и короткоцепочечные фруктоолигосахариды (ФОС). Вторая группа – это галактоолигосахариды (ГОС). Практически в различных молочных смесях используют ГОС, ФОС или обе группы вместе. В ряде работ показано положительное влияние молочных смесей с пребиотиками на состояние здоровья, пищеварение, а также на pH, консистенцию и кратность стула, частоту колик, снижение риска аллергии, частоты респираторных и кишечных инфекций. Многие авторы отмечают достоверное положительное влияние включения пребиотиков в молочные смеси на рост ребенка. Тем не менее, по оценке профессора Т.Н. Сорвачевой, эффективность пребиотиков доказана меньшим числом исследований, чем эффективность пробиотиков. Часто эффекты пребиотиков оказываются статистически незначимыми. В целом накопленный опыт включения в смеси пре- и пробиотиков доказывает их безопасность и наличие нескольких положительных эффектов – снижение риска неспецифических инфекций ЖКТ, частоты применения антибиотиков, частоты колик и явлений раздражения кишки.
Новым этапом стало использование так называемых синбиотиков, то есть молочных смесей, содержащих как пре-, так и пробиотики. Предпосылкой для этого явился отказ от прежнего представления о стерильности грудного молока. Выяснилось, что грудное молоко содержит бифидо- и лактобактерии, клостридии, стрептококки, бактероиды в количестве около 1000 КОЕ/мл. Таким образом, за сутки грудной ребенок получает вместе с материнским молоком около 100 000 КОЕ. Профессор Т.Н. Сорвачева напомнила, что еще в 1970-е гг. русский ученый из Алма-Аты Федотов доказывал, что грудное молоко – это кисломолочный продукт. В то время его слова вызывали у многих коллег насмешку, но в начале XXI века с помощью новейших научных методов правильность этой гипотезы подтвердилась. Первыми из грудного молока были выделены молочнокислые бактерии, в частности, Lactobacillus gasseri, L. fermentum, L. rhamnosum, L. lactis, L. salivarius, L. reuteri. Существует ряд доказательств эндогенного пути поступления бактерий в грудное молоко. Штаммы, выделенные из молока, отличались по своим генотипическим свойствам от штаммов, полученных с кожи молочной железы. При этом установлена тождественность штаммов лактобацилл из грудного молока и из кала ребенка, получающего это молоко.
Как подчеркнула Татьяна Николаевна Сорвачева, путь проникновения бактерий в грудное молоко еще не до конца изучен, споры среди ученых по этому вопросу продолжаются. Однако основная схема определена. Согласно ей, отростки дендритных клеток, проникая в слизистую, захватывают неинвазивные бактерии из просвета кишечника, но могут, при определенных условиях, захватывать и инвазивные бактерии. В дальнейшем с током лимфы или крови бактерии попадают в слизистую молочной железы (рис. 1). Анализу на потенциальные пробиотические свойства подвергли штаммы лактобактерий грудного молока L. gasseri CECT 3714 и L. fermentum hereditum CECT 5716. Штамм L. fermentum hereditum CECT 5716 выбран для практического использования благодаря таким свойствам, как высокая выживаемость, подавление роста патогенных бактерий, положительное влияние на врожденный и адаптивный иммунитет, а также потенциальная безопасность, и техническим характеристикам, позволяющим использовать его в промышленном производстве. Этот штамм не передает устойчивость к антибиотикам, не имеет аллергенных свойств, высокая доза хорошо переносится. Итогом проведенных исследований стала разработка смеси HiPP Combiotic®, включающей L. fermentum hereditum и галактоолигосахарид в дозировке 0,3–0,4 г/100 мл. «Смесь HiPP Combiotic® уже появилась на отечественном рынке и может быть оценена российскими педиатрами. Безусловно, применение полученной из грудного молока Lactobacillus fermentum hereditum, которая отвечает всем требованиям безопасности, может рассматриваться как новый шаг в достижении эффекта естественного вскармливания», – сказала в заключение своего доклада профессор Т.Н. Сорвачева и напомнила слова, произнесенные в 1909 г. Л. Келлером: «Чтобы максимально улучшить искусственное вскармливание, замените его на естественное».
Симпозиум компании HiРР «Вскармливание детей первого года жизни. Новые возможности»
В первые шесть месяцев жизни ребенка лучшим способом питания является грудное вскармливание, так как доказано, что оно снижает частоту инфекционных заболеваний. «Установлено, – заявил в начале своего выступления гость из Испании доктор Эдуардо ЛОПЕС (Испанский высший совет по научным исследованиям, Министерство науки и инноваций Испании), – сегодня в мире менее 40% младенцев до 6 месяцев находятся на исключительно грудном вскармливании». Не случайно Всемирная организация здравоохранения (ВОЗ) считает грудное вскармливание лучшим способом питания для младенцев. В возрасте до 6 месяцев ВОЗ рекомендует исключительно грудное вскармливание, а от 6 месяцев до 2 лет – продолжение кормления грудью наряду с соответствующим дополнительным питанием. Итак, грудное молоко – это «золотой стандарт» питания ребенка, однако грудное вскармливание не всегда возможно, поэтому чрезвычайно широко распространены различные молочные смеси. В этой связи актуален вопрос их совершенствования, то есть максимального приближения к составу и свойствам грудного молока. «У получающих материнское молоко грудных детей гораздо меньше патогенных штаммов по сравнению с теми, кто получает смеси, – отметил доктор Э. Лопес. – Удивительно, но после многолетних и многочисленных исследований мы до сих пор не имеем точной формулы грудного молока». Лишь сравнительно недавно был сделан шаг к разгадке тайны грудного молока. Новаторская статья группы испанских ученых показала, что грудное молоко служит источником молочнокислых бактерий (лактобактерий) для организма новорожденного1. Позже на эту тему появилось еще порядка 30 публикаций.
К настоящему времени исследования в ряде европейских стран – Испании, Финляндии, Франции – доказали, что в материнском молоке содержатся молочнокислые бактерии Lactobacillus и Bifidobacterium. Обследование здоровых матерей и новорожденных позволило установить наличие в грудном молоке до 30 различных видов бактерий, включая 7 видов Lactobacillus и 5 видов Bifidobacterium. Доказано, что бактериальная флора, присутствующая в грудном молоке, включая Lactobacillus, переносится и колонизует желудочно-кишечный тракт новорожденного2, 3. Из грудного молока выделены различные штаммы с пробиотическим потенциалом. Чтобы выбрать из них лучший, провели испытания более 40 штаммов in vitro. «Эти штаммы мы оценивали по специально разработанной шкале, каждому штамму присваивались баллы, – комментирует д-р Э. Лопес. – Исследовалась способность к колонизации, оценивались функциональные и технологические качества. Особенно важно было установить отсутствие у штамма патогенных свойств и способности передавать устойчивость к антибиотикам. Верифицировалось происхождение штаммов из организма матери. Определялся процент выживания после прохождения через ЖКТ, выявлялась адгезия к интестинальным клеткам, определялись антимикробные свойства, способность регулировать иммунную систему. Учитывались органолептические свойства, ферментационные характеристики, стабильность, срок хранения. В результате были отобраны самые жизнеспособные, устойчивые штаммы»4, 5, среди них – Lactobacillus fermentum hereditum®. Эта бактерия получила наивысшие оценки по безопасности и эффективности в ходе испытаний и может считаться лучшим штаммом для применения в детском питании.
Европейское ведомство по безопасности пищевых продуктов (EFSA) присвоило Lactobacillus fermentum статус QPS (qualified presumption of safety). Это означает, что безопасность бактерии не вызывает сомнений, риски для здоровья отсутствуют, дополнительная проверка не требуется. Для проверки безопасности и переносимости Lactobacillus fermentum hereditum® были проведены опыты на мышах. Установлено, что оральное применение L. fermentum безопасно даже в дозах, в 10 000 раз превосходящих обычные человеческие6. «Мы убедились, что никаких инфекционных проявлений у этих мышей не было, они вели себя, как здоровые мыши», – подчеркнул д-р Э. Лопес. В другом опыте на мышах было показано, что применение L. fermentum hereditum увеличивает выживаемость у грызунов, зараженных Salmonella cholerasuis, на 50%. Lactobacillus fermentum hereditum хорошо выживает в желудке человека (74%), имеет высокий уровень адгезии к интестинальным клеткам. Эта бактерия вырабатывает глютатион – естественный и самый мощный антиоксидант, который защищает желудочно-кишечный тракт (ЖКТ) от оксидативного стресса. Доказана высокая безопасность Lactobacillus fermentum hereditum, отсутствие резистентности к антибиотикам и патогенных свойств. Более того, на взрослых добровольцах доказано положительное воздействие L. fermentum hereditum, которое проявилось в снижении заболеваемости гриппом. Еще один положительный эффект лактобацилл был обнаружен, когда смесь, содержащую L. fermentum hereditum, давали кормящим матерям, страдающим маститом. «По результатам исследования мы установили: если в течение 21 дня давать кормящей матери смесь с лактобактериями, в молоке матери снижается количество патогенных бактерий. При этом эффект аналогичен получаемому на фоне антибиотикотерапии», – сообщил испанский ученый. Гарантией безопасности является также тот факт, что весь геном штамма секвенирован и полностью охарактеризован.
Современная тенденция, по мнению Э. Лопеса, заключается в совместном применении пребиотиков и пробиотиков. Изучению свойств синбиотиков посвящены многие недавние и текущие исследования. Так, недавно опубликованы результаты многоцентрового исследования GOLF-1, предпринятого с целью выявить влияние синбиотической смеси из пробиотика L. fermentum CECT 5716 и пребиотика ГОС на рост, развитие и заболеваемость детей в возрасте от 6 до 12 месяцев7. В контрольную группу вошли дети, получавшие только пребиотики (молочная смесь с ГОС, 0,4 г/100 мл). Результаты этого исследования недавно опубликованы. В двойном слепом рандомизированном исследовании учитывали случаи заболевания инфекционными болезнями, лечение антибиотиками, эпизоды лихорадки, а также изменение антропометрических показателей (роста, веса, окружности головы) и состав кишечной микрофлоры. В исследование включали здоровых 6-месячных младенцев с письменного согласия родителей. Критериями исключения в ходе исследования являлись побочные эффекты, а также несоблюдение протокола исследования и неявка родителей с младенцами в больницу в установленные сроки. Родители малышей вели дневники, где отмечали респираторные симптомы, внеплановые визиты к врачу, диагностированные инфекции, случаи лихорадки, прием антибиотиков и др. Базами для исследования служили педиатрическое отделение Университетской больницы в Гранаде и педиатрическое отделение больницы Poniente в Альмерии.
В контрольную группу (дети, получавшие молочную смесь только с пребиотиками) первоначально было включено 98 младенцев, исключено в течение исследования 5, исключено из обработки данных ввиду их неполноты 2 ребенка. Таким образом, в конце исследования учитывались данные 91 ребенка из контрольной группы. В группу исследования (дети, получавшие молочную смесь с пребиотиком (ГОС) и пробиотиком (L. fermentum hereditum)) в начале исследования было включено 110 младенцев, исключено в ходе исследования 8, исключено из обработки данных ввиду их неполноты 5 детей. Таким образом, в конце исследования в этой группе осталось 97 детей. Обе группы были однородны с точки зрения соотношения полов и возрастных характеристик (средний возраст к началу исследования составил 6,5 месяцев). Практически совпадало (в среднем) ежедневное прописанное количество молочной смеси (732 мл в группе исследования и 741 мл в контрольной). 69% младенцев в группе исследования и 71% в контрольной группе в самые первые месяцы (или даже недели) жизни находились на грудном вскармливании, но к началу исследования 100% детей были переведены на искусственное вскармливание. Результаты 6-месячного исследования показали, что все антропометрические показатели (увеличение длины тела, веса, окружности головы) в обеих группах оставались в пределах нормы. Между группами не выявлено никаких различий, не зарегистрировано побочных эффектов. «Мы не зафиксировали аллергических или других нежелательных реакций, связанных, скажем, с повышением температуры или приемом антибиотиков», – сообщил доктор Э. Лопес.
Дети, получавшие молочную смесь с пребиотиком (ГОС) и пробиотиком (L. fermentum hereditum), имели достоверно лучшие показатели, чем дети, получавшие молочную смесь только с пребиотиками, по снижению количества гастроинтестинальных инфекций и заболеваний верхних дыхательных путей. За 6 месяцев наблюдений отмечено 33 случая гастроинтестинальных заболеваний в группе контроля, 19 – в группе синбиотика, снижение риска заболевания составило 46%. Количество случаев заболеваний верхних дыхательных путей составило 121 и 94 случая в группе исследования и группе контроля соответственно, снижение риска заболевания – 27%. Общее число респираторных заболеваний в опытной группе по сравнению с контрольной сократилось на 26% (рис. 2). Было отмечено меньшее число заболеваний нижних дыхательных путей, отитов и болезней мочевыводящих путей в группе детей, получавших молочную смесь с пребиотиком (ГОС) и пробиотиком (L. fermentum hereditum), по сравнению с детьми, получавшими смесь только с пребиотиками, однако различия не были статистически значимыми в связи с малым числом случаев заболеваемости в обеих группах. По общему числу инфекционных заболеваний отмечалось существенное превосходство группы исследования: было зафиксировано 142 случая таких заболеваний по сравнению со 189 в контрольной группе (снижение риска заболевания на 30%).
В группе детей, получавших молочную смесь с пребиотиком (ГОС) и пробиотиком (L. fermentum hereditum), отмечалось меньшее число случаев применения антибиотиков (52 против 57), как и число случаев лихорадки неизвестного происхождения (67 против 78), однако различия не достоверны. Есть основания полагать, что одной из причин различий между двумя группами является формирование кишечной микрофлоры с большим количеством Lactobacillus spp. и Bifidobacteria spp. в группе исследования. В смесях, которые получала контрольная группа, этих полезных молочнокислых бактерий было существенно меньше. Основные выводы, которые были сделаны по результатам исследования: молочная смесь, содержащая пребиотики (галактоолигосахариды) и пробиотики (Lactobacillus fermentum hereditum®), безопасна и хорошо переносится детьми в возрасте от 6 до 12 месяцев; употребление этой смеси способствовало правильному формированию кишечной микрофлоры и позволило снизить заболеваемость гастроинтестинальными инфекциями (на 46%), инфекциями верхних дыхательных путей (на 27%) и общую инфекционную заболеваемость (на 30%). Исследование GOLF-2 по своему дизайну повторяло предыдущее, однако в нем участвовали дети самого младшего возраста – от 21 дня до 6 месяцев, наблюдение велось в течение 5 месяцев. В исследовании изучались безопасность, переносимость и эффективность начальной молочной смеси, содержащей пребиотик ГОС и пробиотик Lactobacillus fermentum hereditum®8. «В этом исследовании главной целью было изучение безопасности, в меньшей степени нас интересовала средняя прибавка в весе», – комментирует доктор Э. Лопес. Тем не менее авторы учитывали среднесуточное увеличение веса и другие антропометрические показатели, исследовали поведенческие реакции, побочные эффекты, случаи заболеваемости, кишечную микрофлору. Базой для исследования служили больницы Гранады, Кордовы и Малаги.
В контрольную группу изначально входил 71 младенец, выбыло по разным причинам 11, проведена обработка данных 60 детей. В опытной группе первоначально насчитывалось 66 детей, выбыло 5, проведена обработка данных 61 ребенка. Показатели увеличения роста, веса, окружности головы в обеих группах в течение 6 месяцев наблюдения были в пределах нормы, между двумя группами не было зафиксировано достоверных различий. Шесть детей в каждой из групп страдали коликами, что не выходит за пределы обычных значений – в среднем у 9% испанских малышей этого возраста наблюдаются колики. Достоверных отличий в поведении, связанном с кормлением, между группами не наблюдалось. В течение 5-месячного срока наблюдения отмечено существенное снижение числа случаев гастроинтестинальных заболеваний в опытной группе (5 случаев) по сравнению с контрольной группой (17 случаев) (рис. 3). Вероятность гастроинтестинальных заболеваний снизилась на 71%. По частоте респираторных заболеваний никаких различий между двумя группами выявлено не было. Общее число инфекционных заболеваний было меньше в опытной группе, однако различия оказались статистически незначимыми. Данные, полученные в ходе исследования, позволили сделать следующие выводы: молочная смесь для младенцев, содержащая пребиотики (ГОС) и пробиотики (Lactobacillus fermentum hereditum), безопасна и хорошо переносится детьми с рождения. Дети, получавшие молочную смесь, содержащую оба компонента, гораздо реже страдали гастроинтестинальными инфекциями, чем младенцы, получавшие смесь только с пребиотиками.





