Афобазол® в терапии тревожных расстройств в общей медицине
- Аннотация
- Статья
- Ссылки
Одним из наиболее перспективных из современных противотревожных средств в этом контексте представляется препарат Афобазол, обладающий селективным анксиолитическим действием с активирующим компонентом (разработан в НИИ фармакологии им. В.В. Закусова РАМН) (6). В отличие от бензодиазепиновых транквилизаторов, Афобазол не связывается с ГАМК-бензодиазепиновыми рецепторами, а восстанавливает их чувствительность к эндогенным медиаторам торможения.
Сопоставимость Афобазола с бензодиазепинами по эффективности купирования тревоги подтверждена в сравнительных исследованиях у пациентов, страдающих генерализованным тревожным расстройством и расстройствами адаптации (1, 6, 9 и др.). При этом Афобазол показал значительно более благоприятный профиль переносимости и безопасности в сравнении с производными бензодиазепина, о чем также свидетельствуют успешные результаты его применения в терапии тревожных состояний у пациентов с предменструальным синдромом (7), нейроциркуляторной дистонией (2), тиреотоксикозом (3).
В данной публикации обобщены результаты трех клинических исследований Афобазола в терапии анксиозных расстройств в рамках нозогенных реакций у пациентов с кардиологической, онкологической и дерматологической патологией, выполненных сотрудниками отдела по изучению пограничной психической патологии и психосоматических расстройств (руководитель – академик РАМН А.Б. Смулевич) Научного центра психического здоровья РАМН (директор – академик РАМН А.С. Тиганов) в сотрудничестве со специалистами клиники кардиологии (руководитель – профессор А.Л. Сыркин) и клиники кафедры кожных и венерических болезней лечебного факультета (зав. кафедрой – профессор О.Л. Иванов) ММА им. И.М. Сеченова, отделений абдоминальной хирургии (заведующий – профессор И.С. Стилиди) и химиотерапии (заведующий – профессор В.А. Горбунова) РОНЦ им. Н.Н. Блохина РАМН (директор – академик РАН и РАМН М.И. Давыдов) (4, 5, 10).
Характеристики исследований и пациентов
Все исследования проводились по единому дизайну, критериям включения (нозогенные тревожные расстройства, расстройства адаптации по МКБ-10) и исключения, проводился 42-дневный курс монотерапии Афобазолом в суточной дозе 30-60 мг. Для верификации клинического эффекта использовались стандартные инструменты – шкала тревоги Гамильтона (HARS) и шкалы общего клинического впечатления – Тяжесть (CGI-S) и Улучшение (CGI-I).
Всего в трех исследованиях участвовало 90 взрослых пациентов, по 30 в клиниках кардиологии (с диагнозами – ишемическая болезнь сердца, стенокардия I, II функционального класса, гипертоническая болезнь I, II степени, аритмии), онкологии (различные злокачественные новообразования, включая рак желудка, легкого, молочной железы и др.) и дерматологии (псориаз, экзема, атопический дерматит, угревая болезнь, розацеа), средний возраст пациентов – 49,8, 47,3 и 38,7 лет соответственно, доля женщин – 56,7%, 56,7% и 80,0% соответственно.
У пациентов преобладали тревожно-депрессивные и тревожно-ипохондрические нозогенные реакции, протекающие со стойкими тревожными опасениями (по типу антиципирующей тревоги), содержание которых обнаруживает тесную связь с диагнозом, а также обстоятельствами обследования и лечения соматической патологии. Клиническая картина представлена явлениями танатофобии, опасениями беспомощности, утяжеления проявлений соматического заболевания и развития осложнений в сочетании с признаками соматизированной тревоги и (в случаях тревожно-депрессивных реакций) легкой гипотимии, не достигающей уровня развернутого депрессивного эпизода. Типична значительная лабильность аффекта с отчетливым обострением тревоги и фобических расстройств в связи с любыми предстоящими диагностическими и лечебными процедурами.
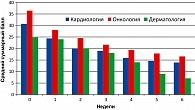
Исходные показатели психометрических шкал свидетельствуют об умеренном уровне тревожных расстройств в изученных выборках: в кардиологической, онкологической и дерматологической выборках средний стартовый суммарный балл шкалы тревоги Гамильтона (HARS) составил 30,7; 36,5 и 24,7 соответственно (см. рисунок), стартовый средний суммарный балл шкалы CGI-тяжесть – 4,2; 4,3 и 4,2 соответственно (интервал между 4 – «умеренно болен» и 5 – «явно болен»).
Результаты
Большинство пациентов (86 из 90) полностью завершило 6-недельный курс терапии Афобазолом. Только в 4 наблюдениях потребовалась преждевременная отмена препарата в связи с нежелательными явлениями (по 2 случая среди онкологических и дерматологических больных). Средняя эффективная суточная доза составила 50 мг.
Редукция симптомов тревоги той или иной степени отмечалась у всех пациентов, что подтверждается динамикой суммарного балла шкалы тревоги Гамильтона, примерно одинаковой во всех трех выборках.
Терапевтический эффект Афобазола развивался достаточно быстро – начальные признаки улучшения состояния наблюдались уже с первых дней лечения, но клинически значимое обратное развитие симптомов начиналось к концу 1-й недели лечения (р < 0,05) с непрерывным улучшением показателей вплоть до последней (6-й) недели терапии (p < 0,001).
Клинический эффект Афобазола характеризовался отчетливым противотревожным действием с редукцией уровня тревоги и тревожных опасений. При этом отмечалась параллельная динамика обратного развития тревожных и соматизированных расстройств, снижение амплитуды колебаний фона настроения и улучшение сна. Проявление анксиолитического действия препарата не сопровождалось признаками седации. Напротив, наблюдался легкий активирующий эффект, сопровождающийся субъективным улучшением внимания и общего уровня активности.
Высокая общая эффективность лечения была подтверждена результатами оценки по шкалам общего клинического впечатления – CGI-S (Тяжесть) и CGI-I (Улучшение). Через 6 недель терапии стартовый средний суммарный балл CGI-S (Тяжесть) уменьшился до 2,1, 2,2 и 2,1 (между 2 – «пограничное состояние» и 3 – «в легкой степени болен») у кардиологических, онкологических и дерматологических пациентов соответственно. Средний балл шкалы CGI-I (Улучшение) на финальном визите (6-я неделя) составил 1,7 (между 1 – «очень выраженное улучшение» и 2 – «выраженное улучшение»).
По завершении терапии зафиксированы примерно равные высокие доли респондеров (пациенты с редукцией стартового суммарного балла шкалы тревоги Гамильтона на ³ 50%), составившие 70%, 67% и 70% в кардиологической, онкологической и дерматологической выборках соответственно.
При сравнительном анализе респондеров и нереспондеров установлены следующие клинические факторы недостаточной эффективности Афобазола: полиморфные фобии и соматизированные расстройства в сочетании с паническими атаками и стойкой инсомнией, определяющей потребность в дополнительном назначении гипнотиков короткого действия (разрешенных протоколом исследования).
Афобазол хорошо переносился пациентами. Зафиксированные нежелательные явления были преимущественно легкими по выраженности, носили транзиторный характер и редуцировались без коррекции дозы Афобазола (как правило, 2-3 неделя лечения). Лишь у 4 пациентов побочные эффекты, развившиеся в первые дни терапии, послужили причиной преждевременного исключения из исследования: тошнота – у 2 пациентов (онкологическая выборка), головная боль и седация в дневное время – по 1 пациенту (оба в дерматологической выборке). В кардиологической выборке случаев прерывания терапии Афобазолом из-за побочных эффектов не было.
На фоне терапии Афобазолом не наблюдалось токсических эффектов и клинически значимых изменений в показателях лабораторных и инструментальных методов обследования. Во всех трех выборках пациентов не выявлено ни одного признака лекарственных взаимодействий Афобазола с медикаментами, использующимися для лечения соматической патологии.
Заключение
Как показали результаты проведенных исследований, Афобазол является эффективным анксиолитическим средством при купировании тревожных расстройств у пациентов, страдающих соматическими заболеваниями. Препарат характеризуется высоким профилем безопасности и может применяться у пациентов, получающих разнообразную лекарственную терапию соматических заболеваний.
Учитывая высокую распространенность тревожных расстройств среди пациентов общемедицинской сети, представляется целесообразным рекомендовать Афобазол как одно из средств психофармакотерапии тревожных расстройств как в амбулаторной, так и госпитальной системе медицинской помощи пациентам с соматическими заболеваниями.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.