Дефицит магния и его коррекция в акушерско-гинекологической практике
- Аннотация
- Статья
- Ссылки
Магний (Mg2+) впервые был выделен английским химиком Гемфри Дэви в 1808 г., является главным двухвалентным металлом (Mg2+) второй группы Периодической системы химических элементов Д.И. Менделеева, с атомной единицей массы 24,305; в ионизированной форме представляет положительный ион (катион) с двойным положительным зарядом (Mg2+); является одним из самых распространенных элементов на земле (занимает 8-е место). Особенно много Mg2+ в воде мирового океана (0,13%), которая по электролитному составу близка к сыворотке крови (5).
Нормальный уровень Mg2+ в организме человека признан основополагающей константой, контролирующей здоровье человека. Mg2+ вместе с 11 основными структурными неорганическими химическими элементами (кальций, калий, натрий, хлор, фосфор, фтор, сера, углерод, кислород, водород, азот) определяет 99% элементарного состава человеческого организма. Среди катионов, присутствующих в организме человека, Mg2+ по концентрации занимает 4-е место в организме, а в клетке среди других катионов (натрий, калий, кальций) – 2-е (5, 10, 13).
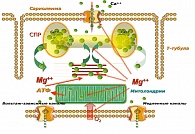
В настоящее время установлено наличие не менее 290 генов и белковых соединений в последовательности генома человека, которые способны связывать Mg2+ как кофактор множества ферментов, участвующих в более чем 300 внутриклеточных биохимических реакциях. Mg2+ – естественный физиологический антагонист кальция (Са2+); универсальный регулятор биохимических и физиологических процессов в организме, обеспечивает гидролиз АТФ, уменьшая разобщение окисления и фосфолирование; регулирует гликолиз, уменьшает накопление лактата, способствует фиксации калия (K1+) в клетках, обеспечивая поляризацию клеточных мембран, контролирует спонтанную электрическую активность нервной ткани и проводящей системы сердца, контролирует нормальное функционирование кардиомиоцита на всех уровнях субклеточных структур – это универсальный цитопротектор (рисунок 1).
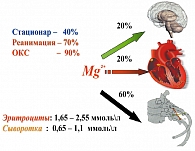
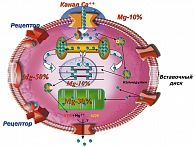
У человека распределение запасов Mg2+ имеет свои особенности: около 60% Mg2+ находится в костной ткани, дентине и эмали зубов; 20% – в тканях с высокой метаболической активностью (сердце, мышечные клетки, печень, надпочечники, почки); 20% – в мозге и нервной ткани; всего 0,3% приходится на плазму крови (рисунок 2). 90% магниевых ионов сконцентрировано внутри клеток в форме фосфатной связи – Mg2+ ↔ АТФ (30% в митохондриях, 50% в цитозоле, 10% в ядре клетки), и только 10% всего содержания Mg2+ в организме человека находится вне клеток (рисунок 3). Основной путь элиминации Mg2+ – почки, кожа (потоотделение), слизистая полости рта (слюноотделение).
Уровни физиологической нормы определяют потребность в Mg2+ взрослого человека: 350 мг/сут. для мужчин и 300 мг/сут. для женщин. Сбалансированная диета должна содержать приблизительно 400 мг Mg2+ в сутки, из которого абсорбируется, как правило, около половины – 200 мг. Согласно докладу комитета экспертов ВОЗ «Микроэлементы в питании человека», ежедневная потребность в Mg2+, составляющая 300 мг для женщин и 350 мг для мужчин, удовлетворяется на 40% пищей и на 60% за счет так называемого водного Mg2+.
Содержание Mg2+ в питьевой воде в различных географических зонах значительно варьирует и зависит от особенностей тех пород, на которых располагаются источники природной воды. Отмечается почти полное отсутствие Mg2+ в природной воде источников Кольского полуострова, Скандинавии, Карелии (5, 7, 9).
Mg2+ – один из основных элементов, определяющих жесткость воды. Мягкой принято считать воду, содержащую менее 10 мг/л Mg2+. Обобщив данные литературы, Ю.В. Новиков и соавт. показали, что каждые 2 мг экв/л жесткости являются источником 6-7% общего поступления Mg2+ в человеческий организм.
Всасывание Mg2+ осуществляется во всем кишечнике вплоть до сигмовидной кишки, однако главной зоной его абсорбции служит 12-перстная кишка. Усвояемость Mg2+ из пищевых продуктов составляет 30-35% (т.е. из 300-350 мг суточной потребности усваивается около 100 мг). Она может увеличиваться под влиянием витамина В6 и ряда органических кислот (молочной, аспарагиновой, оротовой). Молоко и некоторые молочные продукты, содержащие казеин, также способствуют увеличению абсорбции Mg2+ (вероятно, в связи с большим содержанием оротовой кислоты). Ежесуточно с пищеварительными соками в ЖКТ дополнительно к пищевому поступает более 400 мг Mg2+, которые вновь всасываются в кровь.
Абсорбции Mg2+ в ЖКТ препятствует большое содержание в пище веществ, с которыми он образует труднорастворимые или нерастворимые соединения – белки, жиры. Всасывание уменьшается также при избытке ионов Са2+, конкурирующих с Mg2+ на слизистой оболочке кишечного тракта (5).
Биодоступность Mg2+ в организме регулируется рядом генов, контролирующих «сборку» и функционирование белков на поверхности клеточных мембран, выполняющих роль рецепторов или ионных каналов, среди которых TRPM-6 (Transient Receptor Potential Cation Channel) и TRPМ-7 являются наиболее важными. Белок TRPM-6 является ионным каналом, регулирующим транспорт двухвалентных катионов. TRPM-6, специфически взаимодействуя с другим Mg2+ – проницаемым каналом TRPM-7, способствует формированию («сборке») функциональных TRPM-6/TRPM-7 протеиновых комплексов на поверхности клеточных мембран. Экспериментальные и клинические исследования указывают, что изменения функционального состояния TRPM-7 под действием катехоламинов на фоне эмоционального стресса способствуют развитию внутриклеточного дефицита магния (8, 10, 12).
Наиболее общий эффект воздействия Mg2+ на любую ткань заключается в том, что ионы Mg2+ стабилизируют структуру транспортной РНК, контролирующей общую скорость синтеза и ресинтеза белков. При дефиците Mg2+ происходит дестабилизация транспортных – некодирующих РНК (увеличивается число дисфункциональных молекул РНК), что сопровождается снижением и замедлением скорости синтеза белковых структур клеток с относительным преобладанием процессов апоптоза – программируемая «смерть» клеток (8, 10, 12).
Ионы Mg2+ играют важнейшую роль в процессах мембранного транспорта и электролитного баланса, требующих больших энергозатрат. Связываясь с клеточными, митохондриальными и другими внутриклеточными мембранами, ионы Mg2+ регулируют их проницаемость для других ионов. Ионы Mg2+ имеют особое значение в поддержании трансмембранного потенциала. Активируя Mg2+ зависимую Na+-К+-АТФазу, они определяют работу К+/Na+ насосов, осуществляющих накопление калия внутри клетки и выведение натрия в межклеточное пространство, обеспечивая таким образом поляризацию и стабильность мембраны. Регуляцией электролитного баланса в клетке (наряду с влиянием на энергетический обмен) объясняется способность Мg2+ подавлять автоматизм, проводимость и возбудимость, увеличивать абсолютную и укорачивать относительную рефрактерность в тканях, обладающих всеми или какими-то из этих функциями, например в миокарде, в гладких мышцах сосудов и бронхов, миометрии матки и др.
Важную роль Mg2+ играет в обеспечении нормальной структуры и функции нервных клеток, что позволяет ему контролировать деятельность как периферической, так и центральной нервной системы, включая психоэмоциональную сферу. Имеются указания на его способность увеличивать устойчивость организма к стрессу (1, 6, 7, 14). Среди метаболических функций, проявляющихся на уровне целого организма, необходимо подчеркнуть его роль в поддержании нормального липидного спектра, в обеспечении ответа тканей на инсулин и торможении гормона паращитовидной железы.
Для выявления дефицита Mg2+ используют его определение в различных биологических средах организма человека: концентрация Mg2+ в плазме крови – 0,65-1,2 ммоль/л, в эритроцитах – 1,65-2,65 ммоль/л, в моче 2,27-5,8 ммоль/л, слюне 0,08-0,53 ммоль/л, конденсате выдыхаемого воздуха – 0,0094 ммоль/л.
Дефицит Mg2+ – снижение концентрации Мg2+ в эритроците менее 1,6 ммоль/л, о гипомагниемии принято говорить при снижении концентрации Mg2+ в плазме крови менее 0,6 ммоль/л. Дефицит Mg2+ – синдром, обусловленный снижением внутриклеточного содержания Mg2+ в различных органах и системах, множество симптомов которого свидетельствуют о мультиорганных нарушениях функционального состояния целостного организма, наблюдаемый среди различных возрастных групп населения (1, 5, 13).
Несмотря на то что Mg2+ широко распространен в природе, его дефицит среди населения земного шара встречается чрезвычайно часто. Так, по данным разных авторов, гипомагнезиемия регистрируется в 7-11% случаев среди госпитализированных больных, а у пациентов отделений интенсивной терапии в 2 раза чаще – в 25%. Достоверное выявление недостатка Mg2+ представляет определенные трудности, в связи с чем его диагностика на практике нередко проводится на основании клинических признаков.
Так, в одном из скрининговых исследований, проведенных в США, было показано, что гипомагнезиемия (уровень сывороточного Mg2+ был ниже 0,74 ммоль/л) имела место в 47,1% наблюдений, то клинические признаки магниевого дефицита проявлялись более чем у 72% взрослого населения.
В России, по данным эпидемиологических исследований, около 30% жителей получают в день менее 79% суточной нормы Mg2+, при этом дефицит магния манифестируется значительно чаще у женщин, чем у мужчин.
В числе основных клинических состояний, патогенетически связанных с дефицитом Mg2+, выделяют: метаболический синдром (МС), компонентами которого являются АГ, инсулинорезистентность, СД, атерогенная дислипидемия; синдром хронической усталости; болезни сердца (ИБС, ХСН, дилатационная кардиомиопатия); синдром дисплазии соединительной ткани (ДСТ); синдром удлиненного Q-T интервала; «синдром реперфузии»; пролапс митрального клапана; бронхиальная астма; выкидыши в I триместре беременности, преждевременные роды, утяжеление течения беременности и родов.
По этиологии различают первичный и вторичный дефицит Mg2+. Первичный (конституционный, латентный) дефицит Mg2+ обусловлен дефектами в генах, ответственных за трансмембранный обмен Mg2+ в организме, клинически проявляется судорожным синдромом (спазмофилия), «конституционной тетанией» или «нормокальциевой тетанией» на фоне нормального содержания Mg2+ в сыворотке крови; вторичный – обусловлен социальными условиями и образом жизни, экологической обстановкой и особенностями питания, различными стрессорными ситуациями и заболеваниями (1, 5, 6, 8, 13).
Причины магниевого дефицита, связанные с условиями жизни:
- стресс – острый и хронический (особенно): по данным Минздравсоцразвития около 80% населения РФ проживают в условиях хронического стресса;
- напряженная физическая работа и физическое перенапряжение; гиподинамия;
- злоупотребление алкоголем;
- воздействие высоких температур (жаркий климат, горячие цеха, избыточное посещение парных, бань);
- беременность и лактация; гормональная контрацепция.
Причины магниевого дефицита, связанные с питанием:
- потребление продуктов с ограниченным содержанием Mg2+ (мясо, птица, картофель, молоко и молочные продукты);
- потребление продуктов с высоким содержанием животных жиров и белков, фосфора, кальция, которые угнетают (препятствуют) абсорбции Mg2+ в ЖКТ.
Причины магниевого дефицита, связанные с патологическими процессами:
- нарушения абсорбции в ЖКТ в связи с заболеваниями или возрастными изменениями (синдром малой абсорбции – болезнь Крона, хронический дуоденит, дисбактериоз, неспецифический язвенный энтероколит и т.д.);
- сахарный диабет (инсулинорезистентность, гиперинсулинемия, гипергликемия, диабетическая нефропатия); гиперкатехоламинемия; гиперальдостеронизм; гиперкортицизм; гипертиреоз; гиперпаратиреоз;
- ОКС;
- ХСН;
- ожирение (индекс массы тела > 25 кг/м2), которое в начале XXI в. принимает характер эпидемии.
Ятрогенные причины магниевого дефицита могут быть связаны с передозировкой сердечных гликозидов; злоупотреблением диуретиками; гормональной контрацепцией; применением глюкокортикоидов; цитостатической терапией.
Следует отметить, что негативную роль в недостатке Mg2+ играет употребление фастфуда. В Москве приказом Департамента здравоохранения от 2003 г. запрещено продавать в школьных буфетах продукты, содержащие вытеснители Mg2+, – кока-кола, спрайт, чипсы, сушеные кальмары и другие пересоленные продукты, так как соль (NaCl) способствует активному выведению Mg2+ из организма и ингибирует его вхождение в клетку.
Дефицит магния и беременность
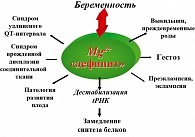
Физиологические нормы потребности в Mg2+ для женщин составляют 300 мг/сут. При беременности суточная потребность в Mg2+ возрастает в 1,5-2 раза, что обусловлено созидательными процессами в организмах матери и плода. Как правило, потребность организма беременной женщины в Mg2+ нередко превышает его поступление. Данное обстоятельство позволяет рассматривать беременность в качестве физиологической модели гипомагниемии. При этом дефицит Mg2+ сопряжен с широким спектром осложнений беременности и родов – преждевременной родовой деятельностью, развитием гестозов, нарушением развития плода и патологией новорожденного (рисунок 4).
По мере увеличения срока беременности концентрация сывороточного Mg2+ снижается. Еще более значительное падение уровня Mg2+ происходит во время родов. Концентрация Mg2+ в плазме крови коррелирует с его концентрацией в миометрии. По данным различных авторов, содержание магния в миометрии к 38-40-й неделе беременности уменьшается до 38% (n ≈ 6,6 мкг/кг), а при активных родах до 47% (практически вдвое). При этом концентрация Сa2+ или других электролитов меняются не значительно, что подтверждает особую роль Mg2+ в физиологии родоразрешения. Отмечено, что снижение содержания Mg2+ приводит к повышению тонуса миометрия и преждевременной маточной контрактильности (1-3, 6, 9, 13).
Токолитическая активность Mg2+ объясняется конкурентным антагонизмом с кальцием и его способностью блокировать медленные кальциевые каналы, что приводит к ослаблению сокращений матки. Назначение препаратов Mg2+ считается оправданным при угрожающем выкидыше и преждевременных родах, гестационной гипертензии, преэклампсии и эклампсии, задержке развития плода и повреждении мозга у новорожденного (3, 4, 13).
Влияние дополнительного приема Mg2+ на течение беременности и развитие плода изучалось в крупнейшем метаанализе, обобщившем результаты 7 исследований, включающих результаты обследования и клинического наблюдения за 2689 беременными женщинами. Пероральное применение препаратов магния (Магнерот® 3 г/сут.) начиная с 25-й недели беременности приводило к снижению частоты преждевременных родов, случаев рождения детей с низким весом, а также меньшей потребности в госпитализации во время беременности в сравнении с плацебо (2, 6, 9).
Особое место в перечне показаний для лечения препаратами магния занимает эклампсия – тяжелое полиорганное расстройство неизвестной этиологии. Эклампсия занимает 3-е место после кровотечений и инфекции среди причин материнской смертности. Патогенез эклампсии сложен и включает такие звенья, как эндотелиальная дисфункция, нарушение реологических свойств крови, генерализованная вазоконстрикция. Особое место в патогенезе преэклампсии и эклампсии занимает нарушение гомеостаза Mg2+. Очевидное снижение его уровня показано во многих работах (4, 9, 14).
Препараты магния традиционно находят широкое применение в профилактике и лечении преэклампсии и эклампсии. В известном рандомизированном плацебо-контролируемом исследовании Magpie лечение сульфатом магния вдвое уменьшало риск возникновения эклампсии. При уже имеющейся преэклампсии в/в введение сульфата магния значительно снижало вероятность прогрессирования процесса и развития эклампсии.
Предполагаемые механизмы лечебного действия Mg2+ при эклампсии разнообразны. Торможение процессов возбуждения в коре головного мозга, блокада нервно-мышечной передачи обеспечивают его противосудорожную активность. За счет подавления синтеза тромбоксана A2 и антагонизма с Ca2+ магний вызывает дилатацию сосудов, улучшая не только маточно-плацентарно-плодовое, но и церебральное кровообращение (3, 11, 13). Определенное значение имеет и способность Mg2+ повышать уровень кальцитонина в сыворотке крови, так как известно, что концентрации кальцитонина и паратиреоидного гормона снижаются у женщин во время беременности с клиническими признаками преэклампсии.
Помимо ведения больных (беременных) с преэклампсией и эклампсией препараты магния до сих пор наиболее популярны и при изолированной гипертензии беременных. Известно, что низкий уровень внутриклеточного Mg2+ может способствовать развитию гестационной гипертонии. Установлена связь между уровнем Mg2+ в эритроцитах и величиной АД в III триместре беременности. Предполагается, что гипотензивный эффект препаратов магния связан с влиянием на баланс простагландина I2 и тромбоксана A2.
Одним из наиболее неоднозначных аспектов применения Mg2+ в акушерской практике является его влияние на состояние эмбриона, плода и новорожденного. Среди обсуждаемых вопросов – эффективность препаратов магния при перинатальном повреждении мозга у плода. Нейропротективный эффект Mg2+ был доказан в эксперименте, и оказалось, что он связан с подавлением апоптоза нейронов. Способность сульфата магния защищать мозг новорожденных отмечена и в ряде клинических исследований. В частности, в многоцентровом рандомизированном исследовании послеродовое назначение указанного препарата в суточной дозе 250 мг/кг младенцам с тяжелой асфиксией при рождении оказалось эффективным и безопасным (6, 9, 11).
Участие Mg2+ в процессе родоразрешения и значение его дефицита в возникновении неблагоприятных исходов у матери, плода и новорожденного обусловливают его широкое применение в акушерской практике.
Для парентерального введения препаратов магния при лечении преэклампсии и эклампсии или для быстрого достижения нормативного уровня Mg2+ в крови наиболее часто применяется раствор магния сульфат. Одним из таких препаратов является Кормагнезин (Wörwag Pharma, Германия), который выгодно отличается от ряда других препаратов магния для парентерального введения отсутствием технических примесей и удобной дозировкой (400 мг элементарного магния в ампуле). Рекомендуемая скорость введения раствора сульфата магния в 5% глюкозе из расчета 0,5-0,6 г/ч Mg2+, максимум при тяжелых клинических проявлениях дефицита Mg2+ до 12-15 г Mg2+ в сутки.
Внутривенная инфузия сульфата магния также показана при осложненном гипертоническом кризе, в частности эклампсии, с выраженной общемозговой симптоматикой, угрозой развития инсульта, желудочковыми нарушениями ритма и для профилактики внезапной смерти на фоне удлиненного Q–T интервала на ЭКГ. В данных ситуациях ионы Mg2+ оказывают не только гипотензивный эффект, но и осуществляют седатацию и кардионейропротективные эффекты.
С учетом положительного влияния препаратов магния на эластичность и подвижность эритроцитов, ингибирующее воздействие на АДФ-индуцированную агрегацию тромбоцитов, показаниями для парентерального применения препаратов магния являются судорожный синдром и эклампсия, в патогенезе которых имеют место нарушения микроциркуляции, вызванные неадекватным функциональным состоянием сосудов, реологическими свойствами крови (повышенная агрегационная активность тромбоцитов, снижение подвижности эритроцитов), образование микротромбов (регионарный ДВС-синдром), перивазальный отек тканей, что, как правило, наблюдается при дефиците Mg2+.
Препарат Магнерот® (Wörwag Pharma, Германия) представляет собой препарат магния для перорального применения, в качестве активного действующего вещества содержит 500 мг оротата магния, что соответствует 32,8 мг чистого магния.
Как указывалось, в организме человека Mg2+ играет ведущую роль – он участвует в метаболизме и катаболизме углеводов, липидов, белков и нуклеиновых кислот; как ко-фактор Mg2+ принимает участие в окислительном фосфорилировании – источник макрофосфатной энергии (АТФ), обеспечивая энергией и регулируя работу мембранных структур клеток (рецепторы канала, «электролитные насосы»).
Mg2+ как физиологический антагонист Ca2+ устраняет спазм и судороги скелетных мышц (судороги в икроножных мышцах), сосудов (мигрень), мочеполовой системы (гипертонус матки и мочевого пузыря), в основе которых лежит относительная или абсолютная (при дефиците Mg2+) гиперкальциемия. Очень важен Mg2+ для поддержания насосной деятельности сердца в условиях увеличенной физической нагрузки, особенно при беременности, он способствует нормализации диастолы и восстановлению сократительной способности миокарда (5).
Во время беременности и кормления грудью потребность в Mg2+ значительно увеличивается, если его содержание в целостном организме не сбалансировано, то это может привести к тяжелым осложнениям, таким как выкидыш, преждевременные роды, неправильное развитие плода или ребенка в первый год его жизни.
Магний в препарате Магнерот® связан с оротовой кислотой, которая в естественном виде не содержится в человеческом материнском молоке. Оротовую кислоту в промышленных масштабах получают из молозива – молока коров или овец после родов. Оротовая кислота способствует росту клеток, играет важную функцию в обмене липидов и в сочетании с Mg2+ потенцирует профилактические и лечебные эффекты Магнерота® в акушерско-гинекологической практике. Суточная доза Магнерота® для женщин во время беременности и кормления при лечении – 3 г (4 табл.), при профилактических мероприятиях 1-2 г (2-4 табл.).
Таким образом, данные литературы и наши наблюдения указывают на высокую частоту (от 40% до 90%) сочетания дефицита Mg2+ с патологией со стороны сердечно-сосудистой системы, имеющих место у женщин во время беременности, родоразрешении и в послеродовом периоде при кормлении грудью. Дефицит Mg2+ лежит в основе таких осложнений, как выкидыш в I триместре беременности, преждевременные роды, преэклампсия и эклампсия, гестационная гипертензия, нарушения развития плода и патологии у новорожденного.
Включение препаратов магния (Магнерот® 1-3 г/сут.) с целью профилактики и комплексной терапии осложнений в акушерской и гинекологической практике способствует нормализации развития плода, своевременному родоразрешению, профилактике осложнений со стороны сердечно-сосудистой системы во время беременности.
Препараты магния, обладая плейотропными фармакологическими эффектами, оказывают антиаритмогенный эффект, способствуют более эффективному снижению инсулинорезистентности, лежащей в основе метаболических нарушений, нормализации гликемического, липидного профилей и реологических свойств крови, что суммарно ведет к нормализации микроциркуляции, артериального давления и насосной деятельности сердца.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.