Диарея неинфекционного генеза в многопрофильном стационаре: рандомизированное исследование
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. Обследовано 169 пациентов с клинической картиной диареи различной степени тяжести, поступивших в ФГБУ «3-й Центральный военный клинический госпиталь им. А.А. Вишневского» Минобороны России. Всем пациентам проводилась конвенциональная терапия. Пациенты случайным образом были разделены на три группы:
62 пациентам 1-й группы назначали Энтеросгель в стандартной дозе 1 столовая ложка 3 раза в день между приемами пищи, 56 пациентам 2-й группы – диоктаэдрический смектит, 51 пациенту 3-й группы энтеросорбенты не назначались. По этиологии диареи пациенты 1-й группы распределились следующим образом:
32 – с антибиотикоассоциированной диареей, 8 – с синдромом раздраженного кишечника с диареей (СРК-Д) и 8 – язвенным колитом, 6 пациентов с дивертикулярной болезнью и 6 – хроническим панкреатитом с внешнесекреторной недостаточностью, 2 пациента с НПВС-энтеропатией. Оценивали частоту стула (количество дефекаций в течение суток) и длительность стационарного лечения (дни). Результаты сравнивали с таковыми пациентов 2-й и 3-й групп.
Результаты. Включение Энтеросгеля в конвенциональную терапию неинфекционной диареи независимо от ее генеза позволяет сократить сроки стационарного лечения и способствует ускорению нормализации стула. Эффективность Энтеросгеля и диоктаэдрического смектита сопоставима. Максимальный эффект получен при использовании Энтеросгеля при антибиотикоассоциированной диарее и СРК-Д.
Заключение. Анализ применения энтеросорбента Энтеросгель при диарее неинфекционного генеза различного происхождения подтверждает эффективность его включения в конвенциональную терапию данных заболеваний.
Материал и методы. Обследовано 169 пациентов с клинической картиной диареи различной степени тяжести, поступивших в ФГБУ «3-й Центральный военный клинический госпиталь им. А.А. Вишневского» Минобороны России. Всем пациентам проводилась конвенциональная терапия. Пациенты случайным образом были разделены на три группы:
62 пациентам 1-й группы назначали Энтеросгель в стандартной дозе 1 столовая ложка 3 раза в день между приемами пищи, 56 пациентам 2-й группы – диоктаэдрический смектит, 51 пациенту 3-й группы энтеросорбенты не назначались. По этиологии диареи пациенты 1-й группы распределились следующим образом:
32 – с антибиотикоассоциированной диареей, 8 – с синдромом раздраженного кишечника с диареей (СРК-Д) и 8 – язвенным колитом, 6 пациентов с дивертикулярной болезнью и 6 – хроническим панкреатитом с внешнесекреторной недостаточностью, 2 пациента с НПВС-энтеропатией. Оценивали частоту стула (количество дефекаций в течение суток) и длительность стационарного лечения (дни). Результаты сравнивали с таковыми пациентов 2-й и 3-й групп.
Результаты. Включение Энтеросгеля в конвенциональную терапию неинфекционной диареи независимо от ее генеза позволяет сократить сроки стационарного лечения и способствует ускорению нормализации стула. Эффективность Энтеросгеля и диоктаэдрического смектита сопоставима. Максимальный эффект получен при использовании Энтеросгеля при антибиотикоассоциированной диарее и СРК-Д.
Заключение. Анализ применения энтеросорбента Энтеросгель при диарее неинфекционного генеза различного происхождения подтверждает эффективность его включения в конвенциональную терапию данных заболеваний.




Введение
Согласно определению Всемирной организации здравоохранения (2018), под диареей (от греч. diarrhea – истекаю) понимается неоформленный или жидкий стул три или более раз в день либо чаще, чем обычно для конкретного человека. При этом содержание воды в кале достигает 85–95% (в норме 60–70%) [1, 2]. Однако провести количественный анализ данного показателя в рутинной практике достаточно трудно. На практике обычно используют установление частоты и/или массы стула [1]. Диагностические критерии диареи представлены в табл. 1 [1, 3].
Диарея – клинический синдром различной этиологии и патогенеза, подразумевающий частое или однократное опорожнение кишечника с выделением жидких или водянистых каловых масс в объеме более 200–300 г в сутки.
Водянистый стул трудно удержать, позывы на дефекацию при диарее носят императивный характер, что существенно снижает качество жизни пациентов и вынуждает их обращаться к врачу.
Острой называют диарею продолжительностью не более двух-трех недель. Сочетание диареи с лихорадкой, симптомами интоксикации, эксикозом требует прежде всего исключения ее инфекционной природы.
Диарея длительностью более трех недель считается хронической и, как правило, имеет неинфекционный генез [2]. Наиболее частые причины неинфекционной диареи представлены в табл. 2 [1, 3, 4].
Механизмы развития диареи
Диарею подразделяют:
- на осмотическую: увеличение осмолярности кишечного содержимого вследствие скопления избытка неабсорбируемых веществ (прием лактулозы, солевых слабительных, антацидов, содержащих магний, нарушение полостного и мембранного пищеварения, лактазная недостаточность);
- экссудативную: секреция воды и электролитов в просвет кишки через поврежденную слизистую оболочку одновременно с экссудацией белка (воспалительные заболевания кишечника (ВЗК), туберкулез, лимфома, ишемия, правожелудочковая недостаточность);
- секреторную: повышение секреции электролитов и воды энтероцитами (карциноид, випома); гиперкинетическую: ускорение транзита кишечного содержимого, уменьшение объема абсорбированной в кишечнике жидкости (синдром раздраженного кишечника с диареей (СРК-Д), тиреотоксикоз, функциональная диарея, резекция участка кишки, ваготомия, диабетическая энтеропатия, склеродермия).
В ряде случаев в развитии диареи могут быть задействованы сразу несколько механизмов. Например, при ВЗК одновременно имеют место экссудативный (секреция воды и электролитов в просвет кишки через поврежденную слизистую оболочку одновременно с экссудацией белка), секреторный (воспалительная экссудация альбумина, секреция макрофагами, моноцитами, эпителиальными клетками провоспалительных цитокинов, активизирующих секреторные процессы), осмотический (увеличение осмолярности кишечного содержимого вследствие нарушения полостного и мембранного пищеварения). Выделение патогенетических вариантов диареи позволяет выбрать оптимальный вариант лечения [1, 5, 6]. Методы обследования пациентов с диареей представлены в табл. 3 [1, 2].
Основные группы препаратов, используемые при лечении заболеваний, протекающих с диарейным синдромом
К таким препаратам относятся:
- препараты, замедляющие моторику;
- энтеросорбенты;
- вяжущие и обволакивающие средства;
- антибиотики и антисептики;
- противовоспалительные препараты;
- пре-, про-, син- и эубиотики;
- ферментные препараты;
- регидратанты;
- препараты для коррекции солевого и электролитного обмена;
- препараты для энтерального и парентерального питания [1–3, 7–10].
В конвенциональной терапии заболеваний, протекающих с диарейным синдромом, традиционно используются энтеросорбенты [11–14].
Энтеросорбенты (от греч. enteron – кишка; лат. sorbens – поглощающий) – вещества различной структуры, связывающие экзо- и эндогенные вещества, надмолекулярные структуры и клетки в желудочно-кишечном тракте (ЖКТ) путем адсорбции, абсорбции, ионообмена, комплексообразования [13–15].
Энтеросорбенты как лечебные средства известны с древних времен. Еще врачеватели Древнего Египта, Индии, Греции использовали внутрь древесный уголь, глину, растертые туфы, пережженный рог при отравлениях, диарее, желтухе и других заболеваниях, а также для наружного применения – для заживления ран. Лекари Древней Руси применяли березовый или костный уголь. Авиценна (Абу Али ибн Сина) в своем Каноне врачебной науки из семи постулатов искусства сохранения здоровья на третье место поставил метод, который по современным понятиям идентичен энтеросорбции [16]. В России Т.Е. Ловиц, изучая химические свойства древесного угля, обосновал его применение для тех же целей [17].
При диареях различного генеза используют диоктаэдрический смектит (классификация по АТХ – А07ВС) на основе широко распространенного глинистого минерала [18–21]. В России и странах СНГ в стандарты лечения различных заболеваний ЖКТ с диареей включен адсорбирующий кишечный лекарственный препарат Энтеросгель (классификация по АТХ – А07В) [6, 14, 15, 22–31].
Активное действующее вещество Энтеросгеля – полиметилсилоксана полигидрат – гелевидное кремнийорганическое соединение [32]. Гель диспергирован в воде до частиц размером не более 300 мкм. Препарат представляет собой суспензию, в которой твердая фаза представлена двухмерными частицами (листы) [33] с пористой глобулярной структурой [32–36]. Поверхность глобул гидрофобна благодаря избытку метильных групп на их поверхности [32, 35–37]. Суспезия Энтеросгеля характеризуется высокой вязкостью [33], что позволяет прочно связывать и удерживать поглощенные субстраты. Энтеросгель не всасывается в кровь и действует только в просвете ЖКТ.
Гелевидная структура Энтеросгеля и свойства гелеобразующей матрицы определяют его поглотительные и защитные свойства. Пористая структура Энтеросгеля обеспечивает поглотительную способность по механизму молекулярной адсорбции и позволяет преимущественно адсорбировать среднемолекулярные токсические вещества (например, билирубин, продукты распада белков). Гелевидной структурой обусловлены:
- поглощение высокомолекулярных токсических веществ (белки, бактериальные токсины) по механизму соосаждения или абсорбции в объем геля [35];
- защитные свойства (эластичные гелевидные частички препарата образуют защитный слой и предохраняют ткани от воздействия различных повреждающих факторов).
Энтеросгель обеспечивает восстановление поврежденного кишечного барьера и местного иммунитета [38, 39].
Энтеросгель связывает эндотоксин грамотрицательных бактерий (липополисахарид (ЛПС)) [35, 36]. Таким образом, Энтеросгель восстанавливает структуру микроциркуляторного русла и регенераторные процессы в слизистой оболочке. Это в свою очередь приводит к восстановлению регенерации кишечного барьера, его регуляторных функций, а также физиологического уровня ЛПС в крови. Восстановление физиологического уровня провоспалительных цитокинов, вероятно, приводит к нормализации процессов секреции [14, 40–42].
Исходя из этих характеристик мы предположили, что применение препарата Энтеросгель в конвенциональной терапии при неинфекционных диареях различного генеза снижает частоту дефекаций и длительность стационарного лечения.
Цель открытого рандомизированного контролируемого проспективного исследования состояла в оценке эффективности и безопасности энтеросорбента полиметилсилоксана полигидрата (Энтеросгеля) при лечении пациентов с неинфекционными заболеваниями, протекающими с диареей.
Материал и методы
С февраля по август 2017 г. в отделениях Центра гастроэнтерологии и гепатологии многопрофильного стационара лечение получили 62 пациента (65% мужчин, 35% женщин) с синдромом диареи неинфекционного генеза препаратом Энтеросгель.
Критерии включения в исследование: клиническое проявление в виде нарушения характера стула – диарея, возраст старше 18 лет.
Критерии исключения из исследования: инфекционные заболевания, клинические, лабораторные (положительный анализ кала на токсины А и В Clostridium difficile) и инструментальные признаки псевдомембранозного колита.
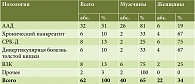
Распределение пациентов по нозологическим формам представлено в табл. 4.
Среди нозологий лидировала антибиотикоассоциированная диарея (ААД) – 51% случаев (26 мужчин, средний возраст 62,7 года, и 6 женщин, средний возраст 59,8 года). СРК-Д и ВЗК (язвенный колит) наблюдались в 13% случаев. ВЗК чаще регистрировались у мужчин (75%), СРК-Д – у женщин (75%). Средний возраст мужчин с СРК-Д составил 36,5 года, женщин – 39,3 года. При ВЗК аналогичные показатели составили 47,2 и 35,3 года соответственно. Дивертикулярная болезнь и хронический панкреатит с внешнесекреторной недостаточностью диагностированы с одинаковой частотой – 10%, причем и дивертикулярная болезнь, и хронический панкреатит чаще имели место у женщин – в 67% (средний возраст женщин с дивертикулярной болезнью – 79 лет, мужчин – 78, при хроническом панкреатите аналогичные показатели составили 70,5 года и 65 лет соответственно).
Кроме того, в исследование были включены 56 пациентов с неинфекционной диареей, которые ранее получали лечение в нашем многопрофильном стационаре и которым в схеме комплексного лечения назначали смектит, и 55 пациентов, не принимавших энтеросорбенты.
Всем пациентам проводилось рутинное обследование, которое включало сбор жалоб, анамнеза, физикальных данных, определение сопутствующих заболеваний, а также общеклинические анализы крови и мочи, биохимический анализ крови, исследование острофазовых реакций (скорость оседания эритроцитов, С-реактивный белок, фибриноген), посев кала на возбудители кишечных инфекций, исследование сыворотки крови для определения кишечного эндотоксина, ультразвуковое исследование органов брюшной полости, кишечника, по показаниям – компьютерная томография органов брюшной полости с болюсным усилением или контрастированием кишечника, гастроскопия, илеоколонокопия с биопсией, ирригоскопия. После установления диагноза проводилась патогенетическая и симптоматическая терапия, согласно принятым для данной нозологической формы стандартам.
Пациентам с ААД назначали ванкомицин 1–2 г/сут и/или метронидазол 1–1,5 г/сут в зависимости от тяжести состояния. При дивертикулярной болезни толстой кишки в случае развития клинических симптомов, в том числе диареи, пациенты получали рифаксимин 800 мг/сут и/или метронидазол 1 г/сут. При язвенном колите применялись месалазин 3–4 г/сут, гидрокортизон 250 мг/сут ректально, при обострении ХП – ингибиторы протонной помпы, ферментные препараты (в средней дозе 60–75 тыс. ед/сут). При наличии избыточного бактериального роста назначались пре- и пробиотики, при спастической боли – спазмолитики. В случае развития тяжелой интоксикации, при эксикозе, синдроме мальабсорбции проводилась инфузионная заместительная и дезинтоксикационная терапия (парентеральное питание, инфузии растворов альбумина, электролитов, глюкозы).
Пациенты основной группы применяли Энтеросгель по 1 столовой ложке 3 раза в день между приемами пищи, пациенты 2-й группы – смектит по 2 пакета 3 раза в день между приемами пищи. Пациенты контрольной группы энтеросорбенты не использовали (табл. 5).
Результаты и их обсуждение
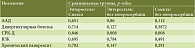
В результате проводимого лечения удалось добиться снижения частоты стула у пациентов независимо от генеза диареи. Тем не менее при использовании энтеросорбентов клинический эффект, как правило, достигался быстрее: при ААД – на 13-е сутки (без энтеросорбентов – на 17-е сутки), при дивертикулярной болезни – на 12–13-е сутки (без энтеросорбентов – на 16-е сутки), при хроническом панкреатите – на 9–10-е сутки (без энтеросорбентов – на 12-е сутки). Различия статистически достоверны (p < 0,05). Наилучший эффект отмечался при СРК-Д: спустя 9 дней лечения Энтеросгелем или Смектой удалось практически нормализовать стул (в отсутствие энтеросорбентов частота стула до одного-двух раз в сутки снижалась на 14-й день). У пациентов с ВЗК использование энтеросорбентов не способствовало более быстрой нормализации стула.
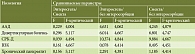
Статистическую обработку полученных результатов проводили с помощью однофакторного дисперсионного анализа. Различия в длительности госпитализации с применением энтеросорбции и без нее оказались статистически значимы в группах больных с ААД, дивертикулярной болезнью, СРК (табл. 6 и 7).
В отношении показателей в группах Энтеросгеля и смектита диоктаэдрического значимые отличия отсутствовали.
Заключение
Неинфекционная диарея часто встречается в практике врача многопрофильного стационара. Различные механизмы развития диареи, как правило, тесно связаны и дополняют друг друга.
Неинфекционная диарея требует патогенетической терапии.
В алгоритме конвенционального лечения диареи важное место занимают энтеросорбенты. Благодаря своей структуре Энтеросгель является эффективным и безопасным препаратом для лечения диареи неинфекционного генеза.
Эффективность Энтеросгеля при неинфекционной диарее сопоставима с таковой диоктаэдрического смектита.
Применение Энтеросгеля в комплексной терапии неинфекционной диареи позволяет ускорить достижение клинического эффекта и сократить сроки госпитализации.
A.I. Pavlov, Zh.V. Fadina, A.O. Buyeverov
FSBI ‘3rd Central Military Clinical Hospital after A.A. Vishnevsky of Ministry of Defense of Russia᾿
FSAI of Higher Education ‘I.M. Sechenov First Moscow State Medical University᾿
SBI MH MO MONIKI after M.F. Vladimirsky
Contact person: Aleksandr Igorevich Pavlov, doctor-pavlov@mail.ru
Material and methods. The patients were randomly divided into 3 groups: 62 patients (group 1) were indicated Enterosgel at a standard dose of 1 tablespoon 3 times a day between meals, 56 patients (group 2) were treated with dioctahedral smectite, 51 patients (group 3) were not prescribed enterosorbents. According to the cause of diarrhoea, the patients of group 1 were distributed as follows: 32 patients had antibiotic-associated diarrhoea, 8 patients – with irritable bowel syndrome and diarrhoea (IBS-D) and 8 patients – with ulcerative colitis, 6 patients with diverticular disease and 6 patients – with exocrine pancreatic insufficiency, 2 patients with NSAID-induced enteropathy. The frequency of stool (the number of defecations during the day) and the duration of inpatient treatment (days) were evaluated. The results were then compared with those of patients from groups 2 and 3.
Results. The study has shown that the inclusion of Enterosgel into standard therapy of non-infectious diarrhoea, regardless of its cause, allows shortening the duration of treatment and contributes to faster stool normalization. The effectiveness of Enterosgel and dioctahedral smectite is comparable. The maximum effect was obtained when Enterosgel was used for the treatment of antibiotic-associated diarrhoea and IBS-D.
Conclusion. The obtained results of using enterosorbent Enterosgel in the treatment of non-infectious diarrhea of various origins prove the effectiveness of including Enterosgel into standard therapy of these diseases.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.