Место энтеросорбентов в терапии неинфекционной диареи
- Аннотация
- Статья
- Ссылки
- English







Диарейный синдром (ДС) нередко встречается при неинфекционных заболеваниях желудочно-кишечного тракта, приводя к потере трудоспособности лиц молодого возраста и утяжеляя состояние пожилых полиморбидных пациентов, способствуя таким образом декомпенсации функционирования основных органов и систем. У госпитализированных пациентов диарея является фактором, приводящим к увеличению длительности и стоимости стационарного лечения. В связи с этим неинфекционные заболевания, протекающие с ДС, являются значимой медико-социальной и экономической проблемой. В комплексной терапии ДС применяются препараты разных групп, одной из которых традиционно являются энтеросорбенты (ЭС). В медицинской литературе имеется множество доказательств эффективности их применения при указанных нозологиях [1–10], что позволило включить их в клинические рекомендации [11]. Однако патогенетическое и клиническое обоснование использования ЭС при таких заболеваниях, как дивертикулярная болезнь (ДБ), хронический панкреатит (ХП), воспалительные заболевания кишечника, антибиотик-ассоциированная диарея (ААД), требует дальнейшего изучения.
Кишечник служит естественным резервуаром грамотрицательной микрофлоры, основного источника эндотоксина (ЭТ). Благодаря барьерной функции кишечника в норме в кровоток проникает относительно небольшое количество ЭТ [12, 13]. При воспалении, кишечном дисбиозе повышается интестинальная проницаемость [14], увеличивается риск развития эндотоксемии и эндотоксиновой агрессии [15–18].
Несмотря на вероятную необходимость диагностики эндотоксемии, систематическое изучение ее уровня при заболеваниях, протекающих с ДС, и взаимосвязи концентрации ЭТ сыворотки крови с тяжестью диареи в широкой клинической практике проводится редко. Одним из методов определения концентрации ЭТ в сыворотке крови является ЛАЛ-тест в различных модификациях. Логично предположить, что при диарее функционального происхождения уровень ЭТ ниже, чем при заболеваниях, протекающих с воспалением кишечной стенки. Однако мы не нашли исследований, в которых бы ЛАЛ-тест рассматривали в качестве маркера, позволяющего облегчить дифференциальную диагностику заболеваний кишечника.
Актуальным представляется подход к лечению ДС, направленный на предотвращение бактериальной транслокации и избыточного поступления ЭТ в системный кровоток. Воздействовать на уровень ЭТ в крови можно различными способами, один из них – это энтеральная детоксикация при помощи современных ЭС, которые эффективно связывают и выводят из организма эндогенные и экзогенные токсичные соединения, надмолекулярные структуры и клетки, а также используются в лечебных и профилактических целях [19]. Однако вопрос об эффективности применения ЭС для снижения эндотоксемии при неинфекционной диарее исследован недостаточно.
Цель исследования – изучение и сравнение эффективности препаратов Энтеросгель (полиметилсилоксана полигидрат, ПМСПГ) и диоктаэдрический смектит (ДЭС) для обоснования возможности и эффективности применения ЭС в комплексной терапии неинфекционной диареи, что впоследствии позволит расширить представления о взаимосвязи концентрации ЭТ сыворотки крови с патогенезом диареи, о влиянии применения ЭС на уровень ЭТ сыворотки крови при диарейном синдроме.
Материал и методы
В исследовании принял участие 171 пациент с неинфекционными заболеваниями органов желудочно-кишечного тракта, протекавшими с ДС различной степени тяжести. Пациенты находились на лечении в Центре гастроэнтерологии и гепатологии 3-го Центрального военного клинического госпиталя им. А.А. Вишневского в 2017–2018 гг. В исследовании после проведенного исключения участвовали 27 (15,7%) пациентов с синдромом раздраженного кишечника с диареей (СРК-Д), 16 (9,4%) – с ДБ толстой кишки, 24 (14,1%) – с язвенным колитом (ЯК), 16 (15,2%) пациентов с обострением ХП. Наибольшую часть составили пациенты с ААД различной степени тяжести – 88 (51,4%) человек.
Исследование было разделено на три этапа.
На первом этапе пациенты с ДБ, ААД, обострением ХП, ЯК и СРК-Д методом простой рандомизации были разделены на три группы в зависимости от проводимой медикаментозной терапии (с использованием ПМСПГ, ДЭС и без ЭС). Группы были сопоставимы по возрасту и характеру нозологии. Все пациенты получали терапию основного заболевания согласно рекомендациям Российской гастроэнтерологической ассоциации по соответствующей нозологии. Пациентам первой группы дополнительно назначали ПМСПГ по 15 г три раза в день в суточной дозе 45 г. Пациенты второй группы дополнительно к базовой терапии получали ДЭС по 3 г – три пакетика в день в суточной дозе 9 г. Пациентам третьей группы ЭС не назначали. Изучали влияние терапии на частоту стула и длительность госпитализации. Проводили сравнение эффективности ПМСПГ и ДЭС.
На втором этапе изучали уровень ЭТ сыворотки крови у 61 пациента с различными заболеваниями кишечника. Пациенты были разделены на две группы: в первую включены 34 человека с воспалительными изменениями слизистой оболочки (10 (29,4%) – с ЯК, 13 (38,1%) – с ДБ, 11 (32,3%) – с ААД); во вторую – пациенты с СРК-Д (27 человек). У пациентов, получавших в составе терапии ПМСПГ, определяли уровень ЭТ методом хромогенного ЛАЛ-теста по конечной точке. Проводили сравнение результатов теста у пациентов с заболеваниями, протекающими с воспалительными изменениями в слизистой оболочке толстой кишки, и при СРК-Д.
На третьем этапе исследования изучали влияние ПМСПГ на концентрацию ЭТ сыворотки крови в процессе проводимого лечения. Из 31 пациента, обследованного с помощью ЛАЛ-теста, у которого при первом заборе крови была выявлена эндотоксемия, сформировали две группы: в первой (17 человек) назначали ПМСПГ в комплексной терапии ДС, во второй, контрольной, группе (14 человек) не назначали ЭС. Всем пациентам ЛАЛ-тест выполняли дважды: при поступлении и при выписке.
Результаты и обсуждение
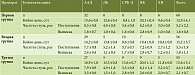
Длительность госпитализации пациентов первой (ПМСПГ) и второй (ДЭС) групп оказалась сопоставимой и значимо меньшей, чем в третьей (без ЭС) группе: 12,9 ± 4,1; 13,2 ± 3,7 и 15,6 ± 3,1 койко-дня соответственно. Частота стула при поступлении в стационар была сопоставима у пациентов всех групп и составляла 4,9 ± 1,9, в среднем 4–5 раз/сут. При выписке в первой и второй группах эта величина колебалась от 1 до 2,9 раз/сут, в третьей группе 1,5–2,6 раз/сут. У пациентов с ДБ, СРК-Д и ХП частота стула составила в группах с применением ЭС 1–1,5 раз/сут, а в третьей группе – 1,5–2,3 раз/сут, у пациентов с ААД – 1,8–2,4 (в третьей группе – 3,5 ± 0,6). У пациентов с ЯК, независимо от проводимой терапии, на момент выписки частота стула составила 2,8 ± 0,8 раз/сут.
Наилучший эффект достигнут у пациентов с СРК-Д: на 8,5 ± 0,2-е сутки терапии с применением ЭС удалось практически нормализовать стул (в отсутствие ЭС сокращение частоты стула до 1–2 раз в день отмечалось на 13,6 ± 0,7-е сутки, р < 0,05). Эффективность ПМСПГ при лечении неинфекционной диареи сопоставима с эффективностью ДЭС. В то же время у пациентов с ЯК назначение в комплексной терапии ЭС существенно не повлияло на достижение клинического эффекта – урежения стула и сокращения койко-дня. Сравнительные данные по частоте стула и длительности госпитализации при назначении различных ЭС и без их применения представлены в табл. 1.
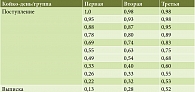
В связи с тем что время пребывания в стационаре и диапазон изменения частоты стула в этот период по нозологиям в группах пациентов значимо различались, для проведения обобщенного анализа изменения частоты стула была построена математическая модель. В табл. 2 представлены усредненные значения динамики частоты стула.
На рисунке 1 представлена математическая модель влияния применения ЭС в комплексной терапии диареи неинфекционного генеза для всех исследуемых нозологий.
В таблице 3 представлено процентное соотношение длительности койко-дня у пациентов, получавших ДЭС и ПМСПГ, по сравнению с пациентами, не получавшими ЭС.
Таким образом, использование ЭС – ПМСПГ и ДЭС в комплексной терапии ДС при ААД, ДБ, ХП и СРК-Д является эффективным и целесообразным. При сравнении этих показателей видно, что наилучший эффект достигнут при лечении СРК-Д: применение ПМСПГ на 38%, а ДЭС на 36% сокращает длительность пребывания пациента с СРК-Д в стационаре (р < 0,05). Эти данные совпадают с данными Е.И. Ткаченко (2015) [20]. На основании этих данных представляется возможным расширить показания для применения ЭС и оправданно включить эту группу препаратов в стандарты лечения вышеуказанных заболеваний. При этом эффективность ЭС при лечении пациентов с ЯК не установлена.
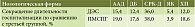
При заболеваниях, сопровождающихся воспалительными изменениями слизистой оболочки толстой кишки, методом ЛАЛ-тест в 77,4% случаев была выявлена гиперэндотоксемия, в то время как при дисфункции кишечника – только в 25,9% случаев.
Таким образом, ЛАЛ-тест может быть использован в качестве дополнительного маркера при дифференциальной диагностике заболеваний кишечника, протекающих с воспалительными изменениями в слизистой оболочке толстой кишки и преимущественно функционального характера. В таблице 4 представлены результаты ЛАЛ-теста пациентов при поступлении.
После выявления гиперэндотоксинемии были сформированы две группы пациентов, у которых по результатам проведенного лечения с помощью ЛАЛ-теста определяли уровень ЭТ. В первую группу вошли 17 пациентов, получавших ПМСПГ, во вторую (контроль) – 14 пациентов, не получавших ЭС.
На рисунках 2–5 показано, как в зависимости от проводимой терапии изменялся уровень ЭТ в сыворотке крови при различных нозологических формах.
Таким образом, в процессе лечения по мере купирования клинической симптоматики уровень ЭТ у большинства пациентов нормализовался. Использование ПМСПГ способствовало снижению эндотоксемии у большего количества пациентов. В первой группе нормализация ЭТ наблюдалась у 12 (70,6%) пациентов, во второй – у 5 (35,7%) пациентов. Однако у некоторых пациентов (с ААД), несмотря на разрешение диареи, уровень ЭТ был выше референсных значений. В таблице 5 представлены результаты влияния терапии на эндотоксемию.
Выводы
- Использование энтеросорбентов в комплексной терапии неинфекционных заболеваний (антибиотик-ассоциированная диарея, хронический панкреатит, дивертикулярная болезнь, синдром раздраженного кишечника с диареей), протекающих с диарейным синдромом различной степени тяжести, позволяет сократить частоту стула и длительность стационарного лечения на 1,89–3,26 суток в зависимости от нозологической формы (p < 0,05), в связи с чем является эффективным и целесообразным. Использование энтеросорбентов при лечении язвенного колита не оказывает влияния на длительность пребывания в стационаре. Наибольшую эффективность показало применение энтеросорбентов при лечении СРК-Д: койко-день при использовании полиметилсилоксана полигидрата сократился на 38%, диоктаэдрического смектита – на 36%. Эффективность полиметилсилоксана полигидрата и диоктаэдрического смектита в комплексной терапии неинфекционных диарей различного генеза является сопоставимой.
- При заболеваниях ЖКТ неинфекционного генеза с диарейным синдромом, сопровождающихся воспалительными изменениями слизистой оболочки, в 77,4% случаев имеет место повышенный уровень эндотоксина от 1,0 до 3,6 EU/ml (р < 0,05). СРК-Д не сопровождается повышением уровня эндотоксина у 76,7% пациентов (средние показатели ЛАЛ-теста – 0,8 ± 0,4 EU/ml).
- Использование полиметилсилоксана полигидрата в комплексной терапии диарейного синдрома приводит к снижению концентрации эндотоксина сыворотки крови. Клиническая эффективность использования полиметилсилоксана полигидрата, в частности, обусловлена его способностью снижать уровень эндотоксина в сыворотке крови до нормальных значений.
Zh.V. Fadina, A.I. Pavlov, PhD, A.V. Khovanov, PhD
3rd Central Military Clinical Hospital named after A.A. Vishnevsky, Krasnogorsk
Moscow State University of Food Production
LLC "TNK SILMA", Moscow
Contact person: Alexander I. Pavlov, doctor-pavlov@mail.ru
The article highlights the methods of treating diarrhea in non-infectious diseases of the gastrointestinal tract.
In particular, the effectiveness of using modern enterosorbents – polymethylasiloxane polyhydrate and dioctahedral smectite in complex pathogenetic therapy. The interrelation of endotoxemia with the pathogenesis of diarrheal syndrome was disclosed, and the LAL-test (methods for determining blood serum endotoxin) was proposed as additional criteria for functional and inflammatory diarrhea. In addition, the effect of the use of the polymethylsiloxane polyhydrate on endotoxemia has been shown.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.