Дополнительные методы функциональной и визуализационной диагностики головного мозга для планирования персонифицированной помощи неврологическому пациенту
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. В исследовании участвовали 50 больных с основным синдромом в виде головокружения с подтвержденными рентгенологически дегенеративно-дистрофическими изменениями в шейном отделе позвоночника и аномалией Киммерле, которым проведена ультразвуковая допплерография, и 120 пациентов, перенесших острый ишемический инсульт, которым выполнены клинико-нейровизуализационные исследования, включая магнитно-резонансно-томографическую нейроморфометрию с трактографией, и 40 лиц без диагностированных заболеваний нервной системы (группа контроля). Возрастной диапазон – от 46 до 89 лет, мужчин – 47%, женщин – 53%.
Результаты. Получены количественные показатели кровотоков и фракционной анизотропии, которые в дальнейшем могут рассматриваться в качестве референтных. Показана гемодинамическая значимость различий между пациентами и лицами контрольной группы. Дана оценка результатов ротационной пробы при дегенеративно-дистрофических изменениях в шейном отделе позвоночника и аномалии Киммерле по динамике Vmax кровотока. Представлен клинический случай с нейроморфометрическими магнитно-резонансно-томографическими данными.
Заключение. Дополнительные методы ультразвуковой и нейровизуализационной диагностики головного мозга могут применяться в ежедневной врачебной практике при ведении пациентов с различными цереброваскулярными заболеваниями для планирования персонифицированной помощи с учетом показателей, полученных в данном исследовании.
Материал и методы. В исследовании участвовали 50 больных с основным синдромом в виде головокружения с подтвержденными рентгенологически дегенеративно-дистрофическими изменениями в шейном отделе позвоночника и аномалией Киммерле, которым проведена ультразвуковая допплерография, и 120 пациентов, перенесших острый ишемический инсульт, которым выполнены клинико-нейровизуализационные исследования, включая магнитно-резонансно-томографическую нейроморфометрию с трактографией, и 40 лиц без диагностированных заболеваний нервной системы (группа контроля). Возрастной диапазон – от 46 до 89 лет, мужчин – 47%, женщин – 53%.
Результаты. Получены количественные показатели кровотоков и фракционной анизотропии, которые в дальнейшем могут рассматриваться в качестве референтных. Показана гемодинамическая значимость различий между пациентами и лицами контрольной группы. Дана оценка результатов ротационной пробы при дегенеративно-дистрофических изменениях в шейном отделе позвоночника и аномалии Киммерле по динамике Vmax кровотока. Представлен клинический случай с нейроморфометрическими магнитно-резонансно-томографическими данными.
Заключение. Дополнительные методы ультразвуковой и нейровизуализационной диагностики головного мозга могут применяться в ежедневной врачебной практике при ведении пациентов с различными цереброваскулярными заболеваниями для планирования персонифицированной помощи с учетом показателей, полученных в данном исследовании.



Введение
Среди пациентов, обращающихся за помощью к неврологу в России и Узбекистане, большинство пациентов с болевым синдромом. Кроме того, частой причиной обращения к неврологу являются двигательные и когнитивные расстройства. Особое место занимают больные с головокружением [1, 2].
Традиционно головокружение подразделяют на системное и несистемное [3]. Системное головокружение зачастую характеризуется острым дебютом и крайне выраженными клиническими проявлениями, что вынуждает пациента обращаться за экстренной и неотложной медицинской помощью [4, 5]. Установление причины системного головокружения нередко становится клинической дилеммой для врача приемного отделения и сопровождается ошибками [6, 7]. Эти ошибки обусловлены как объективными причинами, например гетерогенностью феномена головокружения, низкой степенью информативности инструментальных и лабораторных методов исследования, возможностью сочетания нескольких форм головокружения, так и субъективными – недостаточной информированностью врачей о причинах головокружения, неполноценным объективным осмотром, неиспользованием специфических вестибулярных диагностических тестов [8–10]. Крайне важно исключить потенциально жизнеугрожающие заболевания с поражением центральной нервной системы, такие как инсульт, аномалии краниовертебрального перехода, объемные образования, инфекционные и токсические поражения [11–14]. Необходимо дифференцировать центральные и периферические варианты головокружений.
Считается, что фактором изменения кровотока головного мозга более чем на 50% является патология внечерепных отделов центральных сосудов головы и оптимальная работа головного мозга обеспечивается адекватным притоком крови по брахиоцефальным сосудам. Постоянное поддержание кровотока головного мозга в пределах 50–55 мл на 100 г паренхимы мозговой ткани в одну минуту в области полушарий и 33 мл на 100 г мозговой ткани в одну минуту в области мозжечка необходимо для физиологичного течения обмена мозговой ткани.
Согласно данным литературы, острое нарушение мозгового кровообращения (ОНМК) может быть ошибочно не диагностировано у 35% пациентов в приемном отделении [15–17]. Пациенты, перенесшие ОНМК, представляют отдельную категорию неврологических больных, для которых первоочередными являются вопросы персонифицированной реабилитационной помощи. Для формирования алгоритма оказания такой помощи нужно определиться с прогнозом двигательных исходов. Сегодня имеется возможность использовать в этих целях диффузионно-тензорную магнитно-резонансную томографию [18].
Цель – определить роль дополнительных функциональных и визуализационных методов в диагностике цереброваскулярных заболеваний и для планирования персонифицированной помощи неврологическим пациентам с патологией экстра- и интрацеребральных сосудов на примере ультразвуковых и томографических исследований.
Материал и методы
Для участия в исследовании были отобраны 50 пациентов с жалобами на головокружение, у которых рентгенологически подтверждены дегенеративно-дистрофические изменения в шейном отделе позвоночника и которые находились на стационарном лечении в неврологическом отделении Самаркандского городского медицинского объединения, и 120 пациентов, перенесших ОНМК в виде ишемических инсультов, подтвержденных клинически и с помощью компьютерной томографии, наблюдавшихся в клинике Башкирского государственного медицинского университета (Уфа). Возраст пациентов составил 46–89 лет (47% мужчин, 53% женщин). Применялись общеклинические, клинико-неврологические, транскраниальные допплерографические, рентгенографические и магнитно-резонансно-томографические в различных режимах с построением пирамидных трактов (трактография) методы обследования.
Выполнено ультразвуковое исследование (УЗИ) сосудов шейного отдела: методом цветового дуплексного сканирования оценивались показатели скорости кровотока в субокципитальном участке позвоночной артерии (ПА). Визуализация позвоночных артерий проводилась на аппарате ESoate Mylab class C (Италия) секторным датчиком с частотой 2–8 МГц.
Для оценки нормальных параметров сосудов вертебробазилярного бассейна (ВББ) и трактографии анализировались данные добровольцев (по 20 в каждой подгруппе) без патологии и каких-либо жалоб с аналогичным распределением по полу и возрасту.
В когорте, в которой проводилось ультразвуковое сосудистое исследование, считали, что позвоночная артерия подразделяется на четыре отдела: первый отдел – от устья до входа в костный канал поперечных отростков позвонка CVI; второй отдел – в канале поперечных отростков от СVI до СII2; третий отдел – от выхода из канала поперечного отростка СII до входа в череп через большое затылочное отверстие; после выхода из поперечного отростка СII вертебральная артерия изгибается кзади и кнаружи, проходит до поперечного отростка СI, через него и делает изгиб дугообразного характера, называемый петлей СI. Ротация головы относительно шейных позвонков выполняется петлей СI. Расстояние от входа ПА через большое затылочное отверстие до слияния с другой ПА в непарную, базилярную артерию образует интракраниальный отдел вертебральной артерии, то есть четвертый отдел. Обследование третьего отдела выполняли с помощью линейного датчика с частотой 5–7,5 МГц, а четвертого отдела – секторным датчиком с частотой 2–5 МГц. В ходе исследования обеспечивался трансокципитальный доступ. При этом больной сидел или лежал на животе с максимально согнутой вперед шеей. Транскраниальную допплерографию проводили с помощью системы EDAN instruments, версия 1.2, с использованием фазированного датчика частотного диапазона 2–8 МГц.
Атлантовый сегмент ПА имеет особенности траектории в различных сечениях, то есть четыре изгиба, создающих определенные сложности при выведении этого отдела специалистом УЗ-диагностики по всей его длине в одной плоскости УЗИ. При исследовании разграничивали два отдела: проксимальный, или вертикальный, расположенный в промежутке поперечных отростков СI и СII, и дистальный, или горизонтальный, расположенный между поперечным отростком СI и большим затылочным отверстием.
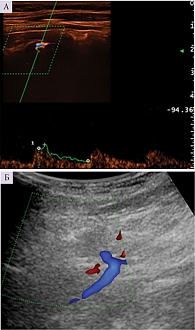
Для визуализации V3- и V4-сегментов ПА в процессе исследования больной находился в горизонтальном положении (лежа на животе) с упором на лоб. Датчик аппарата проецировали между контуром грудино-ключично-сосцевидной мышцы сзади и остистыми отростками CI–СII-позвонков так, чтобы сечение сканирования было выполнено перпендикулярно продольной оси позвоночника. Датчик наклоняли так, чтобы сечение сканирования проецировалось через атлантоокципитальное сочленение и наружную часть большого затылочного отверстия. Таким образом лучше визуализируется конечный отдел V3-сегмента вертебральной артерии от поперечного отростка СI до входа в полость черепа, огибающей на своем пути наружную массу СI, проходящей в одноименном углублении. Этот сегмент артерии на экране выглядит как подкова. Далее при продольном сканировании шеи датчик поворачивали на 90° и выставляли параллельно заднему контуру грудино-ключично-сосцевидной мышцы непосредственно под затылочной костью головы так, чтобы сечение проецировалось параллельно продольной оси позвоночника. В таком виде визуализируется начальный отдел V3-сегмента вертебральной артерии между поперечными отростками CI–СII-позвонков. На экране монитора этот участок сосуда выглядит S-образно (рис. 1).
Общее состояние кровообращения при допплерографии оценивали по качественным и количественным параметрам. К качественной оценке относятся характер звукового допплеровского сигнала, форма допплерограммы, распределение частот в допплерограмме. Допплерограмма при выполнении транскраниальной допплерографии (ТКДГ) позволяет очень точно изучить динамику кровообращения, поскольку при изменениях кровообращения вид спектрограммы претерпевает выраженные изменения. Из качественных показателей были анализированы изначальный максимальный подъем кривой, который соответствовал пиковой систолической скорости (Vmax, см/с), точка кривой, которая предшествовала последующему циклу и соответствовала конечной диастолической скорости (Vmin, см/с). Вырезка, обратный поток на ранней диастоле и отсутствие кровотока в конечной диастоле являются качественными показателями допплеровской спектрограммы.
Количественная оценка заключалась в определении максимальной (Vmax, см/с), средней (Vmean, см/с) и минимальной (конечно-диастолической – Vmin, см/с) скоростей кровотока. Конечная диастолическая скорость (Vmin) определялась периферическим сосудистым сопротивлением. Оцениваемые критерии зависят от угла наклона датчика относительно траектории кровотока. Во время исследования наклон датчика устанавливали так, чтобы иметь выраженную насыщенность отображения спектрограммы, достигаемую при показателях угла приблизительно 45°. Далее это значение угла использовали при расчете указанных параметров.
Чтобы подсчитать количественные критерии кровотока, которые не зависят от угла наклона датчика, применяли конкретные индексы:
- индекс циркуляторного сопротивления RI = (Vmax - Vmin)/Vmax (Pourcelot Index, индекс Пурсело);
- индекс пульсации РI = (Vmax - Vmin)/Vmean (Goesling Index, индекс Геслинга).
Показатели динамики кровообращения в вертебральных артериях изучали, когда пациент находился в горизонтальном положении (лежа на животе), вначале при положении головы лицом вниз, далее при максимальном повороте вправо и затем при максимальном повороте влево. Изменения параметров кровотока при пробах оценивали путем расчета коэффициента реактивности (КР, %) по формуле:
(ПРП/ДП - 1) × 100,
где ПРП и ДП – данные показателя после ротационной пробы и при положении головы лицом вниз (до пробы).
Результаты
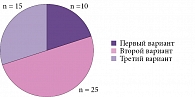
Пациентов с головокружением на основании ультразвукового допплерографического исследования (УЗДГ) в зависимости от состояния кровотока по позвоночной артерии разделили на три подгруппы (рис. 2):
- показатели линейной скорости кровотока (ЛСК) в позвоночной артерии в пределах нормы;
- асимметрия ЛСК по одной из позвоночных артерий;
- двустороннее снижение кровотока по позвоночной артерии.
Первый вариант (кровоток в пределах нормы) отмечался у десяти больных, у 7 (70%) из них имелись клинически выраженные болевые проявления, которые врачи трактовали как мышечно-тонические и вероятно обусловленные локальными проявлениями шейного остеохондроза. У 3 (30%) пациентов доминировали симптомы, обусловленные гемодинамическими нарушениями в ВББ.
Второй вариант (асимметрия кровотока по одной из позвоночных артерий от 20 до 80%) выявлен у 25 больных выборки. При этом 20–50%-ная асимметрия зарегистрирована у 18 (72%) пациентов. В 90% зарегистрированы клинические симптомы, обусловленные гемодинамическими нарушениями в ВББ.
Третий вариант (дефицит кровотока по обеим позвоночным артериям от 20 до 40%) диагностирован у 15 пациентов выборки. При этом 20–30% дефицита кровотока зафиксировано у 10 (66,6%) больных. В 14 (93,4%) случаях имели место клинические симптомы, обусловленные гемодинамическими нарушениями в ВББ.
Проведенное исследование позволяет сделать вывод, что выраженность клинических проявлений, связанных с гемодинамическими нарушениями в ВББ, в значительной степени обусловлена нарушением кровотока в позвоночных артериях, выявленным при выполнении УЗДГ.
При УЗИ ПА учитывали уровень входа ее в костный канал поперечных отростков позвонков, наличие извитости, гипоплазии, тип отхождения от подключичных артерий, диаметр в области петли атланта. ПА располагаются позади сонных артерий. В большинстве случаев их диаметр у лиц контрольной группы колебался в пределах 2,5–4,0 мм, в отдельных случаях достигал 5–6 мм, что согласуется с результатами ряда исследований. По данным других авторов, диаметр ПА в разных отделах колеблется от 2,3 до 4,5 мм с левой стороны и от 3,83 до 7,4 мм – с правой.
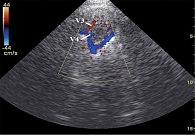
Далее нами было проведено обследование магистральных артерий головного мозга больных с использованием ультразвуковой ТКДГ с лоцированием экстра- и интракраниальных сосудов (рис. 3).
Оценка ТКДГ-сигнала проводилась в два этапа. На первом этапе оценивали огибающие спектральной характеристики сигнала. На втором этапе на основании оценки этих огибающих подсчитывали разные критерии кровотока. Допплеровская спектрограмма кровотока в ПА имела монофазный характер. Четко визуализировали медленное снижение скорости кровотока от максимальной в систоле к минимальной в конце диастолы.
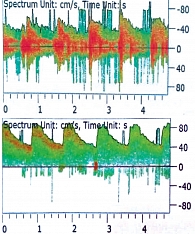
Главной особенностью допплерографического обследования является то, что амплитуда определяемого сигнала не всегда служит надежным критерием, поскольку зависит от множества параметров, не связанных со скоростью кровотока. Но выраженное видоизменение амплитуды получаемого сигнала, особенно при исследовании симметричных артерий, в общем информативно для диагностики. Именно поэтому при оценке допплеровского сигнала мы использовали критерии, взаимосвязанные с формой и амплитудой (рис. 4).
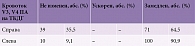
Данные ТКДГ позвоночных артерий V4-сегмента в покое и при проведении ротационной пробы пациентов контрольной группы представлены в табл. 1. Как видим, скоростные показатели при проведении ротационной пробы относительно снижены как в правой, так и в левой ПА в выборке пациентов. В то же время при неизмененных индексах RI и PI в правой ПА в левой отмечалось некоторое повышение этих показателей.
Данные описательной статистики общей выборки пациентов с головокружением при ТКДГ представлены в табл. 2. Для всех исследуемых параметров p ≤ 0,05, что соответсвует критерию достоверности ≥ 95%.
Изначально во всех группах показатели динамики скоростей кровотока в позвоночных артериях справа и слева сравнивались и из-за отсутствия между ними достоверных различий впоследствии оценивались суммарно. При положении головы лицом вниз данные регистрации кровотока в субокципитальном сегменте позвоночных артерий почти не различались между группами.
Исходя из данных, Vmax как справа, так и слева у обследованных пациентов с головокружением и дегенеративно-дистрофическими изменениями в шейном отделе позвоночника снижалась в систолической фазе (35,41 ± 1,63 и 30,74 ± 1,26 см/с). В то же время билатерально снижались диастолические показатели кровотока (Vmin) в V3- и V4-сегментах ПА (18,29 ± 0,97 и 15,97 ± 0,77 см/с соответственно). В результате возникала значительная разность амплитуды скоростей кровотока, чего не наблюдалось у лиц контрольной группы. При наличии сужения сосуда на допплерограмме контралатеральной стороны отмечались небольшое увеличение максимальной скорости, изменение формы волны потока крови. Это расценивалось как результат общей реакции обеих ПА при выраженном уровне компенсаторных, а также различных адаптирующих возможностей.
Сравнительный анализ результатов кровотока в обследуемых группах больных с головокружением и лиц контрольной группы показал незначительную, но отчетливую тенденцию к снижению скоростных показателей кровотока во всех сопоставляемых группах.
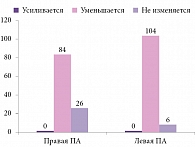
Обобщение результатов исследований V3- и V4-сегментов позвоночных артерий пациентов на ТКДГ (табл. 3) показало изменения кровотока: как в правой, так и в левой ПА преимущественно отмечалось замедление кровотока (64,5 и 90,9% соответственно). Ни в одном из наших наблюдений на патологической стороне ускорения кровотока не зафиксировано.
Основываясь на нормативных показателях кровотока в ПА по Цвибелю и данных контрольной группы, у обследуемых пациентов с головокружением определили снижение скорости кровотока различной степени выраженности (рис. 5). У пациентов с начальными проявлениями дегенеративно-дистрофических изменений в шейном отделе позвоночника гемодинамически значимых изменений скорости кровотока не выявлено: в V4-сегменте ПА средняя скорость кровотока составила 37,65 ± 3,07 см/с справа и 34,55 ± 2,94 см/с слева. У пациентов с диагностированными выраженными дегенеративно-дистрофическими изменениями в шейном отделе позвоночника и деформирующим спондилезом констатировали снижение кровотока в пределах нижней грани нормативных критериев: средняя скорость кровотока в V4-сегменте ПА составила 29,70 ± 3,15 см/с справа и 34,10 ± 3,37 см/с слева.
При невыраженных дегенеративно-дистрофических изменениях в шейном отделе позвоночника Vmean составила 37,0 ± 1,19 см/с справа и 30,39 ± 1,08 см/с слева, что, вероятно, компенсировалось противоположной позвоночной артерией, где скорости кровотока находились в пределах нормы. Выраженные дегенеративно-дистрофические изменения приводили к замедлению кровотока (справа 15,34 ± 0,62 см/с и слева 15,56 ± 0,62 см/с).
На следующем этапе обследуемым больным с головокружением выпоняли ротационую пробу, данные которой фиксировались методом ТКДГ. Данные описательной статистики общей выборки пациентов после ротационной пробы при ТКДГ представлены на рис. 5.
ТКДГ-исследование при поворотных пробах динамики кровотока в V3-, V4-сегментах ПА при спондилогенной вертебробазилярной недостаточности, обусловленной дегенеративно-дистрофическими изменениями в шейном отделе позвоночника, выявило уменьшение линейной скорости кровотока, идентичное при ипсилатеральном боковом вращении головы, особенно у пациентов с выраженными дегенеративно-дистрофическими изменениями.
Скоростные параметры кровообращения в вертебральных артериях при контралатеральном повороте значимо не отличались от соответствующих показателей при ипсилатеральной ротации головы, в результате чего во всех группах испытуемых они также были проанализированы суммарно.
Данные показателей гемодинамики в V3- и V4-отделах ПА в состоянии покоя соответствовали данным других авторов. Межгрупповые различия регистрировались по значению средней линейной скорости кровотока, но при этом динамика Vmean при ротации головы в сравниваемых группах имела тенденцию к снижению.
Просвет позвоночной артерии обычно не изменялся при атлантоаксиальной ротации, а сужение, как правило, индуцировалось экстравазальным воздействием или перегибом сосуда.
Использование магнитно-резонансно-томографической трактографии для диагностики и оптимизации выбора подходов при составлении персонифицированной реабилитационной программы рассмотрим на примере.
Клинический случай
Пациентка Д., 67 лет, с признаками ишемической болезни сердца планово была госпитализирована для проведения аортокоронарного шунтирования. Операция выполнена 9 октября 2023 г. в течение 75 минут, из них 26 минут использовалось искусственное кровообращение. На вторые сутки после проведенного вмешательства у пациентки появились признаки сенсомоторной дисфазии, по поводу чего экстренно выполнена компьютерная томография головного мозга. Ее результаты рентгенолог трактовал как «последствия перенесенных лакунарных инфарктов с обеих сторон, хроническую цереброваскулярную недостаточность, признаки заместительной гидроцефалии, атрофические изменения коры головного мозга». Данные об ОНМК по ишемическому типу на момент исследования отсутствовали.
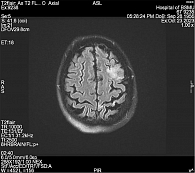
При осмотре пациентка жаловалась на сложности с подбором слов. В неврологическом статусе ведущие синдромы – легкий центральный правосторонний гемипарез, сенсомоторная дисфазия умеренной степени, патологические рефлексы Бабинского с обеих сторон. Оценка по шакалам для мониторинга пациентов с инсультом согласно клиническим рекомендациям Минздрава России: NIHSS – 18; LAMS – 3; Рэнкин – 5; Ривермид – 1. Установлен клинический диагноз: ОНМК по типу ишемического инсульта в бассейне левой средней мозговой артерии. Проведена магнитно-резонансная томография (МРТ), по результатам которой описаны зоны измененного сигнала в режимах DWI в левом полушарии головного мозга (ограничение диффузии) (рис. 6) и Т2 (рис. 7).
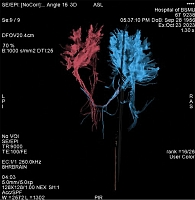
Далее нами была построена трехмерная модель кортикоспинального пути (трактография), результаты которой свидетельствовали о снижении количества проводящих путлей кортикоспинального тракта слева, что полностью соответствовало описанной выше клинической картине в виде правостороннего легкого центрального гемипареза (рис. 8).
В настоящее время нами продолжается работа по анализу данных магнитно-резонансно-томографических исследований пациентов, перенесших инсульт, с построением трехмерных моделей кортикоспинальных путей и расчетом показателей фракционной анизотропии. Выполняется также анализ данных компьютерно-томографических исследований головного мозга с морфометрией стратегических зон из числа церебральных структур, вовлечение которых может оказаться значимым для прогнозирования различных (прежде всего моторных и когнитивных) исходов после инсульта для разработки персонифицированных реабилитационных программ.
Обсуждение
Согласно данным УЗДГ, значимые изменения показателей гемодинамики при ротации головы у здоровых лиц контрольной группы не регистрировались. Вместе с тем у пациентов с вертебробазилярной недостаточностью при дегенеративно-дистрофических изменениях в шейном отделе позвоночника полученные данные указывали на значимое экстравазальное воздействие в V3- и V4-сегментах ПА при ротации головы в зависимости от варианта костной перемычки. Значения максимальной пиковой скорости при нейтральном положении головы и при поворотах не отличались у здоровых лиц, но степень снижения Vmax при поворотах головы у пациентов с дегенеративно-дистрофическими изменениями позвоночника была значительно больше. Кроме того, группы различались по количеству случаев снижения Vmax более 20% (р < 0,05).
Диагностически весомым критерием положительной ротационной пробы при УЗДГ является снижение пиковой скорости кровотока ≥ 20% по сравнению с кровотоком до ротации. Вероятность положительного теста относительно контрольной группы и встречаемость данных изменений в 7,5 раза больше у пациентов с вертебробазилярной недостаточностью и головокружением. По данным ТКДГ, у 72 (65,5%) больных из общего числа пациентов с синдромом позвоночной артерии обнаружены патологические изменения кровотока по ПА в виде асимметрии более 30% (сравнивали ЛСК справа и слева), отмечаемой, по некоторым данным, в 95,5% случаев при компрессионно-ирритативном эффекте вертеброгенного синдрома ПА.
При оценке результатов, выявленных при ТКДГ вертебральных артерий у всех больных со спондилогенной краниовертебральной недостаточностью, было подчеркнуто, что средние показатели величины критериев кровотока в V3-, V4-сегментах в целом существенно не отличались от референтных критериев в покое внутри групп. Выявленные достоверные изменения кровотока по ПА проявлялись прежде всего в снижении ЛСК, преимущественно в одной из ПА.
У лиц контрольной группы величина пиковой скорости кровотока при поворотной пробе, по данным УЗИ, несколько снижалась (в пределах 2%), преимущественно в левой ПА. У пациентов с аномалией Киммерле пиковая скорость кровотока значительно уменьшалась на стороне с костной перемычкой независимо от стороны поворота. Диагностическим порогом для выявления экстравазального воздействия на ПА является 20%-ное снижение пиковой скорости кровотока при поворотах головы.
Выраженность выявленных изменений зачастую зависела от продолжительности заболевания, когда отмечалось снижение показателей гемодинамики. По нашему мнению, это свидетельствовало об истощении компенсаторных механизмов регуляции гемодинамики в вертебробазилярной системе по мере прогрессирования заболевания, что нашло отражение в ряде работ других авторов.
Выводы
Результаты нашего исследования показали, что прохождение ПА через арку или сводчатое отверстие потенциально является причиной периодических нарушений в артериальном кровотоке, а также оказывает давление на периартериальное симпатическое сплетение, особенно во время вращения головы.
Сосудистые формы головокружений, описываемые в современной зарубежной и отечественной [19] литературе, должны быть дифференцированы. В России реализуются высококачественные исследовательские проекты по комбинации нейровизуализационных и ультразвуковых методик при ведении пациентов с различными заболеваниями центральной нервной системы [20, 21].
Таким образом, данные литературы и результаты наших исследований подтверждают ценность УЗИ, в частности ТКДГ, в диагностике нарушений гемодинамики в пределах труднодоступного краниовертебрального сочленения. В данной работе представлены цифровые результаты указанных тестов. Это позволяет говорить о том, что современные ультразвуковые технологии, особенно в сочетании с нейровизуализационными методиками, дают возможность качественно дополнить клинические методы дифференцирования причин нарушения функционирования структур головного мозга, на ранних этапах выявлять патологические изменения в просветах сосудов, оценивать гемодинамические параметры кровотока, проводить нейроморфометрические измерения для оценки состояния системы кровотока головного мозга и подбора персонифицированных методов помощи пациентам с различными цереброваскулярными заболеваниями.
Авторы благодарят Башкирский государственный медицинский университет, на базе которого поддерживается межвузовское международное сотрудничество с Самаркандским государственным медицинским университетом в рамках реализации программы стратегического академического лидерства «Приоритет-2030».
Конфликт интересов отсутствует.
N.Sh. Muzaffarova, S.Z. Khakimova, PhD, Prof., L.R. Akhmadeeva, PhD, Prof., D.E. Baikov, PhD, Prof., R.R. Gizatullin, G.A. Bulyakova
Samarkand State Medical Institute
Bashkir State Medical University, Ufa, Russia
Аcademy of Sciences of Bashkortostan Republic
Contact person: Leila R. Akhmadeeva, Leila_ufa@mail.ru
Modern ultrasound and neurovizualisation techniques are widely used for early and high-quality diagnosis of disorders of nervous system, including cerebrovascular diseases.
Material and methods. The study included 50 patients with dizziness and vertigo with degenerative disorders of the cervical vertebrae confirmed by X-ray and/or Kimmerle anomaly, all of them underwent ultrasonic dopplerography; 120 ischemic stroke survivor after tomographic brain imaging, including MRI-tractography; and 40 healthy volunteers as controls. Age range was from 46 to 89 years (47% men).
Results. The results of blood flow parameters and fractional anisotropy that we present here could be used as reference numbers; hemodynamic difference between patients and controls was significant. The results of rotation test in patients with degenerative vertebral disorders in the cervical spine and Kimmerle anomaly were evaluated following Vmax blood flow dynamics. A clinical observation with neuromorphometric MRI data is presented.
Conclusion. The discussed additional methods of cerebral ultrasound and neuroimaging diagnosis could be applied in every-day clinical practice by physicians working with patients suffering from cerebrovascular conditions for planning personalized management using the data from our study.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.