Эффективность и безопасность тройной антихеликобактерной терапии с добавлением висмута: кларитромицин vs джозамицин
- Аннотация
- Статья
- Ссылки
- English
Представлены результаты рандомизированного клинического исследования эффективности и безопасности кларитромицина и джозамицина в составе десятидневной тройной терапии с добавлением висмута трикалия дицитрата (ВТД) для эрадикации Helicobacter pylori.
Материал и методы. Пациенты с заболеваниями, ассоциированными с H. pylori, были рандомизированы на две группы: 60 больных первой группы получали омепразол (20 мг 2 раза в день), ВТД (240 мг 2 раза в день), амоксициллин (1000 мг 2 раза в день) и кларитромицин (500 мг 2 раза в день), 60 пациентов второй группы – омепразол, ВТД и амоксициллин в комбинации с джозамицином (1000 мг 2 раза в день). Наличие H. pylori подтверждено данными быстрого уреазного теста и/или 13С-уреазного дыхательного теста. Эффективность эрадикации оценивалась с помощью 13С-уреазного дыхательного теста.
Результаты. Эффективность антихеликобактерной терапии в первой и второй группах при ITT-анализе составила 70,0 и 75,0% (p = 0,540), при РР-анализе 82,4 и 84,9% (p = 0,752) соответственно. Нежелательные явления на фоне терапии в первой группе наблюдались чаще, чем во второй, – 47,5 против 31,0%.
Заключение. Эффективность схемы с джозамицином была не ниже, чем с кларитромицином, при меньшей частоте нежелательных явлений и лучшей переносимости.
Представлены результаты рандомизированного клинического исследования эффективности и безопасности кларитромицина и джозамицина в составе десятидневной тройной терапии с добавлением висмута трикалия дицитрата (ВТД) для эрадикации Helicobacter pylori.
Материал и методы. Пациенты с заболеваниями, ассоциированными с H. pylori, были рандомизированы на две группы: 60 больных первой группы получали омепразол (20 мг 2 раза в день), ВТД (240 мг 2 раза в день), амоксициллин (1000 мг 2 раза в день) и кларитромицин (500 мг 2 раза в день), 60 пациентов второй группы – омепразол, ВТД и амоксициллин в комбинации с джозамицином (1000 мг 2 раза в день). Наличие H. pylori подтверждено данными быстрого уреазного теста и/или 13С-уреазного дыхательного теста. Эффективность эрадикации оценивалась с помощью 13С-уреазного дыхательного теста.
Результаты. Эффективность антихеликобактерной терапии в первой и второй группах при ITT-анализе составила 70,0 и 75,0% (p = 0,540), при РР-анализе 82,4 и 84,9% (p = 0,752) соответственно. Нежелательные явления на фоне терапии в первой группе наблюдались чаще, чем во второй, – 47,5 против 31,0%.
Заключение. Эффективность схемы с джозамицином была не ниже, чем с кларитромицином, при меньшей частоте нежелательных явлений и лучшей переносимости.

Helicobacter pylori играет ведущую роль в этиопатогенезе ряда распространенных заболеваний. В разных регионах России H. pylori инфицировано от 60 до 90% взрослого населения [1]. Абсолютным показанием к эрадикации H. pylori являются язвенная болезнь желудка и двенадцатиперстной кишки, MALT-ома желудка, атрофический гастрит, резекция желудка по поводу рака желудка, а также наличие родственников первой степени родства, больных раком желудка, и желание инфицированного H. pylori пациента после консультации с доктором [2]. Эксперты IV Маастрихтского консенсуса рекомендовали эрадикацию H. pylori больным идиопатической тромбоцитопенической пурпурой, железодефицитной анемией неустановленной этиологии, при наличии дефицита витамина В12 и необходимости длительного приема ингибиторов протонной помпы [3].
Метаанализы и систематические обзоры демонстрируют, что наиболее часто назначаемая стандартная семидневная тройная схема терапии первой линии не позволяет достигать целевого уровня эффективности [4, 5]. Это связывают с формированием резистентности H. pylori к макролидам вследствие неуспеха ранее проводившегося лечения, а также широкого применения антибиотиков на популяционном уровне [6].
Включение в состав тройной терапии висмута трикалия дицитрата (ВТД) обеспечивает прирост эффективности примерно на 20% [7–9].
Наиболее частыми нежелательными явлениями приема кларитромицина являются горький вкус во рту, тошнота и диарея, потенциально снижающие приверженность, а значит, и эффективность лечения [10]. Поэтому изучается возможность замены макролида кларитромицина макролидом джозамицином, использование которого реже сопровождается развитием нежелательных явлений [11–13].
В Московском клиническом научно-практическом центре проведено рандомизированное клиническое исследование эффективности и безопасности кларитромицина и джозамицина в составе десятидневной тройной терапии, включавшей омепразол, амоксициллин и ВТД.
Исследование одобрено решением Локального этического комитета Московского клинического научно-практического центра 8 августа 2013 г. Материал и методы исследования
В исследовании участвовали 120 мужчин и женщин в возрасте от 18 до 65 лет с заболеваниями, ассоциированными с H. pylori, подписавшие информированное согласие.
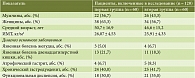
Всем больным проведено комплексное клиническое обследование, эзофагогастродуоденоскопия, выявление H. pylori с помощью быстрого уреазного теста и/или 13С-уреазного дыхательного теста. Пациенты были рандомизированы на две группы по 60 человек, сопоставимые по половозрастным характеристикам и нозологиям (табл. 1).
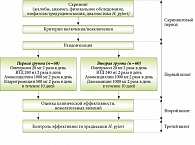
Пациенты первой группы получали омепразол (Ультоп) 20 мг 2 раза в день, ВТД (Де-Нол) 240 мг 2 раза в день, амоксициллин (Флемоксин Солютаб) 1000 мг 2 раза в день и кларитромицин (Клацид) 500 мг 2 раза в день. Больным второй группы назначались омепразол (Ультоп) 20 мг 2 раза в день, ВТД (Де-Нол) 240 мг 2 раза в день, Амоксициллин (Флемоксин Солютаб) 1000 мг 2 раза в день и джозамицин (Вильпрафен Солютаб) 1000 мг 2 раза в день. Длительность терапии в обеих группах составила 10 дней (рис. 1).
В процессе лечения пациенты вели дневники, в которых ежедневно отмечали факт приема препаратов, оценивали выраженность симптомов и фиксировали возможные нежелательные явления. На втором визите (11–12-й день после начала приема препаратов) оценивались клиническая эффективность лечения и возникновение нежелательных явлений. На третьем визите (не ранее чем через 30 дней после завершения приема препаратов) проводили контроль эффективности эрадикации H. pylori с помощью 13С-уреазного дыхательного теста.
Полученные данные были проанализированы с помощью статистического пакета StatSoft Statistica 6.0. Эффективность эрадикации H. pylori оценивали отдельно у всех пациентов, включенных в исследование и рандомизированных в группы (анализ intention-to-treat, ITT), и у пациентов, полностью закончивших лечение по протоколу (анализ per-protocol, PP).
Результаты
Лечение и обследование в соответствии с протоколом полностью завершил 51 пациент первой группы и 53 пациента второй.
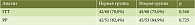
При ITT-анализе эффективность антихеликобактерной терапии составила 70,0% в первой и 75,0% во второй группе (p = 0,540). При PP-анализе эрадикация H. pylori была достигнута у 82,4 и 84,9% пациентов первой и второй группы соответственно (p = 0,752) (табл. 2).
Нежелательные явления были зарегистрированы у 28 пациентов (47,5%) первой группы и 18 пациентов (31,0%) второй группы (рис. 2). Возникновение диареи и горечи во рту у больных первой группы отмечалось чаще, чем у пациентов второй, – 35,1 против 17,2% и 15,8 против 6,9% соответственно.
Нежелательные явления явились основанием для досрочного прекращения лечения у 6 (10,0%) пациентов первой группы и у 3 (5,0%) пациентов второй группы.
Обсуждение
Проведенное нами рандомизированное клиническое исследование продемонстрировало сопоставимую эффективность десятидневных схем тройной терапии с добавлением ВТД, включавших как кларитромицин, так и джозамицин. При ITT-анализе эрадикация была достигнута у 70,0% пациентов, принимавших схему с кларитромицином, и у 75,0% пациентов, получавших в составе антихеликобактерной терапии джозамицин (p = 0,540). При PP-анализе антихеликобактерная терапия оказалась успешной в 82,4 и 84,9% случаев соответственно (p = 0,752).
Побочные эффекты терапии, в основном средние и легкие, чаще наблюдались (47,5 против 31,0%) и становились причиной досрочного прекращения лечения (10 против 5%) в первой группе.
В целом полученные результаты согласуются с данными литературы. Так, в недавно опубликованном китайском исследовании эффективность десятидневной тройной терапии с добавлением препарата висмута при ITT-анализе составила 77,4%, при PP-анализе – 87,0%. При этом эффективность лечения у пациентов с кларитромицин-резистентными штаммами H. pylori составила 82,4%, а у больных с кларитромицин-чувствительными штаммами – 94,4% [14]. Эти данные подтверждают возможность преодоления резистентности к макролидам с помощью добавления к схемам эрадикации ВТД.
В другом сравнительном исследовании изучали эффективность 14-дневной модифицированной квадротерапии, включавшей лансопразол, амоксициллин, ВТД и метронидазол или кларитромицин. Отмечалась высокая эффективность терапии в обеих группах: при РР-анализе – 96,9 и 94,9%, при ITT-анализе – 88,9 и 88,8% соответственно. Резистентность к кларитромицину повлияла на эффективность терапии: при наличии HP-чувствительных штаммов уровень эрадикации составил 98,6%, при наличии HP-резистентных штаммов – 76,9% (p = 0,001). Частота нежелательных явлений была выше в группе, получавшей метронидазол [14].
Эффективность десятидневной тройной терапии, включавшей пантопразол, амоксициллин, кларитромицин и висмута субцитрат в качестве терапии второй линии исследовалась в Иране. При ITT-анализе эрадикация наблюдалась у 79,2% пациентов, при PP-анализе – у 88,4%. Нежелательные явления отметили 51,2% больных, наиболее часто беспокоил горький вкус во рту (43,8%) [15]. Однако другими авторами из Ирана, изучавшими сходную четырехкомпонентную комбинацию в составе омепразола, амоксициллина, кларитромицина и висмута субцитрата в качестве терапии первой линии, были получены не такие хорошие результаты: 61,6% – при ITT-анализе и 67,2% – при PP-анализе [16].
Основными причинами снижения эффективности антихеликобактерной терапии являются формирование устойчивости H. pylori к антибиотикам (приобретенная антибиотикорезистентность) и недостаточная приверженность пациентов лечению – несоблюдение доз, режима и длительности приема препаратов [17]. Показано, что при неудаче тройной терапии первой линии вторичная резистентность к кларитромицину возрастает до 66%, фторхинолонам до 21% и метронидазолу до 62% [18].
Антибактериальный эффект макролидов, в том числе кларитромицина, обусловлен блокадой синтеза белка на рибосомальном уровне [19]. В многоцентровом исследовании первичной резистентности H. pylori к антибиотикам в 18 странах Европы, проведенном в 2008–2009 гг., с участием 2204 взрослых пациентов резистентность к кларитромицину составила 17,5%, к левофлоксацину – 14,1%, к метронидазолу – 34,9%. При этом частота выявления резистентности H. pylori к кларитромицину и левофлоксацину в странах Западной/Центральной и Южной Европы была достоверно выше (> 20%), чем в странах Северной Европы (< 10%) [6]. Согласно результатам бактериологического тестирования, в Санкт-Петербурге резистентность к кларитромицину составила 25%, к амоксицллину – 6,3%, к метронидазолу – 42,5%, к левофлоксацину – 27,1% [20].
Сказанное подчеркивает важность назначения схем, устраняющих инфекцию у подавляющего большинства больных. Доступным и эффективным способом оптимизации антихеликобактерной терапии является включение в ее состав ВТД. Ранее нами было показано, что десятидневная стандартная тройная терапия с включением кларитромицина обеспечивает эрадикацию лишь в 73,3%, в то время как добавление к этой комбинации висмута повышает эффективность лечения до 93,3% [11]. Сходные результаты опубликованы И.В. Маевым и соавт., отметившими успешную эрадикацию у 71,8% пациентов, получавших семидневную стандартную тройную терапию, и у 95,2% обследованных, принимавших эзомепразол, кларитромицин, амоксициллин и ВТД [11].
Эффективность схем терапии с джозамицином также определялась включением в нее ВТД: тройная терапия обеспечивала эрадикацию у 70,0% больных, в то время как при добавлении к препаратам тройной схемы ВТД она возрастала до 95,0% [13].
Заключение
Результаты проведенного нами рандомизированного клинического исследования свидетельствуют о достаточно высокой эффективности десятидневной тройной терапии с добавлением висмута трикалия дицитрата. Схема с джозамицином была не менее эффективна, чем с кларитромицином, при меньшей частоте нежелательных явлений и лучшей переносимости.
D.S. Bordin, O.B. Yanova, I.N. Voynovan, N.A. Shaposhnikova, Yu.A. Orobey, O.I. Berezina, O.I. Kovalyova, N.G. Kalashnikova, Ye.A. Dubtsova
Central Research Institute of Gastroenterology. Moscow Clinical Scientific and Practical Center of the Moscow Healthcare Department
Contact person: Dmitry Stanislavovish Bordin, d.bordin@mknc.ru
Aim. To compare the efficacy and safety of clarithromycin and josamycine in the triple therapy combined with BTD in H. pylori eradication Material and methods. 120 patients with H. pylori-associated diseases were randomized into two groups: 60 patients in the first group were treated with omeprazole (20 mg b.i.d.), BTD (240 mg b.i.d.), amoxicillin (1000 mg b.i.d.) and clarithromycin (500 mg b.i.d.) during 10 days; 60 patients in the second group took the same doses of omeprazole, BTD and amoxicillin in combinations with josamycin (1000 mg b.i.d.) during 10 days. Rapid urea test and/or 13C-UBT were used to detect presence of H. pylori before therapy. Efficacy of eradication was confirmed by 13C-UBT.
Results. The efficacy of eradication therapy in first and second groups was 70,0 and 75,0% ITT (p = 0,540) and 82,4 and 84,9% (p = 0,752) РР, respectively. Adverse events were more common in first group (47,5 vs 31,0%).
Conclusion. The effectiveness of the scheme with josamycin was not lower than with clarithromycin. The scheme with josamycin has lower frequency of adverse events and better tolerability.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.