Эффективность лечения нейропатических поражений нижних конечностей препаратами липоевой кислоты у больных сахарным диабетом
- Аннотация
- Статья
- Ссылки

Для пациентов СД типа 1 причиной развития диабетической нейропатии является длительность заболевания и уровень гликемии. Для больных СД типа 2 помимо перечисленных факторов значимо также гиперлипидемия и системная артериальная гипертония. Именно осложнения являются причиной высокой инвалидизации и смертности больных сахарным диабетом. Лечение осложнений сахарного диабета представляет большую медико-социальную проблему. В настоящее время клиническая медицина располагает целым арсеналом лекарственных средств для коррекции гипергликемии – главного виновника осложнений сахарного диабета. Для поддержания удовлетворительного течения сахарного диабета и достижения нормогликемии необходимы совместные усилия врача и больного. Изменить образ жизни, пересмотреть рацион питания, отношение к физическим нагрузкам, проводить ежедневный контроль уровня гликемии с самостоятельной коррекцией терапии часто – непосильная задача для больного. Избежать развития осложнений не удается. Фармакологическая наука постоянно ведет поиск лекарственных препаратов, препятствующих влиянию гипергликемии на ткани (эндотелий, нервная ткань). Использование этих препаратов в практической деятельности врача иногда является единственной возможностью избежать (или отсрочить) развитие тяжелых состояний.
Окислительный стресс – это один из наиболее важных факторов развития поздних осложнений сахарного диабета. Условиями для избыточного образования свободных радикалов являются: гипоксия, снижение антиоксидантной защиты, аутоокисление глюкозы, активизация полиолового шунта. Избыточная продукция кислородосодержащих свободных радикалов способствует окислению мембранных липидов в нервных клетках. Мишенью для свободных радикалов является и молекула NО, при окислении которой образуется высокотоксичное вещество ONOO (пироксинитрит). Усиливает деградацию NO повышенное образование супероксидного аниона – продукта окислительного стресса. При активизации полиолового шунта, у больных диабетом, резко снижается функция эндотелиальной NO-синтазы – фермента ответственного за синтез NO из L – аргинина. У здорового человека активность окислительного стресса ограничивается супероксиддисмутазой, каталазой, глутатионпероксидазой, витаминами Е, С, А и восстановленным глутатионом. При гипергликемии снижается активность гликированных ферментов, поэтому превалируют прооксидантные факторы. Современная фундаментальная наука ключевую роль в инициации повреждения эндоневрального кровотока отводит окислительному стрессу. В экспериментальной эндокринологии доказана эффективность влияния изосорбита нитрата (источник NO) на скорость проведения возбуждения по нервному волокну и улучшение эндоневрального кровотока.
Первую клиническую классификацию диабетической нейропатии предложил В.М. Прихожан (1981), описав центральную и периферическую (ПДН) ее формы, острые и хронические нарушения со стороны центральной и периферической нервной системы. В 1998 г. в Сан-Антонио была принята классификация, подразделяющая ДН на доклиническую и клиническую стадии. Эта классификация ориентирует врачей на возможность профилактических лечебных мероприятий. Клинические проявления диабетической полинейропатии (ДП) возникают, как правило, не ранее чем через 5 лет после манифестации СД типа 1. У пациентов, страдающих СД типа 2, проявления ДН выявляются одновременно с диагностированием заболевания. Явная форма ПДН проявляется у 50-70% больных. Электромиографическое исследование позволяет выявлять ПДН у 100% больных СД. Больные жалуются на онемение, боли в ногах, мышечную слабость, зябкость конечностей, парестезии. Симметрично нарушается температурная, тактильная и болевая чувствительность, развивается гипо- и арефлексия. Проявлением периферических вегетативных поражений является формирование трофических нарушений вплоть до язвенных дефектов тканей, нарушения потоотделения, изменения цвета кожных покровов и др. Нейропатическая боль – одно из самых сильных страданий больных СД, которое трудно поддается лечению.
Основным условием лечения и профилактики осложнений сахарного диабета является стойкая компенсация углеводного обмена. Но собственная врачебная практика показывает, что даже тщательный контроль гликемии не всегда препятствует развитию осложнений, и первыми проявлениями диабетических осложнений являются именно симптомы периферической нейропатии.
В последние годы препараты альфа-липоевой кислоты занимают ведущее место в метаболической терапии осложнений сахарного диабета. Альфа-липоевая кислота является коферментом пируватдегидрогеназного комплекса и участвует в окислительном декарбоксилировании пирувата и кетокислот в митохондриальном аппарате всех клеточных структур организма. R-изомер липоевой кислоты повышает периферический захват глюкозы и тем самым уменьшает инсулинорезистентность (D.E. Estrada et al., 1996). Назначение больным СД препаратов альфа-липоевой кислоты усиливает метаболизм глюкозы в мышцах и печени, повышает образование АТФ. SH-группы восстановленной формы альфа-липоевой кислоты предохраняют ферментные структуры клеток от окисления, усиливая собственную антиоксидантную защиту клеток. Отмечено воздействие липоевой кислоты на перекисное окисление липидов. Нейротропный эффект альфа-липоевой кислоты заключается в нормализации процессов гликолиза в нервном волокне, функции Nа+/K+ – АТФазы и повышении антиоксидантной защиты как непосредственно, так и через ферментные и витаминные механизмы. Повышается активность эндотелиальной NO-синтазы и синтез оксида азота, улучшается эндоневральный кровоток. Назначение альфа-липоевой кислоты повышает чувствительность сенсорных нейронов к фактору роста нервов (Kunt et al., 2000), тем самым восстанавливая структуру нерва и улучшая аксональный транспорт. Отмечено уменьшение активности Nf-kB-фактора, усиливающего в условиях окислительного стресса выработку вазоконстрикторов.
Было проведено несколько крупных исследований, посвященных эффективности и безопасности альфа-липоевой кислоты. Исследование ALADIN (Ziegler et al., 1995) позволило определить дозу альфа-липоевой кислоты с хорошим терапевтическим результатом. Наиболее эффективной оказалась инфузионная терапия в дозе 600 мг, при которой было отмечено улучшение периферической чувствительности (тепловой, температурной, тактильной, вибрационной). Исследование проводилось в течение трех недель и показало эффективность кратковременной терапии альфа-липоевой кислотой у больных с диабетической нейропатией.
В исследовании ALADIN II, которое проводилось в течение двух лет, оценивалось действие альфа-липоевой кислоты на течение диабетической периферической нейропатии. Препарат назначался орально по 600 и 1200 мг. Длительное назначение показало положительное влияние на течение диабетической периферической полинейропатии и безопасность при длительном назначении альфа-липоевой кислоты.
ALADIN III (1999) – рандомизированное, плацебо-контролируемое, двойное слепое исследование эффективности курсового применения альфа-липоевой кислоты в терапии периферической ДПН с участием 508 пациентов, которые были рандомизированы в 3 группы, сходные по клиническим характеристикам. В ходе исследования ALADIN III (1999) оценку эффективности терапии проводили с использованием показателей TSS. TSS используется для оценки степени выраженности ДПН в баллах по интенсивности наиболее часто встречающихся жалоб (боль, парестезии, онемение, жжение). Показатель TSS может колебаться от 0 (отсутствие симптомов) до 14. В ходе исследования ALADIN III (1999) не было отмечено статистически достоверного изменения показателей TSS между группами больных, получающих альфа-липоевую кислоту и плацебо как после 3-недельного курса внутривенной терапии, так и через 6 месяцев последующего лечения таблетированной формой в дозе 1800 мг/сутки. Статистически достоверные результаты улучшения течения ДПН были показаны при оценке объективных показателей.
В 2001 году в США и России проводилось исследование SYDNEY. Это моноцентровое, рандомизированное, двойное слепое, плацебо-контролируемое исследование, в котором были обследованы 120 больных с сахарным диабетом 1 и 2 типа, из которых 60 человек получали плацебо, 60 – α-липоевую кислоту (Тиоктацид). Проведено изучение влияния Тиоктацида на клинические проявления диабетической периферической полиневропатии, электромиографию, автономную дисфункцию у 60 больных с сахарным диабетом 1 и 2 типов. Показана высокая эффективность Тиоктацида в отношении большинства изученных показателей состояния периферических нервов, на основании чего сделан вывод о том, что Тиоктацид может быть с успехом использован для лечения диабетической невропатии.
Сегодня благодаря новой таблетированной форме препарата альфа-липоевой кислоты – Тиоктациду БВ (быстрого высвобождения), Плива Хрватска д.о.о., появилась возможность оказывать эффективную терапевтическую помощь больным сахарным диабетом с ДПН и в амбулаторных условиях. Изменение структуры и компонентов таблетированной формы позволило улучшить фармакокинетические свойства препарата. Тиоктацид БВ быстро и полностью всасывается из ЖКТ, и через 20-30 минут после приема достигается максимальная концентрация в крови, при этом, что очень важно – в нервном волокне (Packerl at al., 1999). Это отличает его от других препаратов альфа-липоевой кислоты. До настоящего времени чтобы оказать эффективную помощь больному с ДПН, была необходима госпитализация или посещение дневного стационара для 10-15 в/в введений препарата липоевой кислоты, и только после этого рекомендовалось продолжить терапию таблетированными формами. Тиоктацид БВ в дозе 1800 мг в сутки сопоставим с в/в введением 600 мг альфа-липоевой кислоты (Peter ft al., 1999). Недавние исследования, проводимые в мире по оценке влияния Тиоктацида БВ на течение ДПН, убедительно доказывают это.
Исследование ORPIL (Ziegler et al., 1999) – кратковременное, трехнедельное исследование с участием больных сахарным диабетом 2 типа с клиническими проявлениями диабетической полинейропатии. Больные получали Тиоктацид БВ перорально в дозе 1800 мг в сутки. В результате терапии было достигнуто достоверное улучшение субъективных симптомов (боль, онемение, парестезии, жжение и др.) и объективных показателей.
Клиническая эффективность суточной дозы 1800 мг альфа-липоевой кислоты при пероральном приеме (ORPIL) аналогична эффекту внутривенного введения 600 мг (АLАDIN I). Таким образом, можно сделать однозначный вывод о том, что концентрация препарата в плазме при обеих формах введения сопоставима.
Исследование SYDNEY II – многоцентровое, плацебо-контролируемое исследование для оценки влияния различных доз Тиоктацида БВ (600, 1200, 1800 мг) на клинические проявления ДПН. Оценка проводилась по шкале TSS. В результате проведенного исследования получены статистически достоверные положительные результаты во всех исследуемых группах. Разница заключается в сроках наступления терапевтического эффекта. При назначении 600 мг улучшение самочувствия отмечалось через три недели лечения, при назначении более высоких доз улучшение самочувствия наступало в более короткие сроки.
Исследование, проводимое в эндокринологическом диспансере города Москвы, оценивало влияние различных режимов перорального приема Тиоктацида БВ в терапии болевой формы диабетической дистальной нейропатии. Сравнивались результаты лечения Тиоктацидом БВ в дозе 1800 мг (по 600 мг 3 раза в сутки) в течение одного месяца и результаты, полученные в ходе лечения препаратом в дозе 600 мг в сутки в течение трех месяцев. Результаты оценивали с учетом жалоб больного, исследования вибрационной, тактильной и болевой чувствительности. В результате исследования отмечалось улучшение самочувствия больных, уменьшение боли. Пероральный прием Тиоктацида БВ в разных режимах дозирования положительльно влиял на течение ДПН, но меньшие дозы требовали более длительной терапии. Исследователи делают вывод о необходимости при выборе дозы индивидуального подхода к больным с ДПН. Доза препарата определяется степенью выраженности клинических симптомов.
В другом недавно проведенном исследовании в ЭНЦ под руководством проф. В.А. Петерковой исследовали эффективность и безопасность Тиоктацида БВ в дозе 1800 мг в сутки при лечении больных СД 1 типа с ДПН в возрасте от15 до19 лет. Исследование проводилось в течение трех недель. Для оценки результатов использовали шкалу TSS и шкалу неврологических нарушений (NDS по Янгу) с оценкой вибрационной, тактильной, температурной чувствительности и активности сухожильных рефлексов. Проводилось также электромиографическое исследование для оценки функционального состояния периферических нервов. Полученные результаты позволяют сделать вывод, что применение Тиоктацида БВ в дозе 1800 мг в сутки у подростков с СД 1 типа в течение трех недель позволило уменьшить клинические проявления полинейропатии, улучшить показатели температурной, тактильной и вибрационной чувствительности. Достоверно улучшились электромиографические показатели. Исследование показало хорошую переносимость высокой дозы препарата и отсутствие побочных эффектов при лечении ДПН у подростков.
В России широко используются препараты липоевой кислоты различных торговых марок для лечения осложнений сахарного диабета. Это препараты для парэнтерального и орального введения, назначаемые по различным схемам лечения.
Материалы собственного исследования
Целью нашей работы было:
- сравнить эффективность терапии различных препаратов липоевой кислоты, инфузионных форм и оральной формы Тиоктацида БВ;
- доказать, что оральное введение Тиоктацида БВ будет улучшать все основные симптомы диабетической нейропатии (TSS) также, как и инфузионные формы;
- показать, что прием Тиоктацида БВ приводит к улучшению нейропатического дефицита по шкале NDS.
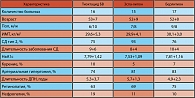
В исследование было включено 48 пациентов с диабетической нейропатией: 18 мужчин (37,5%) и 30 женщин (62,5%). Возраст больных – от 43 до 65 лет. Длительность сахарного диабета – 5-14 лет. 30 пациентов имели сахарный диабет тип 2 (62,5%). Периферическая дистальная нейропатия характеризовалась снижением температурной и тактильной чувствительности, мышечной слабостью и атрофией бедренных и ягодичных мышц. 8 пациентов (15%) имели нейропатические боли в ночное время и судороги мышц голеней. 8 больных (15%) имели язвенные дефекты плантарных поверхностей стоп и межпальцевых промежутков. Для оценки интенсивности симптомов нейропатической боли – жжения, парастезий и онемения (TSS) – использовали оценку в баллах: 0 баллов – отсутствие симптомов, 1 балл – слабо выраженные симптомы, 2 балла – средне выраженные симптомы, 3 балла – сильно выраженные симптомы. По частоте возникновения: редко – 0 баллов, часто – 0,33 балла, постоянно – 0,66 балла. По полученному суммарному результату оценивали эффект проводимой терапии.
Для определения степени тяжести периферической нейропатии оценивали тактильную чувствительность с помощью Thio-Feel, температурную чувствительность с помощью Thio-Therm и вибрационную чувствительность с помощью градуированного камертона 128 Гц. Оценивалась также активность рефлексов коленного и ахиллова сухожилий. Количественная оценка проводилась с помощью шкалы NDS по Янгу.
Все пациенты были рандомизированы в три группы, схожие по возрасту, индексу массы тела, продолжительности сахарного диабета и диабетической нейропатии. Все больные имели нейропатические жалобы по шкале TSS > 5. Уровень НвА1с исходно – не более 10%, в течении курса лечения проводился контроль уровня гликемии в соответствии с рекомендациями ADA.
Характеристика групп представлена в таблице 1.
Схемы терапии
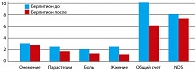
Берлитион – 600 мг в/в капельно медленно на 250 мл физиологического раствора. 10 инъекций с последующим ежедневным приемом оральных форм по 600 мг в день. Весь курс терапии – 3 месяца.
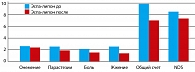
Эспа-липон – 600 мг в/в капельно медленно на 250 мл физиологического раствора. 10 инъекций с последующим ежедневным приемом оральных форм по 600 мг в день. Весь курс терапии – 3 месяца.
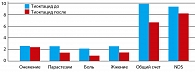
Тиоктацид БВ – 1800 мг/с в течение 3-х недель, с последующим приемом по 600 мг в день. Весь курс лечения – 3 месяца.
Период лечения составил 8 месяцев (2 курса по 3 месяца с перерывом 2 месяца).
Все больные получали лечение витаминами группы В и местное лечение при необходимости.
Полученные результаты позволяют сделать выводы, что лечение больных сахарным диабетом препаратами липоевой кислоты снижает выраженность клинических проявлений нейропатии. Улучшаются показатели по шкалам TSS и NDS.
Сравнение лечебного эффекта разных лекарственных форм и торговых марок липоевой кислоты показало, что оральная форма (Тиоктацид БВ 600 мг) в интенсивном режиме не только не уступает в/в форме введения других препаратов липоевой кислоты, но и имеет преимущества по некоторым показателям нейропатических проявлений.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.