Финеренон – новый высокоселективный нестероидный антагонист минералокортикоидных рецепторов для профилактики кардиоренальных осложнений у пациентов с хронической болезнью почек и сахарным диабетом 2 типа
- Аннотация
- Статья
- Ссылки
- English
В последние годы привлекают внимание и другие патогенетические механизмы поражения органов-мишеней, на которые можно воздействовать. Установлено, что минералокортикоидные рецепторы (МКР) и их высокая активность вносят серьезный вклад в развитие и прогрессирование хронической болезни почек (ХБП) и ССЗ при СД 2 типа за счет стимулирования процессов воспаления и фиброза.
Применение антагонистов МКР (АМКР) в лечении ХБП у пациентов с СД 2 типа патогенетически обоснованно, однако имеет ряд серьезных практических ограничений. Разработка и внедрение препаратов нового класса селективных нестероидных АМКР (нсАМКР) нацелены на преодоление существующих барьеров, характерных для стероидных АМКР.
На данный момент времени финеренон является первым и единственным нсАМКР с надежной доказательной базой в отношении пациентов с ХБП и СД 2 типа, что делает его безальтернативным препаратом для воздействия на патофизиологический путь гиперактивации МКР с целью кардионефропротекции.
В последние годы привлекают внимание и другие патогенетические механизмы поражения органов-мишеней, на которые можно воздействовать. Установлено, что минералокортикоидные рецепторы (МКР) и их высокая активность вносят серьезный вклад в развитие и прогрессирование хронической болезни почек (ХБП) и ССЗ при СД 2 типа за счет стимулирования процессов воспаления и фиброза.
Применение антагонистов МКР (АМКР) в лечении ХБП у пациентов с СД 2 типа патогенетически обоснованно, однако имеет ряд серьезных практических ограничений. Разработка и внедрение препаратов нового класса селективных нестероидных АМКР (нсАМКР) нацелены на преодоление существующих барьеров, характерных для стероидных АМКР.
На данный момент времени финеренон является первым и единственным нсАМКР с надежной доказательной базой в отношении пациентов с ХБП и СД 2 типа, что делает его безальтернативным препаратом для воздействия на патофизиологический путь гиперактивации МКР с целью кардионефропротекции.


Тесная связь функционирования эндокринной системы с деятельностью почек и сердца хорошо известна. Сердце является метаболически активным органом, чувствительным к изменению водно-электролитного баланса и объема циркулирующей крови. Работа почек зависит от адекватной перфузии и гормонального статуса. Это симбиотическое взаимодействие трех систем определяет гомеостаз функционирования. Неудивительно, что сахарный диабет (СД) 2 типа часто сопряжен с сердечно-сосудистыми заболеваниями (ССЗ) и хронической болезнью почек (ХБП). Менее чем у 10% пациентов имеет место изолированный СД 2 типа, то есть без ССЗ или ХБП. В большинстве случаев наблюдается сочетанная патология [1, 2].
Безусловно, СД 2 типа является пусковым фактором поражения почек и сердечно-сосудистой системы, двунаправленная связь между которыми определяет взаимоотягощающий характер поражения данных органов-мишеней. Связь сердца и почек, при которой нарушение в одном органе может приводить к дисфункции другого, определена как кардиоренальный синдром (КРС). В настоящее время выделяют пять типов КРС: первый и третий типы характеризуют острые нарушения, второй и четвертый типы описывают хронические состояния, пятый тип – одновременное поражение органов вследствие острых или хронических системных нарушений, таких как сепсис или амилоидоз. В случае поражения почек и сердца вследствие СД 2 типа имеет место КРС второго и четвертого типов, то есть нарушения в работе сердечно-сосудистой системы обусловливают нарушение функционирования почек, а развитие ХБП потенцирует поражение сердца и ССЗ [3, 4].
Интерес к КРС определяется не только практической актуальностью проблемы, но и появлением новых препаратов, обладающих потенциалом воздействия на патофизиологические процессы, лежащие в основе взаимного поражения и утяжеления течения ХБП и ССЗ у пациентов c СД 2 типа.
Патологическая гиперактивация ренин-ангиотензин-альдостероновой системы (РААС) и минералокортикоидных рецепторов (МКР) рассматривается как один из механизмов развития КРС. Блокирование данного патофизиологического пути у пациентов с ХБП и СД 2 типа способно разорвать порочный круг взаимоотягощающего поражения почек и сердца [1, 5].
Ингибиторы ангиотензинпревращающего фермента (иАПФ) и блокаторы рецепторов ангиотензина (БРА) – альтернативные опции, вошедшие в клиническую практику более двух десятилетий назад и в настоящее время являющиеся стандартной терапией у пациентов с КРС вследствие СД. Появление первого представителя класса селективных нестероидных антагонистов минералокортикоидных рецепторов (нсАМКР) финеренона для одновременной нефро- и кардиопротекции ознаменовало новую веху в терапии пациентов с ХБП, развившейся на фоне СД 2 типа [1, 6].
Патофизиология ренин-ангиотензин-альдостероновой системы
Основными механизмами старения организма, метаболических нарушений и хронических заболеваний являются хроническое воспаление и окислительный стресс. Эти процессы находятся в тесной связи. Известно, что окислительный стресс характеризуется повышенной продукцией свободных радикалов, нарушением окислительно-восстановительного баланса, повреждением клетки и даже ее гибелью.
Долгое время РААС представлялась как система, предназначенная для контроля водного и солевого гомеостаза в организме. Научные исследования доказали роль РААС в качестве одного из главных источников хронического воспаления и окислительного стресса [7–9].
Функционирование РААС ранее описывалось как линейный каскад реакций, финальным этапом которого была регуляция секреции альдостерона. Клетками юкстагломерулярного аппарата почек синтезируется ренин, необходимый для превращения ангиотензиногена – белка, синтезируемого клетками печени, в ангиотензин 1 (АТ-1). АТ-1 обладает слабым вазоконстрикторным эффектом. Под влиянием АПФ, который синтезируется и секретируется клетками почечных канальцев и интерстициальными клетками легочной ткани, АТ-1 превращается в мощный вазоконстриктор – ангиотензин 2 (АТ-2), который стимулирует секрецию альдостерона клубочковой зоной коры надпочечников [10, 11]. Однако важно помнить, что АТ-2 не является единственным триггером секреции альдостерона. В качестве стимуляторов синтеза альдостерона также выступают лептин, адренокортикотропный гормон, допамин, эндотелин, серотонин, вазопрессин, ацетилхолин, ионы калия. Повышение уровня калия всего на 2 промилле приводит к увеличению уровня альдостерона на 25% [12, 13]. Секретируемый в кровь альдостерон практически не связывается с белками плазмы и циркулирует в свободном виде. При исследовании уровня альдостерона в крови необходимо учитывать, что на результат анализа могут влиять количество натрия, потребленного с пищей, положение тела, время суток. Уровень гормона минимален утром и в положении лежа, максимален – во второй половине дня и в вертикальном положении (сидя, стоя). С возрастом нормальный уровень альдостерона в плазме может уменьшиться [12, 14].
В последние годы понимание о путях функционирования РААС расширилось. Установлены альтернативные пути, которые обходят как ренин, так и АПФ и стимулируют выработку ангиотензинов в тканях и клетках. Наличие данных механизмов, а также множества дополнительных стимуляторов выработки альдостерона объясняет феномен ускользания альдостерона, наблюдаемый при применении иАПФ или БРА.
Таким образом, ингибированием начальных звеньев каскада РААС невозможно полностью предотвратить все последствия ее избыточной активации. Для практической медицины это означает, что снижение риска, продемонстрированное в клинических исследованиях иАПФ или БРА, составляет лишь небольшую часть остаточного риска сердечно-сосудистых и почечных событий [13, 15].
Минералокортикоидные рецепторы
Альдостерон, как и другие гормоны, реализует свои эффекты за счет взаимодействия со специфическими белковыми структурами – МКР. Минералокортикоидные рецепторы относятся к семейству стероидных ядерных рецепторов, в которое также входят глюкокортикоидные рецепторы и рецепторы прогестерона и андрогенов [16]. МКР представлены практически во всех тканях организма. Особенно высокая их плотность определяется в клетках почечных канальцев, кардиомиоцитах, клетках эндотелия, клетках нервной системы, фибробластах, миелоидных клетках (макрофагах, нейтрофилах). Минералокортикоидный эффект оказывают и другие гормоны коры надпочечников, такие как дезоксикортикостерон (ДОК), 18-оксикортикостерон, кортикостерон, кортизол. Гормоны пучкового слоя надпочечников, обладая высоким минералокортикоидным воздействием, в норме его не проявляют, так как дезактивируются специфическими ферментами [9, 13, 16].
Вследствие локализации МКР в различных органах и тканях, таких как почки, сердце, сосуды, сетчатка, центральная нервная система (ЦНС), они способны контролировать гомеостаз и регулировать большое количество биологических процессов. При этом могут быть вовлечены и во множество патофизиологических механизмов повреждения органов-мишеней, которые происходят параллельно, определяя коморбидность у пациентов, в том числе при КРС. Это делает МКР актуальным объектом фундаментальных научных исследований, имеющих непосредственное клиническое значение [9, 15, 17].
До 1990 г. считалось, что МКР экспрессируются только в почках и их основной функцией является регуляция водно-электролитного гомеостаза. При этом полагали, что альдостерон является единственным лигандом МКР и имеет решающее значение для жидкостного, электролитного и гемодинамического гомеостаза. Попадая в кровоток, альдостерон взаимодействует с МКР эпителиальных клеток дистальных канальцев и собирательных трубочек нефрона, что, с одной стороны, приводит к увеличению реабсорбции натрия и задержке жидкости, с другой – к усилению экскреции калия и магния. Натрий-задерживающий эффект альдостерона необходим для поддержания гомеостаза в условиях гиповолемии. Понимание роли альдостерона и МКР в регуляции физиологических процессов и патологических процессах существенно расширилось только в последние 30 лет (рис. 1) [9, 13, 18].
На сегодняшний день получены неоспоримые доказательства того, что спектр действия альдостерона лежит далеко за пределами почечных эффектов. Системная или локальная гиперпродукция гормона вызывает целый ряд патологических реакций, затрагивающих весь организм. Данные патологические эффекты альдостерона реализуются через соответствующие рецепторы гормона, вследствие чего можно говорить о патологических эффектах гиперактивации МКР [9, 19].
В патологических условиях гиперактивация МКР является следствием не только повышения продукции альдостерона, но и активации лиганд-независимых путей стимулирования рецепторов в результате гипергликемии, окислительного стресса, высокой солевой нагрузки, Rac-1 и т.д.
Таким образом, не только избыточная продукция альдостерона, но и другие механизмы гиперактивации МКР, а также увеличение экспрессии самих рецепторов приводят к широкому спектру нарушений, способствующих полиорганному повреждению [20, 21].
В отличие от других видов рецепторов ядерные рецепторы, к которым относятся МКР, преимущественно расположены внутри клеток и способны напрямую взаимодействовать с геномной ДНК, регулируя экспрессию генов, тем самым осуществлять контроль различных биологических процессов в организме. В своей цитоплазматической неактивной форме МКР связаны с белками-шаперонами и различными иммунофилинами. Активация МКР происходит лигандным путем при взаимодействии с альдостероном и другими гормонами или нелигандным путем, после чего реализуются классические медленные (геномные) и быстрые (негеномные) эффекты стимуляции рецепторов [22, 23].
Негеномные эффекты МКР не связаны с проникновением комплекса «гормон – рецептор» в ядро. Они предназначены для быстрого реагирования организма на изменяющиеся условия с целью поддержания гомеостаза. Быстрый путь проведения клеточного сигнала опосредован взаимодействием активированного МКР с системой вторичных мессенджеров. Эффект развивается в течение нескольких минут после взаимодействия. Примером негеномного эффекта МКР может служить контроль водно-электролитного гомеостаза. Альдостерон может повысить активность эпителиальных натриевых каналов в почках в течение двух минут за счет негеномных эффектов МКР. При этом активация геномного пути с вовлечением соответствующих генов и синтезом натриевых каналов занимает более 30 минут. К быстрым эффектам МКР, ответственным за поддержание гомеостаза, также относятся регуляция тонуса сосудов (за счет продукции оксида азота (NO)), контроль электрической и сократительной активности миокарда [23, 24].
За счет быстрых негеномных эффектов МКР-сигнальный путь представляет собой высокоадаптивный и мощный механизм контроля гомеостаза.
Геномные эффекты стимуляции МКР требуют значительного времени для транскрипции генов и последующей трансляции белков, однако обеспечивают долгосрочное поддержание гомеостаза [23].
В патофизиологических условиях, например у пациентов с СД 2 типа, может происходить гиперактивация МКР, при которой баланс функционирования МКР-сигнального пути смещается в сторону геномных эффектов, запуская повреждение органов-мишеней и нарушение их функции за счет каскада патологических процессов [24, 25]:
- нарушение водно-электролитного гомеостаза;
- повышение продукции медиаторов воспаления;
- поляризация макрофагов по провоспалительному М1-фенотипу, активация Т-клеток и увеличение образования молекул адгезии;
- повышение продукции медиаторов фиброза и стимуляция пролиферации фибробластов;
- усиление образования коллагена;
- индукция окислительного стресса: увеличение образования активных форм кислорода, экспрессии и активности НАДФ-оксидазы;
- эндотелиальная дисфункция: ухудшение эндотелий-зависимой вазодилатации, снижение активности NO-синтазы;
- нарушение толерантности к глюкозе.
Множественные патологические процессы приводят к структурным изменениям и функциональным нарушениям на уровне тканей и органов [9, 26]:
- повреждению клеток и трансформации белков;
- кальцификации сосудов, увеличению жесткости сосудистой стенки, гемодинамическим нарушениям, повышению артериального давления (АД);
- гипертрофии, диастолической дисфункции левого желудочка;
- нарушению сократимости миокарда и сердечного ритма;
- повышению уровня липидов и атеросклерозу;
- замещению нормальных анатомических структур фиброзом;
- инсулинорезистентности.
Вследствие локализации МКР в различных органах и тканях их гиперактивация может характеризоваться полиорганным поражением, которое, в частности, выражается в патологическом ремоделировании сердца и почек с развитием КРС у пациентов с СД 2 типа (рис. 2) [24–26]. Значимая вовлеченность МКР в развитие и прогрессирование повреждения органов-мишеней позволяет предполагать, что системное блокирование гиперактивации МКР в разных органах способно оказать большой спектр положительных терапевтических эффектов. При этом ввиду комплексности строения МКР и МКР-сигнального пути эффекты блокирования рецепторов будут также зависеть от механизма связывания препарата с рецептором, который различается у существующих стероидных и нестероидных АМКР (сАМКР и нсАМКР) [15, 25, 27].
Блокирование гиперактивации МКР и кардионефропротекция
История разработки и применения АМКР первоначально была историей антагонистов альдостерона, поскольку при изучении первых препаратов в 1950-х гг. ставилась цель синтезировать ингибитор почечных эффектов именно этого гормона. В то время основной ролью альдостерона признавался контроль почечной экскреции натрия и калия. Позднее стало ясно, что изучаемые антагонисты альдостерона блокируют специфический рецепторный белок, который обладает высоким сродством не только с альдостероном, но и с рядом других гормонов. Именно поэтому данный класс препаратов получил название АМКР [28].
Вовлеченность дезоксикортикостерон ацетата (ДОКА) – предшественника альдостерона в патологические процессы в почках и сердце была описана еще в 1942 г. в работах H. Selye [29]. Определение ДНК рецептора альдостерона в 1987 г. позволило получить первое представление о молекулярном механизме действия МКР и роли его гиперактивации в процессах фиброза и воспаления [30]. Впоследствии было проведено большое количество доклинических исследований возможности блокирования эффектов МКР с целью оценки потенциала применения АМКР в клинической практике для предотвращения патологического ремоделирования почек и сердца [28].
Воспалительные изменения и замещение нормальных анатомических структур фиброзом являются анатомической основой ХБП, которая может быть следствием или сопровождаться острым повреждением почек (ОПП).
Острое повреждение почек считается независимым фактором риска как развития, так и прогрессирования ХБП. Каждый эпизод ОПП у пациентов с ХБП и СД вносит значительный вклад в прогрессирование ХБП вплоть до терминальной почечной недостаточности (ТПН) [31].
Экспериментальные исследования, проведенные J. Barrera-Chimal и соавт., показали, что один эпизод ишемического ОПП может вызвать ХБП у крыс, подвергнутых двусторонней ишемии или реперфузии почек. Наблюдение за крысами, перенесшими эпизод ОПП, в течение девяти месяцев выявило характерные для ХБП протеинурию, дисфункцию почек и тяжелые структурные повреждения. Инфильтрация макрофагами, наблюдаемая при ОПП, определяет тяжесть повреждения почечной ткани. МКР макрофагов (миелоидные МКР) могут быть вовлечены в процессы регуляции воспаления и фиброза при ОПП и ХБП и стимулировать поляризацию макрофагов по провоспалительному М1-фенотипу [32, 33].
В одном из экспериментов на модели мыши с ОПП (с двусторонней ишемией или реперфузией) J. Barrera-Chimal и соавт. отметили эффект нсАМКР (финеренона) в предотвращении развития ХБП. Профилактическое введение финеренона характеризовалось отсутствием повышения выработки медиаторов фиброза, в том числе трансформирующего фактора роста β (TGF-β), а также протеинурии, фиброза почек и отложения коллагена. Нефропротективный эффект финеренона, вероятно, был обусловлен уменьшением провоспалительной инфильтрации макрофагов и стимулированием поляризации макрофагов до фенотипа М2 (противовоспалительных макрофагов). М2-фенотип представляет собой ранозаживляющий фенотип в острой фазе после ишемического повреждения. Ингибирование MКР способствовало поляризации макрофагов М2 за счет увеличения экспрессии и активации рецептора интерлейкина 4 макрофагов [33].
Значимый вклад в нефропротективный эффект финеренона у мышей с ОПП, вероятно, могло внести и блокирование МКР гладкомышечных клеток. Гиперактивация МКР гладкомышечных клеток, происходящая вследствие лиганд-независимого пути Rac-1 при ОПП, характеризовалась индукцией окислительного стресса, что успешно подавлялось применением нсАМКР [34].
Еще один предполагаемый механизм нефропротективного эффекта блокирования МКР может быть опосредован рецепторами эндотелина В. В опытах на той же модели мышей с ишемическим ОПП было установлено, что почечная ишемия сопровождается усиленным окислительным повреждением, ведущим к окислению цистеиновых остатков до сульфеновой кислоты, модифицирующей рецептор эндотелина В, с последующим подавлением активации эндотелиальной NO-синтазы. Таким образом, в условиях почечного повреждения и ишемии рецептор эндотелина В эндотелиальных клеток не способен стимулировать продукцию NO. Сниженная продукция NO, вазоконстрикция и нарушение перфузии почек приводят к повреждению почечных структур вследствие ишемии. Было показано, что данный патофизиологический путь, опосредованный модификацией рецептора эндотелина В, блокируется нсАМКР [34, 35].
Трансформирующий фактор роста β является важным цитокином, стимулирующим рост фибробластов, дифференцировку и пролиферацию, активирует синтез и отложение коллагена и ингибирует матриксную металлопротеиназу коллагеназы. У крыс с протеинурией продукция TGF-β из интерстициальных макрофагов коррелировала с воспалительной инфильтрацией.
Уровень TGF-β увеличивается при введении альдостерона и снижается при применении АМКР. У пациентов с СД 2 типа и ХБП отмечается аналогичная корреляционная зависимость между повышением концентрации TGF-β и выраженностью альбуминурии – с повышением альбуминурии наблюдается увеличение уровня TGF-β, определяемое как в сыворотке крови, так и в моче. У пациентов с тяжелой альбуминурией фиксируется трехкратное повышение экспрессии мРНК почечного TGF-β [36]. В регуляцию экспрессии медиаторов фиброза, в том числе TGF-β, вовлечены именно МКР, которые в случае гиперактивации способны усиливать экспрессию эффекторных профибротических генов-мишеней [36, 37].
Повышение продукции медиаторов фиброза при гиперактивации МКР не ограничивается почками, а может затрагивать все органы, в клетках которых локализуются данные рецепторы [27]. В более ранних доклинических исследованиях было продемонстрировано, что активация МКР может способствовать апоптозу кардиомиоцитов и развитию фиброза, приводя к патологическому ремоделированию миокарда и снижению функции сердца.
С появлением нсАМКР возникает вопрос о существовании различий в эффектах блокирования МКР разными препаратами-антагонистами, речь, в частности, идет о сАМКР спиронолактоне и эплереноне и нсАМКР финереноне [27, 38].
Одно из доклинических исследований, в котором сравнивались эффекты разных классов АМКР, было выполнено на мышиной модели кардиального фиброза, вызванного изопротеренолом. Для изучения антифибротических эффектов финеренон и эплеренон брали в эквинатрийуретических дозах, то есть данные дозы препаратов характеризовались сопоставимыми эффектами в отношении влияния на водно-электролитный гомеостаз. Согласно результатам исследования, финеренон в дозе 10 мг/кг значимо снижал выраженность фиброза в сердце и инфильтрацию сердца макрофагами, тогда как аналогичный эффект для эплеренона в дозе 100 мг/кг не наблюдался. В рамках данного исследования были также продемонстрированы значимые различия между финереноном и сАМКР в отношении влияния на профибротические гены. Финеренон в отличие от эплеренона и спиронолактона значимо снижал экспрессию гена TNX, который кодирует гликопротеины внеклеточного матрикса и способствует откладыванию коллагена. Финеренон также значимо уменьшал экспрессию генов TGF-β, коллагена 1 и галектина 3. При этом эффекты сАМКР в отношении сокращения экспрессии данных генов были менее выраженными [38].
Еще одно из недавних доклинических исследований, в котором оценивались антифибротические механизмы действия финеренона и сравнивались эффекты разных АМКР, было проведено на крысах Спрег-Доули с нефрэктомией одной почки (классическая модель ДОКА-соль). Эта модель крыс с индуцированным дезоксикортикостероном ацетатом повреждением сердца и почек. Финеренон оказывал более выраженное влияние на уменьшение фиброза и альбуминурии и менее выраженное – на концентрацию калия в сыворотке крови по сравнению со спиронолактоном. Нефропротективный эффект финеренона проявлялся в меньшей выраженности патологических структурных изменений в почках – менее выраженном гломерулосклерозе и тубулоинтерстициальном фиброзе [39].
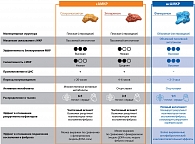
Таким образом, первоначальная стратегия терапии АМКР (исключительно с целью снижения объема циркулирующей крови) с годами существенно расширилась, в том числе благодаря проведенным фундаментальным доклиническим исследованиям. Лучшее понимание ключевой роли МКР в развитии фиброза и воспаления, а также практические ограничения применения сАМКР (риск гиперкалиемии, нежелательные явления со стороны половой системы) привели к созданию нсАМКР (препарата финеренон), так называемых полных АМКР, с более выраженным влиянием на воспаление и фиброз. При этом сАМКР (спиронолактон, эплеренон), также обладающих антифибротическим и антивоспалительным эффектами, называют частичными агонистами из-за особенности связывания с МКР, в результате которого влияние рецептора на воспаление и фиброз блокируется лишь частично (рис. 3) [40–42]. Разный механизм действия, разные фармакокинетические и фармакодинамические характеристики и разные клинические эффекты определяют необходимость разделения стероидных и нестероидных АМКР на два разных класса [27, 40]. И, как отмечено в авторитетных практических руководствах, данные в отношении одного класса АМКР не могут быть экстраполированы на другой [43].
Кардионефропротективный потенциал нсАМКР у пациентов с ХБП и СД 2 типа
Использование АМКР в клинической практике представляет особый интерес. АМКР рассматриваются в качестве терапевтической стратегии при ХБП, для замедления ухудшения почечной функции и снижения сопутствующих сердечно-сосудистых рисков.
В ряде опубликованных небольших непродолжительных клинических исследований сообщалось о нефропротективном эффекте сАМКР, выражавшемся в антипротеинурическом действии у лиц с ХБП.
Согласно результатам двух метаанализов, сАМКР способны уменьшать протеинурию при использовании в комбинации с иАПФ или БРА.
В восьми исследованиях добавление спиронолактона к иАПФ или БРА у пациентов с ХБП и СД привело к снижению 24-часовой экскреции альбумина или белка с мочой, в трех – к более выраженному уменьшению соотношения «альбумин/креатинин» (А/Кр) в моче. Следует отметить, что также сообщалось о значительном снижении АД, поэтому нельзя исключать возможность уменьшения протеинурии, опосредованной снижением АД. Важно также подчеркнуть, что авторами данных метаанализов была установлена высокая степень гетерогенности наблюдаемых терапевтических эффектов сАМКР и низкий или очень низкий уровень доказательности [44, 45]. Вследствие этого, как отмечено в рекомендациях KDIGO 2022 г. по ведению пациентов с ХБП и СД, у cАМКР отсутствует надежная доказательная база для применения с целью кардионефропротекции [46]. Другим фактором, препятствующим широкому назначению сАМКР, особенно у пациентов со скомпрометированной функцией почек, является высокий риск развития гиперкалиемии. У пациентов с ХБП риск возникновения гиперкалиемии при добавлении сАМКР к блокаторам ренин-ангиотензиновой системы может возрастать в 3,0–4,3 раза по сравнению с монотерапией иАПФ или БРА [47, 48].
Разработка и изучение финеренона, как первого представителя нового класса селективных нсАМКР, была нацелена на преодоление барьеров, характерных для сАМКР, и получение надежных доказательств для его применения у пациентов с ХБП и СД 2 типа с целью кардионефропротекции.
Отсутствие нежелательных явлений со стороны половой системы и меньшее влияние на концентрацию калия в крови может обусловливать более благоприятный профиль безопасности финеренона по сравнению с сАМКР.
Завершенные рандомизированные клинические исследования финеренона в популяции пациентов с СД 2 типа и широким спектром ХБП – от первой до четвертой стадии позволяют сделать вывод, что это единственный на сегодняшний день АМКР с надежными доказательствами наличия выраженного кардионефропротективного эффекта в соответствующей популяции [6, 41, 49].
Первым крупным исследованием финеренона у пациентов с ХБП и СД 2 типа стало исследование фазы II ARTS-DN (n = 823). Оно было нацелено на оценку эффективности и профиля безопасности разных доз финеренона по сравнению с плацебо на фоне базовой терапии иАПФ или БРА. Терапия финереноном ассоциировалась с выраженным дозозависимым снижением альбуминурии [50]. Альбуминурия, ее выраженность и персистенция являются общепризнанными и ценными для клинической практики маркерами тяжести течения ХБП, прогноза дальнейшего снижения почечной функции и развития сердечно-сосудистых осложнений. Альбуминурия также является одной из потенциальных причин снижения почечной функции за счет прямого повреждающего воздействия на клубочки и канальцы [51, 52]. Необходимость снижения альбуминурии с целью замедления темпов прогрессирования ХБП рекомендована в гайдлайнах Американской диабетической ассоциации (American Diabetes Association – ADA) 2023 г. В них отмечено, что снижение соотношения А/Кр до < 300 мг/г или на > 30% относительно исходного уровня ассоциировано с улучшением почечных и сердечно-сосудистых исходов, что может предполагать необходимость достижения максимально возможного уменьшения данного показателя при терапии ХБП [43]. Ведущие организации, такие как Управление по санитарному надзору за качеством пищевых продуктов и медикаментов, Национальный почечный фонд, Европейское агентство лекарственных средств, признали изменение альбуминурии надежным суррогатным параметром для оценки эффективности нефропротективной терапии [53].
Согласно результатам ряда наблюдений, сАМКР способны уменьшать альбуминурию, однако данные препараты не изучались в крупных рандомизированных исследованиях с участием пациентов с поздними стадиями ХБП из-за высокого риска развития гиперкалиемии.
Финеренон характеризуется более низким риском возникновения гиперкалиемии по сравнению с сАМКР, вероятно, благодаря более короткому периоду полувыведения, отсутствию активных метаболитов, равномерному распределению между почками и сердцем, а также различиям во влиянии на экспрессию генов (см. рис. 3) [27, 41]. Данные особенности препарата позволили провести крупное рандомизированное клиническое исследование FIDELIO-DKD в популяции пациентов с СД 2 типа и ХБП преимущественно третьей и четвертой стадий [6]. Так, общее количество участников составило 5734.
FIDELIO-DKD – рандомизированное двойное слепое плацебо-контролируемое многоцентровое исследование фазы III. В данное исследование включали лиц с СД 2 типа и ХБП при условии, что соотношение А/Кр в моче составляло 30– < 300 мг/г, расчетная скорость клубочковой фильтрации (рСКФ) – ≥ 25– < 60 мл/мин/1,73 м2 или соотношение А/Кр – ≥ 300 – ≤ 5000 мг/г, рСКФ – ≥ 25– < 75 мл/мин/1,73 м2. У всех пациентов отмечалось выраженное снижение почечной функции. У 88,4% пациентов рСКФ была < 60 мл/мин/1,73 м2 (среднее значение рСКФ – 44,3 мл/мин/1,73 м2), у 87,4% регистрировалось резкое повышение альбуминурии (соотношение А/Кр в моче – ≥ 300 мг/г со средним значением 851 мг/г). Длительность СД 2 типа в среднем составляла 16,6 года. На момент рандомизации уровень гликированного гемоглобина (HbA1c) в среднем достигал 7,7%. У включенных в исследование пациентов регистрировался удовлетворительный контроль АД со средним значением систолического АД 138 мм рт. ст., что позволило оценить нефропротективный эффект финеренона, минимизировав вклад в конечный результат влияния препарата на снижение АД [6].
Финеренон снижал риск развития событий первичной почечной конечной точки (время до развития ТПН, устойчивого снижения СКФ на ≥ 40% от исходного уровня или смерти от почечных причин) на 18% (относительный риск (ОР) 0,82 при 95%-ном доверительном интервале (ДИ) 0,73–0,93; р = 0,001). Обращает на себя внимание выраженное и стойкое снижение альбуминурии на фоне терапии финереноном, которое сохранялось на протяжении всего периода терапии и наблюдения (в среднем 2,6 года). Уменьшение соотношения А/Кр в моче относительно плацебо в группе терапии финереноном составило 31% уже к четвертому месяцу [6].
Финеренон также снижал риск развития событий основной вторичной сердечно-сосудистой конечной точки (время до развития смерти от сердечно-сосудистых причин, нефатального инфаркта миокарда, нефатального инсульта или госпитализации по причине сердечной недостаточности) на 14% (ОР 0,86 (95% ДИ 0,75–0,99); р = 0,03).
Таким образом, результаты исследования FIDELIO-DKD продемонстрировали выраженный кардионефропротективный эффект финеренона у пациентов с СД 2 типа и ХБП с высоким и очень высоким исходным риском прогрессирования ХБП до ТПН, развития неблагоприятных сердечно-сосудистых событий и смерти от сердечно-сосудистых причин [6].
Финеренон характеризовался умеренным и предсказуемым влиянием на динамику концентрации калия в крови. Максимальная разница в концентрации ионов калия в крови между исследуемыми группами финеренона и плацебо наблюдалась на четвертом месяце и составила 0,23 ммоль/л. Финеренон отличался низкой частотой прекращения терапии или госпитализации вследствие гиперкалиемии, независимо от исходной рСКФ. Прекращение лечения исследуемым препаратом вследствие гиперкалиемии зафиксировано у 64 (2,3%) пациентов в группе финеренона и 25 (0,9%) пациентов в группе плацебо. Госпитализация вследствие гиперкалиемии – у 40 (1,4%) и 8 (0,3%) больных соответственно. Важно обратить внимание на то, что в данное исследование включали пациентов с выраженным снижением функции почек, а значит, высоким риском развития гиперкалиемии. У 88,4% участников исследования рСКФ была < 60 мл/мин/1,73 м2. Фармакокинетические и фармакодинамические особенности финеренона (см. рис. 3), вероятно, обусловили возможность контроля гиперкалиемии путем регулярного мониторинга и временного прекращения терапии [6].
Актуальные рекомендации по кардионефропротекции у пациентов с СД
Подход к ведению пациентов с КРС, который зачастую сочетается и является следствием СД, должен носить комплексный характер. В клинических рекомендациях, как зарубежных, так и отечественных, подчеркнута необходимость реализации на практике в отношении каждого пациента с СД полного спектра лечебно-профилактических мероприятий, направленных на контроль факторов риска развития и прогрессирования осложнений диабета. Так называемая многофакторная терапевтическая стратегия одновременно должна включать множество подходов, основанных на фактических доказательствах благоприятного клинического эффекта: контроль гликемии, АД, липидного обмена и специфическую таргетную кардионефропротективную терапию. В сочетании с изменением образа жизни они являются фундаментальными для глобального снижения риска развития и темпов прогрессирования КРС при СД [43, 51, 52].
Достижение и поддержание целевых значений гликемии и АД уже давно признаны необходимым стандартом ведения пациентов с СД. В рекомендациях ADA 2023 г. по оказанию помощи при СД были указаны новые пороговые значения АД для инициации антигипертензивной терапии – ≥ 130/80 мм рт. ст. Целевым значением АД считается < 130/80 мм рт. ст. при возможности его безопасного достижения. При определении персонализированных целевых уровней HbA1c и АД у пациентов с СД необходимо учитывать множество факторов, влияющих на безопасность их достижения. Так, следует учитывать ожидаемую продолжительность жизни, длительность заболевания, наличие или отсутствие микро- и макрососудистых осложнений, факторов риска развития ССЗ, сопутствующих заболеваний, гипогликемии, а также когнитивный и психологический статус пациента [54].
У лиц с ХБП может быть затруднен контроль HbA1c вследствие снижения функции почек, а также повышен риск возникновения гипогликемии. При этом интенсификация гликемического контроля, снижая риск развития ХБП, не уменьшает риск прогрессирования поражения почек и может повышать риск смерти от ССЗ у пациентов с ХБП и СД [43, 55].
Потенциальные нежелательные явления антигипертензивной терапии (гипотензия, синкопе, острое повреждение почек, нарушение электролитного гомеостаза) также следует учитывать при определении целевых значений АД. Для пациентов с ХБП, выраженной коморбидностью, ортостатической гипотензией характерен повышенный риск развития нежелательных явлений. В данной популяции могут быть предпочтительными более высокие целевые значения АД в связи с более благоприятным соотношением «польза – риск» и лучшим качеством жизни [54].
Коморбидность – важный фактор, определяющий возможность безопасного достижения целевой гликемии и АД. Поражение почек и сердечно-сосудистой системы на фоне СД, выражающееся в развитии КРС, само по себе характеризуется высоким риском смерти и вносит значительный вклад в увеличение рисков, связанных с трудностями контроля сахарного диабета и артериальной гипертензии (АГ). В связи со сказанным ранее возрастает важность таргетной кардионефропротекции как одного из столпов многофакторной терапевтической стратегии для снижения риска развития и прогрессирования осложнений СД [43, 54, 55].
С появлением новых препаратов с доказанным благоприятным эффектом в отношении почек и сердца в клинических рекомендациях и практических алгоритмах по ведению пациентов с ХБП и СД 2 типа начали обозначаться три столпа кардионефропротекции: иАПФ или БРА, ингибиторы натрий-глюкозного котранспортера 2 (иНГЛТ-2), нсАМКР (финеренон). В рекомендациях ADA 2023 г. указано, что данные препараты должны быть назначены совместно, а не рассматриваться как альтернатива друг другу при неэффективности предшествующей терапии (рис. 4) [43, 56, 57]. Терапевтический путь воздействия на разные звенья патогенеза ХБП и ССЗ может способствовать синергизму эффектов в отношении замедления прогрессирования ХБП и снижения риска развития сердечно-сосудистых осложнений [43, 54, 58]. Таким образом, для максимизации терапевтического эффекта пациентам с ХБП и СД 2 типа необходимо назначить все три класса препаратов [43, 56].
Заключение
Современная кардиология и нефрология тесно связаны между собой, что обусловлено достижениями науки и практики в отношении вопросов, касающихся общих факторов риска развития заболеваний почек и сердечно-сосудистой системы, универсальных патогенетических механизмов, взаимоотягощающего прогноза и терапевтической стратегии нефро- и кардиопротекции. Такая связь сердца и почек, при которой нарушение в одном органе может приводить к дисфункции другого, определено понятием КРС. Заболевания метаболической и нейрогуморальной этиологии зачастую являются причиной развития КРС, образуют порочный круг взаимоотягощающего влияния полиорганных нарушений и делают междисциплинарный подход к ведению таких пациентов неотъемлемым [4, 5].
Этиология и патогенетические механизмы повреждения почек у пациентов с КРС многофакторны и неоднозначны. Гемодинамический дисбаланс, нейрогормональная активация, симпатическая активность, фармакологические вмешательства, воспаление наряду с окислительным стрессом могут быть вовлечены в патогенез острого повреждения почек при КРС. Гиповолемия, вызванная снижением сердечного выброса или чрезмерно быстрой сосудосуживающей терапией, может привести к нарушению почечной перфузии [3, 21].
Гиперактивация МКР – одно из недавно определенных общих звеньев поражения почек и сердца, а значит, и формирования КРС у пациентов с СД 2 типа. МКР в гиперактивированном состоянии способны запускать каскад патологических реакций, что приводит к развитию воспаления, фиброза и окислительного стресса. Локализация МКР во множественных клетках, органах и тканях обусловливает полиорганный характер повреждений при нарушении их функционирования. Множественность путей гиперактивации МКР определяет комплексность РААС и объясняет необходимость блокирования именно МКР для максимизации положительного эффекта терапии [24, 27].
На сегодняшний день лишь финеренон, являющийся единственным представителем нсАМКР с надежными доказательствами благоприятного эффекта в отношении почек и сердца при СД 2 типа, может применяться у пациентов с ХБП и СД 2 типа для кардионефропротекции, что делает данный препарат безальтернативным для воздействия на патологический путь гиперактивации МКР.
Финеренон включен в ведущие зарубежные рекомендации для замедления темпов прогрессирования ХБП и улучшения сердечно-сосудистых исходов у пациентов с ХБП и СД 2 типа с наивысшим уровнем доказательств [43, 55].
Финеренон зарегистрирован в Российской Федерации весной 2023 г. на основании результатов исследования FIDELIO-DKD и показан для применения у взрослых пациентов с СД 2 типа и ХБП (третья и четвертая стадии с альбуминурией). Можно также ожидать его включение в федеральные клинические рекомендации при их обновлении.
Существующие в настоящее время препараты для кардионефропротекции у лиц с ХБП и СД 2 типа представляют независимые столпы терапии, которые должны быть назначены в рамках многофакторной стратегии вместе, а не в качестве альтернативы друг другу [43, 56, 57].
Конфликт интересов
Публикация подготовлена при поддержке АО «Байер».
Компания «Байер» поддерживала техническую редакцию статьи.
A.M. Mkrtumyan, MD, PhD, Prof., S.V. Podachina, PhD, I.V. Solovyova, PhD
A.I. Yevdokimov Moscow State University of Medicine and Dentistry
A.S. Loginov Moscow Clinic Scientific Center
Contact person: Ashot M. Mkrtumyan, vagrashot@mail.ru
Cardiovascular disease (CVD) is the leading cause of death worldwide. Combination of CVD with diabetes mellitus (DM) and kidney damage complicates patients’ status, aggravates the suffering and increases mortality. Treatment strategy of these patients includes lifestyle modification as well as glycemic, blood pressure and lipid management.
In recent years additional pathophysiological mechanisms of target organ damage were elucidated. Mineralocorticoid receptors (MR) and their excessive activation lead to inflammation and fibrosis resulting in development and progression of CKD and CVD in type 2 diabetes (DM2).
The use of MR antagonists (MRA) in treatment of chronic kidney disease (CKD) in DM2 is pathogenetically justified but has number of limitations. Development of a new class of selective nonsteroidal MRAs (nsMRA) is aimed at overcoming the existing drawbacks of steroidal MRAs.
Finerenone is the first and only nsMRA with robust evidence for its use in patients with CKD and DM2 which makes it the new drug without alternative with respect to its effect on MR hyperactivation pathway to achieve cardionephroprotection.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.