Эндокринотерапия рака молочной железы
- Аннотация
- Статья
- Ссылки
При этом одним из основных критериев отбора больных для терапии является гормонорецепторный статус опухоли.
При этом одним из основных критериев отбора больных для терапии является гормонорецепторный статус опухоли.

Уровень экспрессии рецепторов эстрогенов (РЭ) и прогестерона (РП) определяет эффективность гормональной терапии РМЖ. Рецепторположительные клетки высокодифференцированы и лучше отвечают на гормональное лечение, что в большинстве случаев приводит к более длительной общей и безрецидивной выживаемости. В то же время почти 11% рецепторнегативных опухолей также могут отвечать на гормонотерапию [1–3].
Принципы назначения гормональной терапии в разных возрастных группах имеют некоторые различия. Если для пациенток в постменопаузе, которая характеризуется естественным угасанием функции яичников и минимальным уровнем циркулирующих эстрогенов, специфическая терапия не требует воздействия на яичники, то при лечении молодых женщин большое значение имеет выключение их функции [4, 5].
Историческое развитие гормонотерапии рака молочной железы претерпело ряд этапов. Первыми среди препаратов, применяемых для гормонотерапии РМЖ, были селективные модуляторы рецепторов эстрогенов (Selective Estrogen Receptor Modulators – SERMs), наиболее ярким представителем которых является тамоксифен, более 20 лет считавшийся «золотым стандартом» гормональной терапии. Применение тамоксифена в дозе 20 мг/сут. не менее 5 лет позволяет на 50% снизить вероятность рецидива заболевания и на 25% показатель смертности от РМЖ [6–8]. Однако нельзя не считаться с некоторыми побочными эффектами, которые являются особенно значимыми для пациенток старшей возрастной группы.
К ним относятся увеличение риска тромбоэмболических осложнений, повышение вероятности развития рака эндометрия и гепатоцеллюлярного рака, токсическое воздействие на органы зрения (ретинопатии, кератопатии и т. д.). Биологическая активность тамоксифена варьирует от полного агонизма до полного антагонизма в зависимости от типа органа. Другие препараты данной группы, такие как торемифен, идоксифен, ралоксифен не продемонстрировали большей эффективности и безопасности, сохраняя способность как к агонизму, так и антагонизму.
Относительно новая группа лекарственных средств, прочно занявшая место во второй линии гормональной терапии, – ингибиторы ароматазы. Препятствуя образованию эндогенных эстрогенов, ингибиторы ароматазы блокируют их стимулирующее влияние на опухоль у больных, находящихся в менопаузе. Применение высоких доз эстрогенов, прогестинов и андрогенов для лечения РМЖ ограничено выраженными побочными эффектами. Появление препаратов – ингибиторов ароматазы значительно расширяет возможности гормонотерапии, особенно в группе пожилых пациенток [9]. Ингибиторы ароматазы нецелесообразно назначать женщинам репродуктивного возраста, поскольку снижение продукции эстрогенов, в частности в жировой ткани, неминуемо приведет к увеличению их продукции в функционирующих яичниках.
Однако в последнее время появились работы, в которых при лечении РМЖ у пациенток репродуктивного возраста данные препараты использовались, но после выключения функции яичников [10]. Все препараты данной группы делятся на стероидные (форместан, экземестан) и нестероидные (аминоглутетимид, фадразол, астрозол, летрозол и т. д.). В последних рекомендациях различных ассоциаций по использованию эндокринотерапии при РМЖ ингибиторы ароматазы были названы гормонотерапией I линии в группе постменопаузальных больных. Применение ингибиторов ароматазы также возможно у пременопаузальных пациенток при высокой эстрогеночувствительности, но с обязательным выключением функции яичников [11–13].
Еще в начале клинического применения ингибиторов ароматазы было проведено немало исследований, целью которых был перевод больных, получавших адъювантную терапию тамоксифеном, на лечение данными препаратами. Одним из первых таких исследователей был Франческо Боккардо с соавт. В исследовании участвовали 448 пациенток после 2-3-летнего лечения тамоксифеном, которые слепым методом распределялись на 2 группы: первая получала анастрозол 1 мг/сут, вторая продолжала терапию тамоксифеном 20 мг/сут [14]. Лечение продолжалось 5 лет, в течение которых проводилась оценка общей и безрецидивной выживаемости и безопасности терапии. Данные исследования показали, что применение анастрозола первые 2-3 года в лечении постменопаузальных больных с ранней стадией РМЖ значительно улучшает общую и безрецидивную выживаемость, а также продемонстрировали безопасность проводимой терапии.
Еще два аналогичных исследования (объединенные результаты ABCSG-8 и АRNО 95) также были посвящены лечению постменопаузальных женщин с ранней стадией гормонозависимого РМЖ. В исследованиях приняли участие 3224 пациентки, которые распределялись следующим образом: в первой группе больные после 2 лет адъювантной терапии тамоксифеном 20 мг/сут переводились на ингибиторы ароматазы – анастрозол в дозе 1 мг/сут (n = 1618), во второй пациентки продолжали прием тамоксифена 20 мг/сут (n = 1606) в адъювантном режиме. Исследования установили снижение риска возврата заболевания в группе с анастрозолом по сравнению с группой тамоксифена. Общая 3-летняя выживаемость больных в первой группе составила 95% в сравнении с 92% второй группы.
Вопрос о возможности применения ингибиторов ароматазы в неоадьювантном режиме широко дискутировался. Эта проблема особенно актуальна для тех пожилых пациенток, которым проведение неоадъювантной химиотерапии невозможно из-за сопутствующих заболеваний. Отечественные исследователи, изучавшие эффективность ингибиторов ароматазы III поколения у постменопаузальных больных с высоким содержанием рецепторов эстрогенов (ЭР+), подтвердили, что применение этих препаратов может вызывать уменьшение размеров первичной опухоли [15–17]. Так, в НИИ онкологии им. Н.Н. Петрова (Санкт-Петербург) было проведено рандомизированное исследование, в котором участвовали 87 больных РМЖ постменопаузального возраста (от 55 до 74 лет) с рецепторположительными опухолями (ЭР+ и/или ПР+). Пациентки были разделены на 3 группы: в первой применялся астрозол (Аримидекс) по 1 мг/сут в течение 3 мес (n = 30); во второй – комбинированная эндокринотерапия – астрозол по 1 мг/сут и тамоксифен по 20 мг/сут в течение 3 мес (n = 28); в третьей – тамоксифен по 20 мг/сут в течение 3 мес. (n = 29).
Полный ответ опухоли на лечение отмечен у 13,3% больных первой группы, 10,3% пациенток третьей группы. Во второй группе не было зарегистрировано ни одного полного ответа. При оценке лечебного эффекта с помощью маммографии объективный ответ (частичный или полный регресс опухоли) наблюдался у 55,5% больных, получавших анастрозол (Аримидекс), у 40% при комбинированном лечении (А+Т) и у 36% пациенток, получавших тамоксифен (р = 0,058). Результаты этого исследования показали, что 3-месячное дооперационное лечение анастрозолом предпочтительнее и эффективнее, чем лечение тамоксифеном и их комбинацией в неоадъювантной эндокринотерапии постменопаузальных больных РМЖ с рецепторположительными (ЭР+/ПР+) опухолями.
Первые данные широко известного исследования АТАС (Аримидекс, Тамоксифен – монотерапия или их комбинация) были опубликованы еще 5 лет назад. Это двойное слепое рандомизированное сравнительное исследование, в которое были включены 9366 пациенток в постменопаузе с локальным РМЖ. Больные были рандомизированы на 3 группы: первая получала анастрозол 1 мг/сут вместе с плацебо; вторая – тамоксифен 20 мг/сут и плацебо; третья – анастрозол 1 мг/сут + тамоксифен 20 мг/сут. Рандомизация осуществлялась и в период продолжения лучевой терапии.
Главной целью исследования была оценка эффективности анастрозола по сравнению с тамоксифеном у женщин в постменопаузе с локальным РМЖ, а также безопасности и переносимости лечения в группах сравнения [18]. В настоящее время мы можем проанализировать результат 10-летнего исследования. Цель работы оставалась прежней – оценка эффективности астрозола и тамоксифена и безопасности ингибиторов ароматазы третьего поколения в адъювантной эндокринотерапии женщин в постменопаузе с РМЖ. Полученные данные были представлены на 12-й международной конференции, посвященной проблемам диагностики и лечения РМЖ в Милане 2010 году [19].
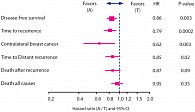
Предыдущий анализ исследования ATAC показал увеличение общей и безрецидивной выживаемости в группе больных, получавших анастрозол, по сравнению с выживаемостью пациенток в группах лечения тамоксифеном и комбинацией препаратов после 5 лет лечения. Далее проводилось сравнение в 2 группах: анастрозол 1 мг/сут и тамоксифен 20 мг/сут. Исключение третьей группы больных было связано с тем, что не было выявлено преимуществ лечения комбинацией анастрозола и тамоксифена по сравнению с лечением только тамоксифеном. На рис. 1 представлены критерии оценки эффективности в группе пациентов с гормоночувствительным РМЖ. Как видно из представленного рисунка, в группе больных, получавших анастрозол, были получены достоверно лучшие результаты общей и безрецидивной выживаемости, снижение риска рака контралатеральной молочной железы, времени до возникновения отдаленных метастазов.
Риск возникновения РМЖ в контралатеральной молочной железе на 38% был ниже в группе больных, получавших анастрозол, в сравнении с группой лечения тамоксифеном (RR (относительный риск) = 0,62 (95% ДИ = 0,45–0,85), p = 0,003) (рис. 1). Абсолютная разница в сравниваемых группах составила 0,8% на 5-летнем интервале и 1,7% на 10-летнем. Летальность: 1149 женщин умерли в общей популяции пациенток с гормонозависимым РМЖ, из них 563 (21,5%) в группе, получавшей анастрозол, и 586 (22,6%) в группе лечения тамоксифеном. Общая выживаемость в обеих группах лечения была аналогичной (RR = 0,95 (95% ДИ = 0,84-1,06), р = 0,35) (рис. 1).
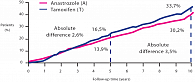
Последующие данные выживаемости без признаков заболевания (рис. 2) в исследуемых группах подтверждают преимущество в эффективности анастрозола над тамоксифеном. Так, если в 5-летнем промежутке абсолютное преимущество составляло 2,6%, то после завершения 10-летнего лечения этот показатель достиг 3,5% (RR = 0,86, (95% ДИ = 0,78–0,95), p = 0,003).
Эти цифры лишь подтверждают ранее полученные результаты.
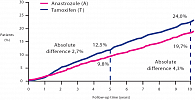
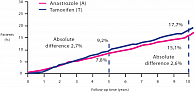
Абсолютная разница в безрецидивной выживаемости между группами анастрозола и тамоксифена у рецепторпозитивных пациентов увеличилась с течением времени. Если на 5-летнем интервале эта разница составляла 2,7%, то к 10 годам лечения она увеличилась до 4,3%. Таким образом, более высокая эффективность анастрозола по сравнению с тамоксифеном была статистически значимой даже после завершения лечения (RR = 0,79 (95% ДИ = 0,70-0,89), p = 0,0002) (рис. 3). Кроме того, в группе больных с гормоночувствительным РМЖ, принимавших анастрозол, сроки до появления отдаленных метастазов были меньше по сравнению с группой лечения тамоксифеном (RR = 0,85 (95% ДИ = 0,73-0,98), р = 0,02) (рис. 4).
Оценка летальности показала, что в обеих группах общее количество погибших больных было сопоставимо – 725 (23,5%) в группе анастрозола и 745 (24,1%) в группе тамоксифена. Однако следует отметить, что у пациенток, принимавших анастрозол, смертность после прогрессирования заболевания была несколько ниже (11,2%) в сравнении с больными, получавшими тамоксифен (12,9%) (RR = 0,87 (95% ДИ = 0,74–1,02), р = 0,09). Сравнение показателей смертности от другой патологии, злокачественных новообразований других органов или смертности, не связанной с прогрессированием, не выявило существенной разницы в исследуемых группах.
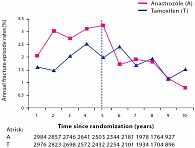
Отмеченный ранее в публикациях повышенный риск переломов в период применения анастрозола в сравнении с лечением тамоксифеном нивелируется к периоду прекращения терапии, и в 8-9-летнем промежутке происходит выравнивание показателей в обеих группах (RR = 0,98 (95% ДИ = 0,81–1,32), р = 0,5) (рис. 5). Оценка безопасности применения препаратов после завершения лечения показала, что серьезные побочные явления в обеих группах лечения были сопоставимы (рис. 5). Никаких новых нежелательных явлений не было выявлено (табл. 1).
Таким образом, проведенный статистический анализ исследования ATAC, проводимого в течении 10 лет показал, что анастрозол имеет ряд преимуществ по сравнению с тамоксифеном при эндокринотерапии гормонопозитивного РМЖ. К ним относятся: увеличение времени до появления отдаленных метастазов, увеличение безрецидивной выживаемости, а также выживаемости без признаков заболевания, существенное снижение риска контралатерального РМЖ. Не выявлено статистической разницы в общей выживаемости больных в обеих группах. Снижение риска переломов отмечено после завершения терапии анастрозолом. Анализ еще раз подтвердил преимущество в эффективности применения анастрозола в адьювантном режиме у пациенток гормонозависимым РМЖ в течение 5 лет лечения.
При этом одним из основных критериев отбора больных для терапии является гормонорецепторный статус опухоли.
" id="sender_art_description" name = "SENDER_ART_DESCRIPTION" />Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.