Использование инсулина аспарт при помповой инсулинотерапии в детской клинической практике
- Аннотация
- Статья
- Ссылки

К настоящему времени более 200 тыс. пациентов в США, более 35 тыс. пациентов в Германии, более 10 тыс. пациентов в Польше находятся на помповой инсулинотерапии. В России помповая инсулинотерапия используется с 2004 года; на текущий момент ее применяют более 3500 человек. В Институте детской эндокринологии наблюдаются 165 пациентов, использующих инсулиновую помпу, в возрасте от 1,5 до 22 лет (1).
Большинство исследований по эффективности и безопасности помповой инсулинотерапии проведено у взрослых пациентов.
К настоящему времени получено достаточно убедительных данных о том, что помповая инсулинотерапия показана и эффективна у детей и подростков при условии адекватной поддержки медицинским персоналом и комплаентности со стороны пациентов. Результатов исследований, посвященных длительному использованию помповой инсулинотерапии у детей и подростков, немного.
Результаты зарубежных исследований помповой терапии
Последний опубликованный мета-анализ исследований, сравнивающих CSII и MDI (multiple daily injection – режим множественных ежедневных инъекций) (2, 3), продемонстрировал улучшение гликемического контроля с использованием помповой инсулинотерапии у пациентов с сахарным диабетом 1 типа (СД 1 типа). В настоящее время существует только несколько обзоров, посвященных применению CSII у взрослых, подростков и маленьких детей с СД 1 типа.
Первые значительные исследования эффективности и безопасности инсулиновых помп в детском возрасте были проведены Weinzimer et al., поддержанные NIH (Национальным институтом здоровья), которые назвали АВС (Adolescents Benefit from Control – польза подросткам от контроля).
В дебюте этого исследования все пациенты получали традиционную схему введения инсулина: ежедневно 2 инъекции инсулина. 75 пациентам, включенным в исследование, было предложено самим выбрать режим интенсифицированной инсулинотерапии: 25 выбрали терапию CSII, и 50 пациентов выбрали MDI (т.е. 3 и более ежедневных инъекций двух видов инсулина – короткого действия и пролонгированного, с помощью шприц-ручек). Получающие как CSII, так и MDI терапию пациенты изначально демонстрировали улучшение метаболического контроля в первые шесть месяцев исследования. Однако этот уровень компенсации углеводного обмена было более сложно удержать на MDI терапии – средний уровень HbA1c был выше по сравнению с пациентами, получающими CSII терапию, через 12 месяцев (8,3% против 7,5%).
Наиболее значимыми явились данные о более низком уровне тяжелых гипогликемий (на 50% меньше при CSII по сравнению с MDI терапией), при том, что уровень HbA1c был также ниже в группе с CSII терапией. При исследовании качества жизни в целом психосоциальное самочувствие улучшилось в обеих группах подростков. Однако пациенты на CSII терапии сообщили, что им было легче справляться с диабетом. По этим результатам сравнения с MDI терапией было заключено, что CSII терапия может обеспечить более безопасное и более легкое достижение целей интенсивной терапии у подростков с СД типа 1.
Основываясь на успехах ABC, мультидисциплинарная врачебная команда начала осуществлять более интенсивное использование CSII в педиатрической диабетической клинике. Так, число пациентов, использующих терапию CSII, растет очень большими темпами, и все они используют аналоги инсулина ультракороткого действия.
В одном из сообщений были описаны клинические результаты первых 161 пациентов (в возрасте от 18 месяцев до 18 лет), у которых терапия CSII с использованием аналогов инсулина ультракороткого действия была начата в Педиатрическом Диабетическом Центре с 1997 года (4). В исследование были включены только пациенты с СД типа 1, которые не менее 1 года получали инсулин-помповую терапию, и их клинические данные были собраны проспективно (перед и после начала применения CSII терапии), используя стандартизованные формы и базу данных, разработанную для этой цели. Из 161 ребенка, включенного в исследование, 26 детей были дошкольного возраста (< 7 лет), 76 – школьного возраста (7-11 лет) и 59 – подросткового возраста (12-18 лет). Перед началом CSII терапии средний уровень HbA1c составлял 7,1% у дошкольников, 7,8% – у школьников и 8,1% – у подростков. Было отмечено статистически достоверное снижение среднего уровня HbA1c на 0,6-0,7% после 12 месяцев CSII терапии во всех трех группах. Этот уровень HbA1c сохранился при последнем визите, через 32 ± 9 месяцев после начала CSII терапии.
Улучшенный контроль диабета был достигнут при использовании CSII терапии без увеличения суточной дозы инсулина, и был ассоциирован со снижением частоты эпизодов тяжелой гипогликемии на 32%. Наибольшее снижение частоты тяжелой гипогликемии отмечалось в группе дошкольников. На основании этих данных было сделано заключение, что CSII терапия – эффективная альтернатива инъекционной терапии в большой Педиатрической Диабетической Клинике, и что даже у самых юных пациентов CSII может использоваться для безопасного снижения уровня HbA1c.
Число детей и подростков, использующих CSII в Диабетической Клинике, продолжает расти. 54,7% пациентов (т.е. 512 из 936 детей) используют помповую терапию с хорошими результатами. Последний уровень HbA1c у пациентов на помпе был 7,3 ± 1,2% (среднее ± SD), в то время как у пациентов, получающих инъекционную терапию, уровень HbA1c составил 7,8 ± 1,6%. Более 95% детей, у которых была начата помповая терапия, остались на ней после последнего визита в клинику.
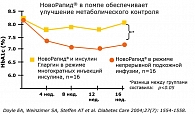
Doyle E. et al. (Йельский университет) докладывали о своем клиническом опыте использования инсулина аспарт в режиме CSII по сравнению с применением инсулинов аспарт и гларгин в режиме MDI у детей и подростков с СД 1 типа (5). Было отмечено статистически достоверное снижение уровня HbA1c с 8,2% до 7,3% до начала и в процессе проведения CSII терапии в группе CSII по сравнению с MDI (рисунок 1).
В исследовании Weinzimer et al. анализировалась эффективность и безопасность инсулина аспарт в режиме CSII по сравнению с инсулином лизпро в группе детей и подростков 4-18 лет. Статистических различий по уровню глюкозы крови натощак, количеству гипогликемических эпизодов отмечено не было. Через 16 недель 59,7% пациентов в группе аспарт и 43,8% в группе лизпро достигли целевых значений гликированного гемоглобина HbA1c по критериям Американской диабетической ассоциации (< 8,5% для детей до 6 лет и < 8% для детей и подростков 6-18 лет). Суточная доза инсулина при этом была статистически значимо ниже в группе аспарт (6).
В исследовании Alemzadeh et al. оценивалась эффективность использования CSII у маленьких детей. В исследовании приняли участие 14 детей в возрасте 3,9 ± 0,8 лет, получающих инсулин аспарт, которые в ходе исследования с режима MDI были переведены на помповую инсулинотерапию. Через год после начала исследования не отмечалось изменений в уровне гликированного гемоглобина HbA1c, частоте гипогликемических эпизодов и среднем уровне гликемии, в то время как средняя амплитуда колебаний гликемии была значительно снижена (210 ± 31 vs 168 ± 22 мг/дл, p < 0,005) (7).
В мультицентровом исследовании Jakisch et al., оценивающем эффективность CSII по сравнению с режимом множественных ежедневных инъекций, приняли участие 434 пары пациентов в возрасте до 18 лет, у которых в течение 3 лет оценивались изменения в уровне HBA1c, частоте гипогликемий, частоте эпизодов диабетического кетоацидоза (ДКА), индекс массы тела (ИМТ). По результатам исследования было показано, что нет статистических отличий в уровне HbA1c, ИМТ в обеих группах увеличился одинаково, в то время как частота гипогликемий и ДКА в группе CSII была статистически значимо ниже (8).
Отмечена наибольшая эффективность помповой инсулинотерапии в плане снижения частоты гипогликемий при одновременном использовании длительного мониторирования гликемии в режиме реального времени (12).
Безопасность и эффективность CSII: рандомизированные клинические исследования
При взгляде на увеличивающееся в последнее время использование CSII терапии у детей, следует отметить, что рандомизированные исследования, сравнивающие CSII и MDI, относительно редки.
Из следующих трех анализируемых рандомизированных контролируемых исследований одно имело перекрестный дизайн (9), в то время как два других – параллельный дизайн (10, 11). В данных исследованиях приняли участие в общей сложности 74 ребенка. Продолжительность периодов лечения и наблюдения была 16 недель в двух исследованиях и 52 недели – в одном исследовании. В двух исследованиях участвовали подростки (9, 10). Одно исследования включало детей младшего возраста, в среднем 4 лет. В исследовании с более старшими детьми использовался инсулин регуляр (10), в двух исследованиях с детьми младшего возраста использовались аналоги инсулина в инсулиновых помпах и в качестве болюса в режиме MDI в группе сравнения. Инсулин гларгин использовался в качестве базального инсулина в группе MDI у всех пациентов в одном исследовании (9) и у 60% детей в конце другого исследования (11), в то время как оставшиеся пациенты в этом исследовании в качестве базиса использовали инсулины NPH и ультраленте.
Гликированный гемоглобин снижался более выражено у пациентов в группе CSII во всех трех анализируемых исследованиях. В конце исследования HbA1/HbA1c был значительно ниже в группе CSII в исследованиях, проведенных у подростков (9, 10). В исследовании, включающем детей младшего возраста (11), гликированный гемоглобин был немного выше в группе CSII, но не достигал статистической значимости.
Во всех трех исследованиях отмечалась более низкая потребность в инсулине в группе CSII по сравнению с MDI в конце периода наблюдения, при этом в исследованиях с подростками (9, 10) эти отличия были статистически значимыми.
Во всех анализируемых исследованиях число тяжелых гипогликемических эпизодов очень мало. Только три тяжелых гипогликемии были зафиксированы у пациентов в группе CSII и шесть эпизодов в группе MDI во всех исследованиях. В одном исследовании (9) четыре пациента в группе MDI и один в группе CSII перенесли тяжелые гипогликемии. Не было найдено различий в группах CSII и MDI в двух других исследованиях, где описывалось по одному эпизоду тяжелой гипогликемии в каждой группе лечения в обеих публикациях (10, 11) соответственно.
В исследовании (9) было по одному эпизоду кетоацидоза в обеих группах лечения, в то время как в другом исследовании (11) во всех группах кетоацидоз зафиксирован не был.
Частота отказов от использования CSII, по данным Hofer et al., невелика и составляет 4% для детей в возрасте 10-15 лет (13).
Проведенные нерандомизированные и рандомизированные исследования продемонстрировали эффективность CSII терапии у детей и подростков с СД 1 типа во всех возрастных группах. Однако не существует единого подхода к лечению, идеального для каждого пациента. Доступность многих терапевтических опций позволяет клиницистам, занимающимся детским диабетом, выбрать лучший метод лечения для каждого отдельного пациента в отдельный период времени.
Результаты собственных исследований
Институтом детской эндокринологии накоплен 6-летний опыт клинического использования инсулиновых помп. На помповую терапию переведено 165 пациентов с СД 1 типа в возрасте от 1,5 до 22 лет, с длительностью сахарного диабета от 0,5 до 20 лет. Уровень гликированного гемоглобина HbA1c исходно составлял от 5,6 до 14,7% (в среднем 9,95% ± 1,77%). Все пациенты проходили индивидуальное обучение по работе с помпой, которое занимало 3 дня и дополнительные занятия, направленные на углубление и совершенствование знаний и навыков работы.
С целью проведения сравнительного исследования эффективности применения помповой инсулинотерапии у детей и подростков по сравнению с режимом множественных ежедневных инъекций, из общей выборки больных были сформированы две группы пациентов с СД 1 типа в возрасте 5-22 лет (12,8 ± 5,4) и длительностью заболевания 3-14 лет (6,2 ± 2,9): I группа получала помповую терапию (n = 31), а II группа находилась на режиме множественных инъекций (n = 30). Группы не различались по возрасту, длительности заболевания и исходному уровню гликированного гемоглобина HbA1c. Использовались инсулиновые помпы Minimed 508, MiniMed 712 и аналог инсулина ультракороткого действия аспарт в группе CSII. В группе MDI использовались аналоги инсулинов гларгин перед сном и аспарт перед основными приемами пищи. Самоконтроль гликемии осуществлялся 4-8 раз в сутки. Все пациенты находились на стационарном лечении 10-14 дней в начале исследования и в дальнейшем посещали клинику амбулаторно не менее 1 раза в 6 месяцев в течение 4 лет для коррекции инсулинотерапии. Уровень HbA1c определялся перед началом исследования и через 12, 24, 36 и 48 месяцев. Также анализировалась частота ДКА и тяжелых гипогликемий.
В группе MDI уровень HbA1c до начала терапии составлял 9,8 ± 2,0%, через 12, 24, 36, 48 месяцев 9,1 ± 1,8%, 8,9 ± 2,6%, 9,2 ± 1,5%, 9,1 ± 1,6% соответственно. В группе CSII уровень HbA1c до начала терапии составлял 9,9 ± 1,77%, через 12, 24, 36, 48 месяцев 8,9 ± 1,29% (p < 0,05), 9,2 ± 2,3%, 8,9 ± 1,94%, 8,9 ± 1,8% соответственно.
Таким образом, через 1 год от начала исследования отмечается статистически значимое снижение уровня гликированного гемоглобина HbA1c, более выраженное в группе CSII. Однако при долгосрочном наблюдении на протяжении 4 лет группы CSII и MDI имели близкие показатели HbA1c (рисунок 2).
Диабетический кетоацидоз имел место у двух пациентов в группе CSII вследствие тромбирования катетера и у двух пациентов в группе MDI вследствие вирусной инфекции.
У 52 пациентов, получающих помповую инсулинотерапию, проводилось длительное мониторирование гликемии с помощью системы CGMS.
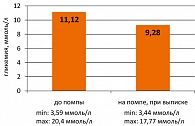
Среднесуточная гликемия до начала помповой терапии составляла 11,12 ± 1,83 ммоль/л (n = 17), с колебаниями гликемии: минимальная – 3,59 ммоль/л, максимальная – 20,4 ммоль/л. После начала помповой терапии и подбора режимов введения инсулина, среднесуточная гликемия составляла 9,28 ммоль/л (p < 0,05), с колебаниями гликемии: минимальная – 3,44 ммоль/л, максимальная – 17,77 ммоль/л (рисунок 3).
Таким образом, было доказано, что при использовании инсулиновой помпы происходит не только снижение среднего уровня гликемии и гликированного гемоглобина, но и вариабельности гликемии, что особенно важно для предотвращения развития сосудистых осложнений.
У большинства пациентов после перевода на помпу доза инсулина уменьшилась в среднем на 9,6%. При этом базисная доза инсулина (количество единиц инсулина в час) после завершения коррекции режимов введения, изменялась в течение суток 3-6 раз (4,5 ± 1,2). У большинства пациентов базисная доза инсулина была больше в ночные часы, в среднем на 0,3 Ед/ч, при этом у маленьких пациентов (до 6-7 лет) отмечалась обратная картина: минимум потребности в инсулине в ночные часы и возрастающая потребность днем.
За время наблюдения развитие тяжелых гипогликемий было отмечено у пяти пациентов. У одного из них тяжелые гипогликемии наблюдались 4 раза вследствие стремления родителей к нормогликемии и завышенной дозы базисного инсулина, при этом гипогликемии не служили поводом для пересмотра дозы инсулина. У 4 остальных пациентов отмечалось по одному эпизоду: в одном случае вследствие большой базисной дозы инсулина в ночные часы, в двух случаях из-за неправильно рассчитанной болюсной дозы перед завтраком, у одного – после физической нагрузки. Таким образом, несмотря на снижение риска тяжелых гипогликемий, необходимо уделять особое внимание этому вопросу при обучении родителей.
Реакция кожи в местах введения катетера наблюдалась у 8 больных в виде небольшой гиперемии, исчезавшей спустя несколько часов после смены места введения. Воспалительные изменения кожи и подкожной клетчатки в местах введения катетера отмечались в 3 случаях (в двух – на 3-й день, в одном – на 4-й день после установки катетера). Со слов родителей, нарушений гигиенического режима при этом не было.
За 6 лет наблюдения тяжелый кетоацидоз был выявлен в 20 случаях (в среднем не более 2% за каждый год наблюдения). В одном случае – в результате недостаточной комплаентности пациента в виде грубых нарушений диеты, без соответствующей коррекции дозы инсулина; в 7 случаях – из-за небрежного обращения с помпой (выпадение катетера); в 3 случаях – из-за технической неисправности помпы и в 9 случаях – в результате тромбирования катетера.
Частота отказов после перевода на помпу составляла 7,2% (13 человек), из них 3 человека спустя 4 месяца–2 года вновь вернулись к помповой терапии. Наиболее частая причина отказов – психологическая (реакция со стороны сверстников). С годами частота отказов снижается (с 15,6% в первые 5 лет до 2,9% в последние 2,5 года), что связано, очевидно, с широким распространением помповой терапии в нашей стране. Применение ее становится привычным методом терапии и не вызывает прежних реакций у окружающих.
Заключение
Помповая терапия у детей и подростков находит все более широкое распространение и ассоциирована с улучшением гликемического контроля и удобства для пациентов. При этом в настоящее время используются практически только инсулиновые аналоги ультракороткого действия, повышающие гибкость дозирования как базисного, так и болюсного инсулина.
Минимизация риска осложнений помповой терапии достигается теми же методами, которые рекомендуются для обеспечения безопасности традиционной инсулинотерапии у всех пациентов с СД 1 типа, и в первую очередь – тщательным и грамотным самоконтролем. Более совершенный контроль уровня глюкозы при сахарном диабете 1 типа как при традиционной, так и при помповой терапии возможен при использовании системы длительного мониторирования гликемии. Еще большее снижение риска использования помп и повышения эффективности их работы будет связано, как ожидается, с совершенствованием технологий и развитием систем с обратной связью.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.