Как повысить приверженность лечению и улучшить контроль при бронхиальной астме, или Невозможное возможно
- Аннотация
- Статья
- Ссылки
- English

Как известно, длительные цели терапии бронхиальной астмы (БА) заключаются в достижении контроля симптомов и поддержании нормального уровня активности пациента, а также в минимизации риска обострений, развития фиксированной обструкции бронхов и побочных эффектов лекарственных препаратов [1, 2].
Результаты международных исследований свидетельствуют, что за последние 15–20 лет доля пациентов с контролируемым течением БА существенно возросла: с 5% в 1999 г. [3] до 55% в 2014 г. [4]. Значительный рост доли больных с контролируемой БА отмечается и в нашей стране. Согласно данным исследования с участием 1000 взрослых больных БА из 12 городов России, у 58% пациентов отмечается контролируемая или частично контролируемая БА по критериям GINA [5]. Вместе с тем сохраняется высокая доля больных с неконтролируемым течением БА, а значит, с высоким риском развития обострений, госпитализаций и низким качеством жизни.
Приверженность лечению пациентов с астмой
Среди основных причин отсутствия контроля БА прежде всего необходимо выделить недостаточную приверженность назначенному лечению, неправильную технику ингаляции и эффективность молекул. Эти причины должны быть рассмотрены в первую очередь у пациента с неконтролируемыми симптомами БА (рис. 1) [2]. Термин «приверженность», часто используемый наравне с термином «комплаенс», в медицине означает степень, с которой пациент следует предписанному лечению. Приверженность включает три специфических компонента:
- принятие рекомендаций (пациент согласен принимать лекарственные средства/следовать рекомендациям);
- соблюдение назначений (пациент применяет лечение, как предписано врачом);
- постоянство (степень, с которой пациент следует назначенному лечению в течение длительного периода времени).
Приверженный лечению пациент вовремя и правильно принимает препарат, в полной назначенной дозе, соблюдает рекомендуемый образ жизни и диету, сохраняет психологическое равновесие и веру в успех терапии. Неприверженный пациент нарушает предписанный режим лечения, в большинстве случаев не осознавая возможные последствия. В клинических исследованиях приверженность часто рассматривают как дихотомическую переменную с порогом 60 или 80% предписанных доз. На практике это непрерывный процесс, имеющий разные формы и степень проявления. Не существует формального консенсуса относительно порога, который определяет плохую или хорошую приверженность: обычно он варьируется от < 70 до < 100% предписанных доз. Вместе с тем в большинстве исследований последних лет по оценке оптимального уровня приверженности при БА установлен уровень 80–100% назначенных доз [5, 6]. При БА оценивают приверженность длительной контролирующей терапии, то есть применению ингаляционных глюкокортикостероидов (ИГКС), антилейкотриеновым препаратам (АЛП), комбинации ИГКС + бета-2-агонисты длительного действия (ДДБА) или ИГКС + АЛП, при легкой/среднетяжелой контролируемой атопической БА – использованию аллергенспецифической иммунотерапии (АСИТ). Плохая приверженность при БА означает недостаточное применение базисных препаратов и, напротив, избыточное использование скоропомощных препаратов – короткодействующих бета-2-агонистов (КДБА) [7].
Результаты многочисленных исследований свидетельствуют, что около половины пациентов с БА, как взрослых, так и детей, имеют низкую приверженность назначенной терапии для контроля симптомов БА, что напрямую связано с увеличением частоты обострений и госпитализаций, назначением пероральных ГКС, незапланированных визитов к врачу по поводу БА, снижением качества жизни. Многие пациенты даже не начинают применять контролирующие БА препараты после их назначения врачом [8, 9] или приходят за рецептом только один раз после первоначального назначения [10, 11] либо преждевременно прекращают прием контролирующих лекарственных препаратов, несмотря на риск обострения [12].
При электронном мониторинге применения лекарственных средств показатели приверженности составляют менее 70% предписанных доз. В ряде исследований этот показатель был еще ниже: около 60% во взрослой популяции[13], около 50% – в педиатрической [14], 33–41% – среди подростков [15].
Как показали результаты европейского online-исследования, всего 48% пациентов с БА принимают контролирующие препараты каждый день, 27% принимают их не каждый день, а 18% – только при возникновении симптомов [4].
Низкую приверженность терапии препаратом, назначенным для контроля симптомов БА, респонденты объясняют отсутствием необходимости в его приеме (50% случаев) или забывчивостью (18%). Интересно, что даже после госпитализации по поводу обострения БА приверженность контролирующим противоастматическим препаратам и пероральным ГКС снижается вдвое к седьмому дню после выписки [16].
Выделяют следующие виды неприверженности:
- непреднамеренную (забывчивость, стоимость, непонимание);
- преднамеренную (предубеждение, боязнь побочных эффектов, культурные вопросы, стоимость).
К факторам, снижающим приверженность пациентов лечению БА, относят сложный режим дозирования, побочные действия и отсроченный эффект лекарственных средств, их стоимость, наличие сопутствующих заболеваний и возраст.
Крайне важно выявить пациента с низкой приверженностью, поскольку плохая приверженность контролирующей терапии – фактор риска развития обострений БА. Как выявить пациентов с низкой приверженностью? Эксперты GINA рекомендуют:
- правильно формулировать вопрос (например: когда вы чаще забываете принять препарат – утром или вечером? как часто вы принимаете препарат – три дня в неделю, чаще или реже?);
- проверять дату назначения, срок годности, счетчик доз;
- спрашивать мнение пациента о назначенном препарате и возможных опасениях.
В ряде исследований изучали вмешательства, направленные на повышение приверженности пациентов лечению. Кохрейновский обзор рандомизированных исследований эффективности различных методов, повышающих приверженность пациентов терапии при разных хронических заболеваниях, включал в том числе 13 клинических исследований по БА [17]. Исследователи анализировали различные виды вмешательств:
- образовательные программы для пациентов, семей пациентов и врачей;
- психотерапевтические методики;
- программы с участием медицинских сестер, фармацевтов;
- использование интернет-технологий;
- различные виды напоминаний (телефонным звонком, SMS);
- изменение режима лечения и др.
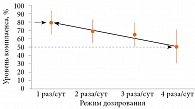
Авторы обзора пришли к заключению, что повысить приверженность при коротком курсе лечения можно с помощью большинства простых вмешательств, тогда как повысить приверженность лечению хронических заболеваний даже с помощью сложных комплексных методов достаточно сложно. В частности, только в шести из 13 клинических исследований с участием больных БА показано улучшение приверженности, которое было умеренным и продолжалось короткий период. Важный вывод: простой режим терапии может иногда повышать приверженность и исходы лечения как при длительном, так и при коротком курсе терапии. Уменьшение кратности применения препаратов в течение дня с четырех до двух или одного раза приводит к увеличению приверженности (рис. 2) [18]. Исследования сравнительной приверженности больных при однократном режиме дозирования препаратов для длительного контроля (ИГКС, ИГКС/ДДБА, АЛП) и по крайней мере двукратном свидетельствуют в пользу первого [18–21].
Таким образом, прогнозировать плохую приверженность сложно, поскольку типичного неприверженного пациента не существует и низкая приверженность обычно обусловлена множеством факторов, в частности характеристиками пациента и внешними факторами, не связанными с больным [22].
Оптимальные методы выявления низкой приверженности лечению – наблюдение за больным, оценка контроля БА, правильно сформулированные вопросы о применении препарата базисной терапии БА и проверка даты назначения, срока годности, счетчика доз. Информирование и обучение пациента, партнерские отношения с больным в вопросе лечения БА, а также простой режим терапии, предусматривающий однократный прием препарата для контроля симптомов БА (один раз в день), или режим единого ингалятора – залог оптимальной приверженности лечению БА.
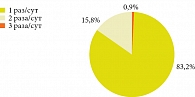
Следует отметить, что большинство пациентов с БА и ХОБЛ предпочитают однократный прием препаратов в течение суток. На рисунке 3 представлены результаты интернет-опроса японских пациентов с БА и ХОБЛ о предпочтительной частоте приема препаратов для контроля заболеваний [23].
Вилантерол/флутиказона фуроат – единственная комбинация для однократного применения в день
Абсолютное большинство комбинированных препаратов (ИГКС/ДДБА) рекомендуют применять для контроля симптомов дважды в день. Тем не менее появление ультрадлительных бета-2-агонистов, а также молекул ИГКС, эффективных на протяжении 24 часов, в частности флутиказона фуроата (ФФ), позволило создать уникальный комбинированный препарат для однократного применения в день – вилантерол/флутиказона фуроат (Релвар Эллипта). По сравнению с флутиказона пропионатом ФФ имеет более длительную продолжительность действия, большую аффинность к рецептору и более эффективен в клетках дыхательных путей, что позволяет использовать его один раз в день для контроля астмы [24, 25]. Вилантерола трифенатат (ВИ) – бета-2-агонист пролонгированного действия, применяемый один раз в день. По сравнению с салметеролом вилантерол обладает более быстрым началом и большей продолжительностью действия с гораздо более высокой селективностью в отношении бета-2-рецепторов [26]. Упрощая режим дозирования для пациента, ВИ/ФФ способен повысить приверженность лечению и тем самым более качественно контролировать симптомы астмы [27]. Препарат ВИ/ФФ (Релвар) в уникальном устройстве доставки Эллипта – первая и единственная фиксированная комбинация ИГКС и ДДБА с 24-часовой эффективностью при однократном применении. Причем разницы в отношении функции легких больных БА при утреннем или вечернем приеме препарата не установлено [28].
Клинические исследования препарата ВИ/ФФ демонстрируют его значимо более высокую эффективность по сравнению с монотерапией ИГКС (флутиказона фуроат), применяемыми в эквипотентных дозах, в отношении функции легких, снижения частоты обострений и улучшения качества жизни [29, 30]. Бронхопротективный эффект на фоне аллергенной провокации специфичным для каждого пациента аллергеном (клещ домашней пыли, шерсть/перхоть кошки, пыльца березы и трав) при использовании ВИ/ФФ выше, чем при применении монокомпонентов [31].
Рандомизированные клинические исследования эффективности и безопасности однократно применяемой комбинации ВИ/ФФ и двукратных комбинаций ИГКС/ДДБА, в частности комбинации салметерола/флутиказона пропионата, для терапии пациентов с БА продемонстрировали схожую эффективность в отношении влияния на функцию легких при меньшей кратности приема в течение суток [32].
Метаанализ исследований сравнительной эффективности ВИ/ФФ показал его преимущество перед монотерапией ФФ или флутиказона пропионатом в отношении улучшения функции легких, снижения частоты обострений, бессимптомных дней, повышения качества жизни, а также сравнимую эффективность и безопасность с двукратным применением салметерола/флутиказона пропионата [33].
Солфордское исследование легких в области БА (Salford Lung Study – SLS-Asthma) стало первым проспективным рандомизированным контролируемым клиническим исследованием III фазы с открытым дизайном, которое проводилось в течение 12 месяцев в условиях, максимально приближенных к реальной клинической практике [34]. Результаты этого исследования были получены на популяции пациентов с БА, наиболее полно представляющей повседневную клиническую практику в связи с минимальными критериями исключения и возможностью сбора информации с помощью электронной медицинской карты в условиях обычной клинической практики, и помогли достоверно оценить потенциал комбинации ВИ/ФФ, применяемой один раз в день. Исследователи сравнивали эффективность в достижении контроля и безопасность препарата Релвар Эллипта и стандартной поддерживающей терапии БА. Всего в исследовании участвовало 4233 пациента с БА, находившихся под наблюдением в амбулаториях города Солфорд (округ Южный Манчестер) [34]. В крупной разнородной популяции больных БА лечение комбинацией ВИ/ФФ (22/92 или 22/184 мкг один раз в день) в порошковом ингаляторе Эллипта обеспечивало лучший контроль заболевания, чем применение других ИГКС или комбинации ИГКС + ДДБА, назначаемой и изменяемой по усмотрению врача [34]. В группе терапии ВИ/ФФ пациентов, достигших или улучшивших контроль БА, было больше, чем в группе терапии другими комбинированными препаратами или монотерапии ИГКС. При этом шансы достичь контроля на терапии ВИ/ФФ были практически в два раза выше. Уровень контроля астмы в группе ВИ/ФФ стабильно поддерживался на протяжении 12 месяцев [34].
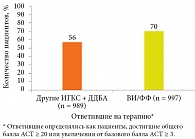
Кроме того, аналогичные результаты получены при изолированном сравнении группы ВИ/ФФ с группой других ИГКС/ДДБА. Так, доля больных, которые достигли или улучшили контроль БА, согласно результатам АСТ-теста, составила 70% в группе ВИ/ФФ и 56% в группе других ИГКС + ДДБА (рис. 4). У большинства пациентов контроль БА улучшился в ранние сроки. Наиболее выраженные изменения отмечались до 12-й недели, впоследствии динамика стабилизировалась [35].
Терапия ВИ/ФФ стабильно улучшала качество жизни и рабочую продуктивность у больных БА по сравнению с терапией ИГКС или другими ИГКС + ДДБА. Так, среднее изменение общей суммы баллов стандартизованного опросника для оценки качества жизни больных БА AQLQ также были выше в группе ВИ/ФФ. При этом клинически значимый ответ на лечение (> 0,5) на 52-й неделе отмечался у 55% больных в группе ВИ/ФФ и у 43% в группе терапии ИГКС или других ИГКС + ДДБА (р < 0,001) [35].
Примечательно, что в исследовании не получено каких-либо новых предупреждений по безопасности. Исследование проводилось в повседневной клинической практике с минимальным вмешательством в жизнь пациентов, но все основные серьезные нежелательные явления учитывались и оказались сопоставимы по частоте в обеих группах лечения. Общая частота развития пневмоний была низкой. Анализ получаемого лечения в момент развития этого нежелательного явления показал, что в 21 случае пневмония развивалась при приеме ВИ/ФФ и в 21 случае – при приеме других ИГКС или ИГКС + ДДБА. Следовательно, ВИ/ФФ помимо эффективности обладает хорошим профилем безопасности.
Таким образом, улучшение симптомов БА по всем показателям АСТ-теста со значительным перевесом наблюдалось в группе ВИ/ФФ (Релвар Эллипта): 70% пациентов в группе ВИ/ФФ и 56% – в группе других ИГКС + ДДБА. Можно предположить несколько составляющих успеха терапии ВИ/ФФ: повышение приверженности вследствие однократного применения препарата, удобство устройства доставки, а также эффективность молекул, входящих в его состав.
Заключение
Современные цели терапии БА заключаются в достижении и поддержании контроля симптомов и профилактики обострений заболевания. Несмотря на широкий выбор препаратов для длительного контроля БА, по крайней мере у половины пациентов наблюдаются неконтролируемое течение астмы и высокий риск обострения. Среди факторов, препятствующих достижению контроля БА, выделяют:
- клинические (сопутствующие заболевания, постоянный контакт с аллергеном, генетические: полиморфизм генов бета-2-адренорецепторов, ГК-рецепторов, рецепторов цис-лейкотриенов и др.);
- факторы, зависящие от пациента (приверженность контролирующей терапии, правильная техника ингаляции, отказ от вредных привычек);
- факторы, зависящие от врача (правильный диагноз, адекватная оценка контроля и адекватная терапия БА).
Одной из ведущих причин недостижения контроля и повышенного риска обострения БА является низкая приверженность базисной контролирующей терапии. Около половины пациентов с БА, как взрослых, так и детей, имеют низкую приверженность назначенной противоастматической терапии. Информирование и обучение пациента, партнерские отношения с больным в вопросе лечения БА, а также простой режим терапии, позволяющий применять препараты для контроля симптомов БА один раз в день, – залог оптимальной приверженности лечению БА.
Среди комбинированных препаратов ИГКС и ДДБА существует единственная фиксированная комбинация ВИ/ФФ с 24-часовой эффективностью при однократном применении. Причем разницы в отношении функции легких больных БА при утреннем или вечернем приеме препарата не установлено, что означает свободу и удобство выбора применения препарата в зависимости от предпочтений пациента.
В Солфордском исследовании, проведенном в условиях реальной клинической практики, улучшение контроля БА со значительным перевесом наблюдалось у пациентов, получавших ВИ/ФФ (Релвар Эллипта), – 70%. При использовании других ИГКС + ДДБА этот показатель составил 56%. Кроме того, ВИ/ФФ улучшал качество жизни и рабочую продуктивность в большей степени, чем терапия ИГКС или другими ИГКС + ДДБА. Это скорее всего обусловлено более высокой приверженностью терапии и удобством применения препарата Релвар Эллипта.
N.M. Nenasheva, DM, Phd, Prof.
Russian Medical Academy for Continuing Professional Education
Contact person: Natalya M. Nenasheva, 1444031@gmail.com
Adherence to treatment with drugs for long-term control of bronchial asthma is one of the key components of successful treatment of the disease and prevention of exacerbations. However, about half of patients both adults and children have insufficient adherence due to various reasons. Simplification of the treatment regimen, in particular single use regimen can increase patient’s adherence to therapy and thus increase asthma control. Vilanterol/fluticasone furoate (VI/FF) is the first and only fixed combination of inhaled corticosteroid and long-acting beta2-agonist with 24-hour efficacy in a single dose per day. In the Salford study in real clinical practice the advantage of VI/FF therapy was demonstrated in comparison with other ICS or ICS + LABA in improvement control of bronchial asthma.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.