Кесарево сечение и сахарный диабет
- Аннотация
- Статья
- Ссылки
Сахарный диабет (СД) относится к группе метаболических (обменных) заболеваний, характеризующихся хронической гипергликемией, которая является результатом нарушения секреции инсулина или его действия либо двух этих факторов.
По данным Всемирной организации здравоохранения, сегодня 422 млн человек во всем мире страдают СД. 1,6 млн летальных исходов, произошедших в 2016 г., обусловлено СД. По прогнозам, к 2030 г. диабет станет седьмой причиной смерти в мире. По данным Управления Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, ежегодно в России диагноз СД 1-го типа устанавливают 70 тыс. подростков в возрасте от 14 лет и старше. Больше всего людей с диабетом насчитывается в Индии – 41 млн [1].
CД 1-го типа – нарушение углеводного обмена, вызванное деструкцией бета-клеток поджелудочной железы, обычно приводящей к абсолютной инсулиновой недостаточности.
Хроническая гипергликемия при СД сопровождается повреждением, дисфункцией и недостаточностью различных органов, особенно глаз, почек, нервов, сердца и кровеносных сосудов [1].
В ряде наблюдений показано, что СД 1-го типа наследуется от ближайших кровных родственников: в 10% от отца и в 3–7% от матери. Если заболевание встречается у обоих родителей, риск патологии увеличивается до 70%.
Лишний вес и ожирение считаются ведущими этиологическими факторами в патогенезе СД. Особую опасность представляют индекс массы тела (ИМТ) выше 30 кг/м2 и абдоминальный тип ожирения, при котором фигура принимает форму яблока.
Острый и хронический панкреатит, рак поджелудочной железы, травмы и некоторые другие патологии вызывают деструкцию клеток органа, что рано или поздно вызывает инсулиновую недостаточность. Согласно результатам исследований, запустить процесс разрушения клеток поджелудочной железы способны даже самые безобидные инфекции: краснуха, ветряная оспа, инфекция, вызванная цитомегаловирусом, вирусный гепатит A, грипп.
Кроме того, на развитие СД влияют частые стрессы, тяжелая психотравмирующая ситуация, малоподвижный образ жизни, гиподинамия, неправильное питание (чрезмерное увлечение сладким, фастфудом и другими легкоусвояемыми углеводами), проживание в неблагоприятных экологических условиях, курение, злоупотребление алкоголем и другими вредными привычками.
Дети, страдающие синдромом Кушинга, акромегалией, гипертиреозом, также находятся в группе риска по развитию предиабета и СД. Аутоиммунные заболевания, например системная красная волчанка, могут нарушить действие инсулина и привести к развитию СД 1-го типа [2].
Ряд лекарственных средств, таких как никотиновая кислота, некоторые виды мочегонных препаратов, антинаркотические средства, психотропные препараты и препараты для лечения вируса иммунодефицита человека (ВИЧ), негативно влияют на функционирование бета-клеток или нарушают действие инсулина. Высокое потребление азотсодержащих химических веществ, в частности нитратов и нитритов, увеличивает риск развития СД. В настоящее время активно изучается микроэлемент мышьяк на наличие потенциальной связи с диабетом [2].
В норвежском популяционном общенациональном исследовании изучали связь между потреблением глютена матерью и ребенком и риском развития СД 1-го типа у ребенка. В исследовании участвовало 86 306 детей. При среднем сроке наблюдения 12,3 года (0,7–16,0) у 346 (0,4%) детей развился СД 1-го типа (показатель заболеваемости – 32,6 на 100 тыс. человеко-лет). Установлено, что прием глютена матерью в середине беременности не связан с развитием СД 1-го типа у ребенка (скорректированное отношение рисков (ОР) 1,02 (95%-ный доверительный интервал (ДИ) 0,73–1,43) на 10 г/сут увеличения потребления глютена). Однако потребление глютена ребенком в возрасте 18 месяцев ассоциировалось с повышенным риском развития СД 1-го типа в более позднем возрасте (скорректированное ОР 1,46 (95% ДИ 1,06–2,01) на 10 г/сут увеличения потребления глютена). Исследователи предположили, что прием глютена ребенком в возрасте 18 месяцев, но не матерью во время беременности увеличивает риск развития у него СД 1-го типа [3].
Ученые изучали влияние дефицита витамина B12 на развитие СД. Предполагается, что дефицит витамина В12 является триггерным фактором для развития СД [4].
В последнее время в связи с ростом операций кесарева сечения в мире появилось большое количество работ, посвященных анализу последствий такой операции для матери и ребенка [5]. Как известно, частым показанием к проведению операции кесарева сечения является СД у матери. Поэтому в связи с развитием диабетической фетопатии у плода данный вопрос представляет особый интерес. Кроме того, изучается вопрос об обратной связи: как часто у детей, родившихся с помощью операции кесарева сечения, реализуется СД.
Доказано, что беременность, развившаяся на фоне СД, сопровождается риском для здоровья матери и плода [1]. Рисками для матери с СД являются прогрессирование сосудистых осложнений, более частое развитие гипогликемии, кетоацидоза, осложнений беременности (преэклампсия, эклампсия, инфекция, многоводие), повышенная смертность. У плода и новорожденного также существуют определенные риски: риск перинатальной смертности из-за крупных размеров и состояния гипогликемии после рождения, врожденные пороки развития, родовой травматизм. Подсчитано, что риск развития СД 1-го типа у детей в течение жизни составляет около 2% – при СД 1-го типа у матери, около 6% – при СД 1-го типа у отца, 30–35% – при СД 1-го типа у обоих родителей [1].
При кесаревом сечении имеют место нарушение передачи материнского микробиома и высокая степень колонизации условно-патогенными микроорганизмами, ассоциированными с больничной средой (в том числе энтерококк, энтеробактерии и клебсиеллы). Метагеномный анализ всего генома 1679 образцов микробиоты кишечника от 596 доношенных младенцев, рожденных в больницах Великобритании, показал, что способ родоразрешения является существенным фактором, влияющим на состав микробиоты на протяжении всего неонатального периода и в младенчестве [6].
Частота послеродовых гнойно-септических заболеваний после самопроизвольных физиологических родов составляет 1–5%. После патологических родов данный показатель увеличивается до 15–20%, а после операции кесарева сечения превышает 20%. Послеродовый эндометрит в случае самопроизвольных родов встречается в 3–10% случаев, после патологических – в 10–20%, после кесарева сечения – в 6–30%. Как следствие, возрастают частота назначения и длительность применения антибиотикотерапии, что негативно сказывается на грудном вскармливании [7].
В большинстве работ показано, что в группе особого риска находятся недоношенные дети, поскольку диеты с использованием специальных смесей, способствующих «догоняющему» росту маловесных новорожденных, статистически достоверно связаны с высоким риском отдаленных сердечно-сосудистых заболеваний. Искусственное вскармливание, по данным многочисленных исследований, значимо повышает риск формирования избыточного веса и ожирения, а также гипертонической болезни, атерогенной дислипидемии. К возможным механизмам реализации наследственной предрасположенности метаболических расстройств на фоне искусственного вскармливания относят усиленный выброс инсулина с последующим формированием инсулинорезистентности. Профилактическая роль грудного молока связывается с наличием в нем гормонов, оказывающих программирующее воздействие на метаболизм индивидуума. Наряду с этим метаболическое и иммунологическое программирование при грудном вскармливании осуществляется через формирование оптимальной микробиоты кишечника ребенка [8].
В настоящее время родоразрешение путем кесарева сечения можно рассматривать как фактор риска развития гипогликемии в раннем неонатальном периоде [9]. Обследовано 330 здоровых доношенных новорожденных, в том числе 254 рожденных вагинально (группа сравнения) и 76 рожденных путем плановой операции кесарева сечения (основная группа). Из исследования исключались дети, родившиеся от матерей с СД. У всех новорожденных определяли уровень глюкозы в сыворотке пуповинной крови. Установлено, что пациенты, рожденные путем операции кесарева сечения, имеют более низкие уровни глюкозы в пуповинной крови, чем дети, рожденные вагинально.
Предикторами развития послеродовой депрессии у беременных являются сопутствующий гестационный СД, а также наличие операции кесарева сечения в анамнезе. Именно эти женщины составляют группу высокого риска развития послеродовой депрессии [10], что негативно отражается на лактации. В результате нарушается формирование микробиома младенца и адекватного иммунного ответа [11].
C.R. Cardwell и соавт. в 2008 г. опубликовали систематический обзор по оценке риска развития СД 1-го типа у детей, рожденных с помощью операции кесарева сечения. Согласно результатам метаанализа, включавшего 20 исследований, у детей, рожденных путем кесарева сечения, значительно возрастает риск развития диабета 1-го типа (отношение шансов (ОШ) 1,23, 95% ДИ 1,15–1,32; р < 0,001) [12].
Между тем имеются данные, демонстрирующие отсутствие связи между операцией кесарева сечения и развитием СД. В 2016 г. в Дании было проведено национальное когортное регистровое исследование неблагоприятных условий, связанных с операцией кесарева сечения, способных влиять на риск развития СД 1-го типа у детей. Показано, что родоразрешение путем операции кесарева сечения не связано с развитием СД 1-го типа у детей [13].
Шведские ученые проанализировали 14 949 случаев развития СД 1-го типа за период с 1 января 1978 г. по 31 декабря 2013 г. Родоразрешение методом кесарева сечения чаще встречалось у возрастных матерей и женщин с более высоким ИМТ. Авторы исследования предположили, что именно факторы, приводящие к операции кесарева сечения (например, более старший возраст и более высокий ИМТ у матери), а не собственно способ родоразрешения связаны с риском развития СД 1-го типа [14].
Некоторые исследователи не исключают наличие связи между операцией кесарева сечения и риском развития иммуноопосредованных заболеваний [15, 16].
В случае кесарева сечения, как и при островковом аутоиммунитете, выявлена корреляция с изменениями транскрипции, наблюдаемыми во время активации изолированных CD4+ Т-лимфоцитов. Отмечались общие молекулярные изменения, связанные с активацией иммунных клеток, у детей, рожденных путем кесарева сечения, и детей, у которых развился аутоиммунитет [17].
Таким образом, в настоящее время вопрос связи между операцией кесарева сечения и последующим развитием СД у детей не до конца изучен.
Материал и методы
Для выяснения частоты встречаемости операции кесарева сечения среди детей с СД проведен ретроспективный анализ историй болезни больных СД 1-го типа, находившихся на лечении в эндокринологическом отделении Детской городской клинической больницы им. З.А. Башляевой.
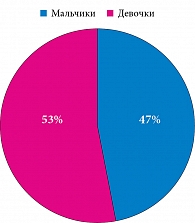
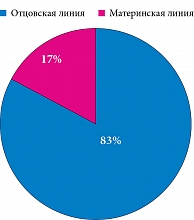
Проанализировано 45 историй – 21 (46,7%) мальчика и 24 (53,3%) девочек (рис. 1). При этом наследственность по СД 1-го типа была отягощена у 6 (13,3%) детей: у трех детей болели отцы, у двух – дедушки по линии отцов, у одного – тетя по материнской линии (рис. 2). Необходимо подчеркнуть, что ни одна из матерей обследованных детей не страдала СД.
Результаты и обсуждение
Анализ беременностей и родов позволил сделать заключение, что 66,6% детей родились от первой беременности, 20,1% – от второй, 13,3% – от третьей. Маловесных детей насчитывалось 6 (13,3%), детей, имевших при рождении массу тела свыше 4 кг (крупный плод), – 6 (13,3%), первые из двойни – 2 (4,4%) ребенка.
С помощью операции кесарева сечения родились 12 (26,7%) детей. Показанием к выполнению операции кесарева сечения стали крупный плод (четыре ребенка), двойня (два ребенка), показания со стороны матери (четыре ребенка), угроза маточного кровотечения (два ребенка, экстренное кесарево сечение).
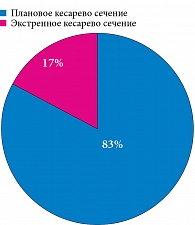
Методом планового кесарева сечения родились 10 (83,3%) детей, экстренного – 2 (16,6%) (рис. 3).
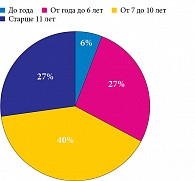
Манифестация СД отмечалась у 3 (6,6%) детей в возрасте до года, 12 (26,6%) – в возрасте от года до шести лет, 18 (40%) – от семи до десяти лет, 12 (26,6%) детей – старше 11 лет (рис. 4). К моменту дебюта заболевания 83,3% детей страдали частыми острыми респираторными инфекциями.
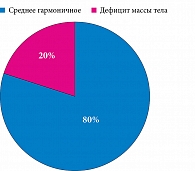
На момент поступления в стационар у 80% наблюдалось среднее гармоничное физическое развитие, у 20% имел место дефицит массы тела (рис. 5).
Выводы
Согласно результатам ретроспективного исследования, проведенного на базе Детской городской клинической больницы им. З.А. Башляевой, частота встречаемости операции кесарева сечения у детей с СД составила 26,6%, что совпадает с данными научной литературы. Чаще СД страдали дети, родившиеся от первой беременности путем планового кесарева сечения, имевшие среднее гармоничное физическое развитие. Дебют заболевания приходился на возраст от семи до десяти лет. У 13,3% имел место отягощенный по СД 1-го типа наследственный анамнез, в большинстве (83,3%) случаев по отцовской линии (причем болели только мужчины). Ни одна из матерей обследованных детей не страдала СД. Из других факторов риска можно отметить респираторные заболевания – ими часто болели 83,3% детей.
Заключение
Установлена связь между операцией кесарева сечения и развитием СД 1-го типа у детей. Можно предположить, что адекватное отношение к показаниям для проведения операции кесарева сечения, уменьшение его частоты – один из факторов, сдерживающих развитие СД. Безусловно, необходимы дальнейшие исследования в этом направлении.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.