Консенсус Маастрихт VI опубликован: что нового?
- Аннотация
- Статья
- Ссылки
- English













Заболевания, ассоциированные с Helicobacter pylori, имеют широкий спектр проявлений и исходов, а подходы к диагностике и эффективной терапии инфекции требуют регулярного критического анализа и пересмотра в соответствии с критериями медицины, основанной на доказательствах. Консенсусный доклад Маастрихт V/Флоренция был опубликован в 2017 г. Последовавшие за этим исследования позволили провести такую работу. В 2021 г. 41 эксперт из 29 стран изучил новые данные, касающиеся инфекции H. pylori, в пяти рабочих группах:
1) показания/ассоциации;
2) диагностика;
3) лечение;
4) профилактика/рак желудочно-кишечного тракта;
5) H. pylori и микробиота кишечника.
Результаты отдельных рабочих групп были представлены для окончательного консенсусного голосования, в котором приняли участие все участники.
Рассмотрим ключевые положения Маастрихт VI, опубликованного 8 августа 2022 г. [1], и проведем анализ наиболее важных произошедших изменений в сравнении с предыдущим консенсусом Маастрихт V.
Рабочая группа 1. Показания/ассоциации
H. pylori поражает более половины населения мира и всегда вызывает хронический гастрит, который может прогрессировать до тяжелых осложнений, таких как язвенная болезнь, рак желудка и MALT-лимфома. Первое положение консенсуса утверждает, что H. pylori всегда вызывает гастрит, независимо от симптомов или осложнений. Таким образом, в документе закреплено, что инфицирование всегда вызывает гастрит, что согласуется с Киотским консенсусом 2015 г., который определил гастрит, вызванный H. pylori, как инфекционное заболевание, независимо от клинических симптомов и осложнений [2]. Настоящим документом определяется предпочтительная стратегия «тестируй и лечи» для пациентов с синдромом диспепсии с более высоким уровнем доказанности данных в сравнении с предшествующим Маастрихт V в отношении необходимости проведения эрадикации при выявлении инфекта у лиц с диспепсией. Подчеркивается, что тактика эрадикации предпочтительна и более эффективна по сравнению с плацебо и кислотосупрессивной стратегией в долгосрочной перспективе, а перед постановкой достоверного диагноза функциональной диспепсии необходимо исключить H. pylori-гастрит.
Блок положений итогового документа в разделе «Показания/ассоциации» касается необходимости тестирования на H. pylori и при обнаружении инфекции назначения эрадикационной терапии при длительной терапии ингибиторами протонной помпы (ИПП), поскольку длительный прием ИПП изменяет топографию H. pylori-ассоциированного гастрита, а элиминация H. pylori улучшает течение гастрита. Кроме того, актуальны выявление и эрадикация H. pylori у больных MALT-лимфомой, в том числе на поздних стадиях, а также у лиц, длительно принимающих нестероидные противовоспалительные препараты (НПВП)/аспирин. Новым и крайне важным в согласительном документе является положение 10, которое говорит об отсутствии данных, позволяющих предположить, что антикоагулянты (кумарины, прямые пероральные антагонисты и антагонисты витамина К) увеличивают риск кровотечения у пациентов с инфекцией H. pylori (согласие 91%, уровень доказательности А1). При этом отмечено, что потенциальное влияние инфекции H. pylori на риск желудочно-кишечного кровотечения у пациентов, принимающих антикоагулянты, изучено недостаточно. Ограниченные данные исследований по типу «случай – контроль» и когортных исследований не продемонстрировали повышенного риска кровотечения у инфицированных H. pylori пациентов, принимающих антикоагулянты [3].
В отношении экстрагастродуоденальных проявлений инфекции H. pylori по-прежнему указывается на недостаточную доказательность имеющихся данных о причинно-следственной связи этих ассоциаций (положение 15). Вместе с тем эрадикация H. pylori рекомендуется пациентам с необъяснимой железодефицитной анемией, идиопатической тромбоцитопенической пурпурой и дефицитом витамина B12.
Еще одно положение, принципиально новое в отличие от предыдущего консенсуса, посвящено коронавирусной инфекции. COVID-19 негативно повлиял на профилактику и лечение множества состояний, включая заболевания, ассоциированные с H. pylori. Многие профилактические и скрининговые мероприятия по онкологическим заболеваниям, в том числе по колоректальному раку, были изменены или даже временно прекращены с последующим более интенсивным наверстыванием в периоды улучшения эпидемиологической ситуации. В период пандемии сократилось количество плановых амбулаторных консультаций, в том числе гастроэнтерологических [4]. Дыхательные тесты были прекращены во многих учреждениях по всей Европе, что привело к снижению качества диагностики H. pylori, поскольку вместо них могли использоваться менее точные методы. Сообщалось о негативном влиянии COVID-19 на показатели выявления рака [5]. Вместе с тем следует отметить, что при соблюдении правил гигиены и стерилизации риск передачи CΟVID-19 при проведении эндоскопии оценивается как низкий [6].
Рабочая группа 2. Диагностика
Вторая рабочая группа традиционно работала в направлении отбора наиболее эффективных и надежных методов диагностики инфекции H. pylori.
Предпочтительной стратегией диагностики инфекции остается неинвазивное тестирование: проведение уреазного дыхательного теста (УДТ) или теста на моноклональный антиген в стуле как для первичной диагностики, так и для контроля эрадикации. Подчеркивается, что 13C-УДТ широко используется для диагностики инфекции H. pylori, а также для контроля эрадикации после лечения. Лимонная кислота помогает замедлить желудочное опорожнение, усиливает распределение субстрата в желудке и увеличивает время контакта H. pylori с уреазой [7, 8]. Серологическое тестирование для выявления антител должно применяться только в качестве скринингового.
Необходимо отметить, что в итоговом согласительном документе несколько положений касаются проведения эндоскопии с забором гастробиоптатов, а именно: обследование больных диспепсией старше 50 лет; в случае проведения эндоскопии должны применяться наилучшие доступные технологии с забором биопсий для последующего стадирования гастрита и выяснения его этиологии. Маастрихт VI ориентирует клиницистов на выявление и гистологическую оценку атрофии слизистой оболочки желудка в соответствии с критериями OLGA/OLGIM для оценки риска развития рака у конкретного пациента. Принципиально важной для реальной клинической практики и эффективной канцеропревенции, по мнению экспертов, является именно оценка атрофии слизистой оболочки желудка. Типирование кишечной метаплазии (полная/неполная, тонко-/толстокишечная) в рутинной практике излишне. Наиболее сложные, тяжелые случаи с выявлением интраэпителиальной неоплазии низкой и высокой степени требуют подтверждающей гистологической оценки и картирования желудка с помощью эндоскопии высокого разрешения. Было отмечено, что после проведения абляции или подслизистой диссекции требуется подтверждение отсутствия или эрадикация H. pylori, а также дальнейшее эндоскопическое наблюдение пациента.
Особое внимание эксперты уделили выявлению атрофии слизистой оболочки желудка не только в ассоциации с инфекцией H. pylori, но и в аспекте аутоиммунного воспаления как этиологического фактора гастрита с формированием атрофии. При клиническом подозрении на аутоиммунный гастрит (АИГ) требуется определение гастрина 17, соотношения пепсиногенов и аутоантител к внутреннему фактору и париетальным клеткам. Серологическое исследование позволяет получить дополнительную информацию и помочь клиницисту с определением необходимости эндоскопии/
биопсии.
С учетом возрастающей антибиотикорезистентности новым в сравнении с предшествующим консенсусом является положение о молекулярных методах диагностики (в частности, ПЦР в реальном времени, полногеномное секвенирование и цифровая ПЦР) для выявления мутаций H. pylori, связанных с устойчивостью к кларитромицину, левофлоксацину, тетрациклину и рифампицину. Более того, перед назначением любых схем терапии, содержащих кларитромицин, рекомендуется проведение теста на чувствительность к кларитромицину с помощью молекулярных или бактериологических методов, если они доступны. Для молекулярного тестирования с помощью ПЦР предлагается использовать биоптаты желудка, извлеченные из экспресс-тестов на уреазу (быстрый уреазный тест).
Особое внимание уделено контролю эрадикации. Он должен проводиться через 4–6 недель после завершения терапии. При этом для повышения диагностической ценности контрольного теста настоятельно не рекомендуется использовать антибиотики или висмут в течение 4–6 недель перед исследованием (положение 10). Ингибиторы протонной помпы следует отменить за 14 дней до теста.
Рабочая группа 3. Лечение
Со времени выхода первого Маастрихтского консенсуса по диагностике и лечению заболеваний, ассоциированных с инфекцией H. pylori, положения, разработанные именно этой рабочей группой экспертов в отношении выбора наиболее эффективной и безопасной терапии, приковывают повышенное внимание прежде всего практикующих специалистов. Как и прежде, раздел, посвященный лечению хеликобактерной инфекции, остается ключевым и наиболее объемным.
Цель эрадикационной терапии заключается в надежном излечении инфекции H. pylori у большинства (≥ 90%) пациентов, что требует использования антибактериальных препаратов, к которым восприимчива инфекция, с учетом региональных (локальных) данных. Стратегия выбора схемы эрадикационной терапии с учетом местных данных получила развитие в новом согласительном документе. Врач получает информацию о резистентности H. pylori к противомикробным препаратам несколькими способами. Первый – посев с последующим исследованием на чувствительность к антибиотикам или молекулярное тестирование, второй – выявление распространенности резистентности других микроорганизмов в сообществе, например респираторных патогенов к кларитромицину. Третий, широкодоступный для всех, предусматривает проведение и систематизацию данных контрольных тестов после эрадикации и отбор наиболее эффективных режимов эмпирической терапии в этой популяции. Неудача лечения оптимизированной современной схемой может четко указывать на наличие резистентности и на то, что такую терапию больше не следует рекомендовать и использовать, если местная чувствительность не подтверждена посевом или молекулярным тестированием [9].
Консенсус Маастрихт VI говорит о целесообразности определения чувствительности к антибиотикам (посев или ПЦР) даже до назначения терапии первой линии с целью рационального использования антибиотиков. Это дает возможность оценить распространенность резистентности к антибиотикам у ранее не получавших лечение пациентов и влияние любой такой устойчивости на эффективность современных методов эрадикации первой линии. Тем не менее доказательства все еще слишком незначительны, чтобы настаивать на всеобщем использовании такой стратегии в рутинной практике.
В реальной клинической практике необходимо постоянно проверять уровень эффективности лечения H. pylori, чтобы подтвердить правильность применяемых схем эрадикации. Одним из самых успешных наблюдательных исследований является Европейский регистр по ведению инфекции H. pylori (Hp-EuReg), анализ данных которого позволяет оценить эффективность применяемых режимов терапии в России [10–12] и Европе [13–15] и который использован при формировании рекомендаций консенсуса Маастрихт VI.
Что же сегодня предлагается в качестве наиболее эффективной эмпирической эрадикационной терапии? В регионах с уровнем резистентности к кларитромицину < 15% в качестве первой линии по-прежнему рекомендуется квадротерапия с висмутом или тройная терапия, при высокой резистентности к кларитромицину (> 15%) – квадротерапия с висмутом или квадротерапия без висмута. Таким образом, в Маастрихте VI, как и в предшествующем консенсусе, сделан упор на важность локальной резистентности с ограничением выбора тройной терапии регионами с низкой резистентностью к кларитромицину, сохранена 14-дневная продолжительность терапии, а при неудаче терапии первой линии предложены следующие линии терапии.
При выборе тройной терапии клиницисты должны отдавать предпочтение ИПП, метаболизм которых не зависит от генетических особенностей макроорганизма. В представленном документе впервые сформулировано заключение об эффективности нового класса антисекреторных средств – блокаторов калиевых каналов (P-CAB). Указано, что блокаторы калиевых каналов в комбинированной терапии превосходят традиционные ИПП или не уступают им в тройной терапии первой и второй линий и имеют преимущество у пациентов с инфекцией, устойчивой к антибиотикам.
Наверное, наиболее важным следует признать присутствие уже хорошо известных практикующим специалистам антибактериальных средств. Именно рациональная антибактериальная терапия, ориентир на выяснение актуальной чувствительности H. pylori к антимикробным средствам являются приоритетными для эффективной эрадикационной терапии.
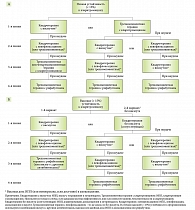
Основные преимущества и ограничения лечения, основанного на восприимчивости, и эмпирического лечения инфекции H. pylori представлены в таблице, алгоритм эмпирического лечения H. pylori первой линии, а также терапии спасения (когда тест на чувствительность к антибиотикам недоступен) – на рисунке.
Рабочая группа 4. Рак желудка и профилактика
Максимальный (100%) уровень согласия с наивысшим уровнем доказанности получило положение о том, что H. pylori является основным этиологическим фактором аденокарциномы желудка, включая проксимальный рак желудка. Авторы консенсуса подчеркнули, что воздействие факторов внешней среды менее значимо, чем влияние инфекции H. pylori.
H. pylori и вирус Эпштейна – Барр – независимые факторы риска развития рака желудка. Остается неясным, связана ли коинфекция H. pylori и вируса Эпштейна – Барр с более высоким риском развития рака желудка, чем каждая из них в отдельности.
Новыми в этом консенсусе являются данные о том, что H. pylori ассоциирован с раком желудочно-пищеводного перехода, который квалифицирован как отдельная единица в классификации IARC [16]. Ряд исследований убедительно показали, что существует по крайней мере два основных этиологических фактора для аденокарциномы желудочно-пищеводного перехода: первый – воспаление, вызванное рефлюксом, второй – воспаление слизистой оболочки желудка, в том числе слизистой оболочки кардиального отдела, вызванное главным образом инфекцией H. pylori [17–20].
Эндоскопия с биопсией рекомендуется бессимптомным пациентам с семейным анамнезом рака желудка (не относится к наследственному раку желудка) в возрасте 45 лет и старше, а также лицам в возрасте старше 50 лет. В ряде западных стран программы скрининга колоректального рака начинаются в возрасте 50 лет. В это время примерно у 10% пациентов, инфицированных H. pylori, уже могут иметь место предраковые поражения желудка (атрофия, кишечная метаплазия). Распространенность поздних предопухолевых поражений в Европе в старшей возрастной группе достигает 19% [21–24]. Для снижения затрат и повышения качества скрининг и лечение инфекции H. pylori можно сочетать со скринингом колоректального рака в странах со средним и высоким риском развития рака желудка.
Эндоскопическое исследование с проведением биопсии слизистой оболочки желудка для стадирования гастрита необходимо для оценки риска развития рака желудка. Тяжелая атрофия (OLGA/OLGIM III–IV) вследствие гастрита, вызванного H. pylori, несет гораздо более высокий риск рака желудка по сравнению с атрофией при аутоиммунном гастрите. Пациенты с поздними стадиями атрофического гастрита (тяжелые атрофические изменения или кишечная метаплазия как в антральном отделе, так и в теле желудка, OLGA/OLGIM III–IV) должны проходить высококачественную эндоскопию каждые три года [25, 26].
Вопреки ранним сообщениям, в которых атрофия желудка и кишечная метаплазия рассматривались как точки невозврата, снижение риска рака желудка на 53% было обнаружено в популяции, в которой проводилась массовая эрадикация H. pylori и в которую также были включены пациенты с атрофическим гастритом. Эффект остановки прогрессирования атрофического гастрита в рак желудка после устранения H. pylori становится более очевидным, риск рака желудка снизился на 50 и 52% у пациентов, перенесших эндоскопическую резекцию рака желудка на ранней стадии [27, 28], и пациентов с предраковыми поражениями соответственно [29].
Особо подчеркивается, что для первичной профилактики рака желудка не существует такой же эффективной альтернативы эрадикации H. pylori. Исследования с добавлением антиоксидантов в пищу имели некоторые незначительные эффекты в снижении заболеваемости раком желудка в долгосрочном дальнейшем исследовании [30, 31]. В настоящее время нет ответа на вопрос, являются ли витамины и другие антиоксидантные добавки полезными для предотвращения прогрессирования предопухолевых изменений (атрофия и кишечная метаплазия). Аспирин, ингибиторы ЦОГ-2, метформин и статины – потенциальные кандидаты на снижение злокачественного прогрессирования предраковых изменений за счет хорошо задокументированных антипролиферативных механизмов. Однако окончательные данные клинических испытаний отсутствуют [32]. Стратегией выбора при ведении лиц из группы высокого риска после эрадикации H. pylori является эндоскопическое наблюдение через регулярные промежутки времени.
С учетом эпидемиологической значимости инфекции H. pylori, нагрузки, вызванной раком желудка, на жизнь отдельного человека и экономику здравоохранения, высокого уровня антибиотикорезистентности крайне актуальной является разработка терапевтической вакцины против H. pylori.
Рабочая группа 5. Helicobacter pylori и микробиота желудка
Накопленные данные о роли микробиоценоза за время после публикации консенсуса Маастрихт V расширили наше представление о взаимодействии H. pylori и микробиоты желудка.
В желудке располагается хорошо адаптированное нише-специфическое микробиологическое сообщество [33]. Желудок человека колонизирован другими микроорганизмами кроме H. pylori, которые в совокупности известны как микробиом желудка. Его состав зависит от физиологических условий в этой уникальной экологической нише. Несколько исследований указывают на отчетливую микробную картину желудка с преобладанием Actinobacteria, Bacteroidetes, Firmicutes, Proteobacteria и Streptococcus в качестве наиболее доминирующего рода. H. pylori существенно влияет на состав микробиоты желудка. Изменение состава микробиома желудка ассоциировано не только с инфицированием H. pylori, но и с модуляцией кислотной продукции как под воздействием антисекреторных средств, так и в результате прогрессирования хронического гастрита на всех этапах каскада Корреа.
Воздействие антибиотиков в раннем возрасте оказывает долгосрочное влияние на кишечную микробиоту. Данные, полученные на животных моделях у младенцев и детей, позволяют предположить, что антибиотики вызывают изменения в составе и функциях микробиоты, которые могут сохраняться в течение многих лет. У младенцев воздействие антибиотиков связано с первоначальным снижением разнообразия микробиоты и влияет на обилие нескольких видов бактерий. Изменение микробиоты, вызванное макролидами, связано с повышенным риском развития астмы и увеличения веса. Изменения микробиоты у детей сохраняются спустя месяцы после применения антибиотиков, полная «перезагрузка» состава микробиоты в сторону «исходного» состава маловероятна. Метаанализ когортных исследований показал, что воздействие разных классов антибиотиков связано с различными рисками развития воспалительных заболеваний кишечника. Применение антибиотиков является важным фактором риска развития болезни Крона у детей младше 18 лет. Разница между детьми, ранее не принимавшими антибиотики, и детьми, получавшими лечение, уменьшается с возрастом.
Лечение антибиотиками значительно обогатило гены устойчивости к антибиотикам. В этой связи отмечается, что эрадикационная терапия H. pylori может способствовать отбору резистентных штаммов микробиоты кишечника. При этом лечение антибиотиками по другим причинам может привести к формированию резистентных штаммов H. pylori.
Подчеркивается, что только некоторые пробиотики эффективны в уменьшении побочных эффектов со стороны желудочно-кишечного тракта, вызванных эрадикационной терапией. Пробиотики могут оказывать благотворное влияние на эрадикацию H. pylori за счет уменьшения побочных эффектов, вызванных антибиотиками. Кроме того, пробиотики ингибируют H. pylori несколькими путями, включая выработку антимикробных веществ или конкуренцию с H. pylori за колонизацию и выживание. Различные метаанализы рандомизированных контролируемых исследований оценивали эффективность пробиотиков в повышении эффективности эрадикационной терапии H. pylori, демонстрируя в целом положительные результаты [34–40], но преимущества показаны только для определенных штаммов Lactobacillus [34, 35, 38], бифидобактерий [34, 35] и S. boulardii [35].
Заключительный блок итогового документа содержит задачи на ближайшие пять лет:
- миссия глобальной профилактики рака желудка;
- необходимость лучше понимать и контролировать устойчивость к антибиотикам, которая продолжает резко расти;
- усовершенствование потенциальных методов лечения/комбинаций, включая достижение оптимального подавления кислотности.
Наконец, остается надежда на новые антибиотики. Понимание роли желудочного микробиома расширяется, и введение селективных пробиотиков может сыграть свою роль.
Заключение
Представленные широкой медицинской общественности обновленные рекомендации по диагностике и лечению заболеваний, ассоциированных с инфекцией H. pylori, определяют наилучшие подходы к ведению пациентов, инфицированных H. pylori, на предстоящий пятилетний период. Основные положения консенсуса, основанные на результатах научных исследований, носят прежде всего практическую направленность и позволяют реализовать в клинической практике достижения с максимальным уровнем доказательности данных.
Глубокий анализ положений консенсуса с учетом региональных особенностей, включая данные о резистентности к антибиотикам, возможности общественного здравоохранения и доступность диагностических методов и лекарственных препаратов, мониторинг реальной клинической практики становятся сегодня необходимой частью реализации рекомендаций Маастрихт VI. Крайне важно консолидировать наши усилия в дальнейшем изучении наиболее актуальных аспектов, прежде всего профилактики рака желудка, оценки резистентности H. pylori к антибиотикам и роли модуляции микробиома при лечении заболеваний, ассоциированных с этой инфекцией.
D.S. Bordin, PhD, Prof., M.A. Livzan, PhD, Prof., Corr.-Mem. of RAS
A.S. Loginov Moscow Clinical Scientific Center
A.I. Yevdokimov Moscow State University of Medicine and Dentistry
Tver State Medical University
Omsk State Medical University
Contact person: Dmitry S. Bordin, d.bordin@mknc.ru
The analysis of the most important changes and the translation into Russian of the provisions of the Maastricht VI Consensus published in August 2022 are presented. The main provisions of the consensus are based on the results of scientific research and are primarily practical. They take into account regional peculiarities, local data on the resistance of Helicobacter pylori to antibiotics, and public health opportunities. Monitoring of the actual clinical practice of H. pylori diagnosis and treatment becomes a necessary part of the implementation of the recommendations of Maastricht VI.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.