количество статей
7396
Загрузка...
Пожалуйста, авторизуйтесь:
Практика
«Квартет здоровья» против «смертельного квартета». Часть вторая: дефицит тестостерона – стратегия проведения заместительной гормональной терапии*
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Урология и Нефрология" №2 (16)
- Аннотация
- Статья
- Ссылки
- English
В статье обосновывается необходимость проведения метаболической терапии, основанной на понимании патогенетических механизмов клеточного старения и направленной против основных болезней цивилизации: ожирения, атеросклероза, артериальной гипертонии и сахарного диабета 2 типа.
Обобщены современные представления о механизмах действия гормонов, приведена их классификация. Особое внимание уделено роли половых гормонов в целом и тестостерона у мужчин в частности. Рассматриваются особенности патогенеза гипогонадизма у мужчин и методы терапии андрогенного дефицита. Обсуждается алгоритм выбора заместительной гормональной терапии с учетом всех преимуществ и недостатков современных препаратов тестостерона.
Обобщены современные представления о механизмах действия гормонов, приведена их классификация. Особое внимание уделено роли половых гормонов в целом и тестостерона у мужчин в частности. Рассматриваются особенности патогенеза гипогонадизма у мужчин и методы терапии андрогенного дефицита. Обсуждается алгоритм выбора заместительной гормональной терапии с учетом всех преимуществ и недостатков современных препаратов тестостерона.
* Первая часть опубликована ранее: Ворслов Л.О., Калинченко С.Ю., Гадзиева И.В. «Квартет здоровья» против «смертельного квартета». Часть первая: метаболическая невропатия – легко диагностировать, трудно лечить // Эффективная фармакотерапия. 1/2013. Урология и нефрология. № 1. С. 32–37.
В статье обосновывается необходимость проведения метаболической терапии, основанной на понимании патогенетических механизмов клеточного старения и направленной против основных болезней цивилизации: ожирения, атеросклероза, артериальной гипертонии и сахарного диабета 2 типа.
Обобщены современные представления о механизмах действия гормонов, приведена их классификация. Особое внимание уделено роли половых гормонов в целом и тестостерона у мужчин в частности. Рассматриваются особенности патогенеза гипогонадизма у мужчин и методы терапии андрогенного дефицита. Обсуждается алгоритм выбора заместительной гормональной терапии с учетом всех преимуществ и недостатков современных препаратов тестостерона.
Обобщены современные представления о механизмах действия гормонов, приведена их классификация. Особое внимание уделено роли половых гормонов в целом и тестостерона у мужчин в частности. Рассматриваются особенности патогенеза гипогонадизма у мужчин и методы терапии андрогенного дефицита. Обсуждается алгоритм выбора заместительной гормональной терапии с учетом всех преимуществ и недостатков современных препаратов тестостерона.
* Первая часть опубликована ранее: Ворслов Л.О., Калинченко С.Ю., Гадзиева И.В. «Квартет здоровья» против «смертельного квартета». Часть первая: метаболическая невропатия – легко диагностировать, трудно лечить // Эффективная фармакотерапия. 1/2013. Урология и нефрология. № 1. С. 32–37.

Таблица 1. Стероидные гормоны человека
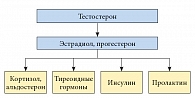
Рис. «Гормональная иерархия»

Таблица 2. Препараты, используемые для лечения андрогенного дефицита
В последнее время заболеваниям, связанным с эндокринно-метаболическими нарушениями в организме, уделяется повышенное внимание. Одним из понятий, объединяющим основные болезни цивилизации (ожирение, атеросклероз, артериальная гипертония и сахарный диабет 2 типа), стал метаболический синдром, также называемый «смертельным квартетом». В разное время в это понятие включались такие нарушения, как подагра, жировой гепатоз, гиперинсулинемия и инсулинорезистентность, активация симпатической нервной системы, повышенный уровень провоспалительных цитокинов и патологических факторов роста. Заболевания, входящие в состав метаболического синдрома, нередко могут вызывать инвалидизацию, снижение работоспособности, общее недомогание, а также негативно влияют на качество жизни и ее продолжительность.
Нами была сформулирована концепция «квартета здоровья» – комплексной метаболической терапии, основанной на понимании патогенетических механизмов клеточного старения и «смертельного квартета». Понятие «метаболическая терапия» подразумевает лечение, направленное в первую очередь на поддержание или восстановление клетки как наименьшей единицы живого, ее физиологических функций, структуры тканей и в итоге организма в целом. Напомним, что «квартет здоровья» включает в себя гормональную терапию (прежде всего заместительную гормональную терапию половыми гормонами при гипогонадизме), поддержание физиологического уровня витамина D и терапию незаменимыми жирными кислотами: омега-3 полиненасыщенными жирными кислотами и тиоктовой (альфа-липоевой) кислотой.
Ранее нами была обоснована необходимость проведения антиоксидантной терапии метаболического синдрома препаратами альфа-липоевой (тиоктовой) кислоты. Эта статья посвящена аспектам назначения заместительной гормональной терапии.
Человеческую жизнь можно условно разделить на несколько стадий: развитие плода, рождение и начало развития, пубертат (начало и собственно половое созревание), активный репродуктивный период и, наконец, угасание, старение и смерть. Трудно не согласиться с существующим представлением о том, что принципиальное отличие этих периодов друг от друга обусловлено различиями в уровне половых гормонов и связанными с этими различиями внешними признаками, скоростью течения биохимических процессов, особенностями поведения, социальной и физической активности. Действительно ли физическое и психологическое состояние человека настолько зависит от уровня половых гормонов, надо ли контролировать и корректировать этот уровень и насколько это безопасно? Мы постараемся ответить на эти вопросы, обобщив существующие теории, современные представления о химии гормонов, механизмах их действия, данные опубликованных исследований и собственный опыт.
Стероидные гормоны: определение, классификация, значение
Гормоны (с др.-греч. «возбуждаю, побуждаю») – биологически активные вещества органической природы, вырабатывающиеся в специализированных клетках желез внутренней секреции, поступающие в кровь и оказывающие регулирующее влияние на обмен веществ и физиологические функции. Гормоны служат гуморальными (переносимыми с кровью) регуляторами определенных процессов в различных органах и системах. Существуют и другие трактовки понятия «гормоны». Так, гормонами называют «сигнальные химические вещества, вырабатываемые клетками тела и влияющие на клетки других частей тела». Это определение представляется предпочтительным, так как охватывает многие традиционно причисляемые к гормонам вещества: гормоны животных, которые лишены кровеносной системы (например, экдизоны круглых червей и др.), гормоны позвоночных, вырабатываемые не в эндокринных железах (простагландины, эритропоэтин и др.), а также гормоны растений.
Впервые ввел в науку понятие «гормон» английский физиолог Э.Г. Старлинг, когда в 1905 г. совместно с У.М. Бейлиссом открыл секретин. На сегодняшний день известно более 40 гормонов человека и животных. В зависимости от химического строения выделяют следующие основные классы гормонов позвоночных:
В рамкой данной публикации мы рассмотрим более подробно стероидные гормоны (табл. 1). Стероидные гормоны содержат в своей основе структуру циклопентанпергидрофенантренового кольца и по числу углеродных атомов делятся на три семейства:
Стероидные гормоны, и прежде всего половые гормоны, «работают» на уровне хромосом (клеточного ядра). Хромосомы представляют собой цепочки нуклеотидов, расположенных в определенной последовательности – наборе генов (геном) – нити ДНК. Каждая клетка человеческого организма, имеющая ядро, несет в себе полный генетический набор. Функции клеток различных тканей, безусловно, различны и определяются активацией и «работой» тех или иных генов (дифференцировка клеток).
Продуктом деятельности гена является белок, таким образом, жизнь – это результат активации и деятельности гена, кодирующего строение любого белка, синтезированного в организме. Белки – это и ферменты, и строительный материал для клеток, и гормоны, и переносчики других веществ и молекул/ионов; они – необходимый компонент всех клеточных мембран, внутриклеточных органелл, пищеварительных ферментов, систем иммунологической защиты (иммуноглобулины), участники высшей нервной деятельности (нейропептиды) и многое другое. Синтез белка – обязательное условие поддержания жизни – это гормонозависимый процесс.
Очевидно, что все белки различаются как по структуре, так и по функции. Условно их можно разделить на структурные белки, рецепторы (это тоже белки, распадающиеся после выполнения функции), ферменты и регуляторные белки. Активацию генов, кодирующих регуляторные белки, осуществляют именно половые стероиды (тестостерон и эстрадиол). Отметим, что именно тестостерон, экспрессируя (активируя) всего около 250 генов, играет роль «дирижера гормонального оркестра» (рис.). Безусловно, эта схема крайне упрощена, не учитывает механизмов регуляции и взаимодействия, однако она облегчает восприятие концепции необходимости заместительной гормональной терапии, главенствующей в современной профилактической медицине.
Диагностика и лечение гипогонадизма у мужчин
Определение уровня тестостерона у мужчин сегодня рекомендовано ведущими международными медицинскими организациями при наличии таких составляющих «смертельного квартета», как сахарный диабет 2 типа и инсулинорезистентность, ожирение, артериальная гипертония, дислипидемия [2]. Это не случайно, так как взаимосвязь дефицита тестостерона у мужчин с компонентами метаболического синдрома подтверждена данными доказательной медицины [3].
Диагностика дефицита тестостерона обычно не вызывает затруднений. Гипогонадизм у мужчин (дефицит тестостерона) – это патологическое состояние, характеризующееся функциональной недостаточностью яичек, сопровождающейся снижением уровня общего тестостерона крови (менее 12 нмоль/л) и/или свободного тестостерона (менее 250 пмоль/л) в сочетании с характерными клиническими проявлениями. Среди них можно выделить хроническую усталость, раздражительность, нарушения сна, депрессию, снижение «жизненного тонуса», нарушения мочеиспускания, снижение либидо и, наконец, эректильную дисфункцию и многое другое, что принято называть психосоциальным дискомфортом. Эти симптомы, по нашему мнению, имеют большее значение, чем определяемый в лабораториях уровень общего тестостерона в сыворотке крови. Это связано с тем, что мужчины не подлежат «стандартизации», поскольку нормальный уровень тестостерона для каждого уникален, обусловлен его конституцией и генетикой. Определять его целесообразно в возрасте 20–21 года.
Дефицит тестостерона может быть обусловлен врожденными или приобретенными заболеваниями собственно яичек, а также нарушением выработки гонадотропных гормонов гипоталамуса и гипофиза. Кроме того, существует неизбежный возрастной гипогонадизм, или андрогенный дефицит, вследствие тяжелых соматических заболеваний. Часто дефицит тестостерона (гипогонадизм) выявляется у мужчин с ожирением и другими проявлениями метаболического синдрома.
Очевидно, что при диагностированном дефиците тестостерона (гипогонадизме) необходимо начинать лечение, целью которого должна быть нормализация уровня тестостерона в организме в пределах физиологических значений. Для достижения компенсации гипогонадизма необходимо использовать либо препараты экзогенного тестостерона, либо стимуляторы его синтеза в яичках.
В таблице 2 представлены препараты тестостерона, применяемые для коррекции андрогенного дефицита в России.
Тестостерон в таблетках (Андриол), как правило, обладает достаточно мягким и слабым действием в отношении проявлений андрогенного дефицита, требует многократного приема в течение суток, связанного с приемом пищи, что затрудняет подбор дозы. В этой связи таблетированные препараты тестостерона применяются достаточно редко, тем не менее таблетки могут оказаться препаратом выбора для тех пациентов, у которых проявления дефицита тестостерона выражены очень слабо и для которых «лекарства в таблетках» являются психологически наиболее приемлемой формой лечения.
Масляные внутримышечные инъекции растворов тестостерона являются достаточно широко применяемым эффективным методом лечения недостаточности тестостерона. Инъекции производятся, в зависимости от препарата, 1 раз в 2–3 недели (Сустанон, Омнадрен) или 1 раз в 6–14 недель (Небидо) и обеспечивают прогнозируемую компенсацию андрогенного дефицита при правильно подобранном интервале между инъекциями. Эффективность этой терапии близка к идеальной и позволяет компенсировать и клинические проявления гипогонадизма, и симптомы метаболического синдрома в целом, что продемонстрировано во многих клинических исследованиях. Эффективность терапии андрогенами у пациентов с гипогонадизмом в отношении профилактики и лечения метаболического синдрома была подтверждена в проведенном нами двойном слепом плацебоконтролируемом исследовании Moscow Study.
При внутримышечном введении растворов тестостерона создается депо, из которого действующее вещество высвобождается в кровеносное русло. Достоинством этих препаратов является длительность терапевтического действия. Однако у некоторых пациентов могут отмечаться резкие изменения в уровне тестостерона, зачастую ощущаемые самим пациентом в виде подъемов и снижения либидо, улучшения/ухудшения общего самочувствия, эмоционального статуса, а также изменяться показатели гематокрита, поэтому при применении внутримышечных инъекций тестостерона необходим особо тщательный контроль со стороны врача.
Этих недостатков лишена трансдермальная форма препарата тестостерона (в России – Андрогель). Гель наносится на кожу живота (можно на кожу плеча, предплечья) 1 раз в сутки. Преимуществами геля являются отсутствие болезненных инъекций, легкость и удобство его применения, возможность проводить лечение самостоятельно в домашних условиях. Трансдермальный (чрескожный) путь введения тестостерона позволяет избежать его первичного метаболизма в печени и инактивации, как это происходит при применении пероральных андрогенных препаратов, а также позволяет имитировать циркадные (суточные) ритмы высвобождения физиологического тестостерона. К тому же терапию с использованием геля в случае необходимости можно легко прервать. Существенными преимуществами заместительной терапии Андрогелем являются отсутствие риска превышения физиологических уровней тестостерона (супрафизиологических пиков) на фоне терапии и повышения гематокрита, стабильный уровень тестостерона (отсутствие периодов гипогонадизма, возможных при использовании инъекционных форм в случае неправильно подобранного интервала между инъекциями), минимальное влияние на секрецию гонадотропинов и, возможно, местное липолитическое действие. Не случайно, согласно рекомендациям Международного общества по изучению здоровья пожилых мужчин (International Society for the Study of the Aging Male, ISSAM), а также Европейской ассоциации урологов (European Association of Urology, EAU) [3], препараты тестостерона короткого (24 ч) действия (к которым относится тестостерон в виде геля) рекомендуются в качестве препаратов выбора для начала заместительной терапии тестостероном.
Заключение
Следует отметить, что все препараты тестостерона, используемые сегодня, эффективны в достижении своей основной цели – устранения симптомов дефицита тестостерона – и безопасны в применении. Важно индивидуально подходить назначению заместительной андрогенной терапии, учитывая преимущества и недостатки современных препаратов тестостерона, а также основываясь на пожеланиях пациента.
Нами была сформулирована концепция «квартета здоровья» – комплексной метаболической терапии, основанной на понимании патогенетических механизмов клеточного старения и «смертельного квартета». Понятие «метаболическая терапия» подразумевает лечение, направленное в первую очередь на поддержание или восстановление клетки как наименьшей единицы живого, ее физиологических функций, структуры тканей и в итоге организма в целом. Напомним, что «квартет здоровья» включает в себя гормональную терапию (прежде всего заместительную гормональную терапию половыми гормонами при гипогонадизме), поддержание физиологического уровня витамина D и терапию незаменимыми жирными кислотами: омега-3 полиненасыщенными жирными кислотами и тиоктовой (альфа-липоевой) кислотой.
Ранее нами была обоснована необходимость проведения антиоксидантной терапии метаболического синдрома препаратами альфа-липоевой (тиоктовой) кислоты. Эта статья посвящена аспектам назначения заместительной гормональной терапии.
Человеческую жизнь можно условно разделить на несколько стадий: развитие плода, рождение и начало развития, пубертат (начало и собственно половое созревание), активный репродуктивный период и, наконец, угасание, старение и смерть. Трудно не согласиться с существующим представлением о том, что принципиальное отличие этих периодов друг от друга обусловлено различиями в уровне половых гормонов и связанными с этими различиями внешними признаками, скоростью течения биохимических процессов, особенностями поведения, социальной и физической активности. Действительно ли физическое и психологическое состояние человека настолько зависит от уровня половых гормонов, надо ли контролировать и корректировать этот уровень и насколько это безопасно? Мы постараемся ответить на эти вопросы, обобщив существующие теории, современные представления о химии гормонов, механизмах их действия, данные опубликованных исследований и собственный опыт.
Стероидные гормоны: определение, классификация, значение
Гормоны (с др.-греч. «возбуждаю, побуждаю») – биологически активные вещества органической природы, вырабатывающиеся в специализированных клетках желез внутренней секреции, поступающие в кровь и оказывающие регулирующее влияние на обмен веществ и физиологические функции. Гормоны служат гуморальными (переносимыми с кровью) регуляторами определенных процессов в различных органах и системах. Существуют и другие трактовки понятия «гормоны». Так, гормонами называют «сигнальные химические вещества, вырабатываемые клетками тела и влияющие на клетки других частей тела». Это определение представляется предпочтительным, так как охватывает многие традиционно причисляемые к гормонам вещества: гормоны животных, которые лишены кровеносной системы (например, экдизоны круглых червей и др.), гормоны позвоночных, вырабатываемые не в эндокринных железах (простагландины, эритропоэтин и др.), а также гормоны растений.
Впервые ввел в науку понятие «гормон» английский физиолог Э.Г. Старлинг, когда в 1905 г. совместно с У.М. Бейлиссом открыл секретин. На сегодняшний день известно более 40 гормонов человека и животных. В зависимости от химического строения выделяют следующие основные классы гормонов позвоночных:
- стероиды;
- производные полиеновых (полиненасыщенных) жирных кислот;
- производные аминокислот;
- белково-пептидные соединения.
В рамкой данной публикации мы рассмотрим более подробно стероидные гормоны (табл. 1). Стероидные гормоны содержат в своей основе структуру циклопентанпергидрофенантренового кольца и по числу углеродных атомов делятся на три семейства:
- гормоны коры надпочечников и прогестерон (С₂₁-стероиды);
- мужские половые гормоны (С₁₉-стероиды);
- женские половые гормоны (С₁₈-стероиды).
Стероидные гормоны, и прежде всего половые гормоны, «работают» на уровне хромосом (клеточного ядра). Хромосомы представляют собой цепочки нуклеотидов, расположенных в определенной последовательности – наборе генов (геном) – нити ДНК. Каждая клетка человеческого организма, имеющая ядро, несет в себе полный генетический набор. Функции клеток различных тканей, безусловно, различны и определяются активацией и «работой» тех или иных генов (дифференцировка клеток).
Продуктом деятельности гена является белок, таким образом, жизнь – это результат активации и деятельности гена, кодирующего строение любого белка, синтезированного в организме. Белки – это и ферменты, и строительный материал для клеток, и гормоны, и переносчики других веществ и молекул/ионов; они – необходимый компонент всех клеточных мембран, внутриклеточных органелл, пищеварительных ферментов, систем иммунологической защиты (иммуноглобулины), участники высшей нервной деятельности (нейропептиды) и многое другое. Синтез белка – обязательное условие поддержания жизни – это гормонозависимый процесс.
Очевидно, что все белки различаются как по структуре, так и по функции. Условно их можно разделить на структурные белки, рецепторы (это тоже белки, распадающиеся после выполнения функции), ферменты и регуляторные белки. Активацию генов, кодирующих регуляторные белки, осуществляют именно половые стероиды (тестостерон и эстрадиол). Отметим, что именно тестостерон, экспрессируя (активируя) всего около 250 генов, играет роль «дирижера гормонального оркестра» (рис.). Безусловно, эта схема крайне упрощена, не учитывает механизмов регуляции и взаимодействия, однако она облегчает восприятие концепции необходимости заместительной гормональной терапии, главенствующей в современной профилактической медицине.
Диагностика и лечение гипогонадизма у мужчин
Определение уровня тестостерона у мужчин сегодня рекомендовано ведущими международными медицинскими организациями при наличии таких составляющих «смертельного квартета», как сахарный диабет 2 типа и инсулинорезистентность, ожирение, артериальная гипертония, дислипидемия [2]. Это не случайно, так как взаимосвязь дефицита тестостерона у мужчин с компонентами метаболического синдрома подтверждена данными доказательной медицины [3].
Диагностика дефицита тестостерона обычно не вызывает затруднений. Гипогонадизм у мужчин (дефицит тестостерона) – это патологическое состояние, характеризующееся функциональной недостаточностью яичек, сопровождающейся снижением уровня общего тестостерона крови (менее 12 нмоль/л) и/или свободного тестостерона (менее 250 пмоль/л) в сочетании с характерными клиническими проявлениями. Среди них можно выделить хроническую усталость, раздражительность, нарушения сна, депрессию, снижение «жизненного тонуса», нарушения мочеиспускания, снижение либидо и, наконец, эректильную дисфункцию и многое другое, что принято называть психосоциальным дискомфортом. Эти симптомы, по нашему мнению, имеют большее значение, чем определяемый в лабораториях уровень общего тестостерона в сыворотке крови. Это связано с тем, что мужчины не подлежат «стандартизации», поскольку нормальный уровень тестостерона для каждого уникален, обусловлен его конституцией и генетикой. Определять его целесообразно в возрасте 20–21 года.
Дефицит тестостерона может быть обусловлен врожденными или приобретенными заболеваниями собственно яичек, а также нарушением выработки гонадотропных гормонов гипоталамуса и гипофиза. Кроме того, существует неизбежный возрастной гипогонадизм, или андрогенный дефицит, вследствие тяжелых соматических заболеваний. Часто дефицит тестостерона (гипогонадизм) выявляется у мужчин с ожирением и другими проявлениями метаболического синдрома.
Очевидно, что при диагностированном дефиците тестостерона (гипогонадизме) необходимо начинать лечение, целью которого должна быть нормализация уровня тестостерона в организме в пределах физиологических значений. Для достижения компенсации гипогонадизма необходимо использовать либо препараты экзогенного тестостерона, либо стимуляторы его синтеза в яичках.
В таблице 2 представлены препараты тестостерона, применяемые для коррекции андрогенного дефицита в России.
Тестостерон в таблетках (Андриол), как правило, обладает достаточно мягким и слабым действием в отношении проявлений андрогенного дефицита, требует многократного приема в течение суток, связанного с приемом пищи, что затрудняет подбор дозы. В этой связи таблетированные препараты тестостерона применяются достаточно редко, тем не менее таблетки могут оказаться препаратом выбора для тех пациентов, у которых проявления дефицита тестостерона выражены очень слабо и для которых «лекарства в таблетках» являются психологически наиболее приемлемой формой лечения.
Масляные внутримышечные инъекции растворов тестостерона являются достаточно широко применяемым эффективным методом лечения недостаточности тестостерона. Инъекции производятся, в зависимости от препарата, 1 раз в 2–3 недели (Сустанон, Омнадрен) или 1 раз в 6–14 недель (Небидо) и обеспечивают прогнозируемую компенсацию андрогенного дефицита при правильно подобранном интервале между инъекциями. Эффективность этой терапии близка к идеальной и позволяет компенсировать и клинические проявления гипогонадизма, и симптомы метаболического синдрома в целом, что продемонстрировано во многих клинических исследованиях. Эффективность терапии андрогенами у пациентов с гипогонадизмом в отношении профилактики и лечения метаболического синдрома была подтверждена в проведенном нами двойном слепом плацебоконтролируемом исследовании Moscow Study.
При внутримышечном введении растворов тестостерона создается депо, из которого действующее вещество высвобождается в кровеносное русло. Достоинством этих препаратов является длительность терапевтического действия. Однако у некоторых пациентов могут отмечаться резкие изменения в уровне тестостерона, зачастую ощущаемые самим пациентом в виде подъемов и снижения либидо, улучшения/ухудшения общего самочувствия, эмоционального статуса, а также изменяться показатели гематокрита, поэтому при применении внутримышечных инъекций тестостерона необходим особо тщательный контроль со стороны врача.
Этих недостатков лишена трансдермальная форма препарата тестостерона (в России – Андрогель). Гель наносится на кожу живота (можно на кожу плеча, предплечья) 1 раз в сутки. Преимуществами геля являются отсутствие болезненных инъекций, легкость и удобство его применения, возможность проводить лечение самостоятельно в домашних условиях. Трансдермальный (чрескожный) путь введения тестостерона позволяет избежать его первичного метаболизма в печени и инактивации, как это происходит при применении пероральных андрогенных препаратов, а также позволяет имитировать циркадные (суточные) ритмы высвобождения физиологического тестостерона. К тому же терапию с использованием геля в случае необходимости можно легко прервать. Существенными преимуществами заместительной терапии Андрогелем являются отсутствие риска превышения физиологических уровней тестостерона (супрафизиологических пиков) на фоне терапии и повышения гематокрита, стабильный уровень тестостерона (отсутствие периодов гипогонадизма, возможных при использовании инъекционных форм в случае неправильно подобранного интервала между инъекциями), минимальное влияние на секрецию гонадотропинов и, возможно, местное липолитическое действие. Не случайно, согласно рекомендациям Международного общества по изучению здоровья пожилых мужчин (International Society for the Study of the Aging Male, ISSAM), а также Европейской ассоциации урологов (European Association of Urology, EAU) [3], препараты тестостерона короткого (24 ч) действия (к которым относится тестостерон в виде геля) рекомендуются в качестве препаратов выбора для начала заместительной терапии тестостероном.
Заключение
Следует отметить, что все препараты тестостерона, используемые сегодня, эффективны в достижении своей основной цели – устранения симптомов дефицита тестостерона – и безопасны в применении. Важно индивидуально подходить назначению заместительной андрогенной терапии, учитывая преимущества и недостатки современных препаратов тестостерона, а также основываясь на пожеланиях пациента.
NB: Применение препарата Андрогель
- Рекомендованная суточная доза составляет 5 г геля (50 мг тестостерона). Дневная доза может корректироваться врачом в зависимости от клинических и лабораторных показателей, но не должна превышать 10 г/сут.
- Гель наносится однократно, предпочтительно в утренние часы на чистую, сухую, неповрежденную кожу плеч и/или живота. Не следует наносить гель на область грудных желез и гениталий, так как высокое содержание этилового спирта в препарате может вызвать местное раздражение.
- После вскрытия пакетика необходимо немедленно нанести на кожу все его содержимое и распределить тонким слоем. Втирать его в кожу не обязательно. Следует дать гелю высохнуть в течение, по крайней мере, 3–5 мин.
1. Розен В.Б. Основы эндокринологии. 3-е изд., перераб. и доп. М.: Изд. МГУ: Медицина, 1994. С. 40–93.
2. Giudelines on Male Hypogonadism. EAU, 2012.
3. Corona G., Monami M., Rastrelli G. et al. Testosterone and metabolic syndrome: a meta-analysis study // J. Sex. Med. 2011. Vol. 8. № 1. P. 272–283.
Long-term phosphodiesterase-5 inhibition: urologic perspectives
I.A. Korneyev
Saint Petersburg Pavlov State Medical University, Department of Urology
Contact person: Igor Alekseyevich Korneyev, iakorneyev@yandex.ru
Numerous studies have demonstrated efficacy of daily administration of phosphodiesterase-5 (PDE-5) inhibitors for restoration of erectile function; the role of PDE-5 inhibitors is highlighted in the guidelines of the European Association of Urology (EAU). Daily regimen may be used in patients with vasculogenic and neurogenic erectile dysfunction associated with surgery or metabolic disorders as well as for combination therapy of dysuria in benign prostatic hyperplasia.
Key words: erectile dysfunction, phosphodiesterase-5 inhibitors, udenafil
I.A. Korneyev
Saint Petersburg Pavlov State Medical University, Department of Urology
Contact person: Igor Alekseyevich Korneyev, iakorneyev@yandex.ru
Numerous studies have demonstrated efficacy of daily administration of phosphodiesterase-5 (PDE-5) inhibitors for restoration of erectile function; the role of PDE-5 inhibitors is highlighted in the guidelines of the European Association of Urology (EAU). Daily regimen may be used in patients with vasculogenic and neurogenic erectile dysfunction associated with surgery or metabolic disorders as well as for combination therapy of dysuria in benign prostatic hyperplasia.
Key words: erectile dysfunction, phosphodiesterase-5 inhibitors, udenafil
Новости на тему
02.02.2024
Отправить статью по электронной почте
Ваш адрес электронной почты:
В статье обосновывается необходимость проведения метаболической терапии, основанной на понимании патогенетических механизмов клеточного старения и направленной против основных болезней цивилизации: ожирения, атеросклероза, артериальной гипертонии и сахарного диабета 2 типа.
Обобщены современные представления о механизмах действия гормонов, приведена их классификация. Особое внимание уделено роли половых гормонов в целом и тестостерона у мужчин в частности. Рассматриваются особенности патогенеза гипогонадизма у мужчин и методы терапии андрогенного дефицита. Обсуждается алгоритм выбора заместительной гормональной терапии с учетом всех преимуществ и недостатков современных препаратов тестостерона.
Обобщены современные представления о механизмах действия гормонов, приведена их классификация. Особое внимание уделено роли половых гормонов в целом и тестостерона у мужчин в частности. Рассматриваются особенности патогенеза гипогонадизма у мужчин и методы терапии андрогенного дефицита. Обсуждается алгоритм выбора заместительной гормональной терапии с учетом всех преимуществ и недостатков современных препаратов тестостерона.
* Первая часть опубликована ранее: Ворслов Л.О., Калинченко С.Ю., Гадзиева И.В. «Квартет здоровья» против «смертельного квартета». Часть первая: метаболическая невропатия – легко диагностировать, трудно лечить // Эффективная фармакотерапия. 1/2013. Урология и нефрология. № 1. С. 32–37.
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
