Согласно современным представлениям, в этиологии хронического аденоидита значимую роль играет хроническая бактериальная инфекция [6]. Именно патогенной бактериальной микрофлорой обусловлено персистирующее воспаление в носоглотке и развитие осложнений. Данные последних исследований свидетельствуют: одним из маркеров хронической бактериальной инфекции являются бактериальные биопленки, роль которых в настоящее время дискутируется. Частое и необоснованное применение топических антибактериальных препаратов и антисептиков оказывает выраженный цилиотоксический эффект, провоцируя застой патологического секрета в носоглотке.
Как следствие, длительное время сохраняются такие симптомы аденоидита, как кашель (вызывается стеканием слизи по стенке носоглотки – постназальный синдром) и заложенность носа (по причине скопления вязкого густого секрета в носоглотке). Кроме того, частое и бесконтрольное применение этих препаратов в лечении аденоидитов у часто болеющих детей приводит к стойкому нарушению микробиоценоза поверхности глоточной миндалины и создает предпосылки для повторной колонизации носоглотки высокопатогенной микрофлорой [7, 8]. В этой связи представляется актуальным поиск альтернативных подходов в терапии и профилактике обострений хронического аденоидита у детей.
На сегодняшний день клиническая эффективность применения мукоактивных препаратов в лечении патологии носоглотки у детей изучалась лишь в небольшом числе исследований [9]. Тем не менее доказанный выраженный муколитический и антиоксидантный эффект N-ацетилцистеина, а также имеющиеся данные о влиянии препарата на бактериальные биопленки [10] (рис. 1) позволяют говорить о патогенетически обоснованном применении назальных форм N-ацетилцистеина в профилактике и лечении хронического аденоидита у детей. Цель нашего исследования: оценить эффективность мукоактивной терапии в профилактике рецидивирующего и обострений хронического аденоидита у детей.
Материалы и методы
В открытое рандомизированное исследование было включено 100 детей в возрасте от 4 до 9 лет с клиникой острого ринита и имеющих клинико-анамнестические признаки часто рецидивирующих или хронических аденоидитов (по данным анамнеза и эндоскопического исследования). В соответствии с принципом рандомизации пациенты были распределены на 2 группы. В первую группу (основную) было включено 50 пациентов, которые помимо стандартной терапии острого ринита (изотонические растворы стерильной морской воды в форме мелкодисперсного аэрозоля интраназально) ежедневно применяли препарат Ринофлуимуцил® интраназально 3 раза в день по 1 впрыскиванию в каждую половину носа в течение 7 дней. Вторую группу (контрольную) составили 50 пациентов, которым проводили орошение полости носа изотоническим раствором стерильной морской воды в форме мелкодисперсного аэрозоля и интраназальное закапывание 2% раствора Протаргола по 3–5 капель 3 раза в день в течение 7 дней.
Применялись следующие критерии исключения из исследования: клинически подтвержденные первичные и вторичные иммунодефициты; онкологические заболевания; клинические признаки острой бактериальной инфекции, требующей проведения системной антибактериальной терапии или стационарного лечения ребенка; патология бронхолегочной системы, требующая применения ингаляционных и/или системных мукоактивных препаратов (бронхиальная астма в стадии обострения, острый ларинготрахеит, острый бронхит и др.); хронические риниты и риносинусит; гипертрофия аденоидных вегетаций III степени; аденотомия в анамнезе; выраженное искривление перегородки носа; наличие у ребенка состояний, оговоренных в разделе «Противопоказания» в инструкции по медицинскому применению препарата Ринофлуимуцил®.
В качестве критериев оценки эффективности лечения использовалась субъективная оценка пациентами выраженности симптомов заболевания (заложенность носа, кашель, выделения из носа) по 10-балльной визуально-аналоговой шкале (ВАШ) и общего результата лечения, оценка врача по данным стандартного оториноларингологического осмотра, включающего риноэндоскопическое исследование, и данным о частоте развития осложнений острого ринита (риносинуситы, отиты) и затяжных (более 10 дней) обострений хронического аденоидита.
Контрольный осмотр пациента проводили на 5-й и 21-й день от начала лечения. Субъективная оценка симптомов ринита (ВАШ) проводилась пациентами самостоятельно (без визита к врачу) на 14-й день от начала лечения, данные учитывались ретроспективно. Анализ побочных эффектов, связанных с применением препарата Ринофлуимуцил®, и осложнений острого ринита проводили ретроспективно при контрольном осмотре. Назначение терапии осложнений острого ринита осуществляли врачи районных поликлиник согласно общепринятым схемам. Статистическую обработку результатов проводили с помощью программы Statistica v.6.0. Для сравнения количественных показателей использовали t-критерий Стьюдента, для сравнения качественных (балльных) показателей – χ2 Пирсона. Разницу считали статистически достоверной при значении p < 0,05.
Результаты и их обсуждение
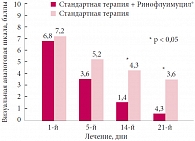
По причине несоблюдения назначения врача-куратора (неявка на контрольные осмотры) в ходе динамического наблюдения из исследования были исключены 2 ребенка основной группы и 4 – контрольной. При первичном осмотре не выявлено статистически достоверного различия между основными симптомами заболевания по данным ВАШ (p > 0,05) у пациентов основной и контрольной групп. При анализе данных субъективной оценки пациентами эффективности лечения (показатели ВАШ) отмечена разница выраженности симптомов на 5-й день от начала лечения у детей основной и контрольной групп (p > 0,05). При этом выявлена значительная разница в выраженности затруднения носового дыхания в основной группе по сравнению с группой контроля – 3,6 ± 0,6 и 5,2 ± 1,0 балла соответственно.
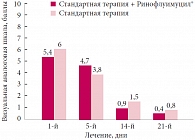
Достоверное различие (p < 0,05) показателей выраженности данного симптома (оценка по ВАШ) было установлено также на 14-й и 21-й день наблюдения. Так, выраженность затруднения носового дыхания в группе пациентов, применявших Ринофлуимуцил®, на 14-й день от начала лечения составила 1,4 ± 0,4 балла, а в группе контроля – 4,3 ± 0,4 балла. К 21-му дню выраженность затруднения носового дыхания в основной группе уменьшилась до 0,6 ± 0,2 балла. В группе контроля также отмечали положительную динамику, однако средний показатель выраженности симптома оставался достаточно высоким – 3,6 ± 0,5 балла (рис. 2). Анализ показателей ВАШ, отражающих выраженность ринореи, не выявил достоверного различия между группами исследования ни на 14-й (основная группа – 0,9 ± 0,3 балла, контрольная – 1,5 ± 0,6 балла), ни на 21-й день наблюдения (основная группа – 0,4 ± 0,1 балла, контрольная – 0,8 ± 0,6 балла) (рис. 3).
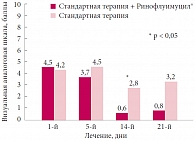
В отношении такого симптома, как выраженность кашля, возникающего вследствие стекания патологического секрета по задней стенке глотки, отмечено достоверное различие (p < 0,05) показателей ВАШ между группами на 14-й день наблюдения: 0,6 ± 0,3 балла в основной группе и 2,8 ± 0,6 балла в контрольной. На 21-й день разница показателей ВАШ, отражающих параметр «выраженность кашля», также была значительной: 0,8 ± 0,5 балла в основной группе и 3,2 ± 1,2 балла в группе контроля. Однако по причине высокого разброса значений в группе контроля данная разница не была достоверной (p > 0,05) (рис. 4). По завершении наблюдения в рамках проведенного исследования родители детей дали субъективную оценку результата лечения. Как «положительный» результат лечения оценили родители 42 (87,5%) детей основной группы и только 24 (52,2%) – контрольной группы.
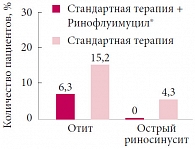
В результате динамического наблюдения за пациентами было диагностировано несколько случаев осложнений. Так, у 3 (6,3%) детей основной группы и 7 (15,2%) (p > 0,05) детей контрольной были установлены отоскопические изменения со стороны барабанных перепонок (без жалоб на ушную боль). Данные тимпанометрии подтвердили наличие у этих пациентов тубарной дисфункции, что потребовало динамического наблюдения за пациентами по завершении исследования. У 2 (4,3%) пациентов контрольной группы при осмотре на 21-й день от начала лечения на основании сохраняющихся жалоб на заложенность носа и выделения из носа и данных риноэндоскопического исследования был поставлен диагноз «острый риносинусит», ни у одного ребенка основной группы этого осложнения не возникло (рис. 5). В дальнейшем дети с острым риносинуситом находились под динамическим наблюдением оториноларинголога и получали терапию заболевания по общепринятой схеме.
Выводы
Данные литературных источников, а также результаты собственного исследования позволяют сделать вывод об обоснованности применения препарата Ринофлуимуцил® (Zambon S.p.A., Италия) в лечении острого ринита у детей с хроническим аденоидитом. Ринофлуимуцил® уменьшает выраженность и продолжительность проявления основных ринологических симптомов и симптомов хронического аденоидита, а также снижает риск развития сопряженных осложнений в виде риносинуситов и отитов. Необходимо дальнейшее изучение эффективности применения препарата Ринофлуимуцил® в комплексной терапии патологии носоглотки у детей.