Неоадъювантная терапия резектабельной меланомы кожи в России. Обновленный анализ данных трех онкологических центров
- Аннотация
- Статья
- Ссылки
- English
Цель. Представить обновленные данные об эффективности и безопасности неоадъювантной иммунотерапии при резектабельной меланоме кожи стадий IIIB–D, полученные в трех ведущих онкологических центрах России, с фокусом на долгосрочных результатах и патоморфологическом ответе.
Материал и методы. Мы провели обновленный анализ объединенных данных 77 пациентов, получавших неоадъювантную иммунотерапию с октября 2020 по ноябрь 2023 г. в трех крупных онкологических центрах России. У 59 (76,6%) проводилась неоадъювантная иммунотерапия пролголимабом, у 13 (16,9%) – пембролизумабом и у пяти (6,5%) – ипилимумабом 3 мг/кг в сочетании с ниволумабом 1 мг/кг. Среднее количество циклов составило 3,6 (45,5 дня) (95%-ный доверительный интервал (ДИ) 3,2–4,0). Оценивались патоморфологический ответ в соответствии с критериями INMC, бессобытийная выживаемость (БСВ), общая выживаемость (ОВ), а также роль последующей адъювантной терапии. Выживаемость оценивалась методом Каплана – Мейера, статистическая значимость – логранговым тестом.
Результаты. Распределение по схемам лечения и среднему количеству циклов (3,6; 95% ДИ 3,2–4,0) не изменилось. Полный патоморфологический ответ (pCR) достигнут у 26 (38,2%) пациентов, почти полный (near-pCR) – у 19 (27,9%), отсутствие ответа (pNR) – у 23 (33,8%). Таким образом, выраженный патоморфологический ответ (pCR + near-pCR) зафиксирован у 45 пациентов (59,4%). Регионарная лимфаденэктомия не была выполнена девяти пациентам: у четырех наблюдалось прогрессирование заболевания и пять отказались от операции на фоне полного клинического ответа. При медиане наблюдения 19,3 мес. (95% ДИ 1,15–50,5) медиана БСВ составила 32,1 мес. в Национальном медицинском исследовательском центре онкологии им. Н.Н. Блохина, 21 мес. – в Национальном медицинском исследовательском центре онкологии им. Н.Н. Петрова и не была достигнута в Московской городской онкологической больнице № 62. Медиана ОВ не достигнута ни в одном из центров.
Выводы. Неоадъювантная иммунотерапия демонстрирует высокую клиническую эффективность в реальной практике. Патоморфологический ответ является мощным предиктором БСВ, что позволяет обоснованно рассматривать стратегию индивидуализации дальнейшего лечения.
Цель. Представить обновленные данные об эффективности и безопасности неоадъювантной иммунотерапии при резектабельной меланоме кожи стадий IIIB–D, полученные в трех ведущих онкологических центрах России, с фокусом на долгосрочных результатах и патоморфологическом ответе.
Материал и методы. Мы провели обновленный анализ объединенных данных 77 пациентов, получавших неоадъювантную иммунотерапию с октября 2020 по ноябрь 2023 г. в трех крупных онкологических центрах России. У 59 (76,6%) проводилась неоадъювантная иммунотерапия пролголимабом, у 13 (16,9%) – пембролизумабом и у пяти (6,5%) – ипилимумабом 3 мг/кг в сочетании с ниволумабом 1 мг/кг. Среднее количество циклов составило 3,6 (45,5 дня) (95%-ный доверительный интервал (ДИ) 3,2–4,0). Оценивались патоморфологический ответ в соответствии с критериями INMC, бессобытийная выживаемость (БСВ), общая выживаемость (ОВ), а также роль последующей адъювантной терапии. Выживаемость оценивалась методом Каплана – Мейера, статистическая значимость – логранговым тестом.
Результаты. Распределение по схемам лечения и среднему количеству циклов (3,6; 95% ДИ 3,2–4,0) не изменилось. Полный патоморфологический ответ (pCR) достигнут у 26 (38,2%) пациентов, почти полный (near-pCR) – у 19 (27,9%), отсутствие ответа (pNR) – у 23 (33,8%). Таким образом, выраженный патоморфологический ответ (pCR + near-pCR) зафиксирован у 45 пациентов (59,4%). Регионарная лимфаденэктомия не была выполнена девяти пациентам: у четырех наблюдалось прогрессирование заболевания и пять отказались от операции на фоне полного клинического ответа. При медиане наблюдения 19,3 мес. (95% ДИ 1,15–50,5) медиана БСВ составила 32,1 мес. в Национальном медицинском исследовательском центре онкологии им. Н.Н. Блохина, 21 мес. – в Национальном медицинском исследовательском центре онкологии им. Н.Н. Петрова и не была достигнута в Московской городской онкологической больнице № 62. Медиана ОВ не достигнута ни в одном из центров.
Выводы. Неоадъювантная иммунотерапия демонстрирует высокую клиническую эффективность в реальной практике. Патоморфологический ответ является мощным предиктором БСВ, что позволяет обоснованно рассматривать стратегию индивидуализации дальнейшего лечения.


Введение
Несмотря на значительный прогресс в системной терапии меланомы, резектабельная III стадия по-прежнему остается прогностически неблагоприятной. Риск рецидива заболевания после хирургического вмешательства продолжает быть высоким даже при последующем назначении адъювантной терапии [1, 2]. Эти данные побудили исследователей к изучению концепции неоадъювантного подхода, позволяющего оценить чувствительность опухоли к терапии in vivo, инициировать системный контроль над микрометастазами еще до операции и индивидуализировать последующую тактику ведения пациента.
Первые проспективные исследования, продемонстрировавшие эффективность неоадъювантной иммунотерапии у пациентов с меланомой III стадии, появились в последние пять лет и легли в основу современного понимания пользы раннего системного вмешательства. Высокая частота полного морфологического ответа (pCR) и его прямая ассоциация с длительной безрецидивной выживаемостью в ряде работ (OpACIN [3], OpACIN-neo [4, 5], PRADO [6]) сформировали предпосылки для клинического внедрения данного подхода в высокоселективных группах пациентов.
В России накопление клинического опыта применения неоадъювантной иммунотерапии происходит по большей части в рамках реальной клинической практики. Ранее мы опубликовали первые объединенные данные трех специализированных центров по эффективности и безопасности данного подхода [7]. Настоящий анализ включает расширенную прослеженность и направлен на верификацию прогностической значимости морфологического ответа, оценку выживаемости и сопоставление хирургических подходов, используемых в практике разных учреждений.
Материал и методы
Исследование представляет собой ретроспективный анализ данных многоцентровой когортной выборки пациентов с резектабельной меланомой кожи III стадии или ее эквивалентом, которые с 2020 по 2023 г. получали неоадъювантную иммунотерапию в трех специализированных онкологических учреждениях Российской Федерации: ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России, ГБУЗ «Московская городская онкологическая больница № 62» Департамента здравоохранения г. Москвы (МГОБ № 62). Критериями включения являлись: гистологически верифицированная меланома кожи III стадии по классификации AJCC (8-я редакция), отсутствие признаков отдаленного метастазирования по радиологической оценке, ECOG 0–1, отсутствие противопоказаний к проведению иммуноонкологической терапии. Все пациенты подписали информированное согласие на лечение и использование обезличенных медицинских данных в научных целях.
Пациенты получали неоадъювантную терапию в виде монотерапии ингибиторами контрольных точек (анти-PD-1: пембролизумаб или пролголимаб) либо комбинированной схемой анти-PD-1 + анти-CTLA-4 (от 2 до 6 циклов). После завершения неоадъювантной терапии проводилась оценка радиологического ответа. Решение о выполнении тотальной лимфодиссекции принималось индивидуально, с учетом клинического ответа.
Основные и дополнительные конечные точки исследования
Патоморфологическая оценка проводилась локальными морфологами согласно руководящим принципам Международного консорциума по неоадъювантной терапии меланомы INMC [1]. Ответ классифицировали как полный (pCR – 0% остаточной опухоли), почти полный (near-pCR – от 1 до 10% витальной опухоли), частичный (pPR – от 11 до 50% остаточной опухоли) или отсутствие ответа (pNR – опухоль составляет более 50%).
После операции в зависимости от патоморфологического ответа планировалась тактика адъювантной терапии. Пациенты могли получать адъювантную терапию на усмотрение врача. Дальнейшее наблюдение осуществлялось в соответствии с клиническими рекомендациями по месту жительства пациента. Бессобытийная выживаемость (БСВ) рассчитывалась от момента первого цикла неоадъювантной терапии до даты объективного прогрессирования или смерти от любых причин. Статистическая обработка выполнялась в SPSS (IBM Corp., США), данные представлены как медианы с 95%-ным доверительным интервалом, категоризированные переменные сравнивались с использованием критерия χ² или точного критерия Фишера. Уровень p < 0,05 считали статистически значимым.
Результаты
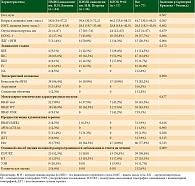
Исходные характеристики пациентов были подробно описаны нами в предыдущей публикации (табл. 1) [7].
Распределение пациентов по режимам неоадъювантной иммунотерапии и среднему количеству циклов представлено в табл. 2.
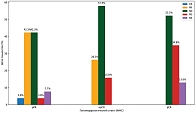
Данные по клинико-радиологическим и патоморфологическим ответам представлены на рис. 1.
В отношении хирургической тактики тотальная лимфодиссекция (TLND) была выполнена у 51 пациента (66,2%). В НМИЦ онкологии им. Н.Н. Блохина TLND не проводилась в девяти случаях: у пяти пациентов из-за прогрессирования до хирургического этапа, у четырех – в связи с отказом пациента от операции на фоне полного клинико-радиологического ответа. В остальных учреждениях TLND выполнялась рутинно: 100% в НМИЦ онкологии им. Н.Н. Петрова и 100% в МГОБ № 62.
Патоморфологический ответ оценивался по критериям INMC [1]. Полный патоморфологический регресс (pCR) был достигнут у 26 пациентов (35,4%), еще у 18 (24%) зафиксирован почти полный ответ (near-pCR), частичный ответ (pPR) отмечен у 22 (28,6%), отсутствие регресса (pNR) – у 11 пациентов (11,4%). Доля пациентов с pCR варьировала по центрам: 16 (36,4%) в НМИЦ онкологии им. Н.Н. Блохина, 4 (25%) в НМИЦ онкологии им. Н.Н. Петрова, 6 (35,3%) в МГОБ № 62. Наблюдались статистически значимые различия в частотах патоморфологических ответов между центрами (p = 0,001), которые могли быть обусловлены различиями в исходных характеристиках пациентов (в уровне лактатдегидрогеназы, способах оценки эффекта и распределении адъювантной терапии – см. табл. 1), что, в свою очередь, отражает различие в локальных клинических стратегиях.
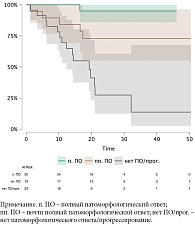
С момента публикации предыдущего анализа прошло более 18 месяцев, что позволило оценить зрелые данные по безрецидивной, бессобытийной и общей выживаемости в когорте из 77 пациентов. Медиана наблюдения составила 17,4 (3,8–55,4) мес. На момент отсечения данных зафиксировано 26 случаев прогрессирования заболевания (33,8%). В группе пациентов с pCR/near-pCR (n = 44) зафиксировано всего два случая прогрессирования, в то время как в подгруппе без выраженного ответа (n = 33) прогрессирование преобладало. Смерть зарегистрирована у 10 (13%) пациентов.
Бессобытийная выживаемость в зависимости от патоморфоза представлена на рис. 2.
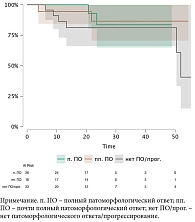
Общая выживаемость (ОВ) не достигнута ни в одной из подгрупп. График ОВ в зависимости от патоморфологического ответа представлен на рис. 3.
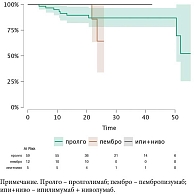
Также необходимо учесть, что схемы терапии отличались, и мы также демонстрируем график ОВ в зависимости от применяемой схемы в неоадъювантном режиме (рис. 4).
Данные о профиле безопасности были представлены у пациентов из НМИЦ онкологии им. Н.Н. Блохина. Всего зарегистрировано 15 нежелательных явлений (НЯ) на фоне неоадъювантной иммунотерапии пролголимабом у 13 субъектов. У единственного пациента, получившего комбинированную иммунотерапию PD-1 + CTLA-4, НЯ не зарегистрированы. Наиболее часто встречались кожная токсичность 1-й степени по CTCAE v. 5.0 (4/13) и тиреоидит 1–2-й степени (4/13). Также были зарегистрированы трансаминазит 1-й степени (1/13), пневмонит 2-й степени (1/13), тубуло-интерстициальный нефрит 2-й степени (1/13), эпидидимит 2-й степени (1/13), саркоидная реакция 2-й степени (1/13). У одного пациента развился фульминантный сахарный диабет 1 типа 4-й степени по CTCAE v. 5.0. Данные представлены в табл. 3.
Адъювантную терапию после регионарной лимфаденэктомии получили 47 пациентов (62,3%), 22 пациента (28,6%) ее не получали, еще у восьми пациентов статус адъювантного этапа неизвестен. Использование адъювантной терапии варьировало по учреждениям: чаще всего ее применяли в МГОБ № 62 (41%), в НМИЦ онкологии им. Н.Н. Блохина – у половины пациентов, в НМИЦ онкологии им. Н.Н. Петрова – только у 25%.
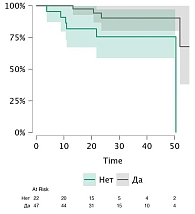
Мы также провели анализ выживаемости методом Каплана – Мейера со сравнением групп пациентов в зависимости от проведения адъювантной терапии. В анализ включено 69 пациентов (исключено восемь наблюдений с пропущенными значениями).
В группе без адъювантной терапии (n = 22) зарегистрировано шесть событий, тогда как в группе с адъювантной терапией (n = 47) – четыре события. Ограниченное среднее время без события составило 41,04 мес. (SE 3,70) в группе без адъювантной терапии и 51,12 мес. (SE 1,96) в группе с адъювантной терапией. Медиана выживаемости достигнута только в группе без адъювантной терапии (50,46 мес.), тогда как в группе с адъювантной терапией медиана не достигнута. Сравнение кривых выживаемости методом логрангового теста выявило статистически значимые различия между группами (χ² = 5,916; df = 1; p = 0,015). Бессобытийная выживаемость в зависимости от проведения адъювантной терапии представлена на рис. 5.
Таким образом, проведение адъювантной терапии ассоциировано с увеличением времени до наступления неблагоприятного события, однако выраженность эффекта менее значительна по сравнению с основной выборкой.
Обсуждение и выводы
Анализ объединенной когорты из 77 пациентов, получивших неоадъювантную иммунотерапию в трех онкологических учреждениях России, продемонстрировал реалистичные, но обнадеживающие результаты. Частота полного патоморфологического ответа (pCR) составила 35,4%, а в совокупности с почти полным ответом – 59,4%, что подчеркивает клиническую эффективность неоадъювантной иммунотерапии в рамках реальной клинической практики. Сравнение с международными исследованиями подтверждает валидность полученных нами результатов. В исследовании OpACIN-neo частота полного патоморфологического ответа при различных режимах терапии составляла от 25 до 45% [4, 5], а в PRADO было показано, что пациенты с pCR имели высокий уровень безрецидивной выживаемости без необходимости проведения тотальной лимфодиссекции [6]. Наши данные о pCR + near-pCR в 59,4% полностью соответствуют этим значениям, несмотря на отсутствие стандартизированного протокола и неоднородность режимов терапии.
Данные по прогрессированию (29,2% на момент среза) указывают на сохраняющийся риск рецидива, особенно в группе пациентов, не достигших выраженного патоморфологического ответа. Эти результаты усиливают обоснование концепции морфологической стратификации, при которой pCR/near-pCR служат не только прогностическим маркером, но и потенциальной точкой деэскалации терапии.
Роль адъювантного этапа после неоадъювантной иммунотерапии требует отдельного обсуждения. Адъювантное лечение было проведено у 57,1% пациентов, и его доля была выше среди тех, кто не достиг полного морфологического ответа. Это указывает на гибкость терапевтической тактики в реальной практике и необходимость индивидуального подхода при принятии решений после операции.
Важно отметить, что частота выполнения лимфаденэктомии варьировала между учреждениями, при этом в НМИЦ онкологии им. Н.Н. Блохина чаще прибегали к отказу от тотальной лимфодиссекции. Данное наблюдение требует дальнейшей оценки в контексте долгосрочных исходов.
Для лучшего обеспечения сопоставимости данных и стандартизации подходов к интерпретации патоморфологического ответа на неоадъювантную терапию целесообразно повсеместное внедрение рекомендаций Международного консорциума по неоадъювантной терапии меланомы (INMC). Использование единой шкалы оценки позволяет не только корректно стратифицировать пациентов по риску, но и проводить межцентровые и межисследовательские сравнения, обеспечивая преемственность результатов.
Отдельного внимания заслуживает вопрос выбора режима неоадъювантной иммунотерапии – между монотерапией ингибиторами PD-1 и их комбинацией с ингибиторами CTLA-4. Международные исследования, включая OpACIN и OpACIN-neo, продемонстрировали более высокие частоты патоморфологического ответа при применении комбинированной терапии, однако это сопровождалось значительно более высоким уровнем иммунопосредованных осложнений. В нашем исследовании различия между режимами неоадъювантной терапии были статистически незначимыми в отношении частоты pCR/near-pCR, БСВ и ОВ. В условиях реальной практики, особенно с учетом медианного возраста пациентов в нашем исследовании (60 лет), вопросы переносимости приобретают особую актуальность. Важно учитывать, что старшая возрастная когорта может иметь сопутствующие заболевания и функциональные ограничения, что делает более оправданным выбор монотерапии ингибиторами PD-1.
В связи с этим определение баланса между эффективностью и безопасностью различных режимов неоадъювантной терапии остается актуальной задачей.
Для оптимизации подходов требуется валидация на более крупных выборках, с подключением биомаркеров ответа, стандартизированных хирургических подходов и анализа качества жизни пациентов.
Таким образом, полученные данные подтверждают практическую реализуемость неоадъювантной терапии при резектабельной меланоме кожи в условиях российской онкологической службы и коррелируют с мировыми тенденциями. Патоморфологический ответ является мощным предиктором БСВ, что позволяет обоснованно рассматривать стратегию индивидуализации дальнейшего лечения.
A.O. Kuzmenko, A.V. Novik, PhD, K.Yu. Kapusta, A.N. Yurchenkov, D.L. Stroyakovsky, PhD, I.V. Samoylenko, PhD
N.N. Blokhin National Medical Cancer Research Center, Moscow
N.N. Petrov National Medical Research Center of Oncology, Saint Petersburg
St. Petersburg State Pediatric Medical University
Moscow City Oncology Hospital No. 62
Contact person: Igor V. Samoylenko, i.samoylenko@ronc.ru
Neoadjuvant immunotherapy for resectable cutaneous melanoma represents a rapidly evolving therapeutic strategy that not only enhances systemic disease control but also enables individualization of surgical management.
Objective. To report updated efficacy and safety data on neoadjuvant immunotherapy in resectable cutaneous melanoma stages IIIB–D, derived from three leading oncology centers in Russia, with emphasis on long-term outcomes and pathomorphological response.
Materials and methods. We performed an updated analysis of pooled data from 77 patients who received NST between October 2020 and November 2023 across three major oncology centers in Russia. Neoadjuvant immunotherapy consisted of prolgolimab in 59 patients (76.6%), pembrolizumab in 13 (16.9%), and ipilimumab 3 mg/kg plus nivolumab 1 mg/kg in five (6.5%). The mean number of cycles was 3.6 (45.5 days; 95% confidence interval [CI] 3.2–4.0). Primary endpoints included pathomorphological response assessed according to International Neoadjuvant Melanoma Consortium (INMC) criteria, event-free survival (EFS), overall survival (OS), and the role of subsequent adjuvant therapy. Survival outcomes were estimated using the Kaplan–Meier method; between-group differences were assessed by the log-rank test.
Results. The distribution across treatment regimens and mean cycle count (3.6; 95% CI 3.2–4.0) remained unchanged from the prior analysis. A complete pathological response (pCR) was achieved in 26 patients (38.2%), a near-complete response (near-pCR) in 19 (27.9%), and no pathological response (pNR) in 23 (33.8%). Accordingly, a major pathological response (pCR + near-pCR) was recorded in 45 patients (59.4%). Regional lymph node dissection was not performed in nine patients: four experienced disease progression prior to surgery, and five declined the procedure in the setting of complete clinical response. At a median follow-up of 19.3 months (95% CI 1.15–50.5), median EFS was 32.1 months at the N.N. Blokhin National Medical Research Center of Oncology, 21 months at the N.N. Petrov National Medical Research Center of Oncology, and was not reached at Moscow Clinical Oncology Hospital No. 62. Median OS was not reached at any of the participating centers.
Conclusions. Neoadjuvant immunotherapy demonstrates robust clinical efficacy in a real-world setting. Pathomorphological response emerges as a powerful independent predictor of EFS, providing a rational basis for response-adapted individualization of subsequent treatment strategies.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.