Неоспоримая важность гликемического контроля в эпоху органопротективной сахароснижающей терапии
- Аннотация
- Статья
- Ссылки
- English
В статье обсуждаются возможности современной сахароснижающей фармакотерапии. Для повышения ее эффективности подчеркивается необходимость назначения комбинаций препаратов.
Несмотря на изменения в современных алгоритмах, одними из часто назначаемых при сахарном диабете 2 типа остаются производные сульфонилмочевины. Представители данной группы существенно отличаются друг от друга структурой, длительностью действия и фармакологическими свойствами, что определяет их терапевтические эффекты.
Оригинальный гликлазид модифицированного высвобождения (Диабетон МВ®) обладает рядом преимуществ перед другими препаратами из группы производных сульфонилмочевины, в том числе в отношении безопасности при различных клинических ситуациях. Перспективной опцией считается комбинация гликлазида МВ и ингибиторов натрий-глюкозного котранспортера 2.
В статье обсуждаются возможности современной сахароснижающей фармакотерапии. Для повышения ее эффективности подчеркивается необходимость назначения комбинаций препаратов.
Несмотря на изменения в современных алгоритмах, одними из часто назначаемых при сахарном диабете 2 типа остаются производные сульфонилмочевины. Представители данной группы существенно отличаются друг от друга структурой, длительностью действия и фармакологическими свойствами, что определяет их терапевтические эффекты.
Оригинальный гликлазид модифицированного высвобождения (Диабетон МВ®) обладает рядом преимуществ перед другими препаратами из группы производных сульфонилмочевины, в том числе в отношении безопасности при различных клинических ситуациях. Перспективной опцией считается комбинация гликлазида МВ и ингибиторов натрий-глюкозного котранспортера 2.

Прогнозы эпидемиологов не оправдываются. С каждым годом наблюдается прирост количества пациентов с сахарным диабетом (СД), при этом преимущественно с СД 2 типа. Как следствие, по-прежнему актуальны вопросы эффективного, безопасного и доступного лечения заболевания [1–3]. Предиабетические нарушения (нарушенная толерантность к глюкозе, нарушение гликемии натощак) на несколько лет опережают манифестацию СД 2 типа. В течение этого периода гипергликемия и сопутствующие факторы сердечно-сосудистого риска (избыточный вес/ожирение, артериальная гипертензия, дислипидемия) обусловливают повышение бремени осложнений к моменту постановки диагноза [4, 5].
В связи с развитием системных сосудистых осложнений, преждевременной инвалидизацией, необходимостью пожизненной фармакотерапии и постоянного контроля гликемии, высокой смертностью СД ассоциируется с существенным увеличением расходов как системы здравоохранения, так и государства в целом [4, 6]. Известно, что не менее 12% общемировых трат на здравоохранение приходятся на долю СД [6]. Присоединение диабетических осложнений повышает стоимость лечения в среднем в три – десять раз [7].
Гликемический контроль и его связь с развитием осложнений
Важность достижения гликемического контроля с самого начала сахароснижающей терапии подтверждена обширной доказательной базой. Так, в исследовании UKPDS были получены данные о долгосрочном влиянии раннего оптимального контроля гликемии на клинические исходы СД 2 типа, в связи с чем была предложена концепция метаболической памяти, или эффекта наследия. Установлено, что у больных с впервые выявленным СД 2 типа интенсивный контроль гликемии в течение 7,5 года при снижении уровня гликированного гемоглобина (HbA1c) на 1% приводит к уменьшению риска развития микроангиопатий на 37%, инфаркта миокарда на 14%, инсульта на 12%, ампутации конечностей на 43% и смерти, связанной с СД 2 типа, на 21% [8].
Следовательно, предшествующий удовлетворительный или неудовлетворительный гликемический контроль способен влиять на развитие и прогрессирование сосудистых осложнений [9]. Показано, что профилактика микро- и макрососудистых осложнений СД 2 типа возможна, если удается достичь и поддерживать целевую гликемию с дебюта заболевания и как минимум в течение последующих семи – десяти лет [10]. Однако проблемы, связанные с достижением должного метаболического контроля и развитием хронических осложнений СД, пока решить не удается. Согласно результатам метаанализа 24 исследований, проведенного K. Khunti и соавт., только 42,8% пациентов (95%-ный доверительный интервал (ДИ) 38,1–47,5%) достигают целевого уровня глюкозы в крови [11].
В последние десятилетия получены результаты крупных исследований сердечно-сосудистых исходов (Cardiovascular Outcome Trials, CVOTs) на фоне применения сахароснижающих препаратов (ССП), что позволило сформировать серьезную доказательную базу в отношении их положительного влияния на сердечно-сосудистые, а также почечные исходы у больных СД 2 типа [12]. В результате претерпела существенные изменения тактика назначения ССП.
В настоящее время лечение можно назначать с учетом доминирующей клинической проблемы (высокий риск развития атеросклеротических сердечно-сосудистых заболеваний (АССЗ) или наличие таковых, хроническая сердечная недостаточность (ХСН), хроническая болезнь почек (ХБП)) и таким образом улучшить прогноз заболевания [13].
Пусковым фактором развития диабетических осложнений, неблагоприятных сердечно-сосудистых и почечных исходов признается именно хроническая гипергликемия. Оценка влияния исходного гликемического контроля на остаточный сердечно-сосудистый риск у больных СД 2 типа с высоким сердечно-сосудистым риском на фоне приема статинов (субанализ результатов исследования ACCELERATE) продемонстрировала, что уровень HbA1c остается независимым прогностическим фактором сердечно-сосудистых событий у получающих оптимальное лечение [14].
Кроме того, установлено, что у большинства пациентов кардио- и нефропротективные эффекты ингибиторов натрий-глюкозного котранспортера 2 (иНГЛТ-2) и агонистов рецепторов глюкагоноподобного пептида 1 (арГПП-1) не могут быть достигнуты без эффективного контроля гликемии. Для снижения риска возникновения осложнений уровень HbA1c должен составлять менее 7% [15, 16].
D. Giugliano и соавт. проанализировали результаты 12 исследований сердечно-сосудистых исходов с участием 120 765 пациентов с целью изучения связи между гликемическим контролем, ранее существовавшими АССЗ и основными сердечно-сосудистыми событиями (Major Adverse Cardiovascular Events, MACE) [17]. Применение как арГПП-1, так и иНГЛТ-2 по сравнению с использованием плацебо способствовало значительному снижению (на 14%) риска развития сердечно-сосудистых осложнений у пациентов с ранее существовавшими АССЗ и незначительному повышению (на 2%) риска достижения MACE у лиц без АССЗ (р = 0,021). Метарегрессионный анализ результатов показал значимую связь между снижением уровня HbА1с и снижением MACE (р = 0,002). Соответственно, большее снижение частоты неблагоприятных сердечно-сосудистых событий ожидалось, если бы во всех CVOTs уровень HbА1с уменьшился на 0,9%, или на 33% от исходного. Был сделан вывод, что иНГЛТ-2 и арГПП-1 должны включаться в схему лечения больных СД 2 типа и манифестными ССЗ с должным вниманием к улучшению гликемического контроля, что способно усилить положительный эффект препаратов в отношении MACE.
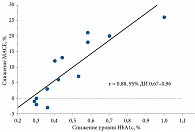
Аналогичные результаты получены P. Ambrosi и соавт. при проведении метаанализа 14 CVOTs (рис. 1). Выявлена связь между уменьшением уровня HbA1c и частоты достижения MACE, которая была значимой при поправке на снижение массы тела (p = 0,019). По мнению ученых, изменения уровня HbA1c следует учитывать при интерпретации влияния ССП на сердечно-сосудистые исходы [18].
Анализ результатов крупномасштабных CVOTs, в частности исследований LEADER и REWIND, показал, что снижение концентрации HbA1c является одним из важных параметров в отношении прогноза кардиопротективных эффектов, на долю которых приходится до 82% [19].
Современная стратегия медикаментозных вмешательств
Пациенты с СД 2 типа как можно раньше должны получать лечение в соответствии с национальными и международными рекомендациями, краеугольным камнем которых является персонализированный подход. Изменение образа жизни (рациональное питание и повышение физической активности) и обучение принципам управления заболеванием рассматриваются как неотъемлемые части терапии и должны проводиться на протяжении всей жизни [13].
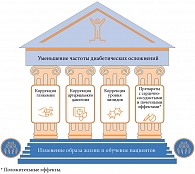
Действующие рекомендации также акцентируют внимание на важности объединения глюкозо- и кардиоцентричного подходов на пути к достижению ключевых целей: снижение кардиоренального риска у пациентов с СД 2 типа и высоким риском (в дополнение к комплексному управлению рисками развития ССЗ), достижение и длительное поддержание целевой гликемии (рис. 2) [20].
При выборе ССП приоритетными являются эффективность, безопасность и возможность влиять на клинические исходы. Кроме того, следует учитывать влияние на массу тела, а также стоимость лечения и предпочтения пациента [13, 20, 21].
На сегодняшний день существует несколько основных групп ССП: бигуаниды (метформин (МЕТ)), производные сульфонилмочевины (ПСМ), тиазолидиндионы (ТЗД), глиниды (ГЛН), ингибиторы дипептидилпептидазы 4 (иДПП-4), арГПП-1, иНГЛТ-2, инсулин. Однако ни один из них пока не способен замедлить прогрессирующую потерю функции β-клеток [22].
Согласно российским рекомендациям [13], при наличии противопоказаний к назначению препаратов первой линии или их плохой переносимости, а также для интенсификации лечения при неудовлетворительном контроле гликемии возможно применение препарата другой группы с оценкой его безопасности/нейтральности в отношении доминирующей клинической проблемы. В качестве второй линии терапии предпочтительны препараты, ассоциированные с низким риском гипогликемий, а при наличии АССЗ, ХСН или ХБП – с доказанным преимуществом при данных состояниях.
Производные сульфонилмочевины
Производные сульфонилмочевины – средства с длительной историей применения, поэтому их преимущества и недостатки хорошо изучены [23, 24]. Применение ПСМ безопасно (нейтрально) при наличии у больных СД 2 типа факторов высокого риска возникновения АССЗ (возраст 55 лет и старше плюс стеноз коронарных, каротидных артерий или артерий нижних конечностей или гипертрофия левого желудочка), АССЗ (не рекомендован глибенкламид), ХБП (до ХБП С4 включительно, глибенкламид не рекомендован при скорости клубочковой фильтрации (СКФ) менее 60 мл/мин/1,73 м2). Пациентам с ХСН не рекомендован глибенкламид, другие ПСМ назначают с осторожностью [13].
Несмотря на изменения в современных алгоритмах лечения, ПСМ остаются одними из часто назначаемых препаратов при СД 2 типа [22–26]. Приверженность ПСМ со стороны врачей обусловлена невысокой ценой, определяющей доступность и экономическую эффективность лечения, эффективностью (на фоне монотерапии уровень HbA1c в среднем снижается на 1–2%), быстрым достижением сахароснижающего эффекта, нефро- и кардиопротекцией (только у гликлазида модифицированного высвобождения (МВ)) [25, 26].
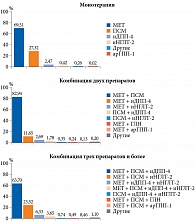
В настоящее время в России представлены следующие ПСМ: гликлазид МВ, гликлазид, глимепирид, гликвидон, глибенкламид. В структуре фармакотерапии СД 2 типа наиболее частыми двойными комбинациями являются «МЕТ + ПСМ» – 82,9%, «МЕТ + иДПП-4» – 11,7% [1]. Доля комбинаций «МЕТ + иНГЛТ-2» составляет 2,7%, «ПСМ + иДПП-4» – 1,8%, «МЕТ + арГПП-1» – 0,1%. Доля новых классов препаратов возрастает в составе тройных комбинаций в основном с ПСМ и МЕТ: «МЕТ + ПСМ + иДПП-4» – 63,7%, «МЕТ + ПСМ + иНГЛТ-2» – 23,5%, «МЕТ + иДПП-4 + иНГЛТ-2» – 6,3% (рис. 3) [1].
Несмотря на общий механизм действия (стимуляция секреции инсулин), представители ПСМ существенно различаются структурой, длительностью действия и другими фармакологическими свойствами. Особенности фармакокинетики, различное сродство, селективность и обратимость связывания с рецептором сульфонилмочевины 1 (SUR-1) β-клеток обусловливают значимые различия в отношении профиля и безопасности действия (гипогликемии, сердечно-сосудистые эффекты), что важно при выборе конкретного препарата из данной группы [27, 28].
Ключевой фактор, определяющий возможность и место препарата в современных руководствах по лечению СД 2 типа, – сердечно-сосудистые эффекты [28]. В отношении большинства представителей ПСМ не получено однозначных данных о сердечно-сосудистой безопасности. При этом гликлазид МВ (оригинальный препарат Диабетон® МВ) продемонстрировал безопасность у пациентов с сердечно-сосудистой патологией. Данные о негативном влиянии препарата у больных с СД 2 типа и ХСН отсутствуют [22, 27, 29].
В современных руководствах гликлазид МВ характеризуется как препарат с благоприятным профилем сердечно-сосудистой безопасности, ренопротективными эффектами, низким риском развития гипогликемий и увеличения массы тела [13, 25, 27]. Не случайно среди ПСМ это один из наиболее широко применяемых в клинической практике препаратов [26, 30, 31].
Фармакологические особенности, возможности и преимущества гликлазида МВ
Разработка ПСМ с модифицированным высвобождением действующего вещества – гликлазида МВ обеспечила важные преимущества, включая лучший контроль заболевания, высокую эффективность при минимальном риске развития побочных эффектов, в частности развитие гипогликемий, прибавка массы тела [22, 24, 32]. Например, оригинальный препарат гликлазида МВ, произведенный с использованием гидрофильного матрикса (гипромелоза), характеризуется постепенным пролонгированным высвобождением активного вещества (в течение 24 часов) с максимальной его концентрацией в дневное время и постепенным снижением ночью, что соответствует суточному профилю гликемии и обусловливает уменьшение риска возникновения гипогликемий [33].
Благодаря восстановлению физиологической секреции инсулина и обратимому характеру связывания с SUR-1 гликлазид МВ обладает высокой сахароснижающей эффективностью, а благодаря образованию неактивных метаболитов – меньшим риском развития гипогликемий [23, 25, 27]. Гликлазид МВ, молекула которого не содержит бензамидной группы, имеющей сродство с клетками сердца и сосудов, проявляет в 16 000 раз большую селективность к SUR-1 β-клеток и практически не блокирует SUR-2 в сердечной и гладких мышцах [34]. Таким образом, в отличие от глибенкламида, селективно взаимодействуя с SUR-1 β-клеток, гликлазид МВ не нарушает процессы ишемического прекондиционирования [24, 29].
Как уже подчеркивалось ранее, терапия СД 2 типа направлена на снижение риска развития системных сосудистых осложнений. Диабетическая нефропатия – распространенное, зачастую поздно диагностируемое микрососудистое осложнение с крайне неблагоприятными исходами, которое ассоциируется с высоким риском возникновения сердечно-сосудистой патологии и смерти. Данное состояние является ведущей причиной развития почечной недостаточности, нередко требующей заместительной почечной терапии [35].
Для замедления прогрессирования диабетической нефропатии, предотвращения острых и хронических осложнений особую роль играют ранний скрининг (выявление повышения альбуминурии, снижения расчетной СКФ (рСКФ)), эффективные стратегии метаболического контроля, кардио- и нефропротекция. Доказано, что раннее лечение диабетической нефропатии может замедлить или предотвратить ее прогрессирование [28, 36–39].
Возможность длительного и безопасного применения оригинального гликлазида МВ при СД 2 типа и улучшения на его фоне прогноза в отношении диабетических осложнений установлена в исследовании ADVANCE [38]. Интенсивный гликемический контроль, основанный на применении гликлазида МВ, на 10% снизил риск наступления комбинированной конечной точки по микро- и макрососудистым осложнениям. Это было достигнуто преимущественно за счет уменьшения риска развития микрососудистой патологии на 14%, включая риск развития или ухудшения течения диабетической нефропатии на 21%, достижения терминальной стадии почечной недостаточности на 65%, развития новых случаев микроальбуминурии и протеинурии на 9 и 30% соответственно, любых почечных исходов на 11%.
Кроме того, оптимальный контроль гликемии на фоне применения гликлазида МВ способствовал регрессу альбуминурии как минимум на одну стадию у 62% пациентов с СД 2 типа, возвращению уровня альбумина к норме у 57% [38]. Эти данные представляют особую ценность, поскольку микроальбуминурия даже у лиц с СКФ более 60 мл/мин/1,73 м2 связана с более высокой сердечно-сосудистой смертностью и быстрыми темпами снижения СКФ [39]. Отсроченный эффект ранней интенсивной стратегии на основе использования оригинального гликлазида МВ (препарата Диабетон МВ®) подтвержден результатами постинтервенционного наблюдательного исследования ADVANCE-ON [40]. Препарат продемонстрировал не только долгосрочную сердечно-сосудистую, но и почечную безопасность. Так, на 46% снизилась частота случаев достижения терминальной стадии почечной недостаточности (относительный риск (ОР) 0,54 (95% ДИ 0,34–0,85; p = 0,007)).
Благодаря нефропротективному воздействию, благоприятному профилю кардиобезопасности гликлазид МВ является единственным ПСМ, рекомендованным к применению в России у лиц с СД 2 типа и ХБП С1–3а [13].
К основным недостаткам ПСМ относят риск развития гипогликемий и увеличения массы тела. Однако в этом отношении ПСМ также достаточно разнородны.
Показана существенная разница риска развития гипогликемий, включая эпизоды тяжелой гипогликемии, между разными препаратами ПСМ [25, 27, 31, 32]. Более низкий риск обусловлен отсутствием активных метаболитов, избирательностью и обратимостью связывания ПСМ с рецепторами SUR-1 на β-клетках поджелудочной железы. Низкая скорость диссоциации комплекса «ПСМ – SUR-1» может определять высокий риск возникновения гипогликемий [23, 41, 42]. Длительно действующие и образующие активные метаболиты ПСМ повышают риски пролонгированной и тяжелой гипогликемии, особенно у пожилых пациентов [22, 23, 43]. Нзкий риск гипогликемий отмечается при лечении гликлазидом МВ. Препарат метаболизируется в печени до неактивных метаболитов, которые выводятся с мочой. Гликлазид не увеличивает частоту эпизодов гипогликемий при ХБП, являющейся фактором риска таковых [25, 27, 28, 31].
Известно, что данные национальных регистров отражают реальную ситуацию в клинической практике. Кроме того, они дополняют информацию, полученную в рандомизированных контролируемых исследованиях (РКИ), поскольку предоставляют данные эффективности и безопасности терапии у не вошедших в исследования по критериям исключения. L.-L. Lim и соавт. провели анализ регистра JADE, который включал данные пациентов с СД 2 типа из 11 стран Азиатского региона с ноября 2007 г. по декабрь 2019 г. [31]. В анализ не включали лиц, получавших инсулин и/или арГПП-1. Общее количество больных составило 62 512, из них 53,6% мужчин, средний возраст – 57,3 ± 11,8 года. Терапию на основе ПСМ получали 59,4%, наиболее частыми двойными комбинациями были «МЕТ + ПСМ» (79,5%) и «ПСМ + иДПП-4» (22,1%). Из 32 558 получавших ПСМ 15 312 находились на терапии гликлазидом МВ. У последних отмечалось более тяжелое течение СД 2 типа. В частности, применявшие гликлазид МВ по сравнению с пациентами, получавшими глимепирид, глибенкламид и глипизид, были старше (59,7 ± 11,5 против 56,5 ± 11,3 года, в возрасте 65 лет и более было 31,6 против 22,3%, р < 0,001), имели большую продолжительность заболевания (семь против шести лет, р < 0,001). Кроме того, у них была более низкая рСКФ (79,7 против 80,6 мл/мин/1,73 м2, р < 0,001). Эта группа превосходила другие группы по числу лиц с ХБП (17,7 против 14,4%; р < 0,001) и другими выявленными осложнениями (диабетическая нейропатия, ретинопатия, сердечно-сосудистые заболевания, р < 0,001). Несмотря на более тяжелое течение СД 2 типа, у принимавших гликлазид частота гипогликемий была на 19% ниже (отношение шансов (ОШ) 0,81 (95% ДИ 0,72–0,92, р = 0,001)), чем у получавших другие ПСМ. Согласно данным регистра, гликлазид превосходил другие ПСМ по эффективности. Так, на фоне терапии гликлазидом чаще отмечалось достижение уровня HbA1c 7% (ОШ 1,09 (95% ДИ 1,02–1,17)) [31].
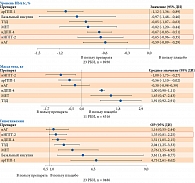
Доказательства эффективности и внутриклассовых преимуществ гликлазида МВ представлены в метаанализе A. Maloney и соавт. Данный метаанализ был посвящен всесторонней оценке сахароснижающей эффективности, влияния на массу тела и риск развития гипогликемий 24 ССП из шести групп (бигуаниды – метформин, арГПП-1 – албиглутид, дулаглутид, эксенатид, лираглутид, ликсисенатид и семаглутид, иНГЛТ-2 – канаглифлозин, дапаглифлозин, эмпаглифлозин и эртуглифлозин, ПСМ – гликлазид, глипизид, глимепирид и глибенкламид, иДПП-4 – алоглиптин, линаглиптин, саксаглиптин, ситаглиптин и вилдаглиптин, тиазолидиндионы – пиоглитазон, росиглитазон) [44]. Итогом метаанализа, объединившего 229 РКИ с участием 121 914 пациентов, стало выявление значимых для клинической практики различий не только между отдельными группами препаратов, но и между препаратами одной группы. Для объективного сравнения разных вариантов лечения результаты корректировали с учетом значимых различий между исследованиями, в том числе по продолжительности терапии, исходному уровню HbA1c и дозам ССП.
Оценка гликемического контроля показала, что наибольшей эффективностью обладали арГПП-1 (снижение уровня HbA1c на 1,77%, но у разных представителей данной группы результат различался), наименьшей – иДПП-4 (снижение уровня HbA1c на 0,58–0,72%). Важно отметить, что гликлазид по эффективности превзошел иДПП-4, иНГЛТ-2 и ТЗД. Уровень HbA1c снизился на 1,04 против 0,58–0,72, 0,65–1,01 и 0,62–0,98% соответственно.
По сравнению с плацебо увеличение ОР развития гипогликемий оказалось наибольшим у ПСМ. Однако внутри группы ПСМ таковой значимо различался с явным преимуществом в пользу гликлазида МВ. В частности, для данного препарата ОР составил 3,6 (2,5–5,1), что существенно меньше, чем для других ПСМ: для глимепирида – 8,9 (7,3–10,9), глибенкламида – 10,2 (7,9–13,2), глипизида – 13,9 (10,6–18,4). Важно отметить, что ОР развития эпизодов гипогликемии при применении гликлазида МВ и метформина был аналогичным – 3,6 и 2,0 соответственно.
Анализ динамики массы тела также продемонстрировал разницу эффектов разных ССП. При применении арГПП-1, кроме албиглутида, снижение массы тела варьировалось от 0,3 до 3,8 кг, иНГЛТ-2 – от 1,7 до 2,4 кг. Метформин ассоциировался с небольшой потерей массы тела – на 0,5 кг. Ингибиторы ДПП-4, напротив, – с незначительным ее увеличением. Прибавка массы тела отмечена при использовании ТЗД (4,9 кг) и ПСМ (2,0–3,0 кг). Наибольшее изменение зафиксировано при применении глибенкламида – увеличение массы тела на 3,0 кг.
Необходимо отметить, что риск гипогликемии может быть связан не только с применением конкретных ССП, но и с изменением питания (увеличение временных промежутков между приемами пищи, недостаточное количество углеводов, голодание), физической активностью и злоупотреблением алкоголем. Поэтому риск гипогликемий может возрастать у пациентов с СД 2 типа, соблюдающих религиозные посты, в частности во время празднования Рамадана (полное воздержание от приема пищи и питья от рассвета до заката) [45].
В проспективном международном исследовании DIA-RAMADAN была показана высокая безопасность оригинального гликлазида МВ в период Рамадана. В данном исследовании приняли участие 1244 пациента с СД 2 типа, 94,9% из которых получали гликлазид МВ в дозе 60 мг и более [46]. Больные принимали гликлазид МВ один раз в день в течение 14–18 недель. Средняя продолжительность поста составила 28,7 ± 3,5 дня, средняя продолжительность поста в сутки – 14,7 ± 1,5 часа. До начала Рамадана пациенты принимали гликлазид МВ однократно во время завтрака. Только 0,2% сообщили об эпизоде симптоматической гипогликемии. В соответствии с рекомендациями Международной диабетической федерации и Американской диабетической ассоциации [45] по стандартной клинической практике лечения СД 2 типа во время Рамадана пациентам был назначен прием гликлазида МВ во время вечернего разговения после заката. Приверженность режиму лечения составила 99,5%.
У лиц с СД 2 типа, которые соблюдали пост и принимали оригинальный гликлазид МВ, не было отмечено эпизодов тяжелой гипогликемии (таблица). Лечение характеризовалось очень низкой частотой симптоматических эпизодов гипогликемии во время (2,2%) и до/после голодания (0,3% и менее) в условиях поддержания стабильного уровня HbA1с (-0,3%) и массы тела (-0,5 кг).
Применение гликлазида МВ (без коррекции дозы во время Рамадана) в условиях реальной практики не было ассоциировано с повышением риска гипогликемий, что еще раз доказывает высокую безопасность терапии, даже в тех ситуациях, когда риск гипогликемий значительно повышен [24, 31].
Согласно действующим рекомендациям Международной диабетической федерации и Американской диабетической ассоциации, больные СД 2 типа, собирающиеся поститься во время празднования Рамадана и принимающие ПСМ в качестве основной терапии, могут продолжить их прием, отдавая предпочтение препаратам с модифицированным высвобождением и более безопасным в отношении риска гипогликемий. Глибенкламид ассоциирован с более высоким риском развития гипогликемии, поэтому во время религиозных постов следует избегать его приема [45].
Влияние на качество жизни
Наличие СД 2 типа влечет за собой снижение качества жизни вследствие развития серьезных сосудистых осложнений, необходимости пожизненной терапии, постоянного контроля гликемии и др. Поэтому важным аспектом эффективности терапии является субъективная оценка пациентом сахароснижающей фармакотерапии – благоприятное или неблагоприятное воздействие препарата на разные аспекты жизни [47].
Не так давно был проведен ретроспективный перекрестный анализ регистра JADE в отношении оценки качества жизни пациентов, получающих ПСМ [47]. Исследователям были доступны данные общего опросника EuroQol-5D (EQ-5D-3L). Опросник EuroQol-5D, разработанный Европейской группой исследования качества жизни, является широко используемым инструментом для оценки состояния здоровья в целях выявления нарушений функционирования по пяти аспектам: передвижение, уход за собой, повседневная деятельность, боль/дискомфорт, тревога/депрессия [48, 49].
Было выбрано 47 895 пациентов, полностью заполнивших опросник EQ-5D-3L, 42 813 из которых наряду с модификацией образа жизни получали ССП, 5082 – только модифицировали образ жизни. В структуре ССП 60% приходилось на ПСМ, 47% из них на гликлазид, 53% – на другие препараты данной группы. Речь, в частности, идет о глимепириде – 39,9%, глибенкламиде – 8,6%.
У получавших гликлазид по сравнению с принимавшими другие ПСМ уровень HbA1c был ниже, а качество жизни выше по всем компонентам EQ-5D-3L (p < 0,001): подвижность (91,7 против 86,2%), уход за собой (97,2 против 93,9%), повседневная деятельность (94,7 против 91,2%), боль/дискомфорт (75,2 против 69,3%), тревога/депрессия (79,8 против 72,7%). При анализе всех компонентов EQ-5D-3L процент пациентов без проблем был также выше среди тех, кто получал гликлазид, по сравнению с принимавшими другие ПСМ – 62,9 и 55,0% соответственно.
Выбор эффективной и безопасной комбинации с производными сульфонилмочевины
Большинство пациентов с СД 2 типа получают несколько сахароснижающих препаратов. В реальной практике самой часто назначаемой является комбинация МЕТ с ПСМ [1]. Однако метформин плохо переносится некоторыми пациентами (нежелательные эффекты со стороны желудочно-кишечного тракта), а в ряде случаев даже противопоказан. Поэтому важно знать другие комбинации с ПСМ, которые хорошо изучены, эффективны и безопасны, особенно с учетом риска возникновения гипогликемий.
В связи со сказанным ранее интерес могут представлять результаты метаанализа D. Qian и соавт. по оценке эффективности и безопасности комбинированной сахароснижающей терапии у пациентов с неудовлетворительным контролем на фоне монотерапии ПСМ [50]. Проанализированы 24 РКИ продолжительностью от 24 до 52 недель с участием 10 032 пациентов. Систематический обзор проведен согласно критериям PRISMA. Ученые оценивали риск развития гипогликемий, эффективность (динамика уровня глюкозы плазмы натощак и HbA1c) и влияние на массу тела разных схем лечения. Средний возраст участников варьировался от 52 до 75 лет. Исходный уровень HbA1c в среднем составлял 8,5 (7,6–9,9)%, ИМТ – 28,6 (23,8–32,2) кг/м2.
В отличие от плацебо все схемы лечения были связаны со значительно более высоким риском возникновения гипогликемий, за исключением комбинаций ПСМ и иНГЛТ-2 (ОШ 1,35 (95% ДИ 0,81–2,25)), ПСМ и ингибитора α-глюкозидазы (иАГ) (ОШ 1,16 (95% ДИ 0,55–2,44)).
При комбинации с ПСМ все ССП в отличие от плацебо улучшали контроль гликемии (снижение уровня HbA1c на 0,59–1,12%, глюкозы плазмы натощак на 0,68–2,37 ммоль/л). Сравнение эффективности препаратов второй линии терапии в сочетании с ПСМ выявило, что добавление арГПП-1 к монотерапии ПСМ способствует наибольшему уменьшению уровня HbA1c. Отмечено достоверно большее снижение значений HbA1c при применении арГПП-1 по сравнению с использованием иНГЛТ-2 (-0,47% (95% ДИ -0,85– -0,09)), иДПП-4 (-0,45% (95% ДИ -0,73– -0,16)) и иАГ (-0,53% (95% ДИ -0,91– -0,15)). Необходимо подчеркнуть, что данные об уровне HbA1c были доступны в отношении 8930 пациентов в 23 РКИ. При применении всех препаратов второго ряда в сочетании с ПСМ выявлено значительное снижение значений глюкозы плазмы натощак – -2,77 ммоль/л (95% ДИ -4,14–-1,40) для ТЗД и -0,62 ммоль/л (95% ДИ -0,78– -0,47) для иДПП-4.
Попарный анализ комбинированных схем терапии, содержащих ПСМ, показал наибольшее снижение массы тела при использовании комбинации ПСМ и иНГЛТ-2 по сравнению с плацебо (-1,00 кг (95% ДИ -1,73– -0,27)). Наибольшее увеличение массы тела отмечено при комбинации ПСМ и иДПП-4 по сравнению с плацебо (1,00 кг (95% ДИ 0,90–1,11)). При комбинации ПСМ с арГПП-1 снижение массы тела составилo 0,56 кг (95% ДИ -1,10– -0,02).
Исходя из результатов метаанализа, проведенного D. Qian и соавт., становится очевидным, что все ССП улучшают гликемический контроль при добавлении к ПСМ. Однако комбинация ПСМ с иНГЛТ-2 демонстрирует клинические преимущества в отношении риска развития гипогликемий и снижения массы тела. Комбинация «ПСМ + иНГЛТ-2» также является альтернативой для пациентов с СД 2 типа с непереносимостью метформина и неэффективностью монотерапии (рис. 4).
Преимущество комбинации гликлазида MВ с иНГЛТ-2 подтверждено при проведении субанализа результатов исследования DIA-RAMADAN, выполненном в подгруппе 102 пациентов, получавших гликлазид MВ в комбинации с иНГЛТ-2 (дапаглифлозин – 50%, эмпаглифлозин – 47%, канаглифлозин – 3%) и другими ССП или без них [51]. Важно отметить, что эти пациенты были моложе (средний возраст 51,4 ± 10,4 против 54,3 ± 10,4 года), имели большую длительность СД 2 типа (5,8 ± 4,5 против 5,4 ± 5,7 года), более высокий уровень HbA1c (7,7 ± 1,0 против 7,5 ± 0,9%) и больший спектр сопутствующих патологий (артериальная гипертензия – 58,8 против 33,7%, дислипидемия – 51,0 против 26,8%) по сравнению с теми, кто не получал такую комбинацию.
Приверженность комбинированной терапии гликлазидом МВ и иНГЛТ-2 составила 80% и более у 95,1% больных.
В исследовании было зафиксировано преимущество комбинации гликлазида MВ и иНГЛТ-2 по целому ряду позиций: низкая частота гипогликемических эпизодов, хорошая переносимость, улучшение контроля гликемии, снижение массы тела. Кроме того, согласно субанализу данных исследования DIA-RAMADAN, такое лечение может быть эффективным и безопасным в период соблюдения постов.
Заключение
Современные стратегии улучшения терапевтических результатов у пациентов с СД 2 типа ориентированы на достижение и долгосрочное удержание гликемического контроля с приоритетным использованием препаратов, доказавших положительное влияние на сердечно-сосудистый риск.
Применение ПСМ в качестве второй и третьей линии терапии СД 2 типа оправданно у большинства больных. Особое место среди препаратов данной группы занимает оригинальный гликлазид МВ (препарат Диабетон МВ®), что обусловлено не только его эффективностью, но и благоприятным профилем сердечно-сосудистой безопасности, нефропротективными эффектами. Препарат характеризуется низким риском развития гипогликемий и прибавки массы тела, что, несомненно, оказывает положительное влияние на качество жизни пациентов.
Более широкое использование гликлазида МВ в составе разных схем лечения СД 2 типа будет способствовать достижению поставленных терапевтических целей.
Конфликт интересов
Статья подготовлена при информационной поддержке компании «Сервье» (Франция).
Ye.V. Biryukova, MD, PhD, Prof.
Federal State Budgetary Educational Institution ‘Russian University of Medicine’ of the Ministry of Health of the Russian Federation
State Budgetary Healthcare Institution ‘A.S. Loginov Moscow Clinic Scientific Center’ Moscow Department of Health
Contact person: Yelena V. Biryukova, lena@obsudim.ru
The treatment of type 2 diabetes mellitus is an important task of modern medicine due to the inexorable spread of the disease.
The article discusses the possibilities of modern sugar-lowering pharmacotherapy. To increase its effectiveness, emphasized the need for prescribing drug combinations.
Despite changes in modern algorithms, sulfonylurea derivatives remain one of the most frequently prescribed for type 2 diabetes. Representatives of this group differ significantly from each other in structure, duration of action and pharmacological properties, which determines their therapeutic effects.
The original modified-release gliclazide (Diabeton MR®) has a number of advantages over other drugs from the group of sulfonylurea derivatives, including in terms of safety in various clinical situations. A combination of gliclazide MR and sodium-glucose cotransporter 2 inhibitors is considered a promising option.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.