Гозоглиптин – первый российский оригинальный ингибитор дипептидилпептидазы 4: эффективность, безопасность, новые показания
- Аннотация
- Статья
- Ссылки
- English
В статье рассматривается один из классов сахароснижающих препаратов – ингибиторы дипептидилпептидазы 4 (иДПП-4), а также их место в современных клинических рекомендациях. Особый акцент сделан на применении гозоглиптина – российского препарата из класса иДПП-4. Появление гозоглиптина на фармацевтическом рынке позволит повысить доступность лечения иДПП-4.
Эффективность и безопасность гозоглиптина оценивались в нескольких клинических рандомизированных исследованиях. Так, согласно результатам исследования SRX-1374-02, гозоглиптин является эффективным сахароснижающим препаратом из класса иДПП-4 и может быть рекомендован к применению у пациентов с СД 2 типа как в виде монотерапии, так и в виде комбинации с метформином. В исследовании SATER-0719 продемонстрировано, что гозоглиптин может быть назначен больным СД 2 типа в качестве дополнения к инсулину (с метформином или без метформина). Результаты исследования SATER-0819 позволяют рекомендовать данный препарат в комбинации с производными сульфонилмочевины для улучшения гликемического контроля у пациентов с СД 2 типа.
Кроме того, уже получены данные исследования реальной клинической практики ОНИКС и наблюдательной крупномасштабной программы ПАЛИТРА.
В статье рассматривается один из классов сахароснижающих препаратов – ингибиторы дипептидилпептидазы 4 (иДПП-4), а также их место в современных клинических рекомендациях. Особый акцент сделан на применении гозоглиптина – российского препарата из класса иДПП-4. Появление гозоглиптина на фармацевтическом рынке позволит повысить доступность лечения иДПП-4.
Эффективность и безопасность гозоглиптина оценивались в нескольких клинических рандомизированных исследованиях. Так, согласно результатам исследования SRX-1374-02, гозоглиптин является эффективным сахароснижающим препаратом из класса иДПП-4 и может быть рекомендован к применению у пациентов с СД 2 типа как в виде монотерапии, так и в виде комбинации с метформином. В исследовании SATER-0719 продемонстрировано, что гозоглиптин может быть назначен больным СД 2 типа в качестве дополнения к инсулину (с метформином или без метформина). Результаты исследования SATER-0819 позволяют рекомендовать данный препарат в комбинации с производными сульфонилмочевины для улучшения гликемического контроля у пациентов с СД 2 типа.
Кроме того, уже получены данные исследования реальной клинической практики ОНИКС и наблюдательной крупномасштабной программы ПАЛИТРА.








Вопросы эффективного и доступного лечения сахарного диабета (СД) 2 типа чрезвычайно актуальны в связи с эпидемическими темпами роста заболеваемости [1]. Согласно результатам масштабного российского эпидемиологического исследования NATION, СД 2 типа диагностируется лишь в 54% случаев, что составляет 5,4% населения, поэтому реальная численность пациентов может достигать 7,0%, то есть не менее 10 млн [2]. Оптимальный контроль гликемии способствует предупреждению или замедлению развития системных сосудистых осложнений (нефропатии, ретинопатии, поражений сосудов сердца, головного мозга, нижних конечностей), которые приводят к преждевременной инвалидизации, снижению качества жизни и смерти больных СД 2 типа [3–5].
Необходимость тщательного гликемического контроля опирается на обширную доказательную базу [6–8]. Однако проблемы, связанные с достижением должного метаболического контроля и развитием хронических осложнений СД, пока решить не удается. Так, согласно результатам метаанализа 24 исследований, проведенного K. Khunti и соавт., только 42,8% пациентов достигают целевого уровня глюкозы в крови [9].
В последнее время подходы к терапии СД 2 типа значительно изменились, что обусловлено активным развитием диабетологии как науки, расширением представлений о патофизиологии заболевания, а также разработкой новых сахароснижающих препаратов (ССП), что нашло отражение в современных клинических рекомендациях [10–13].
Многочисленные патогенетические механизмы СД 2 типа – основание для многосторонней фармакотерапии, направленной на коррекцию различных нарушений, что обеспечивает не только оптимальное снижение гликемии, но и долгосрочный гликемический контроль по мере прогрессирования заболевания. На сегодняшний день для лечения СД 2 типа используются различные по механизму действия, эффективности и переносимости ССП (рис. 1) [10, 11], что расширяет выбор наиболее оптимального препарата для каждого конкретного пациента.
Ингибиторы дипептидилпептидазы 4
Возможности и место в клинических рекомендациях
Ингибиторы дипептидилпептидазы 4 (иДПП-4), или глиптины, относятся к средствам с инкретиновой активностью [14–16]. Благодаря своим свойствам они успешно применяются при СД 2 типа как в виде моно-, так и в виде комбинированной терапии с другими ССП [10, 16, 17].
С учетом важной роли ДПП-4 в метаболизме глюкозы данный фермент рассматривается в качестве основной точки приложения иДПП-4. Подавление каталитической активности фермента замедляет деградацию эндогенных глюкагоноподобного пептида 1 (ГПП-1) и глюкозозависимого инсулинотропного полипептида и сохраняет их биологическую активность. Это пролонгирует взаимодействие ГПП-1 и глюкозозависимого инсулинотропного полипептида с собственными рецепторами, соответственно усиливаются описанные выше эффекты, а главное – нормализуется и поддерживается постпрандиальная секреция инсулина, уменьшается выработка глюкозы печенью за счет снижения секреции глюкагона [12, 18, 19].
Дипептидилпептидаза 4 относится к семейству серин-пептидаз, которое также включает ДПП-8, ДПП-9 и ДПП-2, белок активации фибробластов α (FAP-α). Высокая селективность иДПП-4 в отношении ДПП-4 рассматривается с точки зрения безопасности и минимизации риска развития побочных эффектов препаратов [14, 15, 18]. Молекула ДПП-4 существует в мембраносвязанной и растворимой формах, последняя циркулирует в плазме крови и образуется из мембраносвязанной формы. Сахароснижающий эффект иДПП-4 обусловлен воздействием на растворимую форму фермента. Мембраносвязанная форма ДПП-4 экспрессируется на поверхности многих клеток (эндотелия, почек, легких, дыхательных путей, Т-лимфоцитов, гладких мышц и др.). Воздействие на эту форму ДПП-4 обеспечивает плейотропные эффекты средств с инкретиновой активностью [18–20].
На сегодняшний день ДПП-4 также рассматривается в качестве адипокина, локального маркера метавоспаления и инсулинорезистентности, который может быть одним из связующих звеньев между накоплением массы жировой ткани и развитием ассоциированных с ожирением заболеваний. Ингибирование ДПП-4 способно предотвратить воспаление жировой ткани [21].
Кроме того, иДПП-4 могут воздействовать на ключевой дефект СД 2 типа – недостаточную секрецию инсулина β-клетками поджелудочной железы. При этом благодаря глюкозозависимому механизму действия обеспечивается высокая безопасность лечения, в том числе в отношении риска гипогликемий, который сводится к минимуму [14, 15, 22].
Важным также является воздействие иДПП-4 на дефект α-клеток посредством уменьшения гиперглюкагонемии. Данный эффект может быть обусловлен повышением секреции инсулина и соматостатина. Однако нельзя исключать и прямого влияния ГПП-1 на функцию α-клеток через собственные рецепторы [20, 22]. Описанный феномен также является глюкозозависимым [18].
К преимуществам иДПП-4 относится потенциальный протективный эффект в отношении β-клеток поджелудочной железы, что важно для поддержания инсулиносекреторного потенциала β-клеток и длительного сохранения контроля гликемии [15, 18, 23].
В настоящее время глиптины признаны эффективными и безопасными сахароснижающими средствами, поэтому входят в современные стандарты лечения СД 2 типа.
При инициации терапии и далее на любом из ее этапов необходимо оценивать характеристики пациента и выделять доминирующую клиническую проблему (высокий риск развития атеросклеротических сердечно-сосудистых заболеваний, их наличие, наличие хронической сердечной недостаточности, хронической болезни почек, ожирения и риска гипогликемий), учитывать наличие противопоказаний для назначения тех или иных ССП [10], поскольку индивидуальный подход является приоритетным при выборе тактики лечения. Необходимо отметить, что, согласно российским Алгоритмам специализированной медицинской помощи больным сахарным диабетом, использование иДПП-4 допускается на всех этапах лечения СД 2 типа как в виде монотерапии (при наличии непереносимости или противопоказаний к назначению метформина), так и в виде комбинированной терапии (в том числе с инсулином) в зависимости от исходного уровня гликированного гемоглобина (HbA1c) и клинического профиля пациента. В дебюте СД 2 типа комбинация метформина с иДПП-4 указывается как имеющая преимущества для долгосрочного гликемического контроля вследствие сохранения инсулинсекретирующего потенциала β-клеток [24]. В дебюте СД 2 типа у пациентов без атеросклеротических сердечно-сосудистых заболеваний, хронической сердечной недостаточности и хронической болезни почек раннее назначение такой комбинированной терапии может иметь преимущества в отношении долгосрочного удержания гликемического контроля даже при незначительном превышении целевого уровня HbA1c [10].
Ингибиторы ДПП-4 отличает удобство применения – пероральный прием независимо от приема пищи, умеренная эффективность – снижение уровня HbA1c на 0,5–1,0% и хорошая переносимость, сопоставимая с плацебо, в том числе у пациентов с нарушенной функцией почек и находящихся на гемодиализе [10, 15, 25]. Кроме того, применение иДПП-4 не сопровождается развитием нежелательных явлений (НЯ), свойственных другим классам ССП. Речь, в частности, идет об увеличении массы тела (тиазолидиндионы (ТЗД), производные сульфонилмочевины (ПСМ), меглитиниды, инсулин), риске развития гипогликемии (ПСМ, меглитиниды, инсулин), поражении органов желудочно-кишечного тракта (метформин, агонисты рецепторов ГПП-1 (арГПП-1)), риске развития урогенитальных инфекций (ингибиторы натрий-глюкозного котранспортера 2 (иНГЛТ-2)) [10, 20, 25, 26].
Перед врачами нередко встает вопрос выбора оптимального препарата внутри класса с целью обеспечения пациентов с СД 2 типа современным, эффективным, доступным и качественным лечением. На сегодняшний день в Российской Федерации зарегистрировано несколько иДПП-4: алоглиптин, вилдаглиптин, гемиглиптин, гозоглиптин, линаглиптин, саксаглиптин, ситаглиптин и эвоглиптин [10, 27–34].
Клиническая эффективность и безопасность
Эффективность и безопасность иДПП-4 как в виде монотерапии, так и в комбинации с другими ССП доказаны в рандомизированных контролируемых клинических исследованиях, метаанализах и подтверждены в условиях реальной клинической практики [16, 35–44].
Согласно данным A. Maloney и соавт., проанализировавших 229 рандомизированных клинических исследований с участием 121 914 пациентов, монотерапия иДПП-4 обеспечивала снижение уровня HbA1с в пределах 0,5–1,0% при низком риске гипогликемий, уступая по сахароснижающему эффекту метформину, ТЗД, иНГЛТ-2 и арГПП-1 [38]. При сравнении сахароснижающей эффективности ПСМ и иДПП-4 в краткосрочных исследованиях динамика снижения уровня HbA1c на фоне применения последних была менее выраженной, однако в длительных исследованиях продолжительностью 52 недели и более – схожей [16, 36, 41]. В крупном метаанализе сравнительной эффективности таких иДПП-4, как алоглиптин, линаглиптин, саксаглиптин, ситаглиптин и вилдаглиптин, P. Craddy и соавт. было продемонстрировано сопоставимое снижение уровня HbA1c (монотерапия – на 0,45–0,59%, комбинация с метформином – на 1,02–1,10%) при аналогичном риске развития гипогликемий [42].
Способность стимулировать секрецию инсулина без повышения риска развития гипогликемий и модулировать секрецию глюкагона является отличительной чертой иДПП-4. Вместе с тем для уменьшения риска развития гипогликемий при одновременном их применении с препаратами, потенциально увеличивающими такой риск (ПСМ и инсулин), рекомендуется снижение дозы последних.
Гозоглиптин
В 2016 г. российская компания «Сатерекс» зарегистрировала в Российской Федерации гозоглиптин (Сатерекс®), включенный в перечень жизненно необходимых и важнейших лекарственных препаратов. Применение инновационных технологий позволило локализовать весь цикл производства гозоглиптина на территории России, в том числе изготовление субстанции. Это имеет большое значение для развития российской фармакологии в области лечения СД 2 типа [45].
Отдельного внимания заслуживает ценовое преимущество гозоглиптина перед другими оригинальными иДПП-4, что повышает доступность данного вида лечения СД 2 типа [46].
Гозоглиптин – высокоселективный нековалентный иДПП-4, по химической структуре – дифторпирролидин.
Из организма гозоглиптин выводится преимущественно почками. Так, после приема около 77% дозы выводится почками, причем 48,5% – в неизмененном виде, 10,5% – через кишечник, при этом значительная доля приходится на метаболиты гозоглиптина [30].
Длительный период (около 20 часов) полувыведения препарата обеспечивает стойкое ингибирование ДПП-4 при приеме один раз в сутки.
В исследованиях in vitro с использованием микросомальных ферментов печени человека отмечались низкие константы связывания и ингибирования гозоглиптином цитохромов CYP1A2, CYP2C9, CYP2C19, CYP2D6 и CYP3A4. Поскольку обсуждаемый иДПП-4 не является субстратом микросомальных ферментов печени, а также не ингибирует и не индуцирует эти ферменты, то взаимодействие его с лекарственными средствами, которые являются субстратами, ингибиторами или индукторами микросомальных печеночных ферментов, маловероятно [30].
Эффективность и безопасность гозоглиптина подтверждены результатами клинических исследований, проведенных на территории России. Как следствие, гозоглиптин был включен в перечень жизненно необходимых и важнейших лекарственных препаратов, а также в клинические рекомендации по лечению СД 2 типа [47].
В 2013 и 2014 гг. было проведено многоцентровое (27 российских клинических центров) рандомизированное клиническое исследование III фазы SRX-1374-02 «Изучение эффективности и безопасности гозоглиптина в качестве монотерапии и в комбинации с метформином по сравнению с вилдаглиптином в качестве монотерапии и в комбинации с метформином у пациентов с СД 2 типа, ранее не получавших лекарственной терапии» [40]. Результаты данного исследования заслуживают особого внимания, поскольку прямые сравнительные исследования различных иДПП-4 проводятся довольно редко. В качестве препарата сравнения был выбран наиболее изученный и широко применяемый оригинальный препарат вилдаглиптина (Галвус®).
В процедуре скрининга приняли участие 506 пациентов с впервые выявленным СД 2 типа, из них 299 были рандомизированы в одну из двух групп фармакотерапии в соотношении 1:1. Первая группа получала гозоглиптин в дозе 20 или 30 мг/сут в виде монотерапии и в комбинации с метформином, вторая группа – вилдаглиптин в дозе 50 или 100 мг/сут в виде монотерапии и в комбинации с метформином. Обе группы были сопоставимы по исходным характеристикам.
Длительность монотерапии составила 12 недель (первый этап). По окончании указанного периода на основании результатов оценки углеводного обмена решался вопрос о добавлении к схеме лечения метформина. Длительность комбинированной терапии с метформином составила 24 недели (второй этап). Титрация доз исследуемых препаратов и добавление метформина проводились исходя из показателей гликемии.
Критерии включения в клиническое исследование:
- мужчины и женщины в возрасте от 18 до 78 лет включительно;
- подтвержденный диагноз СД 2 типа;
- пациенты, которые никогда не получали ССП или не получали их в течение по крайней мере 12 недель до скрининга и при этом никогда в прошлом не принимали какой-либо ССП более трех месяцев подряд;
- индекс массы тела (ИМТ) от 22 до 40 кг/м2;
- уровень HbA1c от 7,5 до 11,0% включительно;
- уровень глюкозы плазмы натощак (ГПН) менее 15 ммоль/л.
В качестве первичной конечной точкой эффективности выбрано изменение уровня HbA1c на 12-й и 36-й неделях по сравнению с исходным уровнем между группой гозоглиптина и группой вилдаглиптина. Вторичные оценки эффективности включали сравнение групп по таким показателям, как доля пациентов, достигших уровня HbA1c менее 7% через 12 и 36 недель, изменение концентрации ГПН и показателей постпрандиальной гликемии (ППГ) на 12-й и 36-й неделях по сравнению с исходным уровнем, а также изменение массы тела к 12-й и 36-й неделям по сравнению с исходной массой тела.
В ходе анализа результатов установлено, что по всем параметрам эффективности (первичным и вторичным конечным точкам) гозоглиптин не уступал вилдаглиптину при применении как в виде монотерапии, так и в комбинации с метформином.
На 12-й неделе в группе монотерапии гозоглиптином динамика уровня HbA1c относительно исходного уровня составила -0,93%, в группе монотерапии вилдаглиптином – -1,03% (разница между группами – 0,104% при 95%-ном доверительном интервале (ДИ) – 0,133–0,342). На 36-й неделе в группе комбинированной терапии гозоглиптином и метформином данный показатель отмечен на уровне -1,29%, а в группе комбинированной терапии вилдаглиптином и метформином – на уровне -1,35% (разница между группами – 0,057% (95% ДИ -0,187–0,300)) (рис. 2). В обоих случаях в отношении достижения основной конечной точки доказана не уступающая вилдаглиптину эффективность.
Важным показателем эффективности ССП, включая иДПП-4, применяемых как в виде монотерапии, так и в комбинации с другими ССП, является доля пациентов, достигших целевых значений HbA1c. Согласно результатам исследования SRX-1374-02, количество достигших целевого уровня HbA1c ≤ 7,0% статистически не различалось между группами на всех этапах исследования, в частности, на 12-й неделе таковых было 41,0 и 44,5% в группах гозоглиптина и вилдаглиптина соответственно (р = 0,52). Эффективной оказалась и комбинация иДПП-4 с метформином. В частности, к окончанию 36-недельного периода лечения 54,8% больных в группе гозоглиптина и метформина, а также 55,2% больных в группе вилдаглиптина и метформина достигли целевых показателей HbA1c (р = 0,74).
В обеих группах было зарегистрировано статистически значимое снижение уровней ГПН и ППГ. В отношении снижения указанных показателей эффективность гозоглиптина была сопоставима с эффективностью вилдаглиптина, получаемых как в режиме монотерапии, так и в режиме комбинированной терапии.
За период наблюдения в обеих группах отмечено сопоставимое незначительное снижение массы тела.
Группы не различались ни по одной из вторичных конечных точек (табл. 1) [40].
В ходе клинического исследования III фазы гозоглиптин продемонстрировал высокую безопасность и хорошую переносимость при проведении как моно-, так и комбинированной терапии. Доля пациентов с НЯ, зарегистрированными на фоне приема гозоглиптина, была сравнима с таковой на фоне приема вилдаглиптина. Все зарегистрированные в исследовании НЯ имели легкую или среднюю степень тяжести. Тяжелых НЯ отмечено не было.
Так, на фоне монотерапии гозоглиптином и вилдаглиптином развитие НЯ зафиксировано у 24,8 и 16,7% пациентов соответственно. На этапе комбинированной терапии НЯ отмечены у 23,8% пациентов в группе «гозоглиптин + метформин» и 26,3% пациентов в группе «вилдаглиптин + метформин».
По частоте эпизодов гипогликемий гозоглиптин продемонстрировал лучший результат, чем вилдаглиптин. Так, при проведении монотерапии количество пациентов с эпизодами гипогликемии в группе гозоглиптина составило 4,7%, в группе вилдаглиптина – 7,3% (р > 0,05). На фоне комбинированной терапии с метформином таковых было 4,1 и 10,5% соответственно (р = 0,065). Тяжелые гипогликемии в рамках исследования не были зафиксированы. Однако в группе вилдаглиптина в одном случае для устранения симптомов гипогликемии пациенту потребовалась посторонняя помощь [40].
На основании результатов клинического исследования III фазы SRX-1374-02 гозоглиптин (препарат Сатерекс®) был зарегистрирован в РФ для лечения пациентов с СД 2 типа по двум показаниям:
- в качестве монотерапии в случае неэффективности диетотерапии и физических упражнений у пациентов с противопоказаниями к применению метформина;
- в комбинации с метформином в качестве стартовой терапии или когда диетотерапия и физические упражнения в сочетании с монотерапией метформином или монотерапией гозоглиптином не приводят к адекватному гликемическому контролю.
Важно отметить, что в Алгоритмах специализированной медицинской помощи больным сахарным диабетом предложен вариант начальной интенсификации сахароснижающей терапии, при котором в дебюте СД 2 типа стало возможным назначение комбинации препаратов. Комбинация «метформин + иДПП-4» указана как имеющая определенные преимущества для долгосрочного контроля гликемии вследствие сохранения инсулинсекретирующей функции β-клеток, что приводит к снижению темпов прогрессирования СД 2 типа, а также потребности в интенсификации терапии [10, 24].
С 17 ноября 2022 г. по 4 октября 2023 г. в 19 клинических центрах России было проведено клиническое исследование IV фазы SATER-0719 «Сравнительное многоцентровое проспективное открытое рандомизированное контролируемое в параллельных группах исследование по изучению эффективности, безопасности и переносимости препарата гозоглиптин (Сатерекс®, ООО «Фармасинтез-Тюмень», Россия) по сравнению с препаратом ситаглиптин (Янувия®)» [48].
В данное исследование было отобрано 120 пациентов с СД 2 типа, отвечавших следующим критериям включения:
- уровень HbA1c, превышающий целевой показатель на 1,0–2,5% (индивидуализированный целевой показатель HbA1c определяли на основании Алгоритмов специализированной медицинской помощи больным сахарным диабетом 2021 г.);
- получение постоянной дозы базального инсулина и метформина на протяжении последних восьми недель и недостижение целевых показателей HbA1c.
В исследование SATER-0719 не включали пациентов с СД 1 типа, гестационным диабетом или другими типами диабета (вследствие нарушения функции поджелудочной железы, приема лекарственных или химических веществ), гиперчувствительностью/наличием противопоказаний к гозоглиптину, ситаглиптину и другим иДПП-4, а также к другим компонентам исследуемых препаратов, пациентов, лечившихся в последние три месяца тройной комбинацией ССП, пациентов с заболеваниями почек или сниженной функцией почек (при концентрации креатинина сыворотки ≥ 1,5 и ≥ 1,4 мг/дл у мужчин и женщин соответственно или клиренсе креатинина < 60 мл/мин), в том числе вследствие сердечно-сосудистого коллапса (шока), острого инфаркта миокарда или септицемии, с клинически выраженными проявлениями острых или хронических заболеваний, которые могут приводить к развитию тканевой гипоксии (в том числе хроническая сердечная недостаточность с нестабильными показателями гемодинамики, дыхательная недостаточность, острый инфаркт миокарда), тяжелыми нарушениями функции печени и почек.
Период наблюдения за пациентами составил 24 недели.
В исследовании тестировалась гипотеза не меньшей эффективности препарата гозоглиптин (Сатерекс® 30 мг, ООО «Фармасинтез-Тюмень», Россия) по сравнению с эффективностью ситаглиптина (Янувия® 100 мг) у пациентов с СД 2 типа на фоне применения метформина и базального инсулина. В качестве первичной конечной точки было выбрано относительное изменение уровня HbA1c по сравнению с исходным значением через 24 недели терапии.
Через 24 недели при оценке уровня HbA1c не было выявлено статистически значимых различий в динамике показателя между группами исследуемого препарата (гозоглипин) и препарата сравнения (ситаглиптин) (p = 0,314, t-критерий для независимых выборок, ДИ для разности средних – ноль) (табл. 2). Изменение уровня HbA1c через 24 недели лечения по сравнению с исходным уровнем составило -1,45 ± 1,40% в группе пациентов, принимавших гозоглиптин, и -1,21 ± 1,09% в группе пациентов, принимавших ситаглиптин.
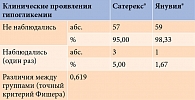
Анализ результатов показал, что 40,68% пациентов в группе гозоглиптина и 38,33% пациентов в группе ситаглиптина достигли целевого уровня HbA1c. Различия между группами оказались статистически незначимы (p = 0,794, критерий χ2 Пирсона) (табл. 3).
Между группой гозоглиптина и группой ситаглиптина не было выявлено статистически значимых различий в частоте возникновения гипогликемий (p = 0,619). Ни у одного из пациентов не было зафиксировано более одного случая клинических проявлений гликемии. Клинические проявления гипогликемии один раз за весь период исследования испытали три (5,00%) пациента в группе гозоглиптина и один (1,67%) пациент в группе ситаглиптина (табл. 4).
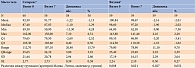
Динамика уровней ГПН и ППГ через 4, 12, 24 недели была следующей. При включении в исследование медиана уровня ГПН в группе гозоглиптина составила 8,30 [7,30; 9,75] ммоль/л, в группе ситаглиптина – 8,95 [7,50; 10,05] ммоль/л. Различия между группами оказались статистически незначимы (p = 0,324, критерий Манна – Уитни). Динамика уровня ГПН на протяжении 24 недель исследования представлена в табл. 5.
В ходе исследования уровень ГПН снижался. Так, при итоговом визите через 24 недели терапии медиана уровня ГПН в группе гозоглиптина составила 7,20 [6,10; 8,10] ммоль/л, в группе ситаглиптина – 7,90 [6,90; 8,90] ммоль/л. Различия между группами достигли статистической значимости (p = 0,043, критерий Манна – Уитни). На 24-й неделе медиана абсолютной динамики уровня ГПН в группе гозоглиптина составила -0,70 [-2,30; 0,40] ммоль/л, в группе ситаглиптина – -0,90 [-2,20; 0,40] ммоль/л. Различия между группами были статистически незначимы (p = 0,906, критерий Манна – Уитни).
Динамика уровня ППГ на протяжении 24 недель исследования представлена в табл. 6.
При включении в исследование медиана уровня ППГ в группе гозоглиптина составила 9,55 [8,45; 11,95] ммоль/л, через 24 недели – 8,10 [6,95; 9,35] ммоль/л, в группе ситаглиптина – 10,10 [8,95; 11,40] и 8,20 [7,20; 9,30] ммоль/л соответственно. Различия между группами были статистически незначимы (p = 0,634, критерий Манна – Уитни).
Медиана абсолютной динамики уровня ППГ при итоговом визите через 24 недели составила -1,45 [-3,85; 0,40] ммоль/л в группе гозоглиптина и -1,90 [-3,60; -0,50] ммоль/л в группе ситаглиптина. Различия между группами оказались статистически незначимы (p = 0,740, критерий Манна – Уитни).
В группах фармакотерапии отмечалось небольшое снижение массы тела по сравнению с исходным уровнем: в группе гозоглиптина – на 1,23 ± 1,86 кг, в группе ситаглиптина – на 1,64 ± 4,94 кг. Различия между группами оказались статистически незначимы (p = 0,553, t-критерий Стьюдента для совокупностей с неравными дисперсиями).
Статистический анализ продемонстрировал отсутствие значимых различий между сравниваемыми препаратами по основным НЯ, что позволило сделать вывод о схожем профиле безопасности гозоглиптина и ситаглиптина. В частности, НЯ были выявлены у 14 (23,33%) пациентов в группе гозоглиптина (всего 23 НЯ) и у 14 (23,33%) пациентов в группе ситаглиптина (всего 18 НЯ). Различия между сравниваемыми препаратами по частоте выявления НЯ также были статистически незначимы (p = 1,000).
Таким образом, клиническое исследование SATER-0719 предоставило доказательства не меньшей эффективности гозоглиптина (препарат Сатерекс®) по сравнению с эффективностью ситаглиптина, а также значимых различий по основным показателям безопасности, что указывает на схожий профиль безопасности исследуемого препарата и препарата сравнения.
На основе результатов данного клинического исследования Министерство здравоохранения РФ одобрило внесение в инструкцию по применению лекарственного препарата гозоглиптин (Сатерекс®) нового показания к применению: препарат Сатерекс® показан пациентам с СД 2 типа в качестве дополнения к инсулину (с метформином или без метформина) в тех случаях, когда диета, физические нагрузки и стабильная доза инсулина не приводят к адекватному гликемическому контролю.
Возможности применения гозоглиптина расширились благодаря результатам недавно завершившегося исследования SATER-0819 – cравнительного многоцентрового проспективного открытого рандомизированного контролируемого исследования в параллельных группах по оценке эффективности, безопасности и переносимости препарата гозоглиптин 30 мг (Сатерекс®, ООО «Фармасинтез-Тюмень», Россия) и препарата ситаглиптин 100 мг (Янувия®) у пациентов с СД 2 типа на фоне приема гликлазида [49]. Данное исследование было проведено в 17 клинических центрах России в период с 10 ноября 2022 г. по 16 сентября 2023 г.
В данное исследование было рандомизировано 120 пациентов, отвечавших следующим критериям:
- уровень HbA1c, превышающий целевой на 1,0–2,5%;
- непереносимость метформина;
- получение постоянной дозы гликлазида на протяжении последних 12 недель.
Период наблюдения в исследовании составил 24 недели.
В качестве первичной конечной точки было выбрано относительное изменение уровня HbA1c спустя 24 недели терапии. Вторичные критерии эффективности включали оценку доли пациентов, достигших целевого уровня HbA1c спустя 24 недели терапии, динамики уровня HbA1c спустя 12 недель терапии, количества случаев клинических проявлений гипогликемии в течение 24 недель терапии, динамики массы тела пациентов спустя 24 недели терапии, динамики уровней ГПН и ППГ через 4, 12, 24 недели.
В исследовании тестировалась гипотеза не меньшей клинической эффективности препарата гозоглиптин 30 мг (Сатерекс®, ООО «Фармасинтез-Тюмень», Россия) относительно референтного препарата ситаглиптин 100 мг (Янувия®) на фоне приема гликлазида.
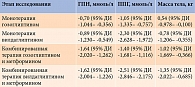
Через 24 недели относительное изменение уровня HbA1c составило -1,71 ± 1,00% в группе гозоглиптина и -1,24 ± 1,00% в группе ситаглиптина (табл. 7). Различия между группами достигли статистической значимости (p = 0,016).
Медиана абсолютной динамики уровня HbA1c при итоговом визите через 24 недели составила -1,70 [-2,10; -1,10]% в группе гозоглиптина и -1,10 [-1,70; -0,60]% в группе ситаглиптина, при этом различия между группами оказались статистически значимы (p = 0,003, критерий Манна – Уитни).
Целевого уровня HbA1c < 7,0% достигли 32 (55,17%) пациента в группе гозоглиптина и 21 (35,59%) пациент в группе ситаглиптина. Различия между группами были статистически значимы (p = 0,052, критерий χ2 Пирсона с поправкой Йейтса).
Оценка динамики уровней ГПН и ППГ через 4, 12, 24 недели показала следующее. Медиана уровня ГПН на исходном визите составила 8,35 [7,35; 9,90] ммоль/л в группе гозоглиптина и 8,50 [6,70; 10,10] ммоль/л в группе ситаглиптина, при этом различия между группами были статистически незначимы (p = 0,394, критерий Манна – Уитни) (табл. 8). Таковая на итоговом визите достигла 7,20 [6,50; 8,40] ммоль/л в группе гозоглиптина и 7,15 [6,10; 8,15] ммоль/л в группе ситаглиптина. Различия между группами были статистически незначимы (p = 0,758, критерий Манна – Уитни).
Медиана уровня ППГ на исходном визите составила 9,35 [8,30; 11,25] ммоль/л в группе гозоглиптина и 9,45 [7,40; 11,10] ммоль/л в группе ситаглиптина. При этом различия между группами оказались статистически незначимы (p = 0,520, критерий Манна – Уитни). Через 24 недели медиана уровня ППГ достигла 7,90 [6,70; 9,10] ммоль/л в группе гозоглиптина и 7,60 [6,50; 9,10] ммоль/л в группе ситаглиптина. Различия между группами были статистически незначимы (p = 0,806, критерий Манна – Уитни).
За период наблюдения ни у одного пациента с СД 2 типа не было зафиксировано более одного случая симптоматической гипогликемии. По одному случаю симптоматической гипогликемии отмечено у трех (5,00%) пациентов, получавших гозоглиптин. Различия между группами были статистически незначимы (p = 0,244, точный критерий Фишера).
Исходно масса тела в группе ситаглиптина была достоверно больше, чем в группе гозоглиптина, – 98,60 [89,10; 114,50] против 87,40 [79,65; 105,30] кг (p = 0,008, критерий Манна – Уитни). Медиана массы тела через 24 недели в группе гозоглиптина составила 87,85 [79,50; 103,60] кг, в группе ситаглиптина – 97,20 [86,90; 110,30] кг. Различия между группами оказались статистически значимы (p = 0,021, критерий Манна – Уитни) (табл. 9).
За весь период наблюдения в исследовании SATER-0819 зарегистрированы 28 НЯ, из них одно (1,67%) серьезное в группе гозоглиптина. НЯ были выявлены у 12 (20,00%) пациентов в группе гозоглиптина (всего 14 НЯ) и у 9 (15,25%) пациентов в группе ситаглиптина (всего 14 НЯ). Различия между препаратами по частоте выявления НЯ оказались статистически незначимы (p = 0,661, критерий χ2 Пирсона с поправкой Йейтса).
Таким образом, проведенное исследование позволило констатировать не меньшую эффективность препарата гозоглиптин (Сатерекс®, ООО «Фармасинтез-Тюмень», Россия), чем эффективность препарата ситаглиптин.
Статистический анализа показал отсутствие значимых различий между сравниваемыми группами по основным показателям безопасности. В целом профили безопасности исследуемого препарата и препарата сравнения оказались схожими.
На основании результатов исследования IV фазы SATER-0819 стало возможным внесение дополнительного показания в инструкцию по медицинскому применению препарата гозоглиптин (Сатерекс®), согласно которому он рекомендуется пациентам с СД 2 типа для улучшения гликемического контроля в комбинации с ПСМ.
В 2024 г. на основании результатов двух клинических исследований IV фазы SATER-0819 и SATER-0719 в инструкцию по применению лекарственного препарата Сатерекс® (гозоглиптин) были внесены два новых показания [30]:
для улучшения гликемического контроля в комбинации с производными сульфонилмочевины, когда диета или физические нагрузки в сочетании с монотерапией производными сульфонилмочевины не приводят к адекватному гликемическому контролю;
в качестве дополнения к инсулину (с метформином или без метформина) в тех случаях, когда диета, физические нагрузки и стабильная доза инсулина не приводят к адекватному гликемическому контролю.
Доказательная база успешного применения первого отечественного оригинального иДПП-4 – препарата гозоглиптин увеличивается и благодаря исследованиям в условиях реальной клинической практики. Так, в наблюдательное исследование ОНИКС был включен 1231 пациент с СД 2 типа, не достигший целевых показателей на фоне текущей терапии метформином [43]. В соответствии с инструкцией по медицинскому применению в данной популяции гозоглиптин был назначен в дозе 30 мг. Исследование проводилось в 39 лечебных учреждениях в 20 городах РФ. Возраст участников варьировался от 30 до 84 лет, при этом средний возраст составлял 56,5 года.
У всех участников исследования имел место СД 2 типа со средней продолжительностью восемь лет с момента установления диагноза. Большинство пациентов на момент включения в исследование получали стандартную пероральную терапию метформином в дозе, не превышающей 3000 мг/сут.
Длительность наблюдения в исследовании ОНИКС составила шесть месяцев.
В исследовании оценивали основные показатели гликемического профиля, достижение целевой гликемии и количество гипогликемий.
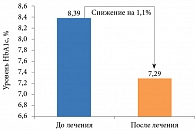
К шестому месяцу терапии отмечено улучшение гликемического контроля в целом: показатель ГПН снизился на 1,63 ммоль/л, ППГ – на 2,68 ммоль/л, HbA1c – на 1,1% (рис. 3).
Результаты исследования ОНИКС подтвердили высокую клиническую эффективность гозоглиптина (препарата Сатерекс®) у пациентов с СД 2 типа, которые до участия в исследовании получали только монотерапию метформином (рис. 4).
В феврале 2020 г. Независимый междисциплинарный комитет по этической экспертизе клинических исследований одобрил протокол наблюдательной программы ПАЛИТРА по оценке удовлетворенности и приверженности лечению пациентов с СД 2 типа, в которой приняли участие 328 врачей из 54 городов РФ. Набор пациентов в наблюдательную программу ПАЛИТРА осуществлялся в период с 28 февраля 2020 г. по 31 марта 2022 г. [50].
Для участия в программе ПАЛИТРА отбирали пациентов обоего пола с установленным диагнозом СД 2 типа в возрасте от 18 до 65 лет включительно и уровнем HbA1c выше индивидуального целевого на 0,5–2,5%, которым в рамках повседневной практики была назначена следующая сахароснижающая терапия: метформин или гозоглиптин либо комбинация этих двух препаратов.
Критериями невключения были наличие СД 1 типа, гестационного СД, других типов диабета, гиперчувствительность/наличие противопоказаний к метформину, гозоглиптину, лечение инсулином, наличие в анамнезе атеросклеротических сердечно-сосудистых заболеваний (инфаркт миокарда, инсульт, стентирование/шунтирование, ишемическая диабетическая стопа, гангрена, реваскуляризация нижних конечностей).
Деперсонифицированные данные собирали у пациентов на трех визитах: исходно, через три и шесть месяцев лечения (визит 2 и визит 3 соответственно), включая оценку антропометрических показателей (масса тела, ИМТ, артериальное давление, частота сердечных сокращений), биохимических показателей (аланинаминотрансфераза, аспартатаминотрансфераза и креатинин плазмы крови) и доступных для анализа показателей углеводного обмена (ГПН, ППГ и HbA1с) после инициации терапии метформином, гозоглиптином или их комбинацией. Приверженность получаемой терапии и удовлетворенность лечением пациентом и врачом определяли с помощью пятибалльной шкалы Лайкерта.
Оценка безопасности лечения проводилась посредством регистрации гипогликемии и любых НЯ в течение всего периода исследования.
Всего в наблюдательную программу ПАЛИТРА был включен 5741 пациент. Количество получавших монотерапию метформином составило 4,37% (n = 245), гозоглиптином – 16,91% (n = 971), комбинированную терапию – 78,71% (n = 4519).
У 25,0% пациентов СД 2 типа был выявлен впервые, у 32,5% больных длительность заболевания превышала один год, у 27,7% – более двух лет, у 13,7% – более пяти лет. При включении в наблюдательную программу ПАЛИТРА 82% пациентов получали различную сахароснижающую терапию: 60,2% – метформин, 14,5% – метформин пролонгированного действия, 24,1% – ПСМ, 7,6% – иДПП-4, 3,7% – иНГЛТ-2. Большинство (64,4%) пациентов получали монотерапию, меньшинство (17,6%) – комбинированную терапию.
Большая часть пациентов с СД 2 типа, включенных в исследование, имели различные сопутствующие заболевания. Ожирение выявлено у 66,5% больных, артериальная гипертензия – у 70,0%, заболевания органов зрения – у 26,0%. Следует отметить, что лица с высоким риском развития атеросклеротических сердечно-сосудистых заболеваний (возраст более 55 лет с наличием 50%-ного стеноза коронарных, каротидных артерий или артерий нижних конечностей либо гипертрофии левого желудочка) или наличием таковых не включались в исследование.
Рекомендации по питанию соблюдали 47,5% пациентов. В рутинной практике в отсутствие контроля гликемии наряду с добавлением дополнительного ССП часто применяется переключение с одного препарата на другой. В данном исследовании перевод пациентов осуществлялся на метформин (Мерифатин®) и гозоглиптин (Сатерекс®) в эквивалентных дозах.
Группы лечения были сопоставимы по полу, возрасту, росту, весу, ИМТ, сопутствующим заболеваниям, исходным уровням HbA1c, ГПН и ППГ.
Среднее значение ИМТ на момент включения в программу ПАЛИТРА составляло 31,3 ± 5,5 кг/м2, в большинстве случаев ИМТ соответствовал избыточной массе тела или ожирению.
Средний уровень артериального давления при включении в программу ПАЛИТРА достигал 133,8/82,4 мм рт. ст.
У большинства пациентов до включения в программу ПАЛИТРА имел место неудовлетворительный контроль гликемии, определяемый по уровням ГПН, ППГ и HbA1c. У 97,55% пациентов средний исходный уровень HbA1c находился в диапазоне от 7,0 до 9,5%.
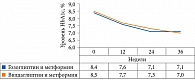
В ходе лечения отмечены положительные изменения всех показателей углеводного обмена – ГПН, ППГ и HbA1c, свидетельствующие об эффективности проводимой сахароснижающей терапии. Так, через три месяца в группе, получавшей терапию метформином, уровень ГПН снизился с 8,0 ± 1,2 до 7,0 ± 0,7 ммоль/л, в группе, получавшей терапию гозоглиптином, – с 8,4 ± 1,8 до 7,3 ± 0,9 ммоль/л, а в группе, получавшей комбинированную терапию этими препаратами, – с 8,2 ± 1,3 до 7,1 ± 0,8 ммоль/л. Дальнейшее снижение уровня ГПН было зафиксировано через 24 недели наблюдения. В частности, в группе монотерапии метформином уровень ГПН достиг 6,9 ± 4,2 ммоль/л, в группе монотерапии гозоглиптином – 6,8 ± 0,7 ммоль/л, в группе комбинированной терапии – 6,7 ± 2,3 ммоль/л.
Через три и шесть месяцев (на визитах 2 и 3) уровень ППГ в группе, получавшей метформин, снизился до 8,5 ± 0,9 и 7,9 ± 0,9 ммоль/л соответственно, в группе, получавшей гозоглиптин, – до 8,8 ± 1,4 и 8,0 ± 1,1 ммоль/л соответственно, а в группе, получавшей комбинированную терапию, – до 8,6 ± 1,1 и 8,0 ± 1,0 ммоль/л соответственно.
Уровень HbA1c к 24-й неделе уменьшился на 1,03% в группе монотерапии метформином и на 0,95% в группах монотерапии гозоглиптином и комбинированной терапии метформином и гозоглиптином.
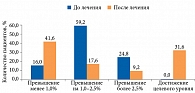
К концу исследования 49,6% пациентов с СД 2 типа достигли целевого уровня HbA1c 7,0%. Доля пациентов с уровнем HbA1c < 7,0% составила 61,0% в группе, принимавшей метформин, 47,75 и 47,20% в группах, получавших гозоглиптин и двойную комбинацию метформин/гозоглиптин соответственно (рис. 5).
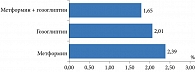
Частота гипогликемических эпизодов была очень низкой на протяжении 24 недель наблюдения. На итоговом визите гипогликемии зарегистрированы у 2,67% пациентов, из них в группе метформина – у 2,39%, в группе гозоглиптина – у 2,01%, в группе комбинированной терапии – у 1,65% пациентов (рис. 6).
Результаты масштабной программы ПАЛИТРА продемонстрировали, как в реальной клинической практике можно достичь эффективного и безопасного контроля уровня глюкозы в крови у пациентов с СД 2 типа при помощи доступных ССП. Это особенно важно в условиях ограниченности ресурсов и разнообразия потребностей пациентов. Полученные данные показали, что правильный подбор ССП с учетом индивидуальных особенностей пациента, включая возраст, сопутствующие заболевания, образ жизни и уровень мотивации, позволяет добиться значительного улучшения контроля гликемии.
Существенными преимуществами гозоглиптина являются удобство применения (прием один раз в сутки), сахароснижающая эффективность, нейтральное влияние на массу тела, низкая частота гипогликемий, хороший профиль безопасности и переносимости и невысокая стоимость по сравнению с другими иДПП-4.
Из-за отсутствия данных о безопасности применение гозоглиптина во время беременности противопоказано.
Гозоглиптин рекомендован при хронической болезни почек С1–3а.
Опыт применения гозоглиптина у пациентов с тяжелой печеночной недостаточностью (уровень аланинаминотрансферазы или аспартатаминотрансферазы более чем в 2,5 раза выше верхней границы нормы) ограничен, поэтому его использование в этой популяции не рекомендовано.
У пожилых пациентов коррекция дозы гозоглиптина не требуется [30].
Заключение
Благодаря разработке современных ССП открываются новые возможности для улучшения гликемического контроля у пациентов с СД 2 типа и снижения риска развития диабетических осложнений.
Ингибиторы ДПП-4 – эффективные и безопасные ССП, которые включены в современные стандарты лечения пациентов с СД 2 типа.
Результаты исследований показали, что российский иДПП-4 гозоглиптин является эффективным и безопасным ССП. Он может быть рекомендован к применению пациентами с СД 2 типа как в виде монотерапии, так и в комбинации с метформином, ПСМ и инсулином (с метформином или без метформина).
Ye.V. Biryukova, MD, PhD, Prof., Yu.A. Shishkova, PhD
Russian University of Medicine
Contact person: Yelena V. Biryukova, lena@obsudim.ru
Currently, treatment options for patients with diabetes mellitus (DM) type 2 have significantly expanded due to the continuous development of diabetology as a science and, in particular, due to more deep understanding of the disease pathophysiology.
The article analyzes one of hypoglycemic preparations – dipeptidyl peptidase 4 inhibitors (DPIs), as well as their place in modern clinical guidelines. A particular attention is paid to gosogliptin – the first Russian preparation of DPI-4 class. Gosogliptin at the pharmaceutical market will improve DPI-4 availability for DM patients.
Gosogliptin efficacy and safety were assessed in several randomized clinical trials. Thus, findings of SRX-1374-02 trial have demonstrated that Gosogliptin is an effective hypoglycemic drug of DPP-4 inhibitor class, and it can be recommended for patients with DM type 2 both as monotherapy and in combination with Metformin. SATER-0719 trial has shown that Gosogliptin can be prescribed to patients with DM type 2 as an addition to insulin (with or without Metformin). SATER-0819 trial fidnings allow to recommend this drug in combination with sulfonylurea derivatives to improve glycemic control in patients with DM type 2.
Besides, data from the real-life clinical practice trial ONIX and the large-scale observational PALITRA program have already been obtained.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.