Первичный билиарный холангит и неполный ответ на терапию урсодезоксихолиевой кислотой: кто виноват и что делать?
- Аннотация
- Статья
- Ссылки
- English



Введение
Первичный билиарный холангит (ПБХ) – редкое хроническое холестатическое заболевание печени аутоимммунного характера, для которого характерно наличие специфических антимитохондриальных антител (АМА-М2) [1–3]. Гистологически ПБХ представлен деструктивным холангитом с поражением внутридольковых и септальных желчных протоков [4, 5]. Распространенность ПБХ колеблется в пределах от 19 до 35 на 100 тыс. населения. Как и большинство заболеваний аутоиммунной природы, ПБХ наиболее распространен среди пациентов женского пола в постменопаузальном периоде [6]. В 30% случаев ПБХ сочетается с другими аутоиммунными заболеваниями: ревматоидным артритом, аутоиммунным тиреоидитом, системной склеродермией, синдромом Рейно, синдромом Шегрена, фиброзирующим альвеолитом, системной красной волчанкой. Точный механизм развития заболевания неизвестен. Есть предположение, что под действием факторов внешней среды (курение, инфекционные агенты, гормональные препараты, ксенобиотики) у генетически предрасположенных пациентов развивается аутоиммунная атака, направленная на билиарные эпителиальные клетки в процессе нарушения толерантности [4, 5, 7]. ПБХ отличается вялотекущим и длительным бессимптомным течением. При наличии уже существенных изменений структуры печени у 50–60% пациентов не наблюдается выраженных симптомов заболевания на момент постановки диагноза [7, 8].
Наиболее распространенным симптомом при ПБХ (50%) является астенический (повышенная усталость, утомляемость, выраженная слабость). Зуд, особенно выраженный в ночное время или после контакта с шерстью, местного или генерализованного характера проявляется у четверти больных с ПБХ. Желтуха является поздним маркером ПБХ и возникает, как правило, через шесть месяцев – два года с момента появления кожного зуда [7, 9, 10].
Внедрение в практику урсодезоксихолиевой кислоты (УДХК) значительно повлияло на продолжительность жизни больных с ПБХ. УДХК на сегодняшний день является препаратом первой линии для лечения пациентов с ПБХ с доказанным клиническим эффектом. Препарат назначается в дозе 13–15 мг/кг в сутки (уровень доказательств – I, сила рекомендаций – 1) на длительный период. Разработан целый ряд критериев оптимального ответа на терапию УДХК [11]. Наиболее широко используются Барселонские и Парижские критерии I и II, а также ряд других, но в меньшей степени [12]. Если активность щелочной фосфатазы снижается более чем на 40% или нормализуется в течение года (Барселонские критерии), вероятность выживаемости без трансплантации печени в течение 14 лет составляет 95%. На ранних стадиях болезни на фоне приема УДХК необходимость в трансплантации печени возникает у 6% пациентов, а через 20 лет – у 22%. У лиц с третьей-четвертой стадиями ПБХ относительный риск развития декомпенсации печени составляет 2,2 [11].
В реальной клинической практике нередко наблюдается неполный ответ на проводимую терапию препаратами УДХК, около 1/3 пациентов не отвечают на терапию адекватно. По данным современного анализа международных регистров, 10-летняя выживаемость у получавших УДХК больных близка к 80% [12]. Согласно результатам статистических исследований, около 45% пациентов оказываются резистентными к терапии УДХК [11]. До сих пор не выявлено точных причин резистентности, но известно, что значимыми прогностическими факторами недостаточного биохимического ответа на терапию являются относительно молодой возраст (< 45 лет) и далекозашедшая стадия заболевания к моменту постановки диагноза. Однако единого алгоритма и понимания развития резистентности к УДХК не разработано.
Цель – оценка распространенности неполного ответа на УДХК и определение ассоциированных с ним факторов риска.
Материал и методы
Исследование носило наблюдательный когортно-ретропроспективный характер. Было проанализировано 250 историй болезни пациентов (n = 59 – ретроспективно и n = 191 – проспективно) с вероятным диагнозом ПБХ, окончательно в исследование было включено 167 пациентов с верифицированным диагнозом ПБХ, находившихся на лечении в отделении заболеваний печени МКНЦ им. А.С. Логинова с 2017 по 2019 г. В данное исследование были включены только взрослые пациенты (возраст ≥ 18 лет). Извлечение данных включало пациентов, зарегистрированных в период с момента создания базы данных (октябрь 2018 – март 2019 г.).
Собранные данные включали диагноз, историю болезни, стадию заболевания печени, сопутствующие, в том числе иммуноассоциированные, заболевания.
Пациентам были проведены лабораторные исследования, УЗИ органов брюшной полости, МРТ-холангиография (по показаниям), эластометрия печени, пункционная биопсия печени (по показаниям). Помимо стандартных лабораторных исследований, было проведено иммунологическое обследование на аутоантитела (АМА-М2, ANA-HEP2, gp210, sp100).
Основные конечные точки включали в себя оценку ответа на лечение УДХК и оценку исходных характеристик пациентов, связанных с неполным ответом на терапию. Ответ на терапию УДХК оценивали через 12 месяцев после начала лечения в соответствии с Парижскими критериями II: уровни щелочной фосфатазы (ЩФ), аспартатаминотрансферазы (АСТ) не должны превышать 1,5 верхней границы нормы и уровень общего билирубина > 1 мг/дл.
От каждого пациента было получено письменное информированное согласие на включение в базу данных.
На первом этапе пациенты были поделены на две группы: ответивших на терапию и группу с неполным ответом на лечение УДХК. Оценку неэффективности терапии УДХК проводили по Парижским критериям II.
На втором этапе выявляли факторы риска неоптимального ответа у пациентов с ПБХ. Эти факторы были условно поделены на два вида: модифицируемые (поздняя диагностика, низкая комплаентность, неадекватная дозировка) и немодифицируемые, к которым относились пациенты с ПБХ и признаками аутоиммунного гепатита и пациенты, у которых, несмотря на своевременную диагностику и правильный прием УДХК, не был получен полный ответ на терапию. В рамках исследования была определена часть пациентов с недостаточной дозой УДХК согласно весу (13–15 мг/кг/сут), которая впоследствии была изменена.
Сравнение двух групп по количественным шкалам проводили на основе непараметрического критерия Манна – Уитни. Сравнение трех и более групп по количественным шкалам проводили на основе непараметрического критерия Краскела – Уоллеса. Для описания количественных показателей использовали среднее значение и стандартное отклонение M ± S, 95%-ный доверительный интервал для отношения (95% ДИ), достоверными считались различия р < 0,05.
Результаты исследования
В исследование было включено 167 человек, средний возраст которых составлял 63,57 ± 10,39 года, в основном женщины (n = 154, 92%). Клинические и лабораторные характеристики пациентов с ПБХ представлены в табл. 1.
Анализ данных ответа на терапию пациентов показал, что оптимальный ответ отмечается лишь у 23% (n = 36) пациентов, в 77% случаев (n = 131) ответа на терапию не было (рис. 1 и табл. 2).
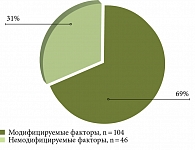
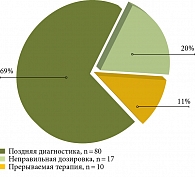
Анализ возможных причин неоптимального ответа на лечение УДХК позволил выделить две группы факторов, ассоциированных с неоптимальным ответом на лечение УДХК, которые условно были разделены на модифицируемые и немодифицируемые (рис. 2). Среди модифицируемых факторов поздняя диагностика составила 69% (n = 80), в 20% (n = 17) случаев пациенты получали дозировку без учета массы тела. Также была отмечена низкая приверженность к лечению – в 11% случаев (n = 10) (рис. 3).
Истинные неответчики (пациенты со своевременно установленным диагнозом, адекватной дозой УДХК, высокой комплаентностью и тем не менее с сохранением устойчивой резистентности к УДХК) составили 30% случаев (n = 11). В группе пациентов с неоптимальным ответом отмечено, что среди мужчин (n = 13) неадекватный ответ на терапию УДХК отмечается в 93,3% (n = 12), у женщин данный показатель ниже – 67,3% (n = 105). Ввиду длительного бессимптомного течения у мужчин отмечены очень высокая частота поздней диагностики (n = 11, 81,2%) и высокая распространенность неблагоприятного течения (n = 10, 80,1%). Подавляющее число пациентов с неполным ответом на лечение УДХК отмечено в группе лиц до 60 лет – 74% (n = 78), что привело, соответственно, к высокой частоте неблагоприятного течения (88%).
Особого внимания среди исследуемых пациентов заслуживают пациенты с ПБХ и признаками аутоиммунного гепатита, которые в данном исследовании составили 11,2% (n = 16) от общей группы обследуемых: женщины – 87,5% (n = 14), мужчины – 12,5% (n = 2). Это категории «трудных» пациентов, с немодифицируемыми факторами неоптимального ответа на комбинированную терапию.
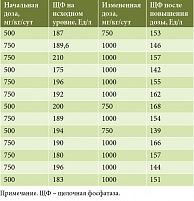
Согласно клиническим данным, частичный ответ на терапию УДХК является независимым предиктором неблагоприятного течения заболевания [13]. Пациент, не отвечающий полностью хотя бы на один показатель по Парижским критериям II, может считаться частичным ответчиком. В результате исследования выявлено 14 пациентов с неоптимальным ответом на терапию, составивших отдельную подгруппу (13 женщин и один мужчина). Большинство пациентов были младше 60 лет (n = 10), средний показатель ЩФ в этой группе больных составлял 193 ед/ммоль/л. В 86% случаев это были АМА-М2-позитивные пациенты. Все пациенты этой группы получали УДХК в стандартной дозе 750 мг без учета массы тела. Всем пациентам этой подгруппы была скорректирована суточная доза УДХК из расчета 15 мг/кг/сут. В течение 6–12 месяцев был отмечен полный ответ на терапию (табл. 3).
Заключение
Первичный билиарный холангит еще в 90-х годах прошлого века представлял для клиницистов неразрешимую задачу. Продолжительность жизни составляла около восьми лет с момента постановки диагноза. Внедрение в практику УДХК кардинально изменило ситуацию – возросла продолжительность и улучшилось качество жизни пациентов с ПБХ. Однако было показано, в том числе и в нашем исследовании, что неоптимальный ответ среди пациентов с ПБХ, вынужденных длительно принимать этот препарат, встречается достаточно часто. Десятилетняя выживаемость у пациентов с неоптимальным ответом на УДХК, по данным ряда авторов, составляет 20% [12]. При неполном ответе на терапию УДХК отмечается более высокая частота осложнений в течение 10 лет: 37,4% по сравнению с 3,2% в группе полного ответа [13].
Наше исследование демонстрирует, что при неоптимальном ответе на лечение УДХК в 69% случаев ситуацию можно изменить благодаря прежде всего адекватному подбору дозы УДХК с учетом массы тела, работе с пациентами, направленной на достижение полной комплаентности, недопустимости прерывания терапии при нормализации биохимических и клинических показателей.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов, финансовой поддержки, грантов и благодарностей.
K.G. Absandze, E.V. Vinnitskaya, PhD, Yu.G. Sandler, PhD, T.Yu. Khaimenova, PhD, D.S. Filina, K.G. Sаliyev
A.S. Loginov Moscow Clinical Scientific Centery
Contact person: Julia G. Sandler, sandlerjulia2012@gmail.com
Ursodeoxycholic acid (UDCA) is a first-line drug for the treatment of all patients with primary biliary cholangitis (PBC). The biochemical response to UDCA therapy is recommended to be evaluated 12 months after the start of treatment to determine the patient's response to therapy. In clinical practice, patients who do not respond sufficiently to therapy with UDCA drugs are often observed. It is known that an incomplete response ultimately correlates with the progression of the disease. The article presents the results of our own research, which studied the factors leading to an incomplete response of patients to UDCA therapy. Analysis of possible causes of incomplete response allowed us to identify two groups of factors associated with a suboptimal response to treatment of UDCA, which were conditionally divided into modifiable and unmodifiable. Significant prognostic factors of insufficient/incomplete response to therapy were identified, as well as categories of "difficult" patients with unmodifiable incomplete response factors. The results obtained make it possible to personalize approaches to the therapy of patients with PBC, reduce the risks of their incomplete response and optimize treatment.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.