количество статей
7376
Загрузка...
Пожалуйста, авторизуйтесь:
Практика
Подходы к терапии аллергического контактного дерматита
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Дерматовенерология и дерматокосметология" № 1
- Аннотация
- Статья
- Ссылки
Одним из наиболее распространенных заболеваний кожи является аллергический контактный дерматит, который диагностируется у 4–7% пациентов, обращающихся в дерматологические лечебные учреждения [1]. Частота заболеваемости аллергическим контактным дерматитом значительно выше в индустриально развитых странах, где отмечается высокая концентрация аллергенов в окружающей среде. Чаще заболевание встречается у женщин 20–40 лет, с возрастом риск его возникновения уменьшается [2]. Аллергический контактный дерматит является иммунологической реакцией замедленного типа и развивается у лиц с наследственной предрасположенностью в результате сенсибилизации преимущественно к низкомолекулярным химическим соединениям.

Таблица 1. Основные вещества, вызывающие контактный дерматит

Таблица 2. Классы кортикостероидов в зависимости от химической структуры
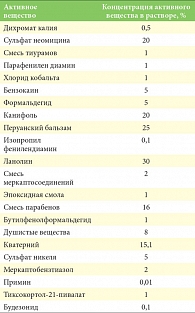
Таблица 3. Аллергены в европейских стандартизированных тест-наборах

Таблица 4. Факторы, провоцирующие развитие аллергического контактного дерматита
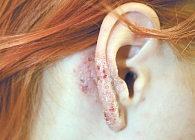
Фото 1. Аллергический контактный дерматит
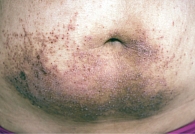
Фото 2. Аллергический контактный дерматит
Список веществ, способных вызывать аллергический контактный дерматит, постоянно расширяется, в настоящее время известно более 3000 таких веществ и соединений [3]. Заболевание чаще всего развивается при контакте с металлами и их солями, растениями, составами, содержащими каучук, медикаментами (табл. 1). Для разных регионов планеты характерны определенные аллергены, вызывающие аллергический контактный дерматит. Наиболее распространенный бытовой аллерген во всем мире – никель, входящий в состав покрытия часов, молний, украшений, пуговиц, пряжек, оправы очков и пр. [4]. Положительные кожные пробы на сульфат никеля отмечаются у 16,7% больных аллергическим контактным дерматитом [5]. Значительную роль в развитии аллергического контактного дерматита играют вещества-компоненты средств декоративной косметики (ланолин, душистые вещества, кватерний-15, парафенилдиамин, канифоль, перуанский бальзам и пр.) [6–8]. Как правило, аллергические реакции развиваются после контакта со средствами для обесцвечивания волос, красками для волос, лаком для ногтей, пудрой, губной помадой, сухими духами и др. Положительные реакции на перуанский бальзам, душистые вещества, кватерний-15 отмечаются у 11,6%, 10,4% и 9,3% больных аллергическим контактным дерматитом соответственно. Нередко заболевание провоцируется моющими и стиральными веществами, шампунями, косметическими препаратами, в состав которых входит формальдегид [5]. У 10,2% больных аллергическим контактным дерматитом выявляется положительная реакция на тимеросал (смесь тиосалициловой и этилмеркуровой кислоты), который используют как консервант в вакцинах, растворах для контактных линз, антисептиках и косметических продуктах [5, 9, 10]. В список основных аллергенов, выделенных Североамериканской группой по изучению контактного дерматита, включены два лекарственных средства – антибиотики для наружного применения неомицина сульфат и бацитрацин. Чаще всего они используются в комбинации друг с другом и топическими стероидами в кремах для офтальмологического применения, антибактериальных мазях. Положительные пробы на неомицина сульфат и бацитрацин отмечены у 11,6 и 7,9% больных аллергическим контактным дерматитом соответственно, описаны случаи развития анафилаксии и крапивницы [11–13]. При развитии профессионального аллергического контактного дерматита чаще всего выявляется сенсибилизация к соединениям хрома, никеля, кобальта, углеводородов нефти, каменного угля, синтетическим смолам, лекарственным веществам, формальдегиду, формалинсодержащим полимерам, кислотам, щелочам и пр. [1, 5].
Широкое распространение при лечении заболеваний получили топические кортикостероиды. Однако необходимо помнить, что у 0,2–6% пациентов они стали причиной развития аллергического контактного дерматита [14, 15]. В зависимости от химической структуры кортикостероиды разделены на четыре группы, внутри которых отмечаются перекрестные реакции (табл. 2) [16]. В отчете Североамериканской исследовательской группы по изучению контактного дерматита за период 2001–2002 годов были отмечены положительные patch-тесты в 3% случаев на тиксокортол-21-пивалат, в 1,1% случаев – на бутенозид, в 0,5% случаев –гидрокортизон-17-бутират [5]. Среди 2000 пациентов немецкой клиники, страдающих аллергическим контактным дерматитом, менее 1% имели положительный кожный тест на топические кортикостероиды. Умеренный риск развития аллергии был определен для гидрокортизона-17-бутирата, амцинонида, бутенозида; низкий риск – для клобетазола пропионата, триамцинолона ацетонида; низкий риск – для преднизолона, гидрокортизона, бетаметазона, дексаметазона [17]. Минимальный риск развития аллергических реакций показан для мометазона фуроата [18]. Только у одного из 15 пациентов, имеющих сенсибилизацию к топическим кортикостероидам, была отмечена перекрестная реакция с мометазона фуроатом. Результаты данного исследования позволили рекомендовать мометазона фуроат в качестве альтернативного лечебного средства больным, сенсибилизированным кортикостероидами.
Аллергический контактный дерматит развивается как результат эпикутанного внедрения аллергена. При этом после латентного периода, который может составлять от 4–10 дней до 6 месяцев и даже 1–5 лет, развивается острое аллергическое воспаление. Очаги поражения появляются на участках, подвергшихся воздействию аллергена, вместе с тем, клинические проявления могут выходить за пределы зон воздействия аллергенных агентов. На фоне эритемы, сопровождающейся ощущением зуда, жжения, жара, наблюдаются папулы, везикулы, эрозии, корочки, чешуйки. Имеется истинный нерезко выраженный полиморфизм высыпаний. Преимущественно наблюдаются эритематозные, папулезные или везикулезные элементы. При прекращении контакта с аллергеном, вызвавшим кожное поражение, явления аллергического контактного дерматита полностью регрессируют, повторение контакта с аллергеном вызывает рецидивы заболевания. При развитии аллергического контактного дерматита, как правило, отмечается моновалентная сенсибилизация. Однако при хронической аллергенной стимуляции организма, определенных изменениях в деятельности нервной, эндокринной, иммунологической систем, иногда при нерациональной терапии заболевание может трансформироваться в истинную экзему, сопровождающуюся развитием поливалентной сенсибилизации.
Диагностика аллергического контактного дерматита основана на данных анамнеза, клинической картине, физикальном обследовании, а также на результатах накожных аппликационных тестов. Аппликационные тесты помогают выявить аллерген, вызывающий аллергический контактный дерматит, подтвердить клинический диагноз, подобрать безопасные для конкретного пациента вещества. Исследования не проводят больным, получающим системные кортикостероиды или иммуносупрессивные препараты. Относительным противопоказанием является острый дерматит любой локализации. Аппликационные тесты рекомендовано проводить не ранее, чем через месяц после появления острого контактного дерматита, когда наступает стадия регресса или ремиссия.
Для разных регионов разработаны стандартные тест-наборы, содержащие аллергены, используемые для постановки аппликационных тестов. Преимуществами стандартизованных тест-наборов являются мотивированный для данного географического региона выбор аллергенов, обоснованная концентрация гаптена, при которой количество положительных результатов максимальное и число реакций раздражения минимальное, а также возможность получения сравнимых результатов [5]. Предложены стандартные тестовые наборы: Североамериканской исследовательской группой по изучению контактного дерматита - актуальные для региона Северной Америки, Европейской исследовательской группой по изучению контактного дерматита (European Environmental and Contact Dermatitis Research Group – EECDRG) (табл. 3) [19, 20]. Кроме того, в ряде стран используют стандартные тесты, предложенные национальными исследовательскими группами по изучению контактного дерматита [1]. Так как в стандартные серии невозможно включить все существующие аллергены, этиологический фактор аллергического контактного дерматита обнаруживается не у всех больных. Этому способствует также развитие ложноположительных и ложноотрицательных реакций. При получении отрицательных результатов исследования продолжают с более специализированными сериями или с веществами и продуктами, принесенными больным. При соблюдении всех правил постановки аппликационные тесты информативны в 80% случаев.
Лечение аллергического контактного дерматита начинают с устранения причины, вызвавшей заболевание. Необходимо устранить аллерген с поверхности кожи, а также исключить повторный контакт пациента с данным агентом. Нередко элиминировать аллерген бывает затруднительно из-за возможных перекрестных реакций с другими агентами, входящими в состав окружающих бытовых предметов. При выраженных распространенных клинических проявлениях рекомендуют общее лечение десенсибилизирующими средствами, антигистаминными препаратами, сорбентами, витаминами [21]. В ряде случаев одним из методов выбора является системное применение кортикостероидов [21]. Местное лечение проводят с учетом выраженности воспалительного процесса и преобладания тех или иных элементов в клинической картине заболевания. При ограниченных процессах для достижения регресса клинических проявлений достаточно использовать только наружные лекарственные средства.
Противовоспалительный, противоаллергический, иммуносупрессивный эффекты глюкокортикоидов в различных тканях и органах, в том числе и в коже, реализуются за счет нескольких механизмов: уменьшения синтеза медиаторов воспаления; уменьшения количества антигенпрезентирующих и тучных клеток; активации гистаминазы и снижения содержания гистамина в очаге воспаления; снижения активности гиалуронидазы и лизосомальных ферментов, что приводит к уменьшению проницаемости стенок сосудов и выраженности отека; уменьшению образования свободных кислородных радикалов; угнетению синтеза мукополисахаридов и нуклеиновых кислот [22]. Помимо противовоспалительной и иммунодепрессивной активности глюкокортикоиды проявляют антимитотическое и сосудосуживающее действие. Антимитотический эффект обусловлен ингибированием синтеза протеинов, а сосудосуживающий – угнетением активности естественных вазодилататоров (гистамина, брадикинина, простагландинов) [23].
В настоящее время накоплен значительный опыт применения при различных аллергодерматозах мометазона фуроата (Элоком) [24]. Препарат получен посредством введения двух атомов хлора и сложного эфира двойной фуранилкарбоновой кислоты в структуру метилпреднизолона. Химическая структура мометазона фуроата обеспечивает достаточную противовоспалительную и противоаллергическую эффективность, которая реализуется благодаря подавлению продукции ИЛ-1, 4-6, фактора некроза опухоли α, торможению экспрессии адгезивных молекул (VCAM-1) [25, 26]. По силе противовоспалительной активности мометазона фуроат превосходит ряд фторированных глюкокортикостероидов, однако в отличие от последних препарат отличается высоким профилем безопасности: при лечении 22 653 больных различными хроническими дерматозами побочные эффекты отмечены только в 0,4% случаев [24]. Благодаря выраженной липофильности он легко проникает через эпидермис в глубокие слои кожи, при этом системная абсорбция вещества невелика. При нанесении препарата под окклюзионную повязку на 8 часов в системный кровоток всасывается не более 0,7% препарата [27]. Высокая эффективность мометазона фуроата и быстрота наступления эффекта во многом обусловлены преимущественно внегеномным механизмом действия мометазона фуроата, что отличает его от других топических глюкокортикостероидов. Мометазон, образовав комплекс «глюкокортикоид – глюкокортикоидный рецептор», может связываться непосредственно с факторами транскрипции, активирующимися под влиянием медиаторов воспаления [28]. Связывание факторов транскрипции позволяет быстро уменьшить продукцию провоспалительных цитокинов. Поскольку влияние на геном минимально, для мометазона фуроата не характерно развитие связанных с этим процессом побочных эффектов. Высокий профиль безопасности препарата позволяет рекомендовать крем и мазь Элоком для лечения пациентов без возрастных ограничений, включая детей до 2 лет.
Длительное взаимодействие с рецепторами обеспечивает продолжительный терапевтический эффект, благодаря чему мометазона фуроат достаточно использовать один раз в сутки. Преимуществом препарата является также наличие нескольких лекарственных форм (мазь, крем, лосьон), которые назначаются в зависимости от остроты аллергического воспаления и локализации процесса. При хронических инфильтративных процессах рекомендуется использовать мазь. Благодаря гигроскопичной основе крема его назначают при остром воспалении, а спиртовая основа лосьона позволяет использовать его на участках мокнутия, экссудации, при локализации процесса на волосистой части головы. Также важно учитывать, что основа мази и крема Элоком обладает рядом терапевтических свойств – увлажняющих, антиоксидантных, антибактериальных, которые способствуют повышению эффективности лечения [29]. Вещества, входящие в ее состав, придают основе увлажняющие, антиоксидантные, антибактериальные свойства. Кроме того, в состав крема Элоком включены компоненты, обладающие фотопротективными свойствами, что позволяет выбирать именно этот топический стероид для нанесения на участки кожи, подверженные инсоляции.
Мы использовали крем и лосьон Элоком в качестве средства наружной терапии при лечении аллергического контактного дерматита. Под наблюдением находились 54 больных (36 женщин и 18 мужчин) в возрасте от 19 до 87 лет. Развитие аллергического контактного дерматита отмечали после контакта с различными веществами (табл. 4). В 19 случаях аллергический контактный дерматит развивался повторно. У 24 больных процесс носил распространенный характер и локализовался на коже туловища, верхних и нижних конечностей, лица. Ограниченные высыпания в 3 случаях были локализованы на коже лица, у 3 пациентов – ушных раковин, у 9 больных – шеи и груди, у 5 – предплечий, у 4 – в аксиллярных областях, у 6 – на коже живота. Отмечались очаги поражения с четкими границами, на отечном гиперемированном фоне располагались множественные везикулы, папулы, эрозии, участки мокнутия, чешуйки, корочки (фото 1). У 8 пациентов на гиперемированном фоне отмечались крупные пузыри. Во всех случаях высыпания сопровождались выраженным зудом и жжением. Все пациенты четко указывали провоцирующий фактор, после контакта с которым развилось заболевание, поэтому им рекомендовали в первую очередь исключить контакт с данными веществами. 30 пациентов с ограниченными высыпаниями получали монотерапию кремом и лосьоном Элоком 1 раз в сутки. Значительное уменьшение зуда и жжения констатировали после первой аппликации, клиническое выздоровление было достигнуто на 3–5-й день лечения. 24 пациента с распространенным процессом получали общую терапию десенсибилизирующими средствами, антигистаминными препаратами, 3 больным с множественными буллезными элементами однократно назначался Дипроспан 1,0 в/м. Местная терапия заключалась в использовании крема и лосьона Элоком 1 раз в сутки. На 2–3-й день лечения все пациенты отмечали значительное улучшение (уменьшение или прекращение зуда и жжения, частичный регресс высыпаний). Разрешение патологического процесса было отмечено на 8–14-й день лечения. Все пациенты отмечали хорошую переносимость крема и лосьона Элоком. Не было отмечено каких-либо побочных эффектов и осложнений.
Клинический пример. Больная Т., 19 лет, предъявляет жалобы на высыпания на коже живота, сильный зуд. Первые высыпания на коже живота после контакта с металлической пряжкой появились 10 лет назад. Периодически после контакта с металлическими пуговицами и пряжками отмечалось обострение процесса. Высыпания разрешались после прекращения контакта с провоцирующим фактором и использования топических кортикостероидов. Настоящее обострение наблюдается в течение 3 недель, когда после контакта с металлической пуговицей на джинсах появились высыпания на коже живота, сопровождающиеся зудом. В качестве лечебного средства больная самостоятельно использовала настойку календулы, применение которой привело к распространению процесса. При осмотре: процесс локализуется на коже средней и нижней части живота (фото 2). Отмечается очаг поражения с четкими границами размером 10,0 х 6,0 см, на фоне застойной гиперемии имеются папулы, точечные эрозии, корочки. Единичные папулы красного цвета и экскориации выходят за границы основного очага. Субъективно – сильный зуд. Проведено лечение: 1) устранение контакта с провоцирующим фактором; 2) антигистаминные препараты; 3) крем Элоком 1 раз в сутки. На 2–3-й день лечения разрешился зуд, регресс высыпаний констатировали на 8–10-й день лечения.
Наш опыт свидетельствует о высокой эффективности крема и лосьона Элоком в терапии аллергического контактного дерматита. Благодаря выраженной противовоспалительной и противозудной активности значительное улучшение патологического процесса и регресс субъективных ощущений отмечаются после первых аппликаций препарата. При ограниченном поражении для достижения клинической ремиссии достаточно монотерапии препаратом Элоком. При распространенном аллергическом контактном дерматите целесообразно использовать Элоком в комплексном лечении. Гигроскопичная основа крема и спиртовая основа лосьона эффективно устраняют явления мокнутия, обладают подсушивающим действием, что способствует быстрому достижению наилучших терапевтических результатов. Минимальный риск развития аллергии на мометазона фуроат делает препарат особенно привлекательным в терапии аллергического контактного дерматита.
1. Bourke J., Coulson I., English J. Guidelines for care of contact dermatitis // British J. Dermatology. Vol. 145. 2001. P. 877–885.
2. Marks J.J., Elsner P., DeLeo V.A. Allergy and ICD // Contact and Occupational Dermatology, 3rd ed. Philadelphia: Mosby. 2002. P. 3–15.
3. Cohen D.E., Brancaccio R., Andersen D., Belsito D.V. Utility of a standard allergen series alone in the evaluation of ACD: a retrospective study of 732 patients // J. Am. Acad. Dermatol. Vol. 36. 1997. P. 914–918.
4. Larsson-Stymne B., Widstrom L. Ear piercing: a cause of nickel allergy in schoolgirls // Contact Dermatitis. Vol. 13. 1985. P. 289–293.
5. Pratt M.D., Belsito D.V., DeLeo V.A. North American Contact Dermatitis Group patch-test results, 2001–2002 study period // Dermatitis. Vol. 15. 2004. P. 176–183.
6. Adams R.M., Maibach H.I. A five-year study of cosmetic reactions // J. Am. Acad. Dermatol. Vol. 13. 1985. P. 1062–1069.
7. Larsen W.G. How to test for fragrance allergy // Cutis. 2000. Vol. 65. P. 39–41.
8. Groot de A.C., Kley van der A.M., Bruynzeel D.P. Frequency of false-negative reactions to the fragrance mix // Contact Dermatitis. 1993. Vol. 28. P. 139–140.
9. Gruvberger B., Bruze M. Contact allergens – what's new? // Preservatives. Clin. Dermatol. 1997. Vol. 15. P. 493–497.
10. Wantke F., Demmer C.M., Gotz M., Jarisch R. Contact dermatitis from thimerosal // Contact Dermatitis. 1994. Vol. 30. P. 115–117.
11. Bjorkner B., Moller H. Bacitracin: a cutaneous allergen and histamine liberator // Acta Derm. Venerol. 1973. Vol. 53. P. 487–492.
12. Katz B.E., Fisher A.A. Bacitracin: a unique topical antibiotic sensitizer // J. Am. Acad. Dermatol. 1987. Vol. 17. P. 1016–1024.
13. Comaish J.S., Cunliffe W.J. Absorption of drugs from varicose ulcers: a cause of anaphylaxis // Br. J. Clin. Pract. 1967. Vol. 21. P. 97–98.
14. Cohen D.E., Brancaccio R. What is new in clinical research in contact dermatitis // Dermatol. Clin. 1997. Vol. 15. P. 137–148.
15. Boffa M.J., Wilkinson S.M., Beck H.M. Screening for corticosteroid contact hypersensitivity // Contact Dermatitis. 1995. Vol. 33. P. 149–151.
16. Jacob S.E., Steele T. Corticosteroid classes: a quick reference guide including patch test substances and cross-reactivity // J. Am. Acad. Dermatol. 2006. Vol. 54. P. 723–727.
17. Uter W., de Pádua C.M., Pfahlberg A., Nink K., Schnuch A., Lessmann H. Contact allergy to topical corticosteroids-results from the IVDK and epidemiological risk assessment // J. Dtsch. Dermatol. Ges. 2009. Vol. 7. P. 34–42.
18. Rasanen L., Tuomi M.L. Cross-sensitization to mometasone furoate in patients with corticosteroid contact allergy // Contact Dermatitis. 1992. Vol. 27. P. 323–325
19. James W.D., Rosenthal L.E., Brancaccio R.R., Marks J.J. American Academy of Dermatology Patch Testing Survey: use and effectiveness of this procedure // J. Am. Acad. Dermatol. 1992. Vol. 26. P. 991–994.
20. Lachapelle J.M., Bruynzeel D.P., Ducombs G. European multi center study of the TRUE test // Contact Dermatitis. 1988. Vol. 19. P. 91–97.
21. Европейское руководство по лечению дерматологических заболеваний / под ред. А.Д. Кацамбас, Т.М. Лотти. М.: Медпресс-информ, 2008.
22. Barnes P.J. Molecular mechanisms of corticosteroids in allergic deseases // Allergy. 2001. Vol. 56. P. 928–936.
23. Falkenstein E., Tillmann H.C., Christ M., Feuring M., Wehling M. Multiple actions of steroid hormones – a focus on rapid, nongenomic effects // Pharmacol. Rev. 2000. Vol. 52. P. 513–556.
24. Scherer R., Nowok K. Erste erfahrungen mit mometason furoat in derpraxiszein neues topisches kortikoid mit verbessertem risikoznutzen verhaltnis // Detch. Derm. 1995. Vol. 43. P. 280–288.
25. Barton B.E., Jakway J.P., Smith S.R., Siegel M.I. Cytokine inhibition by a novel steroid mometasone furoate // Immunopharmacol. Immunotoxicol. 1991. Vol. 13. P. 251–261.
26. Lee S.W., Sterry W., Gille J. Autocrine stimulation of interleukin-1 alpha and transforming growth factor prodaction in human keratinocytes and its antagonism by glucocorticoids // J. Invest. Dermatol. 1991. Vol. 97. P. 106–110.
27. Schoepe S., Billich A. Glucocorticoid-indused skin atrophy // Exp. Dermatol. 2006. Vol. 15. P. 406–420.
28. Емельянов А.В., Монахов К.Н. Молекулярные механизмы действия топических глюкокортикоидов: значение внегеномного эффекта // Украинский журнал дерматологии, венерологии, косметологии. 2003. № 2. С. 38–40.
29. Аравийская Е.А., Соколовский Е.В., Бахтина С.М., Пчелинцев М.В. Роль основы в глюкокортикостероидных препаратах: оптимальный состав и механизм действия // Вестн. дерматол. и венерол. 2010. № 2. С. 64–70.
Новости на тему
29.01.2021
29.07.2015
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.