Применение гликлазида МВ у госпитализированных больных с COVID-19 и сахарным диабетом 2 типа: влияние на клинический статус и гликемический контроль
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. Под наблюдением находилось 40 последовательно госпитализированных в общее отделение лиц с COVID-19 и СД 2 типа, которые нуждались в сахароснижающей терапии и на стационарном этапе получали гликлазид МВ (n = 20) или инсулин (n = 20).
Результаты. Независимо от назначенного лечения в динамике отмечалось снижение активности воспаления (по уровню С-реактивного белка, р < 0,05 в обеих группах), улучшение коагуляционных показателей (по уровню фибриногена, р < 0,05 в обеих группах) и других клинико-лабораторных параметров. Суточные колебания кривых средней гликемии в диапазоне целевых значений в группе гликлазида МВ наблюдались уже через четыре дня, в группе инсулина – через пять дней. Кроме того, обе терапии ассоциировались с редким развитием эпизодов гипогликемии (по данным тестирования на стационарном анализаторе). При этом количество тестов, зафиксировавших гликемию ≤ 3,9 ммоль/л, было особенно низким на фоне лечения гликлазидом МВ – менее 1%, что в 4,3 раза меньше, чем при использовании инсулина (р = 0,003).
Заключение. Гликлазид МВ можно успешно применять на этапе стационарного лечения больных со среднетяжелым течением COVID-19 и СД 2 типа. В пользу целесообразности и безопасности данной терапии свидетельствует положительная динамика как клинического, так и метаболического статуса пациентов. Гликлазид МВ обеспечивает быстрое достижение и поддержание целевой гликемии при минимальном риске развития гипогликемий.
Материал и методы. Под наблюдением находилось 40 последовательно госпитализированных в общее отделение лиц с COVID-19 и СД 2 типа, которые нуждались в сахароснижающей терапии и на стационарном этапе получали гликлазид МВ (n = 20) или инсулин (n = 20).
Результаты. Независимо от назначенного лечения в динамике отмечалось снижение активности воспаления (по уровню С-реактивного белка, р < 0,05 в обеих группах), улучшение коагуляционных показателей (по уровню фибриногена, р < 0,05 в обеих группах) и других клинико-лабораторных параметров. Суточные колебания кривых средней гликемии в диапазоне целевых значений в группе гликлазида МВ наблюдались уже через четыре дня, в группе инсулина – через пять дней. Кроме того, обе терапии ассоциировались с редким развитием эпизодов гипогликемии (по данным тестирования на стационарном анализаторе). При этом количество тестов, зафиксировавших гликемию ≤ 3,9 ммоль/л, было особенно низким на фоне лечения гликлазидом МВ – менее 1%, что в 4,3 раза меньше, чем при использовании инсулина (р = 0,003).
Заключение. Гликлазид МВ можно успешно применять на этапе стационарного лечения больных со среднетяжелым течением COVID-19 и СД 2 типа. В пользу целесообразности и безопасности данной терапии свидетельствует положительная динамика как клинического, так и метаболического статуса пациентов. Гликлазид МВ обеспечивает быстрое достижение и поддержание целевой гликемии при минимальном риске развития гипогликемий.

Поддержание адекватного гликемического контроля является важной задачей при лечении пациентов с сахарным диабетом (СД) 2 типа и COVID-19 с учетом доказанного негативного влияния гипер- и гипогликемии на течение и прогноз заболевания [1–6].
По мнению ряда экспертов, для госпитализированных пациентов со среднетяжелой степенью инфекции, вызванной SARS-CoV-2, не нуждающихся в лечении в отделении реанимации и интенсивной терапии (ОРИТ), целевым диапазоном гликемии можно считать диапазон от 6 до 10 ммоль/л [7–9]. Согласно 13-й версии Временных методических рекомендаций по профилактике, диагностике и лечению новой коронавирусной инфекции Министерства здравоохранения РФ, среднетяжелым пациентам с сопутствующим сахарным диабетом в качестве целевого установлен уровень гликемии натощак менее 7,5 ммоль/л [10].
Вопрос о сахароснижающей терапии, с помощью которой должны поддерживаться целевые значения глюкозы в крови, остается дискутабельным. Согласно отечественным рекомендациям, в случае среднетяжелого течения COVID-19 и гликемии более 15,0 ммоль/л, и/или появления кетонов в моче, и/или повышения содержания лактата в крови необходимо отменить неинсулиновые препараты и начать базис-болюсную терапию инсулином короткого и длительного действия [10]. Безусловно, базис-болюсная инсулинотерапия позволяет достигать целевых значений гликемии даже в сложных клинических ситуациях. Однако для ее безопасной и эффективной инициации необходимы строгий контроль гликемии в течение суток и тщательная титрация доз инсулина под наблюдением специалиста-эндокринолога. Поэтому в условиях общего отделения инфекционного стационара, где в основном концентрируются пациенты со среднетяжелым течением COVID-19 и СД 2 типа, широкое использование базис-болюсной инсулинотерапии существенно увеличивает нагрузку на медицинский персонал. При ухудшении эпидемиологической ситуации и возрастании числа госпитализаций назначение инсулинотерапии всем нетяжелым больным с COVID-19 и СД 2 типа может оказаться трудновыполнимой задачей. В связи с этим закономерно встает вопрос о преимущественном использовании пероральных сахароснижающих препаратов в данной популяции, в первую очередь это касается больных не с поздними стадиями СД 2 типа и без устойчивой высокой гипергликемии, уже получающих такое лечение.
В литературе представлены доказательства в пользу применения у больных со среднетяжелым течением COVID-19 и диабетом некоторых видов пероральных сахароснижающих препаратов, включая ингибиторы дипептидилпептидазы 4 и производные сульфонилмочевины, ассоциированные с низким риском развития гипогликемий, в частности гликлазид модифицированного высвобождения (МВ) [9, 11–14]. Так, согласно результатам недавно проведенного метаанализа, у пациентов с СД 2 типа, получавших производные сульфонилмочевины и глиниды, риск смерти, связанной с COVID-19, был чуть ниже – 0,93 при 95%-ном доверительном интервале 0,89–0,98 (p = 0,004) [11]. Не исключено, что такие данные могли быть обусловлены небольшим стажем СД [12].
Кроме того, уже существуют экспертные рекомендации о продолжении лечения производными сульфонилмочевины у нетяжелых больных COVID-19 и СД 2 типа, а также отмечается большая безопасность гликлазида [13] при условии контроля гликемии и коррекции дозы препарата соответственно клинической ситуации [14].
Рекомендации экспертов о возможности применения гликлазида МВ при среднетяжелом течении COVID-19 основываются на особенностях действия препарата. Он характеризуется общим для всего класса быстрым сахароснижающим эффектом, лучшим профилем безопасности в силу низкого риска развития гипогликемий, а также нефро- и кардиопротекцией [15]. Именно такой комплекс свойств наиболее востребован при COVID-19, когда нужно не только воздействовать на растущую на фоне инфекции гипергликемию, но и избегать гипогликемий, чтобы не усугублять ассоциированные с COVID-19 кардиальные [1, 16, 17] и другие органные повреждения.
Среди причин развития гипогликемий следует выделить необходимость интенсификации у части больных СД 2 типа и COVID-19 сахароснижающей терапии, нарушение питания при среднетяжелой и тяжелой формах инфекции.
Данные в пользу применения гликлазида МВ в условиях ограничения питания были получены в международном исследовании DIA-RAMADAN [18]. В данном исследовании, проведенном в условиях реальной клинической практики, показана безопасность гликлазида МВ в дозе 60 мг в период соблюдения поста во время Рамадана.
В исследовании приняли участие 1214 больных из девяти стран, которые получали гликлазид МВ по крайней мере за 90 дней до включения в исследование, не нуждались в инсулинотерапии и не меняли антидиабетическую терапию в ходе всего периода наблюдения. При этом около 41% из них находились на монотерапии гликлазидом МВ. Согласно результатам исследования DIA-RAMADAN, у пациентов, которые постились и принимали гликлазид МВ, не было зафиксировано ни одного случая тяжелой гипогликемии. Частота симптоматической гипогликемии во время поста, а также до и после него была очень низкой (2,2 и 0,3% и менее соответственно) при сохранении достигнутого гликемического контроля (уровень гликированного гемоглобина (HbA1c) -0,3%) и массы тела (-0,5 кг).
Полученные результаты продемонстрировали преимущество гликлазида МВ в ситуации риска, когда вероятность гипогликемии повышена.
Особый интерес в связи со сказанным также могут представлять результаты исследования CPRD, в котором в условиях реальной клинической практики сравнивалась эффективность гликлазида МВ и ситаглиптина при использовании в качестве препаратов второй линии после монотерапии метформином. При приеме гликлазида МВ вероятность достижения целевого показателя HbA1c была на 35% выше, чем при назначении ситаглиптина. При этом оба вида лечения характеризовались низкой частотой гипогликемий на протяжении всего периода наблюдения – 4,7 vs 2,6 случая на 1000 пациенто-лет соответственно [19].
В целом результаты исследований свидетельствуют об эффективности, о кардио- и нефропротекции, а также о хорошем профиле безопасности гликлазида МВ.
Перечисленные предпосылки определили цель данного исследования – оценить влияние гликлазида МВ у госпитализированных больных со средней тяжестью COVID-19 и СД 2 типа на клинический и гликемический статус.
Материал и методы
Проведено открытое наблюдательное исследование, в ходе которого анализировался клинический, метаболический и гликемический статус пациентов с COVID-19 и сопутствующим СД 2 типа. В исследование последовательно включали больных COVID-19 и СД 2 типа, госпитализированных в течение восьми недель в инфекционный стационар на базе клиники Приволжского исследовательского медицинского университета и нуждавшихся в сахароснижающей терапии.
Критериями включения были:
- положительный анализ на COVID-19 по результатам исследования мазка, взятого из носоглотки;
- вирусный пневмонит по результатам компьютерной томографии (КТ);
- наличие диагноза СД 2 типа при поступлении, подтвержденного данными анамнеза и/или повышением уровня HbA1с;
- необходимость проведения сахароснижающей терапии по решению лечащего врача.
Всего за время наблюдения было госпитализировано 42 пациента с COVID-19 и СД 2 типа. Из них критериям включения соответствовали 40 человек. У двух пожилых пациентов не было зафиксировано значимых подъемов гликемии, по мнению лечащего врача, они не нуждались в сахароснижающей терапии.
В стационаре использовали два вида сахароснижающего лечения: первый – производные сульфонилмочевины, второй – инсулин.
Среди производных сульфонилмочевины выбор пал на гликлазид МВ ввиду низкого риска гипогликемий и наличия кардио- и нефропротективных эффектов [15]. Гликлазид МВ применяли при нетяжелом течении COVID-19, умеренной выраженности гликемических нарушений и на более ранних стадиях СД 2 типа.
Инсулинотерапия назначалась пациентам с тяжелым течением COVID-19, а также на поздних стадиях СД 2 типа и при его значительной декомпенсации, подтвержденной устойчиво высокой гликемией либо увеличением концентрации кетоновых тел или лактата.
Всего за время наблюдения в группы гликлазида МВ (основная группа) и инсулинотерапии (контрольная группа) было отобрано по 20 пациентов.
В основной группе семь больных получали гликлазид МВ в дозе 30 мг/сут, 11 – в дозе 60 мг/сут, один пациент – в дозе 90 мг/сут, еще один – в дозе 120 мг/сут. Пятеро из них помимо перорального препарата применяли базальный инсулин в небольших дозах (8–12 ЕД/сут).
Из 20 больных на инсулинотерапии десять получали ее в базис-болюсном режиме. У остальных пациентов проводилась либо непрерывная внутривенная инфузия инсулина во время лечения в ОРИТ, либо коррекционное подкожное введение инсулина короткого действия.
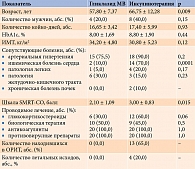
Исходные клинические и демографические показатели пациентов обеих групп представлены в табл. 1.
Как видно из табл. 1, пациенты основной группы были более молодыми, реже страдали ишемической болезнью сердца и хронической болезнью сердца, имели меньшую тяжесть вирусного пневмонита по шкале SMRT-CO (systolicbloodpressure, multilobarinfiltration, respiratoryrate, tachycardia, confusion, oxygenation), не нуждались в лечении в ОРИТ. Различия между группами по перечисленным показателям закономерны и могут объяснять назначение того или иного вида сахароснижающей терапии.
Лечение инфекции, вызванной SARS-CoV-2, в группах было аналогичным. Однако в группе инсулинотерапии наблюдалась тенденция к более частому назначению глюкокортикостероидов, что может быть обусловлено включением в нее пациентов с более тяжелым течением COVID-19.
Потребность в респираторной поддержке, так же как тяжесть вирусного пневмонита, определяли по шкале SMRT-CO. Объем повреждения легочной ткани оценивали по результатам КТ, сатурацию кислорода (SрO2) – по результатам пульсоксиметрии.
Гематологические показатели, С-реактивный белок (СРБ), D-димер, аланин- и аспартатаминотрансферазу (АЛТ и АСТ), креатинин исследовали стандартными методами.
Гликированный гемоглобин определяли с помощью прибора NycoCard Reader II. Профиль гликемии оценивали с помощью стационарного лабораторного анализатора.
Статистическая обработка данных проводилась с использованием пакетов программ Statistica 8.0 и MedCalc. Для сравнения количественных данных в двух независимых выборках применяли метод Манна – Уитни, качественных данных – хи-квадрат Пирсона и критерий Фишера, двух количественных показателей в динамике – метод Уилкоксона. При описании выборок указывали среднее значение и квадратическое отклонение (М ± S). Различия считали статистически значимыми при р ≤ 0,05.
Результаты и их обсуждение
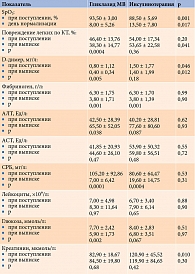
Изменения клинико-лабораторных показателей у госпитализированных пациентов, получавших разную сахароснижающую терапию, представлены в табл. 2.
Принимавшие гликлазид МВ исходно имели лучшие показатели сатурации кислорода, D-димера и креатинина в силу меньшей тяжести COVID-19 и СД 2 типа.
Как на фоне инсулинотерапии, так и на фоне применения гликлазида МВ отмечалось четкое снижение активности системного воспаления (по СРБ) и улучшение коагуляционных показателей (по уровню фибриногена), что косвенно свидетельствовало об успешном лечении инфекции, вызванной SARS-CoV-2, у большинства больных, вне зависимости от вида применяемой сахароснижающей терапии.
В группе гликлазида МВ также наблюдалось значимое сокращение объема поражения легких по результатам КТ и уровню D-димера, что указывало на активное купирование характерных для COVID-19 локальных и системных коагуляционных нарушений.
Положительная динамика показателей клинического и метаболического статуса в основной группе может рассматриваться как дополнительный аргумент в пользу допустимости и безопасности применения гликлазида МВ у госпитализированных лиц со среднетяжелым течением COVID-19 и СД 2 типа.
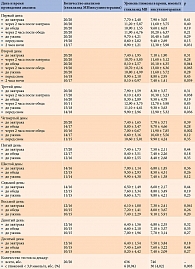
Важнейшей характеристикой сахароснижающего препарата является обеспечение стабильной гликемии в пределах целевого диапазона. Как было сказано ранее, при умеренной тяжести COVID-19 и сопутствующем СД 2 типа таковым считается уровень от 6 до 10 ммоль/л [7–9]. Динамика гликемии в обеих группах в течение первой декады лечения представлена в табл. 3.
Гликемический профиль у получавших разные виды сахароснижающей терапии в целом оказался схожим. Однако среди более тяжелых больных на инсулинотерапии средние результаты измерения уровня глюкозы в крови были значимо выше. В группе гликлазида МВ достоверное увеличение гликемии относительно группы инсулинотерапии отмечалось лишь один раз и, по-видимому, носило случайный характер (рисунок).
В обеих группах суточные колебания кривых средней гликемии не выходили за пределы целевых значений уже через несколько дней стационарного лечения. В группе гликлазида МВ данный эффект отмечался через четыре дня, в группе инсулинотерапии – через пять дней.
Полученные данные подтверждают эффективность обоих видов сахароснижающей терапии у пациентов с COVID-19 и СД 2 типа при условии корректного определения показаний к их назначению.
Следует подчеркнуть, что в двух сравниваемых группах случаи развития гипогликемии были крайне редкими. При этом на фоне приема гликлазида МВ доля тестов, зафиксировавших снижение гликемии до 3,9 ммоль/л и менее, была наименьшей – менее 1%, что более чем в четыре раза ниже, чем на фоне инсулинотерапии (р = 0,003) (см. табл. 3). В этой группе было и меньшее количество пациентов с гипогликемией – 3 (15%) vs 10 (50%) (р = 0,043).
В силу неизбежного ухудшения общего состояния даже среднетяжелые больные COVID-19 и СД 2 типа могут недостаточно и нерегулярно питаться, что уже подразумевает повышенный риск развития гипогликемии. Наши данные подтверждают безопасность применения гликлазида МВ в такой ситуации.
Заключение
Гликлазид МВ может успешно применяться на этапе стационарного лечения больных со среднетяжелым течением COVID-19 и СД 2 типа, что подтверждается положительной динамикой клинического и метаболического статуса.
Гликлазид МВ обеспечивает быстрое (в течение нескольких дней) достижение и длительное сохранение целевых значений гликемии у госпитализированных больных со среднетяжелым течением COVID-19 и сопутствующим СД при условии корректного определения показаний к его назначению. Случаи гипогликемии на фоне терапии гликлазидом МВ редки и составляют менее 1%.
Полученные нами данные свидетельствуют не только об эффективности, но и о безопасности гликлазида МВ у лиц со среднетяжелым течением COVID-19 и СД 2 типа.
T.A. Nekrasova, MD, PhD, Prof., L.G. Strongin, MD, PhD, Prof., Ye.S. Malysheva, PhD, D.V. Belikina, A.A. Nekrasov, MD, PhD, Prof., E.A.A. Mavia
Privolzhsky Research Medical University
Contact person: Tatyana A. Nekrasova, tatnecrasova@yandex.ru
The aim of the study was to evaluate the effect of gliclazide MV in hospitalized patients with moderate severity of COVID-19 and type 2 diabetes mellitus (DM) on clinical and glycemic status.
Material and methods. 40 people with COVID-19 and type 2 diabetes who were successively hospitalized in the general department were under observation, who needed hypoglycemic therapy and received gliclazide MV (n = 20) or insulin (n = 20) at the inpatient stage.
Results. Regardless of the prescribed treatment, there was a decrease in the activity of inflammation (according to the level of C-reactive protein, p < 0.05 in both groups), an improvement in coagulation parameters (according to the level of fibrinogen, p < 0.05 in both groups) and other clinical and laboratory parameters. Daily fluctuations in the curves of average glycaemia in the range of target values in the group of gliclazide MV were observed after four days, in the group of insulin – after five days. In addition, both therapies were associated with the rare development of episodes of hypoglycemia (according to testing on a stationary analyzer). At the same time, the number of tests that recorded glycaemia < 3.9 mmol/l was especially low against the background of treatment with gliclazide MV – less than 1%, which is 4.3 times less than when using insulin (p = 0.003).
Conclusion. Gliclazide MV can be successfully used at the stage of inpatient treatment of patients with moderate COVID-19 and type 2 diabetes. The positive dynamics of both the clinical and metabolic status of patients testifies in favor of the expediency and safety of this therapy. Gliclazide MV provides rapid achievement and maintenance of target glycaemia with minimal risk of hypoglycemia.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.