Применение Кортексина в реабилитации детей первого года жизни с перинатальными гипоксическими поражениями ЦНС
- Аннотация
- Статья
- Ссылки

У 5–15% недоношенных детей, перенесших гипоксическое поражение ЦНС, впоследствии формируются выраженные спастические параличи, эпилепсия, поражение органов слуха и зрения, а у 25–50% детей диагностируется расстройство когнитивных функций и нарушение поведения. У доношенных детей 50% случаев церебрального паралича имеет пренатальную этиологию, 36% являются случаями пери/неонатального происхождения и 14% – неизвестного [1–3].
Развивающийся мозг новорожденного чрезвычайно чувствителен к гипоксии, которая не только вызывает очаговые повреждения мозговой ткани, но и задерживает развитие сосудистой системы и нарушает клеточную дифференциацию. Толерантность к воздействию повреждающих факторов у каждого ребенка различна, поэтому при сравнительно равных условиях у всех детей развиваются неоднозначные последствия. Установлено, что смерть клеток при гипоксии происходит не только по типу некротического поражения, но и с развитием апоптоза клеток, который, в свою очередь, угнетается и индуцируется факторами специфической и неспецифической защиты.
В настоящее время получено значительное количество новой информации о патогенезе гипоксического перинатального поражения ЦНС, его молекулярных и биологических основах. Доказано, что формирование грубых структурных изменений ткани мозга под влиянием гипоксии обусловлено в том числе и неспособностью нейрональных структур синтезировать факторы защиты. В свою очередь антигены, влияющие на деструктивные процессы, обнаруживаются в сыворотке крови новорожденных в значительно превышающих нормативные значения концентрациях уже в первые сутки жизни [3].
В связи с этим большой интерес представляет изучение этих факторов и репаративных механизмов, определяющих течение и исходы гипоксии мозга у новорожденных детей, а также выбор оптимальных программ реабилитации новорожденных, перенесших тяжелые гипоксические поражения.
Современные представления о механизмах нейронального повреждения при длительном или значительном действии таких повреждающих факторов, как гипоксия и ишемия, знание нейропатофизиологических процессов при гипоксическом поражении мозга дает возможность применять в комплексных реабилитационных программах у детей первого года жизни нейропротекторные препараты. Особенное место в ряду этих средств уделяется препаратам пептидной группы, обладающим универсальными, адекватными природе человеческого организма («адресность») свойствами, высокой органотропностью, минимальными побочными эффектами [4–7].
Вышеперечисленные факты определили актуальность, цели и задачи работы, результаты которой представлены ниже.
Цель работы
Изучение эффективности применения Кортексина у доношенных новорожденных, перенесших гипоксическое поражение ЦНС. Препарат давно и успешно используется в детской неврологической практике [8–12]. Особенно эффективно его применение в терапии нарушений психомоторного развития в группе доношенных детей, перенесших гипоксию. Во‑первых, такие дети не всегда рассматриваются как находящиеся в группе риска формирования двигательных нарушений, что обусловлено их способностью хорошо компенсировать нарушения в 3–4‑месячный период жизни, несмотря на тяжесть состояния при рождении. Второй момент, который в определенной степени является спорным, – это отсутствие морфологических маркеров повреждения мозга при проведении нейросонографии. В‑третьих, выбранная группа доношенных детей позволяет четко сравнить развитие с нормативным.
Несомненно, что практикующие неврологи учитывают в реабилитационных программах у детей первого года жизни все симптомы, отрицательно влияющие на развитие (внутричерепная гипертензия, судорожные состояния и т. д.), поэтому в исследование включили только доношенных детей с определенными нарушениями, ведущим из которых стала задержка психомоторного развития.
Материалы и методы:
Под нашим наблюдением находилось 90 доношенных детей. Все дети родились от женщин с отягощенным акушерско-гинекологическим и соматическим анамнезом. Дети были разделены на 3 группы:
- I группа – 30 детей, переживших хроническую внутриутробную гипоксию;
- II группа – 30 детей, переживших острую гипоксию в родах;
- III группа – 30 детей, переживших хроническую внутриутробную гипоксию и острую асфиксию в родах.
Критерием отбора в группы явилось наличие клинической симптоматики и длительность воздействия гипоксического фактора. Все дети постоянно находились под наблюдением педиатра, невролога, офтальмолога. Всем наблюдаемым детям было неоднократно (в среднем 3 раза) проведено ультразвуковое исследование головного мозга (нейросонография, спектральная допплерография сосудов) и электроэнцефалография (ЭЭГ). Исследования проводили по общепринятой методике. Для подтверждения морфологических изменений 21 ребенку с тяжелыми нарушениями развития проведена компьютерная томография головного мозга.
В оценке психомоторного развития (ПМР) применялась методика О. В. Баженовой, позволяющая получить комплексную характеристику психомоторного развития и проводить дифференциальный анализ на основе изучения отдельных групп реакций: двигательных, сенсорных, эмоциональных, голосовых, действий с предметами и способов взаимодействия со взрослыми. Каждая реакция характеризовалась 4 признаками (отсутствие, намеченность, несовершенная и совершенная форма), оцениваемыми по 3‑балльной шкале (от 0 до 3). Суммы контрольных оценок вносились в карту обследования. Определялась степень нарушения по каждой из исследуемых сфер: легкая, средняя, тяжелая. Методика позволяет определить начальный уровень нарушений у каждого ребенка и оценить динамику его состояния при использовании Кортексина.
Результаты исследования
В I группу вошли дети от матерей, имевших отягощенное течение беременности, но физиологические роды. В удовлетворительном состоянии родились 25 детей, 5 пациентов – в состоянии средней тяжести. Степень зрелости у 23 новорожденных соответствовала 36–37 неделям гестации, у 7 детей – 38–39 неделям. С оценкой по Апгар 7/8 баллов родились 22 ребенка, 8/9 – 6 детей, 7/7 – 2 ребенка. Частота внутриутробной гипотрофии составила 26,7%.
Во II группу вошли 30 детей, испытавших острую асфиксию в родах. 20 новорожденных родились в результате самостоятельных родов, 10 – оперативным путем. Все дети этой группы родились в состоянии средней тяжести (19) или в тяжелом (11). Оценка по шкале Апгар ниже 4 баллов была у 4 новорожденных, у 2 – 5/7 баллов, у 15 – 6/7 баллов, у 9 пациентов – 7/8 баллов.
В III группе были дети, испытавшие как хроническое, так и острое гипоксическое воздействие. В состоянии средней тяжести родились 24 ребенка, в тяжелом состоянии – 6.
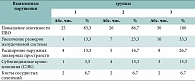
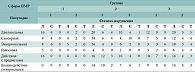
Данные о раннем неонатальном периоде у новорожденных различных групп представлены в таблицах 1 и 2.
Реализация основных клинических нарушений в неврологическом статусе, как в раннем неонатальном периоде, так и в первом полугодии жизни, отмечалась у детей, испытавших острую тяжелую асфиксию. Эти дети находились под очень тщательным наблюдением и осматривались неврологом не реже 1 раза в 3–4 недели. Трудность диагностики и дифдиагностики задержки развития у пациентов с хронической внутриутробной гипоксией (ХВГ) в анамнезе заключается в том, что в раннем неонатальном периоде явная симптоматика неврологических нарушений может отсутствовать.
Во всех группах преимущественными сроками формирования нарушения ПМР были периоды со второго по пятый месяц жизни.
Учитывая наличие и тяжесть задержки ПМР, назначался препарат Кортексин. Первичное назначение всегда осуществлялось в среднем в 2,5–3,5 месяца детям с острой гипоксией, у которых наблюдалась задержка развития не только в двигательной, но и в психоэмоциональной сфере. В 3,5–5,5 месяцев в среднем препарат впервые назначался пациентам, испытавщим ХВГ, у которых формировалась задержка развития.
Кортексин назначали детям с легкой и средней степенью задержки психомоторного развития в дозе 0,5–1,0 мг/кг 1 раз в сутки в/м, курс лечения 10 дней. У детей с тяжелой степенью задержки ПМР, особенно при формировании отставания в психоэмоциональной сфере, препарат назначали в дозе 1 мг/кг в/м, курс лечения 10 дней. Необходимо отметить, что все дети в комплексной реабилитационной программе обязательно получали также массаж, гимнастику, плавание, при необходимости – курсы физиотерапии.
Повторный курс препарата назначался пациентам с тяжелой степенью нарушения ПМР, а также всем детям со средней степенью задержки в формировании психоэмоционального компонента развития и пациентам с низкой возможностью компенсации выявленных нарушений.
В I группе в первом полугодии препарат получали 20 детей, во втором – 6. Во II группе в первом полугодии Кортексин назначали всем пациентам, во втором полугодии – 20. В III группе все дети получали препарат дважды за год наблюдения.
Исследование ПМР выявило различия в оценках как в количественном, так и в качественном отношении (табл. 3).
Из полученных данных видно, что самые тяжелые как в количественном, так и в качественном отношении изменения были отмечены у детей III группы. Это связано со слабыми компенсаторными возможностями пациентов, перенесших как внутриутробную гипоксию, так и острую асфиксию в родах.
Учитывая особенности нарушения психомоторного развития, можно заключить, что в первой группе преобладали нарушения двигательного развития в легкой и среднетяжелой степени, хорошо поддающиеся медикаментозной коррекции. Во второй группе наряду с этими нарушениями отмечались и тяжелые формы задержки развития, в основном за счет двигательного компонента. В третьей же группе формировались самые тяжелые нарушения ПМР – с задержкой не только двигательного, но и когнитивного, эмоционального развития, приводящей к затруднениям в ситуационно-личностном общении.
Несомненно, назначение Кортексина в ранние сроки привело к компенсации имеющихся изменений у пациентов всех групп. Важно отметить, что ни у одного пациента не было отмечено каких-либо побочных эффектов при приеме препарата. Однако выявленные у некоторых детей изменения на НСГ потребовали уточнения картины морфологических изменений в головном мозге, для чего 21 ребенку было проведено МРТ (15 пациентам из III группы и 9 из II группы). Были выявлены следующие изменения: у 8 детей в III группе и у 3 во II – перивентрикулярная лейкомаляция (ПВЛ), у 10 – лейкопатия. Необходимо отметить, что небольшие кисты, как перивентрикулярные, так и субкортикальные, отмеченные в раннем неонатальном периоде, в дальнейшем при проведении НСГ зачастую очень трудно выявить. У 10 пациентов также отмечались умеренные расширения наружных ликворных пространств атрофического характера.
Таким образом, структурные изменения, обусловившие формирование грубой задержки ПМР, были доказаны. Однако динамическое наблюдение, лечебная коррекция с помощью Кортексина позволили компенсировать нарушения ПМР у очень многих из наблюдаемых детей. У всех пациентов первой группы формирующаяся задержка ПМР была полностью компенсирована. С исходом в ДЦП во II группе было 2 детей, в III – 4. При этом у всех этих детей была выявлена ПВЛ, а при рождении зафиксирована оценка по Апгар менее 4 баллов. Грубая задержка в психоэмоциональной сфере отмечалась у 4 детей. У остальных детей наблюдались темповые задержки развития к концу первого года жизни, в основном в двигательной сфере. Программа реабилитации этих пациентов продолжалась в среднем до 1,5 лет.
Выводы
Наиболее актуальной проблемой при динамическом наблюдении доношенных детей, перенесших хроническую внутриутробную гипоксию и острую асфиксию в родах, на первом году жизни является нарушение психомоторного развития. Самыми тяжелыми из таких пациентов, как правило, бывают дети с сочетанием хронического кислородного голодания и острого страдания в родах.
Необходимо комплексное обследование каждого ребенка перед назначением реабилитационных мероприятий: оценка данных внутриутробного развития, родов, особенностей течения неонатального периода, консультация врачей-специалистов, проведение НСГ, ЭЭГ, ДГ.
В работе показана высокая эффективность Кортексина при проведении реабилитационной терапии у доношенных детей в различных группах. Доказано положительное влияние препарата на компенсацию постгипоксических изменений и задержку психомоторного развития.
Несмотря на имеющиеся морфологические структурные изменения, детям, перенесшим гипоксическое поражение, при первых признаках формирования задержки ПМР необходимо назначать препарат Кортексин. Это позволяет значительно сократить сроки реабилитации.
У пациентов с формированием среднетяжелой и тяжелой степени задержки ПМР препарат необходимо назначать дважды в год.
Кортексин отличается хорошей переносимостью.
В терапии рассматриваемой патологии назначение короткого курса лечения Кортексином является предпочтительным по сравнению с другими препаратами этой фармакологической группы.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.