Применение пульс-гормонотерапии у пациента с хлорлейкозом
- Аннотация
- Статья
- Ссылки
- English
Введение
Хлорлейкоз (миелобластная саркома, гранулоцитарная саркома, хлорома) – редкая форма нелейкемического гемобластоза, морфологический субстрат которого состоит из миелобластов и промиелоцитов, содержащих миелопероксидазу. Не случайно на разрезе опухоль приобретает зеленоватую окраску [1].
Клинически хлорлейкоз – один из наиболее злокачественных гемоцитобластозов с типичной клинической картиной, но более выраженной тенденцией к опухолевому росту и его агрессивности.
Миелобластная саркома является облигатной предстадией острого миелобластного лейкоза (ОМЛ) или развивается на терминальной стадии хронического миелолейкоза либо ОМЛ. Заболевание достаточно редкое – два случая на 1 000 000 взрослого населения [2].
Актуальность проблемы миелобластной саркомы в мире обусловлена недостатком опыта и четких рекомендаций по ее лечению, профилактике перехода в ОМЛ, а также отсутствием публикаций на эту тему. Почти во всех зарегистрированных случаях первичного хлорлейкоза вскоре развивался острый лейкоз (медиана времени до развития острого лейкоза – семь месяцев, диапазон – от одного до 25 месяцев) [3]. Таким образом, первичный хлорлейкоз, который можно считать начальным проявлением острого лейкоза, рекомендовано лечить как ОМЛ.
При ОМЛ применяют химиотерапию. Лечение проводится в два этапа: первый – индукционная терапия, второй – постремиссионное лечение (консолидация). Целью первого этапа является достижение полной ремиссии за счет уменьшения количества лейкозных клеток до необнаруживаемого уровня, целью второго – ликвидация не выявленных современными методами остаточных явлений болезни и излечение [4].
Индукционная терапия предполагает применение различных цитостатиков. На первый план выходят схемы с цитарабином и антрациклинами. Лечение крайне токсичное вследствие подавления миелоидного ростка, повышения риска инфекционных осложнений и развития синдрома диссеминированного внутрисосудистого свертывания на фоне поступления содержимого гранул промиелоцитов в периферическую кровь. Кроме того, полная ремиссия не означает полного излечения. Состояние полной ремиссии скорее свидетельствует о невозможности выявить болезнь современными диагностическими способами. Как правило, все случаи ремиссии без дополнительного (консолидирующего) лечения завершаются рецидивом [4].
Клинический случай
В августе 2009 г. пациент 27 лет с болью в эпигастральной области обратился в поликлинику по месту жительства. Назначенная консервативная терапия по поводу обострения хронического панкреатита оказалась неэффективной.
14 сентября отмечались повышение температуры тела до 39 °С, выраженный болевой синдром в эпигастральной области, тошнота, горечь во рту.
В городской больнице г. Братска 17 сентября по поводу кишечной непроходимости выполнена лапаротомия, наложены обходные анастомозы, проведена биопсия опухоли. В ходе операции выявлена опухоль брыжейки тонкой кишки до 10 см. Гистологически подозрение на миелопролиферативный процесс. Пациент направлен к гематологу в областную больницу г. Иркутска, где 12 октября выполнена стернальная пункция. Миелограмма не показала поражения костного мозга.
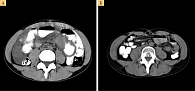
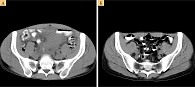
Результаты компьютерной томографии (КТ) легких и средостения от 13 октября: без очаговой патологии, нередуцированная вилочковая железа. Мультиспиральная КТ брюшной полости, забрюшинного пространства и полости малого таза вокруг печени, селезенки и между петель кишечника от 13 октября: в дугласовом пространстве гиподенсивное содержимое; на фоне жидкости справа, ниже края правой доли печени, в проекции брюшины мягкотканное образование неоднородной структуры 86 × 27 мм. На фоне уплотнения жировой ткани брыжейки тонкой кишки – мягкотканное образование неправильной формы 75 × 68 мм на уровне передних подвздошных остей с неровными и нечеткими контурами. Достаточно равномерное утолщение стенки подвздошной кишки до 10–14 мм с сужением просвета нескольких петель, внутренние и наружные контуры кишки нечеткие. Печень обычной формы, увеличена (нижний край на 4 см ниже реберной дуги).
Заключение: проявление миелопролиферативного процесса с поражением забрюшинных лимфатических узлов. Признаки поражения брюшины. Свободная жидкость в брюшной полости. Гепатоспленомегалия. При гастро- и колоноскопии онкопатологии не выявлено.
Во время обследования возникла острая кишечная непроходимость. В отделении неотложной хирургии областной больницы г. Иркутска 18 октября выполнены лапаротомия, резекция большого сальника, илеостомия по Торнболлу, биопсия опухоли. При гистологическом исследовании и иммунофенотипировании (также пересмотрены парафиновые блоки после первой операции) диагностирована миелосаркома, бластный вариант.
27 октября проведена билатеральная биопсия подвздошных костей. Гистологических данных о миелопролиферативном процессе нет.
После выписки из хирургического отделения в ноябре 2009 г. больной с жалобами на выраженную общую слабость, снижение аппетита, уменьшение массы тела до 20 кг за три месяца, боль в эпигастральной области, тяжесть и вздутие живота, жидкий стул направлен в Иркутский областной онкологический диспансер.
При поступлении: рост 182 см, масса тела 48 кг, состояние по шкале ECOG 3 балла, крайне ослаблен, передвигается при помощи родственников, пищу принимает малыми порциями, аппетит отсутствует, постоянная эвакуация съеденного через илеостому, опорожнения кишечника естественным путем нет. В клиническом и биохимическом анализах крови существенных отклонений от нормы нет. Пациент госпитализирован в день обращения с диагнозом миелосаркомы с поражением тонкой кишки, брюшины, забрюшинных лимфатических узлов, селезенки IV стадии.
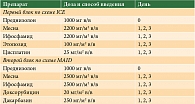
Больному назначили пульс-гормонотерапию (преднизолон 1000 мг внутривенно капельно). Эффект от первого цикла отмечался в день его проведения: уменьшилась слабость, появился аппетит, исчезла боль в эпигастральной области, увеличилась толерантность к физической нагрузке. Для индукции выбрали альтернирующую схему ICE – MAID (таблица).
При контрольном обследовании после четвертого курса на основании результатов КТ от 15 января 2010 г. констатирована полная неподтвержденная ремиссия. Шесть курсов химиотерапии по альтернирующей схеме ICE – MAID + шесть циклов пульс-гормонотерапии (фаза индукции) завершились 28 января. Клинически отмечалась выраженная положительная динамика, купированы все симптомы заболевания, сохранялась умеренная общая слабость, масса тела увеличилась всего на 3 кг (51 кг), что связано с наличием илеостомы. Лечение больной перенес удовлетворительно, выявлена гематологическая токсичность в виде лейкопении второй степени по СТС, курсы химиотерапии не переносились, доза не редуцировалась. Впоследствии проведено два курса химиотерапии (фаза консолидации) по схеме: Цитозар 100 мг/м2 два раза в день (200 мг/м2 в сутки) внутривенно в первый – пятый дни, циклофосфан 650 мг/м2 внутривенно в первый день, интервал между курсами 28 дней. Курсы завершены 2 мая. Лечение осложнилось внебольничной двусторонней нижнедолевой пневмонией и нормохромной анемией тяжелой степени. Проведены курс антибиотикотерапии, переливание компонентов крови (эритропоэтины с положительной динамикой), осложнения купированы. Данные КТ грудной клетки, брюшной полости и малого таза подтвердили полную регрессию.
Спустя три месяца после лечения пациент жалоб не предъявлял, состояние по шкале ECOG – 0, масса тела стабильная – 51 кг. По данным мультиспиральной КТ, фиброколоноскопии (ФКС), фиброгастродуоденоскопии (ФГДС), прогрессирования и рецидива заболевания не выявлено. 5 августа выполнена операция по восстановлению непрерывности кишечника. Через шесть месяцев после закрытия илеостомы масса тела увеличилась до 76 кг. Динамическое наблюдение за пациентом продолжается и предусматривает контрольное обследование (клинический и биохимический анализы крови, КТ грудной клетки, брюшной полости и малого таза, стернальная пункция, ФКС, ФГДС) один раз в три месяца в течение года, один раз в шесть месяцев в течение двух лет и затем один раз в год.
В течение первых трех с половиной лет наблюдения зафиксировано угнетение миелоцитарного ростка кроветворения. И только на пятом году после окончания терапии можно говорить о полном восстановлении полноценного кроветворения.
В настоящее время больной жив, жалоб нет, состояние по ECOG – 0, по данным КТ грудной клетки, брюшной полости и малого таза – полная ремиссия. Миелограмма в норме, масса тела 78 кг на протяжении шести лет (рис. 1 и 2). Продолжает работать, ведет активный образ жизни, катается на горных лыжах, в семье родился второй ребенок.
Обсуждение
Приведенные данные демонстрируют потенциальный благоприятный эффект альтернирующей схемы ICE – MAID в сочетании с пульс-гормонотерапией в качестве индукции у пациента с хлорлейкозом: зафиксирована полная регрессия опухоли, выживаемость без прогрессирования превысила пять лет. Данная схема позволяет не только достичь полной регрессии опухоли, не допустить перехода в ОМЛ, но также максимально продлить выживаемость без прогрессирования и, возможно, добиться излечения.
В случае когда результаты пункции и биопсии костного мозга не демонстрируют отклонений от нормы, миелосаркома является предшественником острого миелоидного лейкоза. Этот тип миелосаркомы называется изолированным, или первичным. В литературе описано несколько клинических случаев и их анализов, в большинстве ретроспективных [2]. Хлорлейкоз может возникнуть в любом возрасте и на любом участке тела. Однако наиболее распространенной считается локализация в мягких тканях, костях, брюшине, лимфатических узлах, желудочно-кишечном тракте. Описаны редкие случаи поражения мочеполовой и нервной систем [5, 6].
Выделяют три основных варианта миелосаркомы в зависимости от преобладающего типа клеток и степени их созревания:
- бластный – преобладание миелобластов;
- незрелый – сочетание миелобласты и промиелоцитов;
- дифференцированный – промиелоциты и более зрелые гранулоциты [7].
ОМЛ в краткосрочной перспективе развивается после постановки диагноза хлорлейкоза. Плохой ответ на индукционную терапию напрямую зависит от крайне неблагоприятного прогноза [8]. Не случайно основные задачи химиотерапии – достижение полной регрессии опухоли, увеличение продолжительности жизни больных и выживаемости без прогрессирования, улучшение качества жизни (облегчение симптомов заболевания, профилактика и лечение осложнений терапии) и профилактика перехода в ОМЛ [8]. Оптимальная схема химиотерапии хлорлейкоза не разработана, ранее использованные режимы похожи на схемы лечения ОМЛ [2].
В исследовании А. Tsimberidou и соавт. [9] в группе пациентов, получавших химиотерапию (идарубицин + цитарабин; флударабин + цитарабин, идарубицин; циклофосфамид + цитарабин + топотекан; даунорубицин и цитарабин) одновременно с лучевой терапией или без таковой, в 65% случаев зафиксирована полная ремиссия, медиана выживаемости составила 20 месяцев.
К. Imrie и соавт. [10] подтвердили, что системная химиотерапия снижает скорость перехода в ОМЛ (41% по сравнению с 71%; р = 0,001) и повышает выживаемость.
В рассматриваемом случае терапию подбирали индивидуально. На старте применяли пульс-гормонотерапию (преднизолон 1000 мг внутривенно капельно). Целей было несколько: во-первых, собственно противоопухолевое воздействие, во-вторых, подготовка к химиотерапии (симптоматическая терапия), в-третьих, профилактика перехода в ОМЛ за счет истощения миелоцитарного ростка костного мозга. Несмотря на то что для индукции применялась новая альтернирующая схема ICE – MAID, содержавшая антрациклины, были соблюдены все принципы терапии крайне злокачественной миелобластной опухоли (широкий спектр препаратов с выраженным цитостатическим действием на всех фазах деления клетки, направленных на достижение полной ремиссии). Выбор был полностью оправдан, поскольку достигнута полная регрессия опухоли. Отсутствие токсичности третьей-четвертой степени позволило сохранить качество жизни пациента. К преимуществу данного лечения относится возможность его повторения при возникновении позднего рецидива.
Механизм антилейкемического действия гормонов коры надпочечников и их синтетических аналогов ученые изучают и сегодня, хотя о лимфоцитолитическом действии этих гормонов во время стресса упоминалось в первых работах (1936 г.) Ганса Селье.
Доказано, что в культуре тканей преднизолон способен тормозить синтез нуклеиновых кислот и протеинов, а впоследствии вызывает гибель клеток [11]. Преднизолон тормозит клеточные митозы и пролиферацию. Антилейкемический эффект глюкокортикостероидов в сочетании со стимуляцией эритроидного и тромбоцитарного ростков выгодно выделяет их из группы других антилейкемических средств. Надо полагать, что в основе лечебного эффекта гормональных препаратов лежит не только их непосредственное цитологическое или цитостатическое действие, но и более сложный комплексный механизм воздействия на физиологические функции поврежденного болезнью организма [11]. Клинический эффект гормональных средств всегда выражается в улучшении самочувствия пациента, повышении аппетита, поднятии эмоционального тонуса. Нередко одновременно с субъективным улучшением нормализуется температура, снижаются геморрагические явления, исчезают некротические изъязвления на коже и слизистых оболочках, проходит интоксикация [11]. Самая важная цель пульс-гормонотерапии преднизолоном – предотвращение перехода миелосаркомы в ОМЛ за счет истощения миелоцитарного ростка костного мозга. Это несет в себе крайне высокий риск инфекционных осложнений, но значительно улучшает прогноз заболевания и дает надежду на излечение. По достижении полной ремиссии на фоне индукционной терапии рассматривается вопрос о смене препаратов, используется стандартная схема на основе цитарабина как препарата выбора для лечения пациентов с ОМЛ, направленного на предотвращение рецидива заболевания.
Заключение
Альтернирующая схема ICE – MAID в качестве индукционной терапии продемонстрировала эффективность у больного хлорлейкозом. Данную схему можно рассматривать как новый перспективный вариант терапии в индукции пациентов при миелобластной саркоме. При выборе и проведении терапии миелосаркомы следует учитывать ее злокачественный характер, агрессивный тип роста, неблагоприятный прогноз и помнить, что заболевание является облигатной стадией острого миелобластного лейкоза.
Пульс-гормонотерапия преднизолоном, проведенная перед каждым курсом химиотерапии в индукции, оказывает противоопухолевое действие, повышает эффективность последующей химиотерапии и играет важную роль в профилактике острого миелобластного лейкоза.
D.Yu. Yukalchuk
Irkutsk Regional Oncological Center
Contact person: Denis Yuryevich Yukalchuk, dyuyu558@mail.ru
Analyzed the effectiveness of treatment with using of alternating scheme ICE – MAID as induction in a patient with common chloroleukosis (myelosarcoma) and consolidation upon the scheme ῾Cytosar + cyclophosphamide’. At zero day of each course of induction pulse-hormone therapy was carried out – as the preparation for the basic treatment. In a patient it was diagnosed complete tumor regression, progression-free survival exceeded five years. The monitoring continues. This scheme can be considered as a new promising therapy option in the induction of patients with myelosarcoma. Pulse-hormone therapy with prednisolone has an antitumor effect, increases the subsequent chemotherapy effectiveness and plays an important role in the prevention of acute myeloblastic leukemia.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.