Прогнозирование риска дислипидемий в период после проведения аллогенной трансплантации гемопоэтических стволовых клеток у пациентов с острым лейкозом на основе программ математического моделирования
- Аннотация
- Статья
- Ссылки
- English
Цель – с помощью программ математического моделирования разработать алгоритм оценки риска развития дислипидемии у пациентов с острым лейкозом, получивших патогенетическую терапию.
Материал и методы. Проведено одномоментное проспективное исследование 39 пациентов с острым лейкозом, получивших патогенетическую терапию, включающую высокодозную химиотерапию и аллогенную трансплантацию гемопоэтических стволовых клеток. Группу контроля составили 30 пациентов без онкогематологической и сердечно-сосудистой патологии в анамнезе. Всем участникам исследования проводилась оценка липидного спектра, общего анализа крови. Построение математической модели прогноза необходимости профилактических мероприятий нарушений липидного статуса осуществлено с помощью алгоритма машинного обучения «Дерево решения», имеющего структуру, соответствующую необходимости принятия решения о начале профилактики дислипидемии.
Результаты. «Дерево решений» позволяет анализировать показатели липидного статуса и гемограммы у пациентов с острым лейкозом, получивших патогенетическую терапию, и выявлять необходимость профилактики дислипидемии. Необходимость профилактических мероприятий нарушений липидного статуса у пациентов с острым лейкозом после аллогенной трансплантации гемопоэтических стволовых клеток наиболее вероятна при сниженном уровне тромбоцитов, а с нормальным уровнем тромбоцитов – при повышении показателей общего холестерина. Полученная математическая модель прогнозирует риск развития дислипидемии у данной категории лиц на обучающей выборке с точностью 97,1%, чувствительностью 98,0% и специфичностью 96,1%, ROC-AUC (ROC – Receiver Operating Characteristic (рабочая характеристика приемника); AUC – Area Underthe Curve (площадь под кривой) 97,1%.
Обсуждение. Своевременная оценка риска развития дислипидемии у этих пациентов может улучшить их долгосрочный прогноз, уменьшить риск развития осложнений в позднем посттрансплантационном периоде. Прогнозирование дислипидемий после проведенной аллогенной трансплантации гемопоэтических стволовых клеток является основанием для разработки мероприятий, направленных на снижение кардиоваскулярного риска у данной когорты пациентов.
Заключение. Прогностическая модель развития дислипидемии, разработанная с использованием методов машинного обучения, позволяет с высокой точностью оценить риск развития данного осложнения и дает возможность разработки индивидуализированных профилактических программ, направленных на предотвращение развития атеросклероза.
Цель – с помощью программ математического моделирования разработать алгоритм оценки риска развития дислипидемии у пациентов с острым лейкозом, получивших патогенетическую терапию.
Материал и методы. Проведено одномоментное проспективное исследование 39 пациентов с острым лейкозом, получивших патогенетическую терапию, включающую высокодозную химиотерапию и аллогенную трансплантацию гемопоэтических стволовых клеток. Группу контроля составили 30 пациентов без онкогематологической и сердечно-сосудистой патологии в анамнезе. Всем участникам исследования проводилась оценка липидного спектра, общего анализа крови. Построение математической модели прогноза необходимости профилактических мероприятий нарушений липидного статуса осуществлено с помощью алгоритма машинного обучения «Дерево решения», имеющего структуру, соответствующую необходимости принятия решения о начале профилактики дислипидемии.
Результаты. «Дерево решений» позволяет анализировать показатели липидного статуса и гемограммы у пациентов с острым лейкозом, получивших патогенетическую терапию, и выявлять необходимость профилактики дислипидемии. Необходимость профилактических мероприятий нарушений липидного статуса у пациентов с острым лейкозом после аллогенной трансплантации гемопоэтических стволовых клеток наиболее вероятна при сниженном уровне тромбоцитов, а с нормальным уровнем тромбоцитов – при повышении показателей общего холестерина. Полученная математическая модель прогнозирует риск развития дислипидемии у данной категории лиц на обучающей выборке с точностью 97,1%, чувствительностью 98,0% и специфичностью 96,1%, ROC-AUC (ROC – Receiver Operating Characteristic (рабочая характеристика приемника); AUC – Area Underthe Curve (площадь под кривой) 97,1%.
Обсуждение. Своевременная оценка риска развития дислипидемии у этих пациентов может улучшить их долгосрочный прогноз, уменьшить риск развития осложнений в позднем посттрансплантационном периоде. Прогнозирование дислипидемий после проведенной аллогенной трансплантации гемопоэтических стволовых клеток является основанием для разработки мероприятий, направленных на снижение кардиоваскулярного риска у данной когорты пациентов.
Заключение. Прогностическая модель развития дислипидемии, разработанная с использованием методов машинного обучения, позволяет с высокой точностью оценить риск развития данного осложнения и дает возможность разработки индивидуализированных профилактических программ, направленных на предотвращение развития атеросклероза.

Введение
В настоящее время для лечения пациентов с острыми лейкозами (ОЛ) успешно применяются современные протоколы программной противоопухолевой терапии в сочетании с аллогенной трансплантацией гемопоэтических стволовых клеток (алло-ТГСК). Однако, обладая высоким противоопухолевым потенциалом, цитостатические и таргетные препараты в отдаленном периоде индуцируют развитие различных осложнений, в том числе сердечно-сосудистых заболеваний (ССЗ) [1].
Проведение алло-ТГСК у пациентов с ОЛ имеет потенциал более серьезного вмешательства в обменные процессы липидов по причине большей токсичности, которая суммируется с ранее проведенными курсами высоких доз химиотерапевтических препаратов (ВДХТ). Данные процессы приводят к увеличению развития поздних осложнений после патогенетического лечения, требующих разработки особых, современных клинико-диагностических подходов и своевременных профилактических мероприятий [2].
Дислипидемия у пациентов с ОЛ, получивших ВДХТ и алло-ТГСК, является одним из неблагоприятных факторов риска, обусловливающих развитие сердечно-сосудистых заболеваний. Нарушения липидного спектра в первую очередь связаны с гормональными нарушениями, острой и хронической реакцией «трансплантат против хозяина» (РТПХ), применением иммуносупрессивной терапии и другими факторами. При этом остаются не до конца понятны молекулярные пути, приводящие к изменению липидов, не разработаны стандартные рекомендации по диагностике и ведению пациентов с ОЛ и дислипидемией после алло-ТГСК [2].
Применение принципов индивидуализации современных подходов в лечении и профилактике осложнений у пациентов с ОЛ выдвигает в качестве условия глубокое понимание механизмов прогрессирования заболевания и путей реализации эффектов лечения. Применение прогностических моделей позволяет идентифицировать параметры, специфичные для конкретного пациента, и, следовательно, обеспечивает персонифицированный прогноз эффекта различных вмешательств. Это также ассоциируется с внедрением принципов превентивно-профилактической медицины, направленной на диагностику заболеваний на доклиническом этапе. Прогнозирование позволяет разработать профилактические мероприятия, в том числе на основе оценки воздействия экзогенных и эндогенных факторов на состояние здоровья человека, что достигается путем математического анализа данных электронно-вычислительными машинами [3].
В последнее время медицинские информационные технологии становятся все более популярными. Все большее распространение находят методы математического моделирования в медицине для точного прогнозирования с учетом факторов, оказывающих влияние на развитие осложнений или заболеваний в раннем и отдаленном периоде. Использование программ математического прогноза во многом основывается на информации ретроспективных сведений [4].
При этом прогностические модели создаются путем применения многомерных методов регрессионного и дискриминантного анализа. Это позволяет, в частности, рассчитать относительный риск развития целого ряда осложнений. Как правило, целью создания математических моделей прогноза является улучшение процесса принятия врачебного решения и качества медицинской помощи [4].
Отмечается высокая распространенность использования прогностических моделей и в онкогематологии, что связано с риском частых осложнений на фоне проводимой патогенетической терапии [5]. Хотя применение современных протоколов противоопухолевой терапии, включающей ВДХТ и глюкокортикостероиды, а также алло-ТГСК, сопровождается улучшением общей выживаемости данной категории пациентов, единый подход к их ведению до сих пор не сформулирован, следовательно, риск развития осложнений, в том числе сердечно-сосудистых, в разных ситуациях может существенно варьировать. Вопрос объективной оценки риска развития процессов, лежащих в их основе, в частности дислипидемий, у лиц с ОЛ после алло-ТГСК является актуальным и требует разработки персонифицированного подхода.
Цель – с помощью программ математического моделирования разработать алгоритм оценки риска развития дислипидемии у пациентов с острым лейкозом, получивших высокодозную химиотерапию и в дополнение к ней – аллогенную трансплантацию гемопоэтических стволовых клеток.
Материал и методы
Проведено одномоментное проспективное исследование 39 пациентов с ОЛ, получивших ВДХТ и алло-ТГСК. Группу контроля составили 30 участников без онкогематологической и сердечно-сосудистой патологий в анамнезе, с медианой возраста 35 лет – 12 (40%) женщин и 18 (60%) мужчин.
Всем пациентам с ОЛ диагноз установлен на основании цитологического, цитогенетического и молекулярно-генетического исследований костного мозга. В группу вошли 39 пациентов с ОЛ – 24 (61%) женщины и 15 (39%) мужчин с медианой возраста 42 года, которым была проведена ВДХТ и алло-ТГСК. Острый лимфобластный лейкоз выявлен у 12 (31%) пациентов данной группы, острый миелобластный лейкоз – у 27 (69%) пациентов.
Все пациенты с ОЛ получили патогенетическую терапию в соответствии со стандартами оказания медицинской помощи и клиническими рекомендациями. При проведении алло-ТГСК всем пациентам с ОЛ назначили такие схемы кондиционирования: бусульфан + флударабин 12. В качестве трансплантата все больные получили периферические стволовые клетки. Для профилактики острой РТПХ назначали введение циклофосфамида в день 1 ± 3 и в день 1 ± 5 после алло-ТГСК и в день 1 ± 5 – прием ингибиторов кальциневрина и микофенолата мофетила.
Критерии включения пациентов в исследование:
- возраст более 18 лет;
- верифицированный диагноз ОЛ;
- лечение по стандартным схемам ВДХТ.
Критерии исключения пациентов из исследования:
- возраст менее 18 лет;
- отсутствие достоверно подтвержденного диагноза ОЛ;
- наличие в анамнезе тяжелых эндокринных, системно-воспалительных или других онкологических заболеваний;
- беременность и период лактации.
Всем участникам исследования с использованием биохимического анализатора ILabTaurus (Instrumentation Laboratory S.P.A., Италия), общего анализа крови на аппарате ВС 5800 (Mindray, Китай) проведена оценка липидного спектра:
- общий холестерин (ОХС);
- липопротеины низкой плотности (ЛПНП);
- липопротеины высокой плотности (ЛПВП);
- триглицериды (ТГ);
- липопротеины очень низкой плотности (ЛПОНП);
- холестерин не липопротеинов высокой плотности (ХС не-ЛПВП);
- коэффициент атерогенности (КА).
Морфологический состав периферической крови определялся на микроскопе в окрашенных мазках методом Романовского – Гимзе.
Построение математической модели прогноза необходимости профилактических мероприятий нарушений липидного статуса проводили с помощью алгоритма машинного обучения «Дерево решения», имеющего структуру, соответствующую необходимости принятия решения о начале профилактики дислипидемии.
На первом этапе исходная выборка была разделена случайным отбором на обучающую и тестовую выборки (80 и 20% соответственно). На втором этапе обучающая выборка была проверена на сбалансированность в зависимости от количества пациентов с исходом – 1 (есть дислипидемия) и 0 (нет дислипидемии). Для балансировки базы данных в части обучающей выборки в целях получения более стабильной модели прогнозирования был использован метод SMOTE (Synthetic Minority Over-sampling Technique).
Для построения модели предсказания наличия/отсутствия исхода были применены алгоритмы машинного обучения, позволяющие построить «Дерево решений». Алгоритм «Дерево решений» выполняет выбор переменных для построения прогностической модели самостоятельно на основе снижения значения энтропии, являющейся мерой беспорядка или неизвестности.
Построенная модель была протестирована с использованием независимого тестового набора. Для оценки качества построенной модели были использованы следующие метрики качества на обучающей и тестовой выборках: точность, чувствительность, специфичность и ROC-AUC, где ROC – Receiver Operating Characteristic (рабочая характеристика приемника); AUC – Area Underthe Curve (площадь под кривой). Метрики были рассчитаны с доверительным интервалом, составлявшим 95%. Рассчитывали 95%-ный доверительный интервал методом Бутстреп (Bootstrap) при выборке 1000 экземпляров. Также для максимизации чувствительности и специфичности было определено пороговое значение для наличия/отсутствия изучаемого исхода.
Для оценки клинической полезности модели проведен анализ кривой принятия решений (DCA – Decision Curve Analysis) путем расчета чистых преимуществ модели прогнозирования по сравнению с решением «лечить всех» и «не лечить никого».
Результаты
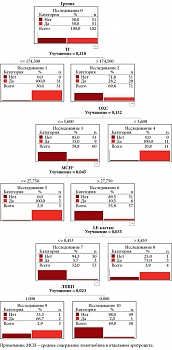
Алгоритм, построенный методом машинного обучения «Дерево решений», позволяет анализировать показатели липидного статуса и гемограммы у пациентов с ОЛ, получивших дополнительно к ВДХТ алло-ТГСК, в зависимости от их влияния на необходимость начала профилактики дислипидемии (рис. 1).
Как видно из анализа данного алгоритма, наиболее вероятна необходимость профилактических мероприятий против нарушений липидного статуса у пациентов с ОЛ после алло-ТГСК со сниженным уровнем тромбоцитов, а при нормальном уровне тромбоцитов – с повышенными показателями ОХС [6]. При этом меньшая вероятность профилактических мероприятий отмечена у лиц с ОЛ, получивших алло-ТГСК, при наличии нормального уровня тромбоцитов и ОХС.
Разработанная прогностическая модель показывает риск развития дислипидемии у пациентов с ОЛ, получивших патогенетическую терапию, включающую ВДХТ и алло-ТГСК, и необходимость начала профилактических мероприятий. Оценка эффективности, качества и информативности данной математической модели прогнозирования нарушений липидного обмена у пациентов с ОЛ проведена с расчетом вероятности потребности в профилактических мероприятиях, где в качестве исхода выделено два состояния: 1 – есть дислипидемия, 0 – нет дислипидемии.
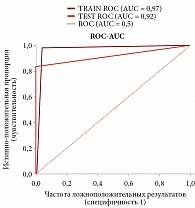
Для апробации полученного алгоритма произведен анализ полученных данных на основании результатов липидного спектра и гемограммы у пациентов с ОЛ после алло-ТГСК. Для каждого пациента рассчитаны значения, определяющие вероятность развития дислипидемии и необходимости начала профилактических мероприятий. На основании полученных результатов построена ROC-кривая для данной модели прогноза и определены значения площади под этой кривой (рис. 2).
Как видно из рис. 2, анализ полученных данных показал, что алгоритм прогноза риска развития дислипидемии у пациентов с ОЛ после алло-ТГСК имеет площадь под ROC-кривой 0,92, что получено в случае бинарного учета параметров, среди которых учитывается разделение пациентов по наличию/отсутствию признаков нарушений липидного обмена, где площадь под ROC-кривой более 0,97. Для данной прогностической модели была определена точка отсечения, позволяющая разделить пациентов на группы с благоприятным и неблагоприятным исходами. Указанная точка отсечения определяет ценность модели и чувствительность, значение данного параметра в нашей модели – 0,5: при врожденных пороках развития (ВПР) < 0,5 существует низкий риск развития дислипидемии; при ВПР ≥ 0,5 определяется высокий риск развития дислипидемии.
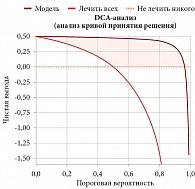
Проведен анализ кривой принятия решения (DCA) для оценки клинической полезности прогностической модели. DCA-кривая количественно оценивает чистые преимущества модели при ее различных пороговых вероятностях, уравновешивая между собой ложноположительные и положительные результаты [7]. Данная кривая помогает определить клинические значимые пороговые значения, в которых модель показывает преимущества при принятии решения.
На рис. 3 показана номограмма DCA, демонстрирующая клиническую пользу чистой выгоды от прогностической модели. В диапазоне пороговых вероятностей значений она составляет от 0 до 1 для тестовой и обучающей выборок, в которых модель имеет бóльшую ценность, чем решение «лечить всех» или «не лечить никого». При этом кривая DCA представляет собой изображение кривой принятия решения, что позволяет применять результаты модели.
Проведена оценка эффективности разработанной модели прогноза оценки риска развития дислипидемии у пациентов с ОЛ, получивших алло-ТГСК, с расчетом ее информативности, параметров чувствительности и точности.
Как видно из таблицы, полученный алгоритм прогноза развития дислипидемии у пациентов с ОЛ после алло-ТГСК обладает хорошим качеством (80–100%), имеет высокие значения точности (88,5%), специфичности (100%) и чувствительности (83,3%). При этом высокая чувствительность и специфичность указывают на высокое качество данной модели по прогнозированию того, что пациенту требуется профилактика дислипидемии. Полученный алгоритм оценки риска дислипидемии имеет отличное качество, ROC-AUC составляет на тестовой выборке 0,92.
Таким образом, данная модель прогнозирует риск развития дислипидемии у данной категории лиц на обучающей выборке:
- с точностью (%) 97,1 [94,1; 99,0];
- чувствительностью (%) 98,0 [94,3; 100,0];
- специфичностью (%) 96,1 [91,1; 100,0,];
- ROC-AUC (%) 97,1 [94,2; 99,2].
Данная математическая модель оценки риска развития дислипидемии позволяет определить необходимость начала проатерогенных профилактических мероприятий у пациентов с ОЛ, которые получили дополнительно к ВДХТ алло-ТГСК.
Обсуждение
Прогнозирование сердечно-сосудистых событий у пациентов с ОЛ, получивших алло-ТГСК, по-прежнему остается нерешенной проблемой, поскольку не всегда удается объяснить высокий кардиоваскулярный риск влиянием «традиционных» факторов риска или противоопухолевой терапии.
Дислипидемии являются основной причиной сердечно-сосудистых заболеваний, в основе которых лежит нарушение липидного профиля с высоким уровнем ТГ, ОХС или ЛПНП либо низким уровнем ЛПВП. Исследования показали, что уровень ЛПНП ассоциируется с повышенным риском развития ишемической болезни сердца [8].
Пациенты с ОЛ, перенесшие алло-ТГСК, обычно относительно молодые. Выживаемость их выше, чем у лиц, перенесших только паллиативную химиотерапию. Своевременная оценка риска развития дислипидемии у данной группы пациентов может улучшить их долгосрочный прогноз, уменьшить риск развития осложнений в позднем посттрансплантационном периоде.
По данным исследования 2001 г. Armenian S.H. и соавт., согласно оценке поздних сердечно-сосудистых осложнений у выживших после ТГСК, среди 3287 исследуемых у 44 (69,8%) отмечались коронарные и у 19 (30,2%) – цереброваскулярные осложнения. При этом наличие двух и более факторов риска (дислипидемия, ожирение, артериальная гипертензия и сахарный диабет) в 5,2 раза увеличивало риск развития ССЗ [9].
Оценка абсолютного риска развития дислипидемии – необходимого определения показаний для профилактики обычно основывается на моделях прогнозирования, разработанных на основе данных проспективных когортных исследований [8]. Однако в нашем исследовании для изучения связи некоторых факторов с дислипидемией использовалась модель математического прогнозирования «Дерево решений». Результаты, полученные на основе обучающего набора данных, выявили общие параметры, значительно связанные с повышением риска развития дислипидемий (уровни тромбоцитов, ОХС, MCH, лейкоцитов и ЛПВП).
В немногочисленных исследованиях показано, что нарушение липидного профиля у пациентов с ОЛ связано с высокой токсичностью проводимых противоопухолевых схем лечения и является следствием неопластического процесса [10]. Однако в данных работах анализ взаимодействия параметров липидного профиля, общего анализа крови и оценки риска развития дислипидемии не проводился.
Математическая модель позволяет проанализировать послойно с выявлением связи между параметрами липидного профиля, гемограммы и оценкой риска развития дислипидемии у пациентов с ОЛ, получивших алло-ТГСК. Созданная нами модель оценки рисков развития дислипидемий на основе клинико-лабораторных данных обладает высокими параметрами чувствительности, точности и специфичности.
В целом прогнозирование дислипидемий у лиц с ОЛ после алло-ТГСК является основанием для разработки мероприятий, направленных на снижение кардиоваскулярного риска у данной группы пациентов. Таким образом, необходимо отметить, что использование прогностической модели оценки риска развития дислипидемии у пациентов с ОЛ после алло-ТГСК может способствовать снижению ССЗ в позднем посттрансплантационном периоде.
Благодаря доступности данной шкалы с учетом используемых параметров крови ее могут применять не только врачи-гематологи, которые впоследствии длительно наблюдают данную группу пациентов, но и врачи других специальностей, включая кардиологов, неврологов, эндокринологов.
Разработанная нами модель демонстрирует хорошие результаты и позволяет прогнозировать дислипидемию у пациентов с ОЛ. Однако необходимо отметить, что, согласно современным рекомендациям, изучение липидного профиля не входит в стандарт оказания помощи пациентам с ОЛ, получившим алло-ТГСК.
Заключение
Разработанная с помощью методов машинного обучения прогностическая модель развития дислипидемии у пациентов с ОЛ, получивших патогенетическую терапию, включавшую и алло-ТГСК, позволяет с высокой точностью оценить риск развития дислипидемии. Благодаря этому открывается возможность разработки у данной категории пациентов индивидуализированных профилактических программ, направленных на предотвращение заболеваний, патогенетически связанных с атеросклерозом.
Конфликт интересов. Авторы не заявили о возможном конфликте интересов.
Финансирование. Авторы заявляют об отсутствии финансирования при проведении исследования.
E.A. Praskurnichiy, V.O. Dzidzaria, Yu.S. Kitaeva
Pirogov Russian National Research Medical University
State Scientific Center of the Russian Federation — Federal Medical Biophysical Center Named after A.I. Burnazyan
Contact person: Vera O. Dzidzaria, vera-dzidzaria@mail.ru
Antitumor therapy in combination with allogeneic hematopoietic stem cell transplantation has been successfully used in patients with acute leukemia, but it is often complicated by the development of cardiovascular diseases. Dyslipidemia is one of the risk factors for the development of cardiovascular complications in patients after pathogenetic therapy of acute leukemia. Predicting the development of lipid metabolism disorders in patients with acute leukemia after pathogenetic therapy can have a positive effect on their overall prognosis and quality of life.
The aim is to develop an algorithm for assessing the risk of dyslipidemia in patients with acute leukemia who have received pathogenetic therapy using mathematical modeling programs.
Material and methods. A single-stage prospective study of 39 patients with acute leukemia who received pathogenetic therapy, including high-dose chemotherapy and allogeneic hematopoietic stem cell transplantation, was conducted. The control group consisted of 30 patients without a history of hematological and cardiovascular pathology. All study participants underwent an assessment of the lipid spectrum and a general blood test. The construction of a mathematical model for predicting the need for preventive measures for lipid status disorders was carried out using the Decision Tree machine learning algorithm, which has a structure corresponding to the need to make a decision on the initiation of dyslipidemia prevention.
Results. The decision tree makes it possible to analyze lipid status and hemograms in patients with acute leukemia who have received pathogenetic therapy and identify the need for dyslipidemia prevention. The need for preventive measures for lipid status disorders in patients with acute leukemia after allogeneic hematopoietic stem cell transplantation is most likely with a reduced platelet count, and with a normal platelet count – with an increase in total cholesterol. The obtained mathematical model predicts the risk of dyslipidemia in this category of individuals in the training sample with an accuracy of 97.1%, sensitivity of 98.0% and specificity of 96.1%, ROC-AUC of 97.1%.
Discussion. Timely assessment of the risk of dyslipidemia in these patients can improve their long-term prognosis and reduce the risk of complications in the late post-transplant period. The prediction of dyslipidemia after allogeneic hematopoietic stem cell transplantation is the basis for the development of measures aimed at reducing cardiovascular risk in this cohort of patients.
Conclusion. The prognostic model of dyslipidemia development, developed using machine learning methods, makes it possible to accurately assess the risk of developing this complication and makes it possible to develop individualized preventive programs aimed at preventing the development of atherosclerosis.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.


