Распределение жировой ткани и поражение сердца как органа-мишени у пациентов с артериальной гипертензией
- Аннотация
- Статья
- Ссылки
- English
Цель. Сравнить распределение жировой ткани и показатели системного провоспалительного статуса у пациентов среднего возраста с неосложненной АГ в зависимости от наличия гипертрофии левого желудочка (ГЛЖ).
Материал и методы. В одномоментное ретроспективное когортное исследование включены данные историй болезни 53 пациентов с эссенциальной АГ, медиана возраста 52 (42; 61,5) года; 52,8% мужчин. Анализировались результаты клинического осмотра, эхокардиографии с оценкой толщины эпикардиальной жировой ткани (ЭЖТ), биоимпедансного анализа состава тела, лабораторного исследования крови. Пациенты были разделены на группы с ГЛЖ (n = 20) и без таковой (n = 33).
Результаты. У пациентов с ГЛЖ, в сравнении с пациентами без таковой, отмечены статистически значимо более высокие значения индекса массы тела – 35,1 (33,9; 36,8) и 28,4 (25,8; 32,5) кг/м2 соответственно, р < 0,001, окружности талии у мужчин (р < 0,001) и женщин (р = 0,01), толщины ЭЖТ – 0,54 (0,4; 0,7) и 0,4 (0,3; 0,5) см соответственно, р = 0,006, массы – 35,7 ± 7,4 и 25,4 ± 8,0 кг соответственно (р < 0,001) и доли жировой ткани в составе тела – 37,9 ± 7,7 и 30,0 ± 9,7% соответственно (р = 0,005), а также более высокая частота абдоминального ожирения. Среди индексов воспаления отношение моноцитов к холестерину липопротеидов высокой плотности было статистически значимо (p = 0,049) больше у пациентов с ГЛЖ – 0,5 (0,4; 0,7) в сравнении с группой без таковой – 0,4 (0,3; 0,6).
Заключение. У пациентов среднего возраста на начальных стадиях АГ в развитие поражения сердца могут вносить вклад метаболические и иммуновоспалительные факторы, помимо непосредственно уровня АД.
Цель. Сравнить распределение жировой ткани и показатели системного провоспалительного статуса у пациентов среднего возраста с неосложненной АГ в зависимости от наличия гипертрофии левого желудочка (ГЛЖ).
Материал и методы. В одномоментное ретроспективное когортное исследование включены данные историй болезни 53 пациентов с эссенциальной АГ, медиана возраста 52 (42; 61,5) года; 52,8% мужчин. Анализировались результаты клинического осмотра, эхокардиографии с оценкой толщины эпикардиальной жировой ткани (ЭЖТ), биоимпедансного анализа состава тела, лабораторного исследования крови. Пациенты были разделены на группы с ГЛЖ (n = 20) и без таковой (n = 33).
Результаты. У пациентов с ГЛЖ, в сравнении с пациентами без таковой, отмечены статистически значимо более высокие значения индекса массы тела – 35,1 (33,9; 36,8) и 28,4 (25,8; 32,5) кг/м2 соответственно, р < 0,001, окружности талии у мужчин (р < 0,001) и женщин (р = 0,01), толщины ЭЖТ – 0,54 (0,4; 0,7) и 0,4 (0,3; 0,5) см соответственно, р = 0,006, массы – 35,7 ± 7,4 и 25,4 ± 8,0 кг соответственно (р < 0,001) и доли жировой ткани в составе тела – 37,9 ± 7,7 и 30,0 ± 9,7% соответственно (р = 0,005), а также более высокая частота абдоминального ожирения. Среди индексов воспаления отношение моноцитов к холестерину липопротеидов высокой плотности было статистически значимо (p = 0,049) больше у пациентов с ГЛЖ – 0,5 (0,4; 0,7) в сравнении с группой без таковой – 0,4 (0,3; 0,6).
Заключение. У пациентов среднего возраста на начальных стадиях АГ в развитие поражения сердца могут вносить вклад метаболические и иммуновоспалительные факторы, помимо непосредственно уровня АД.

Введение
Артериальная гипертензия (АГ) остается одной из наиболее значимых медико-социальных проблем, выступая ведущим фактором риска развития сердечно-сосудистых осложнений, инвалидизации и смертности населения трудоспособного возраста [1]. Распространенность АГ в мире достигает 30–45% среди взрослого населения [1], а в Российской Федерации превышает 53% [2]. Это приводит к тому, что примерно каждое пятое фатальное событие в мире ассоциировано с повышенным артериальным давлением (АД) [3]. Данные факты в свою очередь диктуют необходимость постоянного поиска новых патогенетических звеньев развития и прогрессирования органных поражений при АГ, поскольку органопротекция и регресс изменений в органах-мишенях АГ рассматривается как одна из центральных задач при ведении пациентов с этим заболеванием после непосредственно достижения целевых уровней АД [4].
Признаком поражения сердца как органа-мишени АГ является гипертрофия левого желудочка (ГЛЖ), которая изначально формируется как адаптивный ответ миокарда на персистирующую перегрузку давлением и объемом, а в последующем трансформируется в самостоятельный прогностически неблагоприятный фактор риска [5], ассоциирующийся с увеличением риска развития инфаркта миокарда, инсульта, фатальных аритмий и внезапной сердечной смерти, независимо от уровня АД [6, 7]. Таким образом, ГЛЖ является не просто морфологическим феноменом, а интегральным маркером неблагоприятного прогноза, что делает изучение механизмов ее развития и прогрессирования первостепенной задачей.
Вместе с тем в последние десятилетия внимание исследователей все больше привлекает роль метаболических нарушений, в частности ожирения, в патогенезе АГ и сопутствующего структурного ремоделирования сердца [8]. Эпидемиологические данные свидетельствуют о том, что не менее 70% пациентов с АГ имеют избыточную массу тела или ожирение, что формирует особый кардиометаболический фенотип заболевания [9]. При этом ключевое значение имеет не столько общее количество жировой ткани, оцениваемое по индексу массы тела (ИМТ), сколько ее распределение: доказано, что именно висцеральное, и в частности абдоминальное, ожирение, диагностируемое по увеличению окружности талии (ОТ), является мощным независимым фактором сердечно-сосудистого риска [10]. Активная эндокринная и паракринная функция висцеральной жировой ткани заключается в секреции широкого спектра биологически активных веществ – адипокинов, свободных жирных кислот, провоспалительных цитокинов, что формирует состояние хронического системного воспаления низкой степени выраженности. Этот процесс, вероятно, лежит в основе взаимосвязи между ожирением, инсулинорезистентностью и дисфункцией эндотелия, усугубляя течение АГ [11].
Особый интерес в контексте поражения сердца представляет эпикардиальная жировая ткань (ЭЖТ), являющаяся депо висцерального жира, окружающим миокард [12]. ЭЖТ имеет общее кровоснабжение с миокардом и способна через паракринные механизмы непосредственно неблагоприятно влиять на кардиомиоциты. Потенциальный механизм этого влияния связывают не только с механическим воздействием ЭЖТ на миокард, но и с локальной секрецией провоспалительных медиаторов, таких как, например, фактор некроза опухоли альфа и интерлейкин 6, которые могут инфильтрировать стенку желудочка и запускать процессы фиброза и гипертрофии [12, 13].
Наряду с оценкой распределения жировой ткани современная кардиология все шире использует гематологические индексы системного воспаления, рассчитываемые на основе клинического анализа крови, поскольку они могут иметь прогностическую значимость при различных сердечно-сосудистых заболеваниях, включая атеросклероз и в дальнейшем формирование хронической сердечной недостаточности [14, 15]. Данные показатели отражают дисбаланс между провоспалительными и противовоспалительными компонентами иммунной системы и, являясь стабильными и воспроизводимыми маркерами, могут служить удобным инструментом для стратификации риска [14, 15]. Однако их роль во взаимосвязи с особенностями распределения жировой ткани и развитием ГЛЖ у пациентов с неосложненной АГ мало изучена.
Таким образом, формирование ГЛЖ при АГ представляет собой многокомпонентный процесс, в котором классическая гемодинамическая нагрузка может потенцироваться и модулироваться метаболическими и иммуновоспалительными факторами. Комплексный анализ, включающий оценку характера распределения жировой ткани (с использованием измерения ОТ, расчета ИМТ, биоимпедансометрии и эхокардиографии с измерением ЭЖТ) в сочетании с определением гематологических индексов воспаления у пациентов с неосложненной АГ, может потенциально выявить дополнительные патогенетические механизмы структурно-функционального ремоделирования миокарда и открыть перспективы для разработки превентивных стратегий, нацеленных не только на контроль АД, но и на коррекцию метаболических и воспалительных нарушений с целью предотвращения прогрессирования поражения сердца и улучшения долгосрочного прогноза у данной категории больных. Принимая во внимание данные факты, мы провели исследование, целью которого стал сравнительный анализ распределения жировой ткани и показателей провоспалительного статуса у пациентов среднего возраста с неосложненной АГ в зависимости от наличия ГЛЖ.
Материал и методы
Протокол исследования одобрен Независимым этическим комитетом при ФГБОУ ДПО РМАНПО Минздрава России (протокол № 15 от 18.12.2024 г.).
Проведено одномоментное ретроспективное когортное исследование, в которое включены данные историй болезни 53 пациентов с эссенциальной АГ, обратившихся за медицинской помощью в ООО «Скандинавский центр здоровья» (клиническая база кафедры терапии и полиморбидной патологии им. акад. М.С. Вовси Российской медицинской академии непрерывного профессионального образования).
В исследование включены пациенты в возрасте 18 лет и старше с эссенциальной АГ.
Критерии невключения. Возраст менее 18 лет; беременность, лактация; симптоматическая артериальная гипертензия; хронические и острые формы ишемической болезни сердца; перенесенные в анамнезе инфаркт миокарда или инсульт; кардиомиопатии; наличие жидкости в полости перикарда; хроническая ревматическая болезнь сердца; фибрилляция и трепетание предсердий; блокада левой ножки пучка Гиса и атриовентрикулярные блокады II–III степени; хроническая сердечная недостаточность с низкой фракцией выброса (менее 40%); тромбоэмболия легочной артерии; бронхиальная астма; хроническая обструктивная болезнь легких; сахарный диабет 1–2 типа; наличие у пациента онкологического заболевания; расчетная скорость клубочковой фильтрации (рСКФ) < 30 мл/мин/1,73 м2); получение заместительной почечной терапии; врожденные или приобретенные пороки сердца; цирроз печени В или С класса по классификации Чайлда – Пью; наличие системных иммуновоспалительных заболеваний (моногенные аутовоспалительные заболевания (периодическая болезнь, криопиринипатии, недостаточность мевалонаткиназы и другие); полигенные аутовоспалительные заболевания (болезнь Стилла, синдром Шницлер); воспалительные заболевания кишечника, подагра и другие, смешанные заболевания (болезнь Бехчета, псориаз, реактивный артрит, анкилозирующий спондилит); полигенные аутоиммунные заболевания (ревматоидный артрит, системная красная волчанка, миастения, АНЦА-ассоциированные васкулиты), моногенные аутоиммунные заболевания (аутоиммунный лимфопролиферативный синдром и другие); злоупотребление алкоголем, и/или наркотическими средствами, и/или психоактивными веществами; психические и поведенческие расстройства, которые могут оказать влияние на результаты исследования.
В обследование входили: клинический осмотр участников исследования с оценкой показателей офисного АД согласно клиническим рекомендациям Минздрава России [4], суточное мониторирование артериального давления (монитор ABPM-05, Meditech), клинический анализ крови (гематологический анализатор MEK-7300K, Nihon Kohden), биохимический анализ крови (биохимические анализаторы RХ-IMOL, Randox, ARCHITECT, Abbott; платформа Cobas 8000 c биохимическим модулем с702, Roche), клинический анализ мочи, трансторакальная эхокардиография (ультразвуковой сканер Affiniti 50, Philips), регистрация 12-канальной электрокардиограммы (электрокардиограф EASY ECG, ATES DIAGNOSTIC), биоимпедансный анализ состава тела (анализатор состава тела InBody 230, InBody).
На основании данных клинического и биохимического исследований проведен расчет следующих индексов системного воспаления:
- SII (индекс системного иммунного воспаления; англ. Systemic immune-inflammation index) – количество тромбоцитов × количество нейтрофилов / количество лимфоцитов [16–18];
- SIRI (индекс системного воспалительного ответа; англ. Systemic inflammation response index) – количество нейтрофилов × количество моноцитов / количество лимфоцитов [17, 18];
- AISI (совокупный системный индекс воспаления; англ. Aggregate index of systemic inflammation) – количество нейтрофилов × количество моноцитов × количество тромбоцитов / количество лимфоцитов [18];
- MHR (англ. Monocyte/high-density lipoprotein cholesterol ratio) – отношение моноцитов к холестерину липопротеидов высокой плотности [19];
- PLR (англ. Platelet/lymphocyte ratio) – отношение количества тромбоцитов к количеству лимфоцитов [19];
- NLR (англ. Neutrophil/lymphocyte ratio) – отношение количества нейтрофилов к количеству лимфоцитов [19].
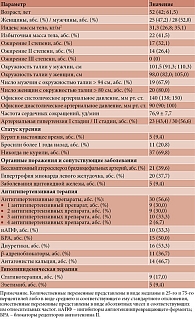
Исходная характеристика пациентов представлена в табл. 1.
Среди включенных в исследование пациентов в несколько большем количестве (52,8%) были представлены мужчины. Обращает на себя внимание преобладание лиц с ожирением (58,5% участников), в том числе с абдоминальным (67,9% среди мужчин и 80,0% – среди женщин). При этом участники исследования, согласно анализируемым историям болезни, в большинстве своем не курили (69,8%). Антигипертензивные препараты (АГП) принимали 56,6% участников исследования, наиболее часто используемыми классами препаратов были блокаторы рецепторов ангиотензина II (50,0% пациентов, принимающих АГП), диуретики (53,3%) и антагонисты кальция (46,7%).
В дальнейшем, в зависимости от наличия ГЛЖ согласно индексу массы миокарда левого желудочка (иММЛЖ): критерием ГЛЖ [4] для мужчин были его значения, превышающие 50 г/м2,7, для женщин – превышающие 47 г/м2,7, пациенты были разделены на две группы: с наличием ГЛЖ (n = 20) и без таковой (n = 33), и между ними был проведен сравнительный анализ содержания и распределения жировой ткани в организме, а также выполнена оценка системного провоспалительного статуса.
Статистический анализ данных выполнен с использованием программы IBM SPSS Statistics Base 27.0. Нормальность распределения данных оценивалась с помощью критерия Шапиро – Уилка. Непрерывные переменные представлены в виде медианы с указанием 25-го и 75-го перцентилей. При нормальном распределении количественных переменных достоверность различий между группами анализировалась с помощью t-критерия Стьюдента, в противном случае применялся критерий Манна – Уитни. В случае качественных признаков статистическая значимость различий определялась с помощью точного критерия Фишера и критерия χ2. Различия считались статистически значимыми при p < 0,05.
Результаты
Группы пациентов с наличием ГЛЖ и без таковой были сопоставимы по полу (женщины – 50,0% и 45,5% соответственно, р = 0,970), возрасту (51 (41; 56,5) и 56,5 (43,2; 65) года соответственно, р = 0,270), уровню офисного систолического АД (145 (135; 150) и 140 (138; 147,5) мм рт. ст. соответственно, р = 0,443) и диастолического АД (90 (85; 110) и 90 (90; 100) мм рт. ст. соответственно, р = 0,461).
Данные сравнительного анализа параметров конституционального, висцерального ожирения и состава тела пациентов в группах с наличием ГЛЖ и без таковой представлены в табл. 2. В группе пациентов с наличием ГЛЖ отмечено статистически значимо более высокое значение ИМТ (р < 0,001), ОТ среди мужчин и женщин (р < 0,001 и р = 0,010 соответственно) и толщины ЭЖТ (р = 0,006). Кроме того, в первой группе в сравнении со второй статистически значимо большее количество мужчин и женщин имели абдоминальное ожирение (100% случаев в группе с ГЛЖ у лиц обоего пола, р < 0,001), а также зарегистрирована статистически значимо бóльшая масса жировой ткани в теле согласно биоимпедансному анализу (р < 0,001) и статистически значимо бóльшая доля содержания жира (%) в организме (р = 0,005) (см. табл. 2).
При сравнительном анализе значений индексов системного воспаления в группах с наличием ГЛЖ и без таковой выявлено единственное статистически значимое различие: в первой группе в сравнении со второй индекс MHR был статистически значимо больше (0,5 [0,4; 0,7] и 0,4 [0,3; 0,6] соответственно, р = 0,049). Иных статистически значимых различий между группами не обнаружено. Следует также отметить, что среди пациентов с ГЛЖ по сравнению с лицами без нее наблюдалась тенденция к более высокому уровню высокочувствительного С-реактивного белка: 0,5 [0,2; 1,63] и 0,3 [0,1; 1,0] мг/л соответственно (р = 0,274).
Обсуждение
Результаты настоящего исследования демонстрируют, что у пациентов с неосложненной АГ наличие ГЛЖ ассоциируется с более выраженными признаками конституционального (согласно ИМТ), абдоминального и висцерального ожирения, включая бóльшую толщину ЭЖТ и бóльшую долю жировой ткани в структуре состава тела. Эти данные согласуются с накопленными сведениями о тесной взаимосвязи между ожирением, в особенности его висцеральным вариантом, и структурным ремоделированием сердца в условиях кардиометаболического фенотипа сердечно-сосудистых факторов риска [9, 20, 21].
Так, в одном из систематических обзоров и метаанализов оценивались структурные изменения ЛЖ согласно данным эхокардиографии у взрослых лиц с ожирением (ИМТ ≥ 30 кг/м2): в анализ были включены 22 исследования, из которых в 15 работах имелись сведения о распространенности ГЛЖ в группах лиц с ожирением (n = 4999) и без такового (n = 6623) [21]. В результате было установлено, что ожирение выступает статистически значимым предиктором наличия ГЛЖ: отношение шансов (ОШ) 4,19 (95%-ный доверительный интервал (95% ДИ) 2,67–6,53; p < 0,01). По данным метарегрессионного анализа (n = 2214; 14 исследований) выявлена прямая корреляционная взаимосвязь между ИМТ и массой миокарда левого желудочка (p < 0,01).
Вклад различных типов ожирения в сочетании с АГ в риск развития ГЛЖ изучен в популяционном исследовании, проведенном в Китае, в которое вошли 9134 человека в возрасте ≥ 35 лет, ГЛЖ имелась у 10,0% из них (n = 915) [22]. Среди прочих результатов было обнаружено, что после поправки на возраст, образование, уровень в крови мочевой кислоты, глюкозы, триглицеридов, холестерина липопротеидов низкой и высокой плотности, семейный статус, образование, рСКФ, статус курения, употребление алкоголя, наличие АГ (как у пациента, так и в семейном анамнезе), физическую активность и прием АГП статистически значимыми (в публикации для всех значимых данных значение р унифицировано и представлено исключительно в виде p < 0,05) предикторами наличия ГЛЖ являлись: АГ – ОШ 3,94 (95% ДИ 3,27–4,75), конституциональное ожирение (согласно ИМТ) – ОШ 1,90 (95% ДИ 1,60–2,26), а также висцеральное ожирение, причем значимость сохранялась вне зависимости от используемого критерия этого состояния – для ОТ ОШ 1,45 (95% ДИ 1,25–1,69), для отношения ОТ/рост – ОШ 1,69 (95% ДИ 1,43–2,00), для отношения ОТ/окружность бедра – ОШ 1,54 (95% ДИ 1,33–1,79). При добавлении в ту же модель регрессионного анализа в качестве независимого предиктора факта наличия АГ (помимо ожирения) риск ГЛЖ не только сохранял свою статистическую значимость, но и существенно возрастал во всех возрастных группах (наиболее выраженно среди лиц в возрасте 35–45 лет): для ожирения, согласно ИМТ, ОТ, отношений ОТ/рост, ОТ/окружность бедра соответствующие ОШ составили 14,14; 10,84; 7,97 и 9,95.
В доступной литературе имеются единичные данные, согласующиеся с полученными нами результатами об увеличении при наличии ГЛЖ жирового компонента в составе тела согласно биоимпедансному анализу. Так, изучена взаимосвязь между составом тела и иММЛЖ у пациентов с впервые диагностированной АГ: в исследование включены 120 пациентов (средний возраст 45 ± 8 лет, 50% – мужчины), обратившихся в нефрологическую клинику [23]. Авторы выявили, что у женщин по сравнению с мужчинами были статистически значимо выше средние значения отношения ОТ/окружность бедра (88 ± 10 и 82 ± 9 соответственно), ИМТ (28,4 ± 1,8 и 26,3 ± 3,6 кг/м2 соответственно), доли жировой ткани в составе тела (38,8 ± 11,8% и 32,6 ± 12,0% соответственно), систолического АД (142,8 ± 12,8 и 136,4 ± 10,8 мм рт. ст. соответственно), диастолического АД (88,5 ± 10,0 и 83,9 ± 11,1 мм рт. ст. соответственно) и иММЛЖ (94,8 ± 13,1 и 89,2 ± 14,6 г/м2,7 соответственно). Все участники исследования были разделены на три группы в зависимости от доли жировой ткани в составе тела по данным биоимпедансного анализа. Обращает на себя внимание тот факт, что в группе с наибольшим содержанием жировой ткани были статистически значимо (p < 0,05 во всех случаях) выше возраст, ИМТ, уровень лейкоцитов, С-реактивного белка, триглицеридов, а также преобладали женщины. Однако наиболее важным результатом стало увеличение иММЛЖ по мере роста содержания жира в организме: в группе 1 (площадь висцеральной жировой области (ВЖТ) ≤ 102,6 см2) иММЛЖ составил 88,9 ± 13,1 г/м2,7, в группе 2 (площадь ВЖТ – 102,6–127,1 см2) – 92,6 ± 10,1 г/м2,7, в группе 3 (площадь ВЖТ > 127,1 см2) – 95,2 ± 8,9 г/м2,7 (p < 0,05). Согласно данным логистического регрессионного анализа, доля содержания жировой ткани в составе тела входила в число независимых факторов, ассоциированных с ростом иММЛЖ. Сходные результаты получены и в другом исследовании [24].
Наконец, в нашем исследовании у пациентов с ГЛЖ была обнаружена статистически значимо бóльшая толщина ЭЖТ в сравнении с лицами без ГЛЖ. Это также согласуется с данными доступной литературы. Так, в работе R. Zhu и соавт. оценивали возможную взаимосвязь между индексированным объемом ЭЖТ (в публикации не указано, по какому именно традиционному показателю выполнялась индексация – росту или площади поверхности тела) и ГЛЖ у пациентов с АГ [25]. В отличие от настоящего исследования в рассматриваемой работе для визуализации сердца использовали магнитно-резонансную томографию, а не эхокардиографию. В исследование были включены 209 пациентов с АГ (из них 133 человека с ГЛЖ, остальные – без нее) и 50 здоровых лиц без АГ и ГЛЖ (контрольная группа). Согласно полученным результатам, у пациентов с АГ и сопутствующей ГЛЖ были выявлены статистически значимо бóльшие значения индексированного объема ЭЖТ (79,05 ± 17,16 мл) в сравнении с лицами с АГ без ГЛЖ (64,95 ± 15,70 мл; р < 0,001), а также в сравнении с контрольной группой (51,66 ± 13,01 мл; р < 0,001). При этом следует подчеркнуть, что между указанными группами отсутствовали статистически значимые различия значений ИМТ. В дополнение к этому у пациентов с АГ и ГЛЖ, по сравнению с пациентами с АГ без ГЛЖ, отмечены более выраженный диффузный фиброз миокарда и сниженная деформация (анализировался продольный, радиальный и циркулярный стрейн) левого желудочка (по всем показателям p < 0,001). При многофакторном логистическом регрессионном анализе установлено, что индексированный объем ЭЖТ (p = 0,001), объем внеклеточного соединительнотканного матрикса (p = 0,012) и глобальная продольная деформация (p = 0,024) являются независимыми факторами, ассоциированными с ГЛЖ. В рамках статистического медиационного анализа дополнительно показана роль величин объема внеклеточного матрикса, нативного показателя Т1, глобального продольного, радиального, циркулярного стрейна как факторов, опосредующих взаимосвязь между увеличенным объемом ЭЖТ и ГЛЖ (p < 0,05 во всех случаях).
В настоящем исследовании также обнаружено, что из всего спектра рассчитанных индексов системного воспаления (SII, SIRI, AISI, PLR, MHR, NLR) статистически значимые различия между группами пациентов с ГЛЖ и без таковой наблюдались только для индекса MHR, который был значимо выше в группе с ГЛЖ. Этот индекс интегрально отражает два патологических процесса: активацию моноцитарного звена иммунитета (как маркера системного воспаления) и снижение уровня антиатерогенных липопротеидов высокой плотности [26]. Взаимосвязь МНR c наличием ГЛЖ была также подтверждена в исследовании W. Sang и соавт., в которое вошли данные пациентов молодого и среднего возраста (от 18 до 65 лет) с АГ; цитируемое исследование было ретроспективным [26]. На основании данных иММЛЖ пациенты были разделены на группу с ГЛЖ (n = 98) и группу без таковой (n = 196): в группе с ГЛЖ значения индекса MHR были статистически значимо выше по сравнению с группой сравнения – 0,47 ± 0,11 против 0,33 ± 0,12 соответственно (р < 0,001), а в рамках корреляционного анализа подтверждена положительная взаимосвязь между МHR и иММЛЖ (r = 0,381, р < 0,001). Согласно многофакторному логистическому регрессионному анализу, МНR являлся независимым предиктором ГЛЖ (ОШ 2,914; 95% ДИ 2,084–4,068, р < 0,001) после поправки на ИМТ, курение, уровень холестерина липопротеидов высокой плотности и ряд прочих факторов. Согласно ROC-анализу, значение MHR, равное 0,37, c чувствительностью 93,9% и специфичностью 75,5%, служило признаком возможного наличия ГЛЖ у пациентов.
В нашем исследовании отсутствовали статистически значимые различия в прочих индексах воспаления между группами с ГЛЖ и без таковой. Мы предполагаем, что это может быть объяснено особенностями когорты, которая состояла из пациентов с неосложненной АГ, без сопутствующих установленных атеросклеротических сердечно-сосудистых заболеваний, сахарного диабета и прочих ассоциированных клинических состояний. В подобной популяции потенциально системное воспаление может быть выражено умеренно и не отражаться во взаимосвязи с органными поражениями в широком спектре показателей.
Ожирение, АГ и ГЛЖ образуют тесно взаимосвязанный кардиометаболический континуум, в котором ключевую роль играют именно висцеральные жировые депо и связанное с ними вялотекущее воспаление. По современным эпидемиологическим и экспериментальным данным убедительно показано, что не столько общая масса жировой ткани, сколько ее распределение – преимущественно висцеральное, и в особенности эпикардиальное, – определяет риск ремоделирования миокарда и формирования ГЛЖ у пациентов с АГ [27–30].
Ожирение усиливает гемодинамическую нагрузку на миокард через увеличение объема циркулирующей крови, минутного объема и активацию симпатоадреналовой и ренин-ангиотензин-альдостероновой систем, что ускоряет формирование ГЛЖ [28]. ЭЖТ представляет собой особый вид висцерального жира, локализованный между миокардом и висцеральным листком перикарда и лишенный фасциальной перегородки; это создает уникальные условия для тесного анатомического и функционального взаимодействия с миокардом через паракринные и вазокринные механизмы [31]. ЭЖТ обладает более выраженным провоспалительным фенотипом по сравнению с подкожной жировой тканью: в ней выше экспрессия интерлейкина 6, фактора некроза опухоли альфа, а также снижена экспрессия кардиопротективного адипокина – адипонектина [31].
Современные представления об ЭЖТ как о динамически ремоделирующемся органе подтверждаются данными транскриптомики и липидомики. В частности показано, что эпикардиальные адипоциты сочетают свойства белой и бурой жировой ткани, отличаются высокой экспрессией UCP1 (англ. Uncoupling Protein 1, разобщающий белок 1; ключевой митохондриальный белок бурой и бежевой жировой ткани, играющий важную роль в термогенезе, энергетическом обмене), и при ожирении происходит «сдвиг» к провоспалительному фенотипу с накоплением липотоксичных метаболитов [32]. Подобное ремоделирование и дисфункция ЭЖТ при ожирении включает активацию провоспалительных путей, фиброз стромы и снижение продукции вазодилатирующих и антиоксидантных молекул, что напрямую стимулирует поражение миокарда [33]. Молекулярные механизмы, связывающие висцеральное и эпикардиальное ожирение с ГЛЖ, могут включать в себя каскад взаимосвязанных иммунометаболических процессов: дисфункцию адипоцитов, инфильтрацию жировой ткани воспалительными клетками, активацию врожденных иммунных структур (в частности, NLRP3-инфламмасомы), усиление оксидативного стресса, эндотелиальную дисфункцию и рарефикацию микрососудистой сети [34, 35].
В дополнение к этому висцеральная жировая ткань, в отличие от подкожной, содержит большее количество инфильтрирующих макрофагов и T-клеток, продуцирующих цитокины, которые в свою очередь стимулируют синтез в печени С-реактивного белка и поддерживают системное субклиническое воспаление [28, 36]. Следовательно, ЭЖТ выступает не только пассивным маркером висцерального ожирения, но и активным участником воспалительно-метаболического взаимодействия с миокардом.
Заключение
Таким образом, полученные в настоящем исследовании результаты свидетельствуют о том, что у пациентов среднего возраста на начальных стадиях АГ при наличии ГЛЖ статистически значимо чаще встречается как конституциональное, так и абдоминальное (висцеральное) ожирение, а также статистически значимо более выражена ЭЖТ, выше доля жира в структуре состава тела и более выражены признаки системного воспаления низкой степени интенсивности. Это может указывать на то, что висцеральное ожирение, в особенности толщина ЭЖТ, в сочетании с хроническим низкоинтенсивным воспалением служат одним из ключевых механизмов формирования и прогрессирования ГЛЖ в дополнение непосредственно к уровню АД. Будущие исследования должны быть направлены на уточнение причинно-следственных связей, выявление пороговых значений толщины ЭЖТ и маркеров воспаления, ассоциированных с клинически значимым ремоделированием сердца, а также на разработку таргетных вмешательств, направленных на модификацию фенотипа висцеральной жировой ткани и ЭЖТ.
Yu.S. Moryakova, A.I. Kochetkov, PhD, Ass. Prof., N.E. Gavrilova, PhD, О.D. Ostroumova, PhD, Prof.
Russian Medical Academy of Continuous Professional Education, Moscow
Scandinavian Health Center, Moscow
I.M. Sechenov First Moscow State Medical University, Moscow
Contact person: Olga D. Ostroumova, ostroumova.olga@mail.ru
Arterial hypertension (AH) is often associated with obesity and the presence of cardiometabolic risk factors in patients; however, the complex role of body fat distribution combined with low-grade systemic inflammation in heart damage under conditions of elevated blood pressure (BP) has not been thoroughly studied.
Aim. To compare body fat distribution and systemic pro-inflammatory status in middle-aged patients with uncomplicated AH depending on the presence of left ventricular hypertrophy (LVH).
Material and methods. A cross-sectional retrospective cohort study included data from the medical records of 53 patients with essential AH, median age 52 (42; 61.5) years; 52.8% men. The results of clinical examination, echocardiography with assessment of epicardial fat thickness (EFT), body composition bioimpedance analysis, and laboratory blood tests were analyzed. Patients were divided into groups with LVH (n = 20) and without LVH (n = 33).
Results. In patients with LVH, compared to those without LVH, significantly higher values of body mass index – 35.1 (33.9; 36.8) vs. 28.4 (25.8; 32.5) kg/m², p < 0.001, waist circumference in men (p < 0.001) and women (p = 0.01), EFT – 0.54 (0.4; 0.7) vs. 0.4 (0.3; 0.5) cm, p = 0.006), body fat mass – 35.7 ± 7.4 vs. 25.4 ± 8.0 kg, p < 0.001, and fat percentage – 37.9 ± 7.7% vs. 30.0 ± 9.7%, p = 0.005, were observed, as well as a higher frequency of abdominal obesity. Among the inflammatory indices, the monocyte/high-density lipoprotein cholesterol ratio was significantly higher (p = 0.049) in patients with LVH – 0.5 (0.4; 0.7) compared to those without LVH – 0.4 (0.3; 0.6).
Conclusion. In middle-aged patients with early-stage AH, metabolic and immunoinflammatory factors, in addition to the BP level itself, may contribute to the development of heart damage.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.