количество статей
7414
Загрузка...
Пожалуйста, авторизуйтесь:
Практика
Сердечно-сосудистая форма диабетической автономной нейропатии
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Эндокринология" Спецвыпуск
- Аннотация
- Статья
- Ссылки
В статье рассматриваются особенности диагностики сердечно сосудистой формы ДАН, обсуждаются способы предупреждения развития и прогрессирования этого опасного осложнения сахарного диабета.
На примере нейротропного комплекса витаминов группы B (Мильгамма композитум) показана роль активаторов транскетолазы как патогенетической терапии, направленной на блокирование конечных продуктов гликирования у больных сахарным диабетом с диабетической нейропатией.
Каждый пятый больной сахарным диабетом имеет клинические проявления диабетической автономной нейропатии (ДАН): синусовую тахикардию, снижение вариабельности сердечного ритма, ортостатическую гипотензию, безболевую ишемию и безболевой инфаркт миокарда и др.
Диабетическая нейропатия (ДН) в различной форме встречается у 30–100% пациентов, страдающих сахарным диабетом (СД) 2 типа [1]. Традиционно основное внимание уделяется сенсо-моторной форме ДН, обусловливающей развитие синдрома диабетической стопы, в то время как диабетической автономной нейропатии (ДАН) внимания уделяется относительно мало. Однако наряду с другими поздними осложнениями СД, сердечно-сосудистая форма ДАН относится к основным причинам инвалидизации и смерти этих больных. Кроме того, ДАН может проявляться ортостатической гипотонией, снижением вариабельности сердечного ритма, повышением частоты сердечных сокращений (ЧСС) в покое; безболевой ишемией и инфарктом миокарда; неадекватной реакцией ЧСС и артериального давления (АД) на физическую нагрузку; удлинением интервала QT; дисфункцией левого желудочка. Примерно 20% больных СД как 1, так и 2 типа имеют клинические проявления ДАН. Поражение сердца значительно снижает качество и прогноз жизни пациента за счет высокой частоты развития безболевых форм инфаркта миокарда и угрожающих жизни аритмий. Поражение сердца при СД обусловлено рядом нарушений метаболических процессов в миокарде и проводящей системе, что происходит вследствие не только гипергликемии, но и повышенной утилизации свободных жирных кислот, тканевой гипоксии, нарушений кровоснабжения, микроангиопатии и других факторов. Смертность больных, имеющих проявления автономной сердечно-сосудистой нейропатии, за 10-летний период составляет 25%, по сравнению с 4% у лиц с СД, не имеющих данного осложнения [2, 3]. Сердечно-сосудистая форма ДАН делится на субклиническую, выявляемую только с помощью тестов, и клиническую. Разберем отдельно все названные проявления сердечно-сосудистой формы ДАН.
В статье рассматриваются особенности диагностики сердечно сосудистой формы ДАН, обсуждаются способы предупреждения развития и прогрессирования этого опасного осложнения сахарного диабета.
На примере нейротропного комплекса витаминов группы B (Мильгамма композитум) показана роль активаторов транскетолазы как патогенетической терапии, направленной на блокирование конечных продуктов гликирования у больных сахарным диабетом с диабетической нейропатией.
Синусовая тахикардия
Она может возникнуть как в спокойном состоянии, так и при волнении или физической нагрузке. У здорового человека частота сердечных сокращений составляет 60–70 ударов в минуту. При синусовой тахикардии ЧСС может достигать 120 и более ударов в минуту, в том числе в период покоя ночью. Напротив, при физической нагрузке сердце оказывается неспособным существенно увеличить частоту сокращений, что ведет к дефициту кислорода и питательных веществ в интенсивно функционирующих органах и тканях.
Она может возникнуть как в спокойном состоянии, так и при волнении или физической нагрузке. У здорового человека частота сердечных сокращений составляет 60–70 ударов в минуту. При синусовой тахикардии ЧСС может достигать 120 и более ударов в минуту, в том числе в период покоя ночью. Напротив, при физической нагрузке сердце оказывается неспособным существенно увеличить частоту сокращений, что ведет к дефициту кислорода и питательных веществ в интенсивно функционирующих органах и тканях.
Вариабельность сердечного ритма
При сердечно-сосудистой форме ДАН может наблюдаться фиксированный сердечный ритм, или «тотальная денервация сердца» – отсутствие четкой зависимости частоты сердечного ритма от физической активности и фазы дыхания. Например, глубокий вдох не сопровождается учащением сердечного ритма, как это наблюдается в норме. Рекомендуется записать ЭКГ в течение 1 минуты на одном из отведений, затем найти разницу между самым большим и самым коротким интервалами R-R. Если эта разница составляет менее 7 мм, можно предполагать автономную кардиопатию.
При сердечно-сосудистой форме ДАН может наблюдаться фиксированный сердечный ритм, или «тотальная денервация сердца» – отсутствие четкой зависимости частоты сердечного ритма от физической активности и фазы дыхания. Например, глубокий вдох не сопровождается учащением сердечного ритма, как это наблюдается в норме. Рекомендуется записать ЭКГ в течение 1 минуты на одном из отведений, затем найти разницу между самым большим и самым коротким интервалами R-R. Если эта разница составляет менее 7 мм, можно предполагать автономную кардиопатию.
Ортостатическая гипотензия
Для ортостатической гипотензии (снижение АД более чем на 20% от исходного уровня после перехода из горизонтального положения в вертикальное) характерны слабость, головокружение, синкопальное состояние, зрительные нарушения, бледность кожных покровов при переходе пациента из положения лежа в положение стоя. В некоторых случаях гипотензия остается бессимптомной. Важно проводить дифференциальную диагностику с гипогликемическими состояниями. Характерно, что артериальная гипотония при ДАН не сопровождается компенсаторной тахикардией. Артериальная гипотония также может быть спровоцирована приемом лекарственных средств: трициклических антидепрессантов, диуретиков, вазодилататоров. Иногда ортостатическая гипотония проявляется длительной головной болью и резким снижением трудоспособности в утренние часы. Интенсивность головной боли снижается после перехода в горизонтальное положение, часто приносит облегчение вынужденное положение, когда голова находится ниже туловища или на его уровне (многие пациенты не используют подушку во время сна). В ряде случаев применение стандартного набора препаратов для лечения головной боли оказывается неэффективным. Больным СД 2 типа, имеющим эпизоды ортостатической гипотензии, следует соблюдать некоторые правила осторожности [4]:
По результатам исследования DIAD (Detection of Ischemia in Asymptomatic Diabetes), в которое были включены 1123 пациента с СД 2 типа, кардиальная форма автономной нейропатии была четким прогностическим критерием развития ишемии миокарда [6]. Одной из возможных причин внезапной смерти может быть тяжелая бессимптомная ишемия, индуцирующая развитие летальных аритмий. Патологическое удлинение интервала QT, продолжительность которого регулируется вегетативной нервной системой, также ассоциировано с повышенным риском фатальных нарушений сердечного ритма. Необходимо отметить, что кардиальная форма автономной диабетической нейропатии не всегда является независимым фактором риска внезапной смерти, так как часто сочетается с тяжелой сердечной недостаточностью на фоне коронарного атеросклероза.
Для ортостатической гипотензии (снижение АД более чем на 20% от исходного уровня после перехода из горизонтального положения в вертикальное) характерны слабость, головокружение, синкопальное состояние, зрительные нарушения, бледность кожных покровов при переходе пациента из положения лежа в положение стоя. В некоторых случаях гипотензия остается бессимптомной. Важно проводить дифференциальную диагностику с гипогликемическими состояниями. Характерно, что артериальная гипотония при ДАН не сопровождается компенсаторной тахикардией. Артериальная гипотония также может быть спровоцирована приемом лекарственных средств: трициклических антидепрессантов, диуретиков, вазодилататоров. Иногда ортостатическая гипотония проявляется длительной головной болью и резким снижением трудоспособности в утренние часы. Интенсивность головной боли снижается после перехода в горизонтальное положение, часто приносит облегчение вынужденное положение, когда голова находится ниже туловища или на его уровне (многие пациенты не используют подушку во время сна). В ряде случаев применение стандартного набора препаратов для лечения головной боли оказывается неэффективным. Больным СД 2 типа, имеющим эпизоды ортостатической гипотензии, следует соблюдать некоторые правила осторожности [4]:
- избегать резких перемен положения тела;
- собираясь встать с кровати, необходимо посидеть несколько секунд (глубоко подышать, сосчитать до 10);
- вставая со стула, кресла и т.п., также не нужно спешить.
- Безболевой инфаркт миокарда
По результатам исследования DIAD (Detection of Ischemia in Asymptomatic Diabetes), в которое были включены 1123 пациента с СД 2 типа, кардиальная форма автономной нейропатии была четким прогностическим критерием развития ишемии миокарда [6]. Одной из возможных причин внезапной смерти может быть тяжелая бессимптомная ишемия, индуцирующая развитие летальных аритмий. Патологическое удлинение интервала QT, продолжительность которого регулируется вегетативной нервной системой, также ассоциировано с повышенным риском фатальных нарушений сердечного ритма. Необходимо отметить, что кардиальная форма автономной диабетической нейропатии не всегда является независимым фактором риска внезапной смерти, так как часто сочетается с тяжелой сердечной недостаточностью на фоне коронарного атеросклероза.
Диагностика сердечно-сосудистой формы ДАН
В настоящее время диагностика данной формы ДАН проводится на основании исследования кардиоваскулярных рефлексов, так называемых 5 стандартных тестов по Ewing, предложенных в 1975 г. [4] и одобренных на конференции по диабетической нейропатии в 1988 г. в Сан-Антонио. Использование данных тестов может быть достаточным для выявления раннего, субклинического поражения вегетативной нервной системы. Однако в дополнение для диагностики сердечно-сосудистой формы ДАН возможно исследование вариабельности ритма сердца (ВРС) и измерение корригированного интервала QT и дисперсии интервала QT [6, 7]. При этом подчеркнем, что удлинение интервала QT является чувствительным, но недостаточно специфичным маркером сердечно-сосудистой формы ДАН. Измерения только интервала QT и дисперсии интервала QT недостаточно для постановки диагноза, однако этот фактор является ценным вспомогательным критерием.
На доклинической стадии сердечно-сосудистой формы ДАН может присутствовать целый ряд метаболических нарушений в миокарде, в том числе приводящих к развитию диастолической дисфункции [8]. Тем не менее структурные изменения сердца и нарушения его насосной функции часто отсутствуют, и ранняя диагностика ДАН с поражением сердечно-сосудистой системы может основываться только на небольших изменениях электрокардиограммы (ЭКГ). Так, при анализе ЭКГ в 12 отведениях могут выявляться изменения Р-волны (например, увеличение продолжительности P-волны, удлинение интервала PR), изменения атриовентрикулярной проводимости, аритмия [9], также возможны изменения, указывающие наличие легкой гипертрофии левого желудочка.
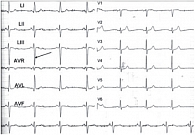
На рисунке представлена ЭКГ от 2005 г. 48-летнего пациента, наблюдающегося в течение 7 лет на нашей кафедре. При первичном обследовании в 2005 г. у него был диагностирован СД 2 типа с уровнем НbА1с 7,2%, гликемией натощак 7,3 ммоль/л, при этом на ЭКГ было выявлено углубление зубца S в III отведении и увеличение R в aVL-отведении, что могло указывать на наличие гипертрофии левого желудочка; никаких признаков сердечно-сосудистой формы ДАН выявлено не было. Однако при проведении стресс-ЭКГ была выявлена 2 мм депрессия сегмента ST. При эхокардиографии выявлена легкая гипертрофия левого желудочка (индекс массы = 126 г/м2) и нарушение релаксации левого желудочка (отношение скоростей раннедиастолического и позднедиастолического трансмитрального кровотока (E / A) < 1) при сохраненной систолической функции левого желудочка (фракция выброса левого желудочка (ФВ ЛЖ) > 60%). В связи с выявленным высоким сердечно-сосудистым риском пациент находился под регулярным наблюдением на кафедре, начал выполнять рекомендации по диете и терапии СД, получать гипотензивную, антиагрегантную и гиполипидемическую терапию. В результате на протяжении 7-летнего наблюдения СД остается хорошо компенсированным, а ЭКГ – неизменной, никаких клинических или ЭКГ-признаков сердечно-сосудистой формы ДАН не обнаруживается.
В связи с вышеизложенным для пациентов с недавно диагностированным СД 2 типа с нормальной ЭКГ покоя остается крайне актуальным вопрос ранней диагностики скрытых «немых, безболевых» повреждений миокарда. Кроме того, по данным современных обзоров, точность в постановке правильного диагноза при стресс-ЭКГ составляет 79%, а проведение коронарной ангиографии при наличии показаний является «золотым стандартом» диагностики безболевых ишемий у пациентов с СД, как было опубликовано в недавнем научном заявлении Американской кардиологической ассоциации [10]. Среди основных ЭКГ-проявлений сердечно-сосудистой формы ДАН выделяют следующие:
В настоящее время диагностика данной формы ДАН проводится на основании исследования кардиоваскулярных рефлексов, так называемых 5 стандартных тестов по Ewing, предложенных в 1975 г. [4] и одобренных на конференции по диабетической нейропатии в 1988 г. в Сан-Антонио. Использование данных тестов может быть достаточным для выявления раннего, субклинического поражения вегетативной нервной системы. Однако в дополнение для диагностики сердечно-сосудистой формы ДАН возможно исследование вариабельности ритма сердца (ВРС) и измерение корригированного интервала QT и дисперсии интервала QT [6, 7]. При этом подчеркнем, что удлинение интервала QT является чувствительным, но недостаточно специфичным маркером сердечно-сосудистой формы ДАН. Измерения только интервала QT и дисперсии интервала QT недостаточно для постановки диагноза, однако этот фактор является ценным вспомогательным критерием.
На доклинической стадии сердечно-сосудистой формы ДАН может присутствовать целый ряд метаболических нарушений в миокарде, в том числе приводящих к развитию диастолической дисфункции [8]. Тем не менее структурные изменения сердца и нарушения его насосной функции часто отсутствуют, и ранняя диагностика ДАН с поражением сердечно-сосудистой системы может основываться только на небольших изменениях электрокардиограммы (ЭКГ). Так, при анализе ЭКГ в 12 отведениях могут выявляться изменения Р-волны (например, увеличение продолжительности P-волны, удлинение интервала PR), изменения атриовентрикулярной проводимости, аритмия [9], также возможны изменения, указывающие наличие легкой гипертрофии левого желудочка.
На рисунке представлена ЭКГ от 2005 г. 48-летнего пациента, наблюдающегося в течение 7 лет на нашей кафедре. При первичном обследовании в 2005 г. у него был диагностирован СД 2 типа с уровнем НbА1с 7,2%, гликемией натощак 7,3 ммоль/л, при этом на ЭКГ было выявлено углубление зубца S в III отведении и увеличение R в aVL-отведении, что могло указывать на наличие гипертрофии левого желудочка; никаких признаков сердечно-сосудистой формы ДАН выявлено не было. Однако при проведении стресс-ЭКГ была выявлена 2 мм депрессия сегмента ST. При эхокардиографии выявлена легкая гипертрофия левого желудочка (индекс массы = 126 г/м2) и нарушение релаксации левого желудочка (отношение скоростей раннедиастолического и позднедиастолического трансмитрального кровотока (E / A) < 1) при сохраненной систолической функции левого желудочка (фракция выброса левого желудочка (ФВ ЛЖ) > 60%). В связи с выявленным высоким сердечно-сосудистым риском пациент находился под регулярным наблюдением на кафедре, начал выполнять рекомендации по диете и терапии СД, получать гипотензивную, антиагрегантную и гиполипидемическую терапию. В результате на протяжении 7-летнего наблюдения СД остается хорошо компенсированным, а ЭКГ – неизменной, никаких клинических или ЭКГ-признаков сердечно-сосудистой формы ДАН не обнаруживается.
В связи с вышеизложенным для пациентов с недавно диагностированным СД 2 типа с нормальной ЭКГ покоя остается крайне актуальным вопрос ранней диагностики скрытых «немых, безболевых» повреждений миокарда. Кроме того, по данным современных обзоров, точность в постановке правильного диагноза при стресс-ЭКГ составляет 79%, а проведение коронарной ангиографии при наличии показаний является «золотым стандартом» диагностики безболевых ишемий у пациентов с СД, как было опубликовано в недавнем научном заявлении Американской кардиологической ассоциации [10]. Среди основных ЭКГ-проявлений сердечно-сосудистой формы ДАН выделяют следующие:
- синусовая тахикардия;
- удлинение интервала QTc;
- измененная вариабельность сердечного ритма;
- гипертрофия левого желудочка;
- дисперсия интервала ST;
- инверсия положительного зубца Т;
- псевдокоронарный подъем сегмента ST.
- Консультации невропатолога и кардиолога.
- Применение специальных вопросников позволяет лучше разобраться и выявить основные признаки данной формы ДАН.
- Эхокардиография позволяет оценить ряд необходимых параметров функционального состояния сердечной мышцы.
- Проведение специфических тестов – проба с применением бета-адреноблокаторов, проба с физической нагрузкой – позволяет оценить влияние автономной нервной системы на сердце и сосуды.
- Электронейромиографическое исследование включает в себя комплекс относительно самостоятельных методик, направленных на диагностику диабетической нейропатии в ее «зародыше», то есть на выявление нарушений на доклиническом уровне.
- неудовлетворительная компенсация СД;
- длительность заболевания;
- наличие других осложнений СД;
- избыточная масса тела;
- андроидный тип ожирения;
- артериальная гипертония;
- курение.
Лечение сердечно-сосудистой формы ДАН
Лечение сердечно-сосудистой формы ДАН должно быть комплексным и включать в себя несколько этапов:
Отдельного внимания заслуживает терапия антиоксидантами, направленная на ликвидацию окислительного стресса у больных СД. Такое лечение сопровождается повышением уровня оксида азота в сыворотке крови, снижением степени выраженности клинических симптомов, обусловленных дисфункцией эндотелия. Именно поэтому одним из основных направлений лечения диабетической нейропатии является назначение антиоксидантов – витаминов группы В. Нейротропное действие витаминов группы В доказано результатами многочисленных клинических исследований, в которых было показано, что между распределением тиамина в глюкозозависимых клетках и расщеплением глюкозы существует непосредственная взаимосвязь [11, 12]. Бенфотиамин в нервной ткани способствует повышению активности ферментных систем и нейтрализации конечных продуктов гликирования, оказывает влияние на дегенеративные процессы в нервном волокне. Пиридоксин также участвует в метаболизме белка (синтез норадреналина и серотонина) и частично в метаболизме жировой ткани [11, 12]. С практической точки зрения целесообразно применение комбинированных нейротропных комплексов витаминов группы В, что значительно упрощает процедуру лечения больных. Использование в клинике препарата Мильгамма композитум (содержит по 100 мг бенфотиамина и пиридоксина) может предотвратить образование конечных продуктов ускоренного гликозилирования белков (в частности сорбитола) и повысить активность транскетолазы [11]. Пиридоксин является кофактором более чем для 100 ферментов, влияет на структуру и функцию нервной ткани. В одном из российских исследований, проведенных в Ростове-на-Дону, были обследованы 103 пациента с метаболическим синдромом (возраст составил от 36 до 72 лет). У 10 из них имелось нарушение толерантности к глюкозе (НТГ), у 80 – СД 2 типа средней продолжительностью 7,36 ± 0,41 года, у 13 больных не было обнаружено нарушений углеводного обмена.
Диагноз автономной нейропатии (АН) ставился при выявлении ее сердечно-сосудистой формы методом кардиоинтервалографии по Р.М. Баевскому [13]. В зависимости от наличия этого осложнения больные были разделены на две группы: в первую группу вошли 27 пациентов без электрофизиологических признаков АН, вторую группу составили 76 больных с сердечно-сосудистой АН. У всех пациентов, у которых в ходе кардиоинтервалографии была выявлена АН (вторая группа), метаболический синдром сопровождался выраженными нарушениями углеводного обмена в виде СД 2 типа. Большую часть первой группы (без изменений вариабельности сердечного ритма) составили больные без нарушений обмена углеводов или с НТГ. Из обследованных больных СД 2 типа, развившегося на фоне метаболического синдрома, у подавляющего большинства – 95% – имелись признаки АН [14]. Из кардиоваскулярных симптомов у пациентов второй группы преобладала липотимия – внезапное легкое затуманивание сознания, головокружение, звон в ушах (71%), у 34% наблюдались дискомфорт или боли в области сердца. После 6-недельного курса патогенетической терапии улучшение самочувствия и субъективных проявлений АН отметили 59% больных, получавших монотерапию бенфотиамином, 62% и 78% получавших двойную терапию – «бенфотиамин + тиоктовая кислота». Наилучший ответ на лечение отмечен со стороны симптомов липотимии. Так, частота обмороков уменьшилась в 5 раз (с 71 до 14%), что указывает на положительные изменения функции вегетативной нервной системы [15]. Подводя итоги вышеизложенному, отметим, что применение Мильгаммы композитум в качестве монотерапии, а также использование комбинаций Мильгаммы композитум и Тиогаммы оказывает эффективное патогенетическое действие у пациентов с сердечно-сосудистой формой ДАН [12, 14], что делает эти препараты средствами выбора в терапии этого осложнения СД.
Лечение сердечно-сосудистой формы ДАН должно быть комплексным и включать в себя несколько этапов:
- Достижение индивидуального целевого уровня гликемии.
- Назначение сопутствующей необходимой при СД 2 типа терапии (статины, гипотензивная, антиагрегантная терапия и др.).
- Назначение симптоматической терапии с целью устранения имеющихся проявлений ДАН.
- Патогенетическая терапия ДАН.
Отдельного внимания заслуживает терапия антиоксидантами, направленная на ликвидацию окислительного стресса у больных СД. Такое лечение сопровождается повышением уровня оксида азота в сыворотке крови, снижением степени выраженности клинических симптомов, обусловленных дисфункцией эндотелия. Именно поэтому одним из основных направлений лечения диабетической нейропатии является назначение антиоксидантов – витаминов группы В. Нейротропное действие витаминов группы В доказано результатами многочисленных клинических исследований, в которых было показано, что между распределением тиамина в глюкозозависимых клетках и расщеплением глюкозы существует непосредственная взаимосвязь [11, 12]. Бенфотиамин в нервной ткани способствует повышению активности ферментных систем и нейтрализации конечных продуктов гликирования, оказывает влияние на дегенеративные процессы в нервном волокне. Пиридоксин также участвует в метаболизме белка (синтез норадреналина и серотонина) и частично в метаболизме жировой ткани [11, 12]. С практической точки зрения целесообразно применение комбинированных нейротропных комплексов витаминов группы В, что значительно упрощает процедуру лечения больных. Использование в клинике препарата Мильгамма композитум (содержит по 100 мг бенфотиамина и пиридоксина) может предотвратить образование конечных продуктов ускоренного гликозилирования белков (в частности сорбитола) и повысить активность транскетолазы [11]. Пиридоксин является кофактором более чем для 100 ферментов, влияет на структуру и функцию нервной ткани. В одном из российских исследований, проведенных в Ростове-на-Дону, были обследованы 103 пациента с метаболическим синдромом (возраст составил от 36 до 72 лет). У 10 из них имелось нарушение толерантности к глюкозе (НТГ), у 80 – СД 2 типа средней продолжительностью 7,36 ± 0,41 года, у 13 больных не было обнаружено нарушений углеводного обмена.
Диагноз автономной нейропатии (АН) ставился при выявлении ее сердечно-сосудистой формы методом кардиоинтервалографии по Р.М. Баевскому [13]. В зависимости от наличия этого осложнения больные были разделены на две группы: в первую группу вошли 27 пациентов без электрофизиологических признаков АН, вторую группу составили 76 больных с сердечно-сосудистой АН. У всех пациентов, у которых в ходе кардиоинтервалографии была выявлена АН (вторая группа), метаболический синдром сопровождался выраженными нарушениями углеводного обмена в виде СД 2 типа. Большую часть первой группы (без изменений вариабельности сердечного ритма) составили больные без нарушений обмена углеводов или с НТГ. Из обследованных больных СД 2 типа, развившегося на фоне метаболического синдрома, у подавляющего большинства – 95% – имелись признаки АН [14]. Из кардиоваскулярных симптомов у пациентов второй группы преобладала липотимия – внезапное легкое затуманивание сознания, головокружение, звон в ушах (71%), у 34% наблюдались дискомфорт или боли в области сердца. После 6-недельного курса патогенетической терапии улучшение самочувствия и субъективных проявлений АН отметили 59% больных, получавших монотерапию бенфотиамином, 62% и 78% получавших двойную терапию – «бенфотиамин + тиоктовая кислота». Наилучший ответ на лечение отмечен со стороны симптомов липотимии. Так, частота обмороков уменьшилась в 5 раз (с 71 до 14%), что указывает на положительные изменения функции вегетативной нервной системы [15]. Подводя итоги вышеизложенному, отметим, что применение Мильгаммы композитум в качестве монотерапии, а также использование комбинаций Мильгаммы композитум и Тиогаммы оказывает эффективное патогенетическое действие у пациентов с сердечно-сосудистой формой ДАН [12, 14], что делает эти препараты средствами выбора в терапии этого осложнения СД.
1. Дедов И.И., Шестакова М.В. Сахарный диабет. Руководство для врачей. М.: Универсум Паблишинг, 2003. 378 с.
2. Casellini C.M., Vinik A.I. Clinical manifestations and current treatment options for diabetic neuropathies // Endocr. Pract. 2007. Vol. 13. № 5. P. 550–566.
3. Herman W.H., Kennedy L. Underdiagnosis of peripheral neuropathy in type 2 diabetes // Diabetes Care. 2005. Vol. 28. № 6. P. 1480–1481.
4. Vinik A., Erbas T., Pfeifer M.A. et al. Diabetic autonomic neuropathy // Ellenberg & Rifkin’s Diabetes Mellitus / Ed. by D. Porte, R.S. Sherwin, A. Baron. 6th ed. New York: McGraw-Hill, 2003. P. 789–804.
5. Rosen S.D., Camici P.G. The brain-heart axis in the perception of cardiac pain: the elusive link between ischaemia and pain // Ann. Med. 2000. Vol. 32. № 5. P. 350–364.
6. Wackers F.J., Young L.H., Inzucchi S.E. et al. Detection of silent myocardial ischemia in asymptomatic diabetic subjects: the DIAD study // Diabetes Care. 2004. Vol. 27. № 8. P. 1954–1961.
7. Beller G.A. Noninvasive screening for coronary atherosclerosis and silent ischemia in asymptomatic type 2 diabetic patients: is it appropriate and cost-effective? // J. Am. Coll. Cardiol. 2007. Vol. 49. № 19. P. 1918–1923.
8. Schannwell C.M., Schneppenheim M., Perings S. et al. Left ventricular diastolic dysfunction as an early manifestation of diabetic cardiomyopathy // Cardiology. 2002. Vol. 98. № 1–2. P. 33–39.
9. Kumar A., Prineas R.J., Arnold A.M. et al. Prevalence, prognosis, and implications of isolated minor nonspecific ST-segment and T-wave abnormalities in older adults cardiovascular health study // Circulation. 2008. Vol. 118. № 25. P. 2790–2796.
10. Lloyd-Jones D., Adams R.J., Brown T.M. et al. Heart disease and stroke statistics--2010 update: a report from the American Heart Association // Circulation. 2010. Vol. 121. № 7. P. e46–e215.
11. Schreeb K.H., Freudenthaler S., Vormfelde S.V. et al. Comparative bioavailability of two vitamin B1 preparations: benfotiamine and thiamine mononitrate // Eur. J. Clin. Pharmacol. 1997. Vol. 52. № 4. P. 319–320.
12. Stirban A., Negrean M., Stratmann B. et al. Benfotiamine prevents macro- and microvascular endothelial dysfunction and oxidative stress following a meal rich in advanced glycation end products in individuals with type 2 diabetes // Diabetes Care. 2006. Vol. 29. № 9. P. 2064–2071.
13. Баевский Р.М., Кириллов О.И., Клецкин С.З. Математический анализ сердечного ритма при стрессе. М., 1984.
14. Воробьев С.В., Караханян К.С., Кириченко Д.А. и др. Диагностика и лечение вегетативной дисфункции у больных с метаболическим синдромом и нарушением углеводного обмена // Лечащий врач. 2009. № 1. С. 64–66.
Новости на тему
02.02.2024
21.09.2023
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.