Национальные календари прививок и программы иммунопрофилактики, существующие в различных странах, постоянно обновляются, что связано с изменяющейся эпидемиологической ситуацией в регионах и мире в целом, совершенствованием системы здравоохранения, созданием новых вакцинных препаратов, а также анализом эффективности и безопасности вакцин, что находит отражение в рекомендациях ВОЗ. Действующий национальный календарь профилактических прививок России был введен с 2002 г. (приказ МЗиСР № 229 от 27.06.2001), в дальнейшем в него были внесены изменения согласно приказам № 27 (от 17.01.2006), № 673 (от 30.10.2007) и № 166 (от 09.04.2009) [2, 3]. Последние изменения введены приказом МЗиСР № 51н от 31.01.2011 [4]. Календарь прививок включает профилактику 11 инфекционных заболеваний (табл. 1) и является основным нормативным актом, согласно которому реализуются программы иммунопрофилактики, определяются сроки введения вакцин, число необходимых доз, совместимость различных препаратов и пр. Для выполнения календаря прививок разрешены к использованию как отечественные, так и зарубежные вакцинные препараты, зарегистрированные в РФ. Действующая в настоящее время редакция календаря имеет следующие отличия от предшествующих:
- использование различных схем вакцинации против гепатита В здоровых и детей, рожденных матерями, относящимися к группам риска;
- вакцинация против полиомиелита детей первого года жизни осуществляется инактивированной (первые два введения) и живой (третье введение) вакцинами;
- ежегодная иммунизация против гриппа детей с 6-месячного возраста, подростков, студентов, а также пожилых и взрослых ряда декретированных групп (группы риска);
- разрешение совмещения при нарушении графика всех положенных по возрасту вакцин (использование комбинированных вакцинных препаратов или одномоментное введение монопрепаратов в разные участки тела), за исключением БЦЖ и БЦЖ-М.
Одним из самых дискутируемых вопросов современного российского календаря является возраст начала вакцинации против гепатита В (ГВ). Массовая вакцинация против ГВ, в том числе новорожденных в первые сутки жизни, проводится с 2002 г., на фоне чего за 9 лет произошло снижение заболеваемости ГВ в России более чем в 15 раз (с 42,1 в 2001 г. до 2,7 в 2009 г. на 100 тыс. населения за 9 месяцев). Во многих странах Европы (Великобритания, Германия, Италия, Франция и др.) вакцинацию ГВ начинают в 2–3 месяца одновременно с вакцинацией против коклюша, столбняка, дифтерии, полиомиелита, и только детям матерей из группы риска первую прививку делают после рождения. В то же время в большинстве стран Восточной Европы (Болгария, Польша, Румыния, страны бывшего СССР), а также в США календарь прививок предусматривает вакцинацию для всех детей в первый день жизни. Сторонники переноса вакцинации на более поздний срок аргументируют это возможным негативным влиянием на иммунитет к туберкулезу, ростом количества случаев желтухи у детей в период новорожденности, незнанием особенностей состояния здоровья и заболеваний новорожденных, которые могут проявляться не в первый день жизни, а позднее.
Cторонники вакцинации новорожденных в первые сутки в своих доводах обращают внимание на значительное число инфицированных ГВ в России (более 3 млн человек), большинство из которых – лица репродуктивного возраста, недостаточную чувствительность используемых тест-систем для выявления вирусоносительства у беременных женщин (число ложноотрицательных результатов при обследовании беременных, по данным НЦЗД РАМН, достигает 10%). Это является фактором риска заражения новорожденных. Известно, что до 90% новорожденных от матерей с ГВ инфицируются в процессе родов, при этом заболевание у детей, как правило, принимает хроническое течение. Эффективной мерой профилактики вертикальной передачи вируса является иммунизация новорожденных. Проведенные исследования показали, что частота случаев желтухи одинакова среди привитых и непривитых детей, отсутствует негативное взаимовлияние вакцин БЦЖ и ГВ на формирование иммунитета как к туберкулезу (критерии: размер рубчика и реакции Манту), так и к ГВ (титры антител) [5–7]. Таким образом, на сегодняшний день наиболее целесообразным следует признать сохранение положения действующего календаря, по которому вакцинация ГВ начинается у всех детей в первые 24 часа жизни.
В последние десятилетия эпидемиологическая ситуация по полиомиелиту коренным образом изменилась, и с 2002 г. Европейский регион, в том числе и Россия, сертифицирован ВОЗ как территория, свободная от полиомиелита. В прежнем календаре с 2008 г. все дети первого года жизни получают прививки только инактивированной вакциной. Следует отметить, что в России до введения в календарь прививок инактивированной вакцины ежегодно регистрировалось от 4 до 7 случаев вакциноассоциированного паралитического полиомиелита (ВАПП). В 2009 г. в России не зарегистрировано ни одного случая ВАПП. Сочетанный график вакцинации против полиомиелита – первые 2–3 введения инактивированной вакцины (ИПВ), а затем 2–3 введения оральной живой полиомиелитной вакцины (ОПВ) – используют многие страны, сертифицированные как свободные от полиомиелита, но граничащие с государствами, где есть случаи заболевания, вызванные «диким» вирусом.
Это позволяет предупредить развитие ВАПП и гарантирует эпидемиологическую безопасность при завозе заболевания из приграничных территорий, как в 2010 г. произошло с заносом полиомиелита из Таджикистана в Россию. Новый календарь прививок закрепляет эти рекомендации, и в РФ введен сочетанный вариант использования инактивированной и живой вакцины при профилактике полиомиелита: первые два введения осуществляются инактивированной вакциной, а последующие (вакцинация и ревакцинация) – живой вакциной. Обращаем внимание практикующих врачей, что по показаниям в декретированных группах допускается трехкратное использование инактивированной вакцины при проведении иммунизации на первом году жизни. Это относится к детям, находящимся в закрытых детских дошкольных учреждениях: домах ребенка, детских домах, специализированных интернатах (для детей с психоневрологическими заболеваниями и др.), противотуберкулезных санаторно-оздоровительных учреждениях. Детям, рожденным ВИЧ-инфицированными матерями, вакцинация против полиомиелита проводится только инактивированной вакциной независимо от их ВИЧ-статуса.
Серьезной проблемой для практического здравоохранения остается гемофильная инфекция, вызывающая, по оценкам специалистов, около 3 млн случаев тяжелых заболеваний в мире и более 350 тыс. случаев летальных исходов в год. Почти все жертвы – дети в возрасте до пяти лет, при этом наиболее уязвимы к инфекции дети в возрасте от 4 до 18 месяцев. Гемофильная инфекция включает в себя различные нозологические формы заболеваний, возбудителем которых является грамотрицательная бактерия Haemophilus influenzae типа b (палочка Афанасьева – Пфейффера). Носительство гемофильной палочки в верхних дыхательных путях широко распространено, особенно в организованных детских коллективах [9–11]. Наиболее часто ХИБ является возбудителем респираторных инфекций – острого среднего отита, синусита, бронхита, пневмонии. Однако наиболее опасными формами ХИБ-инфекции являются гнойный менингит, сепсис и эпиглоттит. Встречаются и более редкие клинические варианты течения инфекции: гнойный целлюлит, артрит. В РФ в этиологической структуре гнойного менингита у детей до 5 лет ХИБ занимает 2-е место, уступая лишь менингококку, а в ряде регионов данный патоген является ведущим в этиологической структуре заболевания [12].
По современным данным, иммунная система детей раннего возраста не способна формировать самостоятельный адекватный иммунитет к гемофильной инфекции типа В. Поэтому только иммунизация способна защитить детей от всех форм ХИБ-инфекции. Более чем в 140 странах мира вакцины против гемофильной инфекции типа В включены в национальные календари прививок, что привело к снижению заболеваемости гемофильным менингитом на 90–100% и уменьшению распространенности респираторных форм инфекции (отитов и пневмоний) на 20%. По данным систематического обзора Cochrane, вакцины против ХИБ-инфекции являются эффективными и безопасными [13]. Российские исследования, проведенные в домах ребенка, показали, что в результате вакцинации значительно снижается носительство ХИБ – в 2,8–14,9 раза [9, 14]. Заболеваемость респираторными инфекциями после вакцинации в среднем снижается в 2,7 раза, при этом число отитов уменьшилось в 5,8 раза, бронхитов и пневмоний – в 1,9, крупов – в 1,8, синуситов – в 1,6 раза.
Прививка против ХИБ-инфекции рекомендована Минздравом России еще в конце ХХ столетия, а с 2008–2009 гг. вакцинация против ХИБ-инфекции включена в региональные календари прививок Свердловской области и Москвы. Новый календарь профилактических прививок впервые включает обязательную вакцинацию детей против гемофильной инфекции с 3-месячного возраста. Классическая схема вакцинации состоит из трех введений (в возрасте 3; 4,5 и 6 месяцев), что позволяет обеспечить защиту от всех форм ХИБ-инфекции к возрасту 6 месяцев и сократить число визитов к педиатру за счет совмещения введения вакцин АКДС, ИПВ, ХИБ. При этой схеме четвертое введение вакцины (ревакцинация) также проводят одномоментно с ревакцинацией АКДС и ОПВ в 18-месячном возрасте. Обязательной вакцинации подлежат дети, относящиеся к группам риска:
- дети с иммунодефицитными состояниями или анатомическими дефектами, резко увеличивающими опасность заболевания ХИБ-инфекцией;
- дети с онкогематологическими заболеваниями и/или длительно получающие иммуносупрессивную терапию;
- ВИЧ-инфицированные или рожденные от ВИЧ-инфицированных матерей;
- дети, находящиеся в закрытых детских дошкольных учреждениях (дома ребенка, детские дома, специализированные интернаты, противотуберкулезные санаторно-оздоровительные учреждения).
Вакцинные препараты, применяемые для иммунопрофилактики ХИБ-инфекции в России, содержат полисахарид Haemophilus influenzae типа b, конъюгированный со столбнячным анатоксином, и показаны для плановой иммунизации всех детей с 2–3-месячного возраста до 5 лет. ХИБ-вакцины являются высокоиммуногенными, создают длительный напряженный иммунитет, основанный на эффекте иммунологической памяти. Прививочная доза составляет 0,5 мл (10 мкг полисахарида).
Допускается использование и других схем иммунизации: если ребенка начинают прививать после 6 месяцев, то вакцину вводят 2 раза с интервалом 1,5–2 месяца и ревакцинацией через 12 месяцев. При проведении вакцинации детям от 1 года до 5 лет достаточно однократного введения вакцины. Следует отметить, что при использовании этих графиков введения вакцин они способны защищать преимущественно от неинвазивных форм гемофильной инфекции (отиты, синуситы, тонзиллофарингиты и пр.). Вносимые в календарь профилактических прививок изменения в целом соответствуют стратегии совершенствования программ вакцинопрофилактики, рекомендованной ВОЗ. Например, для профилактики коклюша, дифтерии и столбняка предусмотрена возможность использования бесклеточной (ацеллюлярной) вакцины (АаКДС) вместо цельноклеточной (АКДС), что повышает безопасность иммунопрофилактики, сохраняя перспективу дальнейшего снижения заболеваемости коклюшем. Имеющийся опыт зарубежных и российских специалистов показывает, что применение АаКДС более безопасно для детей с поражением нервной системы и судорогами в анамнезе [15, 16]. Метаанализ 36 исследований за период с 1987 по 2006 г. показал, что ацеллюлярные вакцины сравнимы по эффективности с цельноклеточными [1, 17], а различное количество антигенов в них не оказывает влияния на иммуногенность [18, 19].
Значительным вкладом в развитие вакцинопрофилактики стало доказательство независимости иммунного ответа при введении нескольких антигенов. Теоретически подсчитано, что индивидуум может ответить на 105 антигенов, вводимых одномоментно [1]. Это позволило вводить разные вакцины одновременно и послужило стимулом для создания комбинированных вакцин, защищающих от нескольких инфекций. В действующих календарях прививок многих стран данные комбинированные препараты занимают ведущее место, так как имеют ряд преимуществ по сравнению с моновакцинами:
- уменьшается количество дополнительных веществ (стабилизаторов, консервантов), которые ребенок получает с каждой дозой вакцины;
- значительно сокращается число инъекций;
- сокращается число визитов к врачу;
- уменьшается суммарное количество нежелательных явлений после вакцинации;
- сокращаются расходы на хранение и транспортировку вакцин, организацию вакцинопрофилактики и пр.
При реализации национального календаря прививок России широко используются комбинированные вакцинные препараты: инактивированная полиомиелитная вакцина Солка (Иммовакс Полио) и живая полиомиелитная вакцина Сэбина, защищающие от заболеваний, вызванных вирусами полиомиелита 3 типов (с 1950-х гг.); вакцина против коклюша, столбняка, дифтерии (АКДС); инактивированные трехкомпонентные вакцины против гриппа; дивакцина против кори и эпидемического паротита; АКДС вместе с ГепВ (Бубо-кок) и АДС-М вместе с ГепВ (Бубо-М). Современный календарь при реализации программ иммунопрофилактики допускает применение зарубежных комбинированных вакцин, зарегистрированных в РФ. В настоящее время в различных регионах России стали широко использоваться такие многокомпонентные вакцинные препараты, как, например, Приорикс (корь, краснуха, паротит), Инфанрикс (АаКДС). С 2008 г. в России применяется пятикомпонентная вакцина Пентаксим (АаКДС, ИПВ, ХИБ), которая позволяет значительно сократить инъекционную нагрузку на ребенка и может быть рекомендована детям из групп риска [40].
Использование современных комбинированных вакцинных препаратов в наше время стало насущной необходимостью, а отставание в создании и регистрации отечественных вакцин подобного типа является препятствием на пути совершенствования программ специфической иммунопрофилактики. Важное место в профилактической медицине занимают вопросы вакцинации детей с хроническими заболеваниями органов дыхания. Длительное время иммунизация этой категории пациентов была ограничена. Однако именно эти дети имеют более высокий уровень заболеваемости управляемыми инфекциями, у них чаще наблюдается тяжелое течение и осложнения при интеркуррентных респираторных инфекциях, выше уровень неблагоприятных исходов [10]. Как правило, острые заболевания в этой группе пациентов приводят к обострению имеющегося хронического патологического процесса [20]. Все это обосновывает необходимость проведения у детей с заболеваниями респираторной системы своевременной безопасной вакцинации в соответствии с календарем прививок, а также дополнительного введения в их индивидуальный график прививок вакцинации против гриппа, пневмококковой и гемофильной типа В (ХИБ) инфекций. Практика показывает, что управление инфекциями дыхательной системы с помощью иммунизации представляет собой трудную задачу по целому ряду причин:
- при заражении в естественных условиях дикими штаммами респираторных возбудителей создаваемый в организме специфический иммунитет непродолжителен, что требует при вакцинации против этих инфекций введения поддерживающих доз;
- имеется широкое разнообразие антигенных вариантов одного и того же возбудителя (например, пневмококка), что вызывает необходимость создания и применения комбинированных вакцин;
- при гриппе почти ежегодно изменяется антигенный состав возбудителей;
- при разработке стратегии иммунизации необходимо учитывать характер инвазивности возбудителей, скорость распространения той или иной инфекции, значение возбудителя в массовом поражении населения.
Исходя из этого предполагается, что наибольший медицинский и экономический эффект может быть достигнут при массовой иммунизации. Снижение заболеваемости гриппом – одна из актуальнейших научных задач последнего столетия. Среди вирусных респираторных инфекций грипп занимает особое место ввиду его распространенности, более тяжелого течения и возможности возникновения жизнеугрожающих осложнений. Распространение его в современных условиях в значительной степени обусловлено глобализацией (миграция населения, быстрота авиасообщения), а также социально-экономическими факторами (птичий и частично свиной штаммы гриппа первично связаны с определенными группами населения). Высокому уровню заболеваемости гриппом способствует и наше поведение в быту: несоблюдение мер по изоляции больного, появление заболевших в общественных местах, на работе, в школе. Наиболее восприимчивы к инфекции дети начиная со второго полугодия жизни, а также лица после 65 лет, которые утрачивают накопленные за жизнь антитела к вирусам разной антигенной структуры [10, 21].
Чаще гриппом болеют лица, имеющие широкий круг профессиональных контактов (медицинские работники, педагоги, сотрудники коммунальной сферы и пр.). У людей, как правило, заболевание вызывают вирусы двух типов: А и B. Многоликость и непредсказуемость этой инфекции обусловлена множеством подтипов основного возбудителя – вируса гриппа А – и его чрезвычайной изменчивостью. Антигенная изменчивость наблюдается в виде небольших (антигенный дрейф) или значительных (антигенный шифт) изменений наружных белков вируса – нейраминидазы и гемагглютинина. Заболеваемость гриппом наблюдается ежегодно, при этом практически каждый сезон меняются штаммы циркулирующих вирусов. Поэтому необходима ежегодная прививка вакциной, антигенный состав которой рекомендован ВОЗ. Наиболее целесообразна вакцинация с сентября по декабрь – до подъема уровня заболеваемости. Иммунопрофилактика гриппа – наиболее эффективный метод снижения уровня заболеваемости, случаев осложненного течения и смертности от гриппа как в группах риска, так и среди населения в целом. Защитный эффект от вакцинации, проводимой в течение 2 лет и более, был достоверно выше, чем при однократной вакцинации непосредственно перед эпидемией. Исследования показывают, что заболеваемость у иммунизированных людей снижается на 70–80%. Кроме того, среди вакцинированных детей установлено снижение заболеваемости отитами от 5 до 31% в зависимости от формы их течения [22, 23].
В настоящее время используют два типа вакцин против гриппа: живые (содержащие живые аттенуированные вирусы) и убитые – цельновирионные, субъединичные и расщепленные (сплит-вакцины). Живые вакцины просты в применении, стимулируют клеточный, секреторный и гуморальный иммунитет, но противопоказаны людям с иммунодефицитными состояниями, членам семей таких пациентов, беременным и т.п. В группе неживых вакцин убитые, содержащие целиком вирус гриппа, относительно более реактогенны и не рекомендуются для детей. Современным, максимально безопасным вариантом для иммунизации детей и лиц с хроническими заболеваниями является использование расщепленных и субъединичных вакцин. Субъединичные вакцины (Гриппол, Агриппал, Инфлювак и др.) содержат только наружные антигены вирусов гриппа. Сплит-вакцины (Ваксигрип, Бегривак и Флюарикс) содержат как наружные антигены, так и внутренние типоспецифические белки. Вакцинации против гриппа проводятся с 6 месяцев. Прививочная доза составляет 0,25 мл для детей до 3 лет и 0,5 мл для детей старше 3 лет и взрослых. Детям младше 9 лет, ранее не болевшим гриппом и впервые вакцинируемым против гриппа, показано введение двух доз вакцины с интервалом 4 недели. Вакцина вводится внутримышечно или глубоко подкожно.
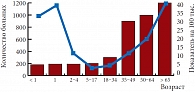
Среди вакциноуправляемых заболеваний пневмококковая инфекция до настоящего времени остается важной причиной высокой заболеваемости и смертности во всем мире. По данным ВОЗ, от заболеваний, вызванных различными серотипами пневмококка, в мире ежегодно погибает около 1,6 млн человек [24]. Заболевания пневмококковой этиологии остаются ведущей причиной летальности у детей до 5 лет – на их долю приходится 28% [25]. Наибольшая частота заболеваемости отмечается у детей первых двух лет жизни и пожилых людей старше 65 лет (рис. 1). В структуре заболеваемости на долю последних приходится свыше 32% всех случаев пневмококковой инфекции, более половины из них имеют неблагоприятный исход [26, 27]. Существует более 90 серотипов пневмококка (Streptococcus pneumoniae), обладающих разной вирулентностью и патогенностью. Высокая восприимчивость детей к пневмококковой инфекции обусловлена тем, что антигены полисахаридной капсулы пневмококка не иммуногенны в возрасте до 2 лет. В детском возрасте наиболее частыми клиническими формами пневмококковой инфекции являются острый средний отит, синусит, трахеобронхит и пневмония. Особой тяжестью течения отличается оккультная (скрытая) бактериемия и менингит, частота которого в России составляет 5–8 на 100 тыс. детей дошкольного возраста. Доля пневмококков в этиологии внебольничных пневмоний колеблется в пределах от 35 до 76%. Пневмококк выступает в роли основного возбудителя вторичной бактериальной пневмонии при гриппе. Проведенные исследования показали, что в период эпидемии гриппа частота инвазивных пневмококковых инфекций в 2 раза выше, чем в среднем за год [28, 29].
- пациенты, имеющие пониженный иммунный ответ против пневмококковой инфекции – первичный иммунодефицит, – ВИЧ-инфекция, онкогематологические заболевания, трансплантация органов или костного мозга, иммуносупрессивная терапия;
- пациенты с анатомической или функциональной аспленией (поскольку нарушается элиминация инкапсулированных бактерий) – спленэктомия, серповидно-клеточная анемия, системная красная волчанка;
- пациенты с хроническими бронхолегочными заболеваниями – бронхиальная астма, ХОБЛ, наследственные и врожденные заболевания легких;
- лица без нарушений иммунитета, но имеющие тяжелые поражения сердечно-сосудистой системы (врожденные пороки сердца, сердечная недостаточность, кардиомиопатия), почек или печени, сахарный диабет;
- дети, часто болеющие респираторными инфекциями нижних дыхательных путей, в том числе тубинфицированные;
- дети дошкольного возраста, находящиеся в закрытых детских образовательных учреждениях с круглосуточным пребыванием;
- взрослые в возрасте 65 лет и старше.
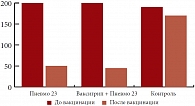
Многочисленными исследованиями, проведенными в России и за рубежом, убедительно подтверждена высокая эффективность полисахаридной пневмококковой вакцины: снижается заболеваемость тяжелыми формами пневмонии и бактериемии на 50–70%, уменьшается число эпизодов острых респираторных инфекций, обострений хронических необструктивных заболеваний легких (ХНЗЛ) и аденоидных вегетаций, отмечается исчезновение кондуктивной тугоухости I–II степени, уменьшение сенсибилизации к пневмококку у пациентов с бронхиальной астмой [20, 26, 32]. Проведенные исследования эффективности полисахаридной вакцины (отдельно или в сочетании с вакцинацией против гриппа) у часто болеющих детей дошкольного возраста установили достоверное снижение кратности и длительности эпизодов респираторных инфекций в группе привитых (рис. 2). Следует отметить, что проведение вакцинации не сопровождалось возникновением нежелательных явлений в раннем постпрививочном периоде: лишь в 3 случаях зарегистрированы легкие местные или общие реакции, не изменяющие состояния ребенка и не требующие медикаментозной коррекции. Кратковременное повышение температуры до субфебрильных цифр отмечено у троих детей, в том числе у двоих детей в сочетании с местными реакциями в виде умеренной гиперемии и болезненности в месте введения. Лишь у одного ребенка при сочетанном варианте вакцинации имело место кратковременное повышение температуры до фебрильных значений, существенно не изменяющее самочувствия и нормализовавшееся после однократного приема антипиретических средств.
По данным ВОЗ и систематического обзора Cochrane, эффективность конъюгированной вакцины у детей младше 2 лет составляет порядка 80–90%, если инвазивная инфекция вызвана вакцинным серотипом, и более 50% в целом [36]. В США после внедрения массовой иммунизации PCV7 в календарь прививок у детей до 2 лет отмечено снижение числа инвазивных пневмококковых инфекций на 77%, в том числе и в группах непривитых детей, за счет снижения циркуляции возбудителей. Необходимо отметить, что резкое снижение заболеваний, вызванных вакцинными серотипами пневмококка, сопровождалось небольшим увеличением частоты заболеваний, вызванных невакцинными серотипами. В связи с этим разрабатываются и внедряются вакцины с большим спектром пневмококков: с 2010 г. в календаре прививок США применяется конъюгированная 13-валентная вакцина. На сегодняшний день конъюгированная пневмококковая вакцина включена в календари прививок детей 43 стран мира [37, 38].
Иммунизация конъюгированной вакциной PCV7 может проводиться с 6 недель жизни, как при вакцинации против ХИБ-инфекции. График иммунопрофилактики и количество доз зависят от возраста, но разовая доза всегда составляет 0,5 мл. При начале вакцинации в возрасте от 2 до 6 месяцев вводятся 3 дозы с интервалом не менее 1 месяца, и в 12–15 месяцев проводится однократная ревакцинация. В России рекомендованная схема вакцинации предусматривает введение вакцины в 2; 4,5 и 7 месяцев с ревакцинацией в 15 месяцев. Однако вакцинацию можно проводить одновременно с АКДС, ИПВ и ХИБ. При проведении прививок после 6 месяцев используют две вакцинирующие дозы с интервалом 1,5–2 месяца с ревакцинацией на втором году жизни. При начале вакцинации с 1 года до 2 лет вводят две дозы с интервалом 1,5–2 месяца, а детям, начинающим прививки с 2 до 5 лет, достаточно однократного введения. Детям до 2 лет вакцину вводят внутримышечно в переднелатеральную поверхность бедра, а в более старшем возрасте – в дельтовидную мышцу плеча. Опыт применения PCV7 в России подтверждает не только ее высокую эффективность, но и безопасность [37]. Тяжелых поствакцинальных общих и местных реакций и осложнений зафиксировано не было. Поствакцинальные реакции слабой и средней силы в виде фебрильной лихорадки наблюдались у 3,4% детей. Это свидетельствует о низкой реактогенности вакцины и возможности ее более широкого применения у детей раннего возраста [38, 39].
В международных рекомендациях по применению конъюгированных пневмококковых вакцин у детей указывается, что дети в возрасте 2–18 лет с сопутствующими заболеваниями должны получать 23-валентную полисахаридную пневмококковую вакцину после завершения всех рекомендованных для данного возраста доз конъюгированной пневмококковой вакцины, которая может быть введена не ранее чем 2 месяца или позже после завершения курса вакцинации конъюгированной вакциной [43]. Несмотря на изменения, произошедшие в последнее десятилетие в национальном календаре прививок РФ, он все же отличается от календарей прививок многих развитых стран мира. В него не включены прививки против пневмококковой, ротавирусной инфекций, ветряной оспы. Целесообразно пересмотреть отношение к некоторым прививкам, рекомендуемым сейчас по эпидемиологическим показаниям, и ввести их в национальный календарь. Актуально внедрение региональных компонентов в национальный календарь плановых прививок: например, для ряда регионов важной является обязательная вакцинация против клещевого энцефалита и/или гепатита А, так как в них выше уровень заболеваемости этими инфекциями, чем в других областях. Подтверждением эффективности использования данного подхода может служить позитивный опыт широкой иммунизации детей против гепатита А в Краснодарском крае и Екатеринбурге, что привело к снижению заболеваемости в 5–6 раз.
В 2009 г. в региональный календарь Москвы включена вакцинация детей в возрасте 2 лет против ветряной оспы. Данное заболевание к 15 годам жизни переносят до 90% детей, пик заболеваемости приходится на возраст от 2 до 6 лет. Экономический ущерб от заболеваний ветряной оспой, по экспертным оценкам, только за последние 2 года составил 4–4,5 млрд руб. Ветряная оспа относится к легким и самокупирующимся детским заболеваниям, но она может сопровождаться рядом тяжелых и потенциально смертельных осложнений, которые развиваются преимущественно у детей с ослабленным иммунитетом и взрослых. В России ежегодно регистрируются случаи смерти от ветряной оспы (в 2007–2008 гг. – 10 человек, в том числе 6 детей). Таким образом, актуальность проблемы ветряной оспы очевидна, что требует внедрения в практику здравоохранения России эффективного средства профилактики – иммунизации. На сегодняшний день в мире существуют три живые аттенуированные вакцины против ветряной оспы, в России зарегистрированы две из них – Окавакс и Варилрикс. В исследованиях, проведенных в Японии, было показано, что вакцина индуцирует у 100% привитых защитный иммунитет, сохраняющийся в течение 20 лет. В отличие от других вакцин, Окавакс вводится всем лицам старше 1 года всего в одной дозе.
Следовательно, известная с давних времен профилактическая медицинская технология (иммунопрофилактика) на современном этапе приобрела более высокую значимость, чем исключительно эпидемиологическая мера, призванная защитить население от инфекционных заболеваний. Данные доказательной медицины свидетельствуют о безопасности и эффективности современных вакцин для детей и позволяют считать их наиболее значимой медицинской технологией в комплексе первичной и вторичной профилактики. Дальнейшее совершенствование национального календаря прививок предусматривает замену моновакцин на современные поликомпонентные (комбинированные) вакцинные препараты, которые эффективны как у здоровых детей, так и у пациентов с отклонениями в сроках вакцинации.
СПРАВКА
- Вакцинация против вирусного гепатита B проводится всем новорожденным в первые 24 часа жизни.
-
Вакцинация против вирусного гепатита B детям, не относящимся к группам риска, проводится по схеме 0–1–6(первая доза – в момент начала вакцинации, вторая доза – через 1 месяц после 1-й прививки, третья доза – через 6 месяцев от начала иммунизации).
- Вакцинация против вирусного гепатита B детям из групп риска проводится по схеме 0–1–2–12 (первая доза – в первые 24 часа жизни, вторая доза – в возрасте 1 месяца, третья доза – в возрасте 2 месяцев, четвертая доза – в возрасте 12 месяцев). Группы риска включают новорожденных, родившихся от матерей: носителей HBsAg, больных вирусным гепатитом B; перенесших вирусный гепатит B в третьем триместре беременности; не имеющих результатов обследования на маркеры гепатита B; наркозависимых, в семьях, где есть носитель HbsAg, больной острым или хроническим вирусным гепатитом B.
-
Вакцинация новорожденных против туберкулеза проводится новорожденным вакцинами для щадящей первичной иммунизации (БЦЖ-М). В субъектах Российской Федерации с показателями заболеваемости, превышающими 80 на 100 тыс. населения, а также при наличии в окружении новорожденного больных туберкулезом –проводится вакциной для профилактики туберкулеза (БЦЖ).
- Ревакцинация против туберкулеза проводится не инфицированным микобактериями туберкулеза туберкулиноотрицательным детям в 7 и 14 лет. В субъектах Российской Федерации с показателями заболеваемости туберкулезом, не превышающими 40 на 100 тыс. населения, ревакцинация против туберкулеза в 14 лет проводится туберкулиноотрицательным детям, не получившим прививку в 7 лет.
- Вакцинация против дифтерии, столбняка, коклюша проводится детям, относящимся к группам риска: с иммунодефицитными состояниями или анатомическими дефектами, приводящими к резко повышенной опасности заболевания ХИБ-инфекцией; с онкогематологическими заболеваниями и/или длительно получающие иммуносупрессивную терапию; ВИЧ-инфицированным или рожденным от ВИЧ-инфицированных матерей; находящимся в закрытых детских дошкольных учреждениях (дома ребенка, детские дома, специализированные интернаты (для детей с психоневрологическими заболеваниями и др.), противотуберкулезные санаторно-оздоровительные учреждения).
- Курс вакцинации против гемофильной инфекции для детей в возрасте от 3 до 6 месяцев состоит из 3 инъекций по 0,5 мл с интервалом 1–1,5 месяца. Для детей, не получивших первую вакцинацию в 3 месяца, иммунизация проводится по следующей схеме: для детей в возрасте от 6 до 12 месяцев – из 2 инъекций по 0,5 мл с интервалом в 1–1,5 месяца; для детей от 1 года до 5 лет – однократная инъекция 0,5 мл.
- Вакцинация против полиомиелита проводится трехкратно: первый и второй раз – инактивированной вакциной против полиомиелита (ИПВ), третий раз – живой оральной вакциной против полиомиелита (ОПВ).
-
Вакцинация против кори проводится детям в возрасте до 15–17 лет включительно и взрослым в возрасте до35 лет, не привитым ранее, не имеющим сведений о прививках против кори и не болевшим корью ранее двукратно с интервалом не менее 3 месяцев между прививками. Лица, привитые ранее однократно, подлежат однократной иммунизации с интервалом не менее 3 месяцев между прививками.
- Вакцинация против краснухи проводится от 1 года до 18 лет не болевшим, не привитым, привитым однократно против краснухи и девушкам от 18 до 25 лет, не болевшим, не привитым ранее.
- Вакцинация против гриппа проводится: детям с 6 месяцев; учащимся 1–11 классов; студентам высших профессиональных и средних профессиональных учебных заведений; взрослым, работающим по отдельным профессиям и должностям (работникам медицинских и образовательных учреждений, транспорта, коммунальной сферы и др.); взрослым старше 60 лет.