Современные взгляды на иммуномодулирующую терапию при респираторных инфекциях у взрослых и детей: преимущества Полиоксидония
- Аннотация
- Статья
- Ссылки
- English

Введение
К наиболее распространенным инфекционно-воспалительным заболеваниям у взрослых и детей относятся респираторные инфекции, заражение которыми в отличие от других инфекций, например кишечных и урогенитальных, происходит через респираторный тракт. Респираторные инфекции могут вызывать различные возбудители – вирусы, бактерии, грибы и др. Но доминируют вирусы. Чаще развиваются острые респираторные вирусные инфекции (ОРВИ), на долю которых в структуре всей инфекционной патологии приходится 90%. ОРВИ или острые респираторные заболевания (ОРЗ) носят преимущественно сезонный характер. Вспышки обострений наблюдаются обычно в поздний осенний (ноябрь), зимний и ранний весенний (март) периоды. ОРВИ чаще болеют дети – до шести – десяти раз в год, взрослые – до четырех – шести раз в год.
Группу респираторных вирусов составляют вирусы, обладающие выраженным тропизмом к мукополисахаридам клеток слизистых оболочек респираторного тракта.
Вирусы, вызывающие ОРВИ
Как правило, инфекции респираторного тракта протекают с однотипными клиническими проявлениями в виде катаральных симптомов со стороны верхних дыхательных путей. Респираторные вирусные инфекции в основном вызываются вирусами пяти семейств, включающих как ДНК-, так и РНК-содержащие вирусы.
1. Семейство пикорнавирусов (Picornaviridae). В семейство входит четыре рода. К возбудителям ОРВИ относятся представители родов риновирусов и энтеровирусов. Это мелкие вирусы, геном которых представлен молекулой РНК. Риновирусы – один из самых многочисленных родов в царстве вирусов и содержит 113 серотипов. В половине случаев риновирусы становятся причиной ОРВИ у взрослых. Риновирусная инфекция имеет место в основном в холодное время года. Поскольку число серотипов вируса огромно, а перекрестный иммунитет отсутствует, не исключены рецидивы заболевания в одном и том же сезоне.
Энтеровирусы – вирусы Коксаки (Coxsackievirus) В, отдельные серотипы ЕСНО также способны вызывать ОРЗ, протекающие с лихорадкой, фарингитом, осложнениями в виде пневмонии и поражений плевры. ECHO-вирусы – это кишечные вирусы человека, представляющие собой мелкие РНК-содержащие вирусы из группы пикорнавирусов. Отдельные типы ECHO-вирусов могут вызывать асептический менингит, лихорадку, диарею, гастроэнтерит, респираторные инфекции и т.д.
2. Семейство коронавирусов (Coronaviridae). Семейство включает 13 видов вирусов: респираторные и энтеральные коронавирусы человека и животных. Их геном представлен одноцепочечной РНК. При коронавирусной инфекции чаще развивается острый профузный насморк, который продолжается до семи дней без повышения температуры. Характерны головная боль, кашель, фарингит. У детей болезнь имеет более тяжелое течение (бронхит, пневмония, лимфоаденит шейных узлов). Коронавирусные инфекции носят сезонный характер и распространены в основном в осенне-зимний период. Заболевание часто носит характер внутрисемейных и внутрибольничных вспышек.
3. Семейство парамиксовирусов (Paramyxoviridae). Это РНК-содержащие вирусы, покрытые суперкапсидной оболочкой. Род парамиксовирусов включает четыре серотипа вирусов парагриппа человека. У детей типы 1 и 2 вызывают тяжелые ларингиты с острым отеком и развитием стеноза гортани (ложный круп). Серотип 3 вируса парагриппа чаще ассоциируется с поражениями нижних дыхательных путей. Представитель семейства парамиксовирусов – респираторно-синцитиальный вирус (РС-вирус) – один из основных возбудителей тяжелых поражений нижних дыхательных путей у детей первого года жизни. РС-вирусная инфекция характеризуется развитием бронхита, бронхиолита, пневмонии. На этом фоне возможно формирование астматического синдрома, поскольку РС-вирус иногда служит пусковым механизмом развития аллергической реакции. Парагрипп и РС-инфекцию отличает отсутствие стойкого иммунитета, а высокий уровень антител в крови детей не является надежной гарантией против РС-вируса. В связи с этим данные вирусы представляют особую опасность, прежде всего для ослабленных детей. Вспышки могут протекать в виде внутрибольничных инфекций.
4. Семейство аденовирусов (Adenoviridae). Геном аденовирусов представлен линейной молекулой двунитевой ДНК. Среди аденовирусов человека выявлено 47 серотипов, объединенных в семь групп. Поскольку аденовирусная инфекция способна передаваться не только воздушно-капельным путем, но и при купании в бассейнах, наряду с осенне-зимними возможны летние вспышки инфекции. Особенностью аденовирусов является их способность длительно сохраняться (персистировать) в клетках миндалин, в связи с чем инфекция может принимать хроническую форму.
5. Семейство ортомиксовирусов (Orthomyxoviridae). Семейство ортомиксовирусов включает вирусы гриппа человека (Influenza virus A, Influenza virus B, Influenza virus C). С клинической точки зрения пречисление гриппа к ОРВИ вполне оправданно, поскольку полностью соответствует патогенезу и клиническим проявлениям заболевания.
Из-за способности данных вирусов вызывать глобальные вспышки – эпидемии и пандемии грипп уже давно выделен в отдельную нозологическую форму среди прочих ОРВИ. Эпидемии гриппа с завидным постоянством обрушиваются на человечество и в XXI веке [1–3].
Стадии патологического процесса
В патогенезе гриппа и ОРВИ выделяют пять основных стадий:
-
репродукцию вируса в клетках дыхательных путей;
-
вирусемию, приводящую к развитию токсических и токсико-аллергических реакций;
-
поражение слизистой оболочки респираторного тракта с преимущественной локализацией процесса в каком-либо его отделе;
-
возможные бактериальные осложнения со стороны респираторного тракта и других систем организма;
-
обратное развитие патологического процесса.
При поражении эпителия респираторного тракта вирусы подавляют его двигательную активность, функцию клиренса мукоцилиарного аппарата, функцию макрофагов и Т-лимфоцитов. Нейраминидаза вируса гриппа обладает способностью к модифицированию поверхностных гликопротеинов клеток, способствуя созданию новых мест для адгезии бактерий и развитию вторичной гнойной инфекции.
Иммунная система и иммунодефицит
Благодаря факторам врожденного (моноциты/макрофаги, нейтрофилы, дендритные клетки, NK- и Т-NK-лимфоциты) и приобретенного (Т- и В-клетки, ответственные за клеточный и гуморальный иммунный ответ) иммунитета у здоровых людей иммунная система эффективно защищает организм от инфекции путем распознавания и элиминации из организма чужеродных веществ антигенной природы, в частности возбудителей инфекции [1–3]. Тем не менее даже у здорового человека чрезмерное воздействие неблагоприятных факторов, как экзогенных, так и эндогенных, на иммунную систему способно приводить к нарушению (как правило, обратимому) ее функционирования и развитию иммунной недостаточности.
Иммунная недостаточность, или иммунодефицит, характеризуется дефицитом способности распознавать, элиминировать из внутренней среды и запоминать агенты чужеродной генетической природы, прежде всего микробные. В результате развиваются повышенная восприимчивость организма к инфекциям и другие иммунопатологические состояния. Причинами развития иммунной недостаточности, в частности, являются:
-
недоношенность (незрелость иммунной системы);
-
внутриутробная гипотрофия (голодание плода из-за недостаточного поступления питательных веществ из организма матери);
-
внутриутробная гипоксия (кислородное голодание плода, например, из-за анемии или токсикоза у матери);
-
внутриутробное инфицирование плода (грипп, цитомегаловирус, герпес, гепатиты, сифилис, хламидиоз, токсоплазмоз, микоплазмоз, мононуклеоз);
-
родовая травма (повреждение головного или спинного мозга);
-
постнатальная энцефалопатия или детский церебральный паралич;
-
резус-конфликт и гемолитическая болезнь новорожденного.
Клинические проявления вторичной иммунной недостаточности (ВИН) (часто рецидивирующие инфекционно-воспалительные заболевания, отличающиеся тяжестью течения, развитием осложнений, торпидностью к проводимой стандартной фармакотерапии) отмечаются и у других лиц, в частности из так называемых групп риска. Речь идет:
-
о лицах определенных возрастных групп (пожилого и старческого возраста, раннего детского возраста);
-
лицах, проживающих или работающих в экологически неблагоприятных условиях и подвергающихся постоянному воздействию радиационного, химического фактора;
-
часто и длительно болеющих детях;
-
беременных, страдающих рецидивирующими гнойно-воспалительными заболеваниями, перенесших тяжелые инфекции или травмы;
-
представителях определенных профессий (летчики, подводники, подвергающиеся постоянному стрессу, космонавты, испытывающие сверхвысокие физические нагрузки, перепады высоких и низких температур, специалисты МЧС, военнослужащие).
Более высокая заболеваемость гриппом и ОРВИ в некоторых возрастных группах обусловлена особенностями функционирования иммунной системы. Так, у новорожденных, особенно недоношенных детей, и детей с дефектами физического и психического развития к моменту рождения отмечаются незавершенное формирование гуморального и клеточного иммунитета, ограничения способности к дифференцированной выработке антител разного изотипа, а следовательно, к снижению иммунного ответа.
В пожилом и старческом возрасте имеют место необратимые изменения в системе гуморального и клеточного иммунитета в основном за счет инволюции тимуса и снижения секреции его гормонов (тимулина).
Пациентам с нарушениями функционирования иммунной системы требуется коррекция стандартной терапии с учетом выраженности клинико-иммунологических показателей при любой патологии, в том числе при ОРВИ и гриппе.
Подбор терапии
Особого подхода к подбору терапии требуют пациенты из группы риска, у которых грипп характеризуется тяжелым течением, развитием осложнений, непредсказуемостью прогноза. Например, у 18–40% детей раннего возраста из группы риска после перенесенного гриппа развиваются различные осложнения [4]. Частота госпитализации у детей от шести до 12 месяцев почти в шесть раз выше, чем у детей двух – четырех лет, и в 12 раз выше, чем y детей от пяти до 17 лет [5].
Терапия гриппа и ОРВИ прежде всего должна быть патогенетически обоснованной и воздействовать на все пять основных стадий заболевания.
Основным стандартом лечения ОРВИ и гриппа считается этиотропная (противовирусная, интерфероны (ИФН), индукторы ИФН), симптоматическая (устранение клинических проявлений и контроль за состоянием сопутствующих заболеваний: антипиретики, муколитики, бронхолитики, сердечные средства, антибактериальные препараты, комбинированные средства (ТераФлю и др.), другие по показаниям), профилактическая (вакцинация, иммуномодуляторы) терапия.
К противовирусным препаратам относятся ингибиторы нейраминидазы (осельтамивир (Тамифлю), занамивир (Реленза)), ингибиторы М2-белка (амантадин, Ремантадин), ингибиторы олигомеризации NP-белка вируса гриппа (Ингавирин).
Недостатки противовирусной терапии при гриппе и ОРВИ:
-
эффективность только при использовании в первые 24 часа от начала заболевания;
-
высокая стоимость курса лечения;
-
высокий риск побочных эффектов;
-
развитие устойчивости вируса к противовирусным препаратам;
-
противопоказания или ограничения к применению у конкретных лиц (например, беременных).
Основные усилия врача при лечении пациентов с респираторными инфекциями должны быть направлены на оптимизацию этиотропной терапии, в частности на борьбу с неоправданными назначениями антибактериальных и других средств, снижение тяжести клинических проявлений заболевания, нормализацию ослабленных реакций иммунитета (иммуномодуляторы) и профилактику осложнений.
Последние годы особое внимание уделяется иммуномодулирующей терапии при респираторных инфекциях у взрослых и детей.
В отличие от химиотерапии (противовирусные препараты, антибиотики) иммуномодуляторы не оказывают этиотропного влияния на возбудители инфекции, но, восстанавливая нормальный иммунный ответ, способствуют уничтожению инфекции, элиминации инфекционных агентов из организма и выздоровлению. Кроме того, на фоне иммуномодулирующей терапии снижается риск развития множественной резистентности инфекционной флоры к противоинфекционным средствам.
В 2005 г. по инициативе Научного центра института аллергии и инфекционных заболеваний США международной экспертной группой Комитета по изучению новых направлений в антимикробной терапии был создан согласительный документ «Иммуномодуляция». В нем сказано, что стратегия использования модуляции иммунного ответа в терапевтической практике имеет преимущества перед применением только стандартного лечения [6].
Разногласия и разночтения по этому вопросу обусловлены недостаточной информированностью практических врачей о механизмах действия, свойствах, показаниях и противопоказаниях к назначению иммуномодуляторов в клинической практике. Как следствие – ошибки назначения иммуномодулирующей терапии, ее неэффективность и даже развитие осложнений у лиц, имеющих противопоказания к применению иммуномодуляторов.
Распространенными ошибками при назначении иммуномодуляторов в клинике в целом и при респираторных заболеваниях в частности считаются:
-
необоснованное установление ВИН и отсутствие показаний к назначению иммуномодуляторов;
-
неправильное толкование причинно-следственных связей симптомов болезни;
-
установление иммунной недостаточности только на основании изменений на иммунограмме (в единичных исследованиях), в отсутствие клинических симптомов ВИН или при наличии клинических симптомов, не соответствующих таковым при иммунодефиците.
Прежде чем назначить иммуномодуляторы в комплексной этиотропной терапии респираторных заболеваний, необходимо:
-
установить основной и сопутствующие диагнозы, то есть выявить причинно-следственную связь симптомов болезни;
-
провести анализ объема и адекватности терапии по поводу основного заболевания и при необходимости скорректировать лечебные мероприятия по поводу выявленной патологии;
-
оценить функциональное состояние иммунной системы и при необходимости верифицировать нарушения в иммунологическом ответе.
Только после этого можно решать вопрос о целесообразности включения в схему лечения иммунотропной терапии, выбирать иммуномодулятор, который показан конкретному пациенту, схему и продолжительность иммунотропной терапии, а также схему контроля иммунологических маркеров.
Как правило, иммуномодуляторы назначают в комплексном лечении одновременно с базисной терапией, в частности с противовирусными (антибактериальными) препаратами, чтобы по возбудителю нанести двойной удар:
-
противовирусный (антибактериальный) препарат снижает функциональную активность возбудителя;
-
иммуномодулятор повышает функциональную активность клеток иммунной системы.
Добиться достаточного клинического эффекта только одним методом не представляется возможным.
В настоящее время на фармацевтическом рынке представлено множество лекарственных средств, относящихся к группе иммуномодуляторов [7].
В клинической практике предпочтение отдают химически чистым синтезированным препаратам, которые имеют существенные преимущества перед иммуномодуляторами других групп. При химическом синтезе в молекулу закладывают те свойства, которые хотят получить. Химически синтезированные иммуномодуляторы отличаются чистотой, не содержат балластных примесей (растительного и животного происхождения) и патогенных включений, способных спровоцировать развитие побочных фармакологических и аллергических реакций. Химически чистые иммуномодуляторы наиболее безопасны.
Полиоксидоний – приоритетный иммуномодулятор
К приоритетным иммуномодуляторам относятся только препараты, соответствующие основным требованиям, предъявляемым к этой группе лекарственных средств:
-
высокий профиль безопасности;
-
возможность применения в любом возрасте;
-
использование при различных сопутствующих заболеваниях любой стадии и степени тяжести болезни;
-
отсутствие взаимодействия с другими лекарственными средствами (антибактериальными, противовирусными, противогрибковыми, сердечно-сосудистыми);
-
возможность применения у пациентов с аллергическими заболеваниями.
Этим требованиям в полной мере соответствует иммуномодулятор из группы высокомолекулярных химически чистых, синтетических препаратов Полиоксидоний [8, 9]. Препарат характеризуется высоким профилем безопасности и высокой клинической эффективностью.
Полиоксидоний (азоксимера бромид), который по своему химическому строению близок к веществам природного происхождения, не имеет ни растительных, ни животных, ни иных примесей и применяется у пациентов с различными формами аллергической, аутоиммунной и онкологической патологии. Наличие нескольких лекарственных форм (свечи, таблетки, лиофилизаты для приготовления растворов для инъекций при различных способах парентерального введения) позволяет практическому врачу выбрать способ введения в зависимости от нозологической формы заболевания, степени тяжести, стадии болезни, возраста, сопутствующих заболеваний.
В чем состоят преимущества Полиоксидония?
Препарат можно назначать на любой стадии болезни, в том числе острой, в комплексной терапии с любыми лекарственными средствами.
Полиоксидоний характеризуется высоким профилем безопасности, не вызывает побочных эффектов, хорошо переносится, сочетается с любыми медикаментами.
Препарат не только относится к классическим иммуномодуляторам, но и обладает выраженными антиоксидантными, антитоксическими, мембранопротекторными и хелатирующими фармакологическими эффектами, что крайне важно для пациентов с рецидивирующими инфекциями.
Выраженная иммуномодулирующая активность Полиоксидония обусловлена прямым воздействием на факторы врожденного иммунитета и опосредованным – на факторы адаптивного иммунитета.
Полиоксидоний активирует фагоцитарные клетки, повышает естественную резистентность организма к бактериальным и вирусным инфекциям; усиливает антителообразование к Т-зависимым и Т-независимым антигенам как животного, так и микробного происхождения. Усиливая цитотоксическую активность NK-клеток, особенно при их исходно пониженных уровнях, препарат воздействует на естественные киллеры и стимулирует антителообразование.
Полиоксидоний активирует синтез цитокинов – интерлейкинов 1 и 6, фактора некроза опухоли альфа только при исходно пониженных уровнях их продукции, что исключает возможность гиперактивации иммунной системы. В настоящее время и в России, и за рубежом существует проблема, связанная с созданием антиген-неспецифических иммуномодуляторов, которые, активируя иммунную систему в целом (в том числе к конкретному антигену), не приводили бы к ее чрезмерному неадекватному истощению [10].
В отсутствие антигенного раздражителя Полиоксидоний не вызывает множественных циклов клеточных делений В- и Т-лимфоцитов, что отличает его от таких митогенов, как бактериальные липополисахариды и растительные лектины.
При активации иммунной системы препарат не истощает резервных возможностей системы кроветворения.
Полиоксидоний не приводит к изменению клеточного состава периферической крови, а наоборот, нормализует его.
Стимулируя иммунные реакции, препарат не нарушает естественных механизмов их торможения (нормальный процесс как формирования, так и функционирования уже сформировавшихся Т-супрессоров).
Достичь более быстрого и высокого клинического эффекта и предупредить развитие осложнений при инфицировании вирусом можно, решив две основные задачи. Первая – активировать защитные резервы организма, вторая – снизить симптомы интоксикации.
Детоксицирующие свойства Полиоксидония определяются уникальной химической структурой, включающей N-оксидные группы (70%), введенные в основную цепь макромолекулы и «якорные» функциональные группы (20%). N-оксидные соединения отличаются от других соединений самой высокой полярностью (дипольный момент N-оксида полиэтиленпиперазина около 5 Д, в то время как дипольный момент исходного полиамина 0,65 Д). Этим и обусловлена уникальная способность сорбировать циркулирующие в крови растворимые токсические субстанции и микрочастицы и снижать концентрацию токсических веществ в крови. Избавляя организм от токсинов, Полиоксидоний обеспечивает более легкое течение болезни.
Таким образом, Полиоксидоний – лекарственный препарат, сочетающий свойства иммуномодулятора и детоксиканта. Он помогает не только активировать иммунитет, но и выводить токсины из организма. Облегчение симптомов и улучшение самочувствия наблюдаются уже с первых дней лечения [11–15].
Антиоксидантные свойства Полиоксидония связаны с его способностью перехватывать в водной среде активные формы кислорода, супероксидного аниона, перекиси водорода, гидроксильного радикала и удалять их из организма. Полиоксидоний подавляет образование внеклеточного кислорода, но стимулирует образование внутриклеточных активных форм кислорода, от которых зависит гибель бактерий в клетке.
Мембранопротективные свойства препарата обеспечивают защиту клетки от повреждающего действия различных токсических веществ.
Большой клинический опыт многолетнего эффективного применения Полиоксидония у взрослых и детей в комплексной терапии респираторных и других заболеваний в сочетании с клиническими проявлениями ВИН позволяет рекомендовать его для включения в стандарты лечения и профилактики заболеваний, протекающих на фоне дисфункций иммунной системы [16–22].
В клинических исследованиях с участием часто болеющих детей (ЧБД) показано, что только включение Полиоксидония в комплексную терапию ЧБД с частыми рецидивами ОРВИ позволяет достоверно снизить частоту и длительность обострений инфекций [11–13, 20, 22]. При этом высокая клиническая эффективность комплексной терапии с включением Полиоксидония установлена при использовании как таблетированных, так и парентеральных форм.
Добавление Полиоксидония к комплексной терапии детей (табл. 1) [22] и взрослых в три раза снижает частоту обострений и увеличивает длительность ремиссии заболеваний.
Включение Полиоксидония в комплексное лечение ЧБД с вовлечением лимфоглоточного кольца позволяет добиваться высокого клинического эффекта, коррелирующего с нормализацией клинико-лабораторных и иммунологических показателей [19].
На фоне комплексного лечения с использованием Полиоксидония у пациентов в два раза быстрее снижаются болевые ощущения и местные воспалительные проявления, температура тела. Нормализация гемограммы отмечается в течение двух – пяти суток в сравнении с 6–17 сутками при традиционной терапии.
Полиоксидоний оказывает выраженный клинический эффект при разных способах введения (внутрь, местно, парентерально) при любых заболеваниях, протекающих на фоне дисфункции иммунной системы. Подтверждение тому – результаты многочисленных открытых сравнительных исследований, проведенных в ведущих клиниках российских государственных медицинских и медико-стоматологическом университетах.
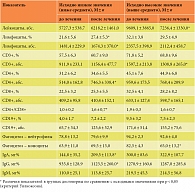
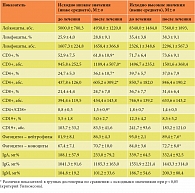
Кроме того, доказано, что Полиоксидоний влияет только на исходно сниженные показатели иммунитета независимо от способа введения (ректальное или внутримышечное). На исходно повышенные показатели иммунитета Полиоксидоний либо не влияет, либо несколько снижает их (табл. 2 и 3).
В группах пожилых лиц, получавших Полиоксидоний при исходно низких значениях указанных параметров, после курса отмечалось увеличение показателей на 20–50% от исходного уровня. Это свидетельствует о том, что выявленные изменения указанных параметров иммунного статуса обусловлены именно действием Полиоксидония.
Изменения в иммунном статусе, которые также можно связать с применением Полиоксидония, отмечались и в отношении фагоцитарной активности нейтрофилов и моноцитов периферической крови. У пациентов, получавших Полиоксидоний и имевших исходные показатели фагоцитоза на уровне верхней границы нормы и выше, после лечения показатели фагоцитоза приходили в норму.
Полиоксидоний используется не только в комплексном лечении любых заболеваний, протекающих в сочетании с иммунной недостаточностью, но и в виде монотерапии при проведении иммунореабилитационных мероприятий.
Показана клиническая эффективность профилактического предсезонного применения препарата как в виде ректальных суппозиториев, так и при внутримышечном введении у пациентов пожилого и старческого возраста, получавших лечение по разным схемам. Проведение предсезонного профилактического курса Полиоксидонием привело к увеличению в два раза длительности ремиссии хронических очагов инфекции. У большинства пациентов ремиссия составила четыре-пять месяцев. Примерно в два раза уменьшилась частота обострений, сократилась их длительность и частота госпитализаций [23, 24].
Заключение
К основным задачам иммунотропного лечения относятся активация сниженной иммунореактивности, подавление повышенного иммунного ответа при аутоиммунных и аллергических заболеваниях и заместительное лечение при дефектах иммунореактивности.
Перед назначением иммуномодуляторов прежде всего необходимо определить показания к их применению, установить возможность использования конкретного препарата у пациента, предложить дозы и схемы иммуномодулирующего лечения.
L.V. Luss
Institute of Immunology of the Russian Federal Medical and Biological Agency
Moscow State University of Medicine and Dentistry named after A.I. Evdokimov
Contact person: Lyudmila Vasilyevna Luss, lusslv@yandex.ru
Therapy of influenza and acute respiratory viral infections must be justified and act on the main arms of pathogenesis. Usually, immunomodulators are prescribed simultaneously with basic therapy. In clinical practice, chemically pure synthetic drugs displaying significant benefits are preferred over immunomodulators belonging to other pharmaceutic drugs. Polyoxidonium belongs to prioritized immunomodulators, which is characterized by high safety profile and high clinical efficacy.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.