Успешное применение комбинации иммунотерапии атезолизумабом и химиотерапии в первой линии при мелкоклеточном раке легкого
- Аннотация
- Статья
- Ссылки
- English
Введение
По заболеваемости рак легкого занимает первое место среди других злокачественных новообразований у мужчин в России, а по смертности – первое место среди мужчин и женщин как в России, так и в мире. В 2018 г. раком легкого заболели 51 573 человека, в Сибирском федеральном округе – 7378 человек. В Иркутской области выявлено 1113 новых случаев заболевания раком легкого. В подавляющем большинстве случаев заболевание диагностировано на III–IV стадии. Практически половина пациентов умерли в течение первого года [1, 2].
Рак легкого – собирательное понятие, объединяющее различные по происхождению, гистологической структуре, клиническому течению и результатам лечения злокачественные опухоли. К наиболее злокачественно протекающим опухолям с коротким анамнезом, быстрым течением и тенденцией к раннему метастазированию относится мелкоклеточный рак легкого (МКРЛ) [3].
Несмотря на то что МКРЛ считается опухолью, высокочувствительной к химиотерапии, и у многих пациентов достигается объективный ответ, лечение цитостатиками не может удовлетворить онкологов всего мира в эпоху расцвета таргетной терапии и революционной иммунотерапии опухолей. В противоопухолевой лекарственной терапии опухолей, несомненно, произошел прорыв. Тем не менее за последние 20 лет не было найдено и зарегистрировано ни одного эффективного таргетного препарата для лечения МКРЛ [4].
МКРЛ – опухоль с высоким уровнем соматических мутаций, в том числе в системе репарации ДНК. Именно появление нео-антигенов в опухоли в результате этих мутаций свидетельствует о том, что МКРЛ – опухоль с большим иммуногенным потенциалом. Для различных опухолей доказано, что мутационная нагрузка служит предиктором эффективности иммунотерапии. Это и заставляет задуматься об эффективности иммунотерапии в отношении МКРЛ [4–8].
В последнее время проводится много клинических исследований эффективности различных ингибиторов контрольных точек при МКРЛ. Одним из таких исследований является рандомизированное двойное слепое исследование I/III фазы IMpower133. В исследовании участвовали 403 пациента с распространенным МКРЛ, ранее не получавших химиотерапии. Пациентам одной группы назначали этопозид + карбоплатин + плацебо, пациентам другой – этопозид + карбоплатин + атезолизумаб. Атезолизумаб 1200 мг вводили внутривенно каждые три недели сначала вместе с каждым курсом химиотерапии, затем в качестве поддерживающей терапии до прогрессирования заболевания. В результате достоверное увеличение как выживаемости без прогрессирования (ВБП), так и общей выживаемости (ОВ) достигнуто на фоне применения атезолизумаба [9].
IMpower133 – первое исследование III фазы за последние три десятилетия, показавшее достоверное увеличение ОВ у больных диссеминированным МКРЛ [9]. На основании полученных результатов комбинация атезолизумаба, этопозида и карбоплатина стала новым стандартом первой линии терапии распространенного МКРЛ и официально разрешена к применению в России [3, 4, 9].
Клинический случай
Пациентка Л. 57 лет обратилась в Иркутский областной онкологический диспансер в апреле 2019 г. с жалобами на общую слабость, одышку при незначительной физической нагрузке, малопродуктивный кашель, дискомфорт в грудной клетке, отечность лица и шеи, осиплость голоса. Выраженность указанных симптомов постепенно увеличивалась в течение полугода.
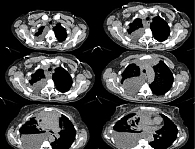
При осмотре пациентки обращали на себя внимание отечность и цианоз лица и шеи, варикозно-расширенные вены передней грудной клетки и шеи. Состояние по шкале ECOG – 1 балл, индекс Карновского – 80%. По данным дополнительных методов исследования, в переднем средостении выявлено новообразование с четкими бугристыми контурами, выраженно неоднородной структуры, с жидкостными компонентами по периферии, размером 226 × 160 × 235 мм, с инвазией в мягкие ткани грудной клетки, сосудистые структуры, перикард, сердце, плевру (рис. 1). Эндоскопически в правом верхнедолевом бронхе обнаружена опухоль с распространением на карину бифуркации трахеи, морфологически представляющая собой злокачественную мелкокруглоклеточную опухоль. Правосторонний парез гортани. Кроме того, обнаружены множественные очаговые образования правого легкого. Гидроперикард.
На основании данных комплексного обследования установлен диагноз: рак верхней доли правого легкого, Т4N3М1, IV стадия. Канцероматоз медиастинальной плевры, метастазы в легких. Синдром сдавления верхней полой вены.
В соответствии с клиническими рекомендации Ассоциации онкологов России, консилиумом врачей Иркутского областного онкологического диспансера составлен план лечения: противоопухолевая лекарственная терапия. Проведено четыре цикла терапии по схеме: этопозид 100 мг/м2 в 1–3-й дни + карбоплатин AUC 5 в 1-й день + атезолизумаб 1200 мг в 1-й день. Цикл – 21 день. Уже после первого введения препаратов клинически купировано сдавление верхней полой вены. На фоне терапии осложнений 3–4-й степени CTCAE не отмечалось, только после первого цикла терапии зафиксирована нейтропения 2-й степени СТСАЕ: протекала бессимптомно, купирована самостоятельно.
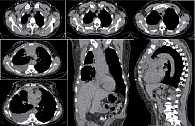
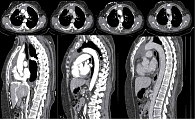
На фоне лечения достигнут частичный ответ. По данным контрольной мультиспиральной компьютерной томографии (МСКТ) органов грудной клетки (ОГК) – картина с положительной динамикой за счет уменьшения общих размеров образования в корне легкого и вдоль костальной плевры, восстановление просвета среднедолевого бронха справа. Инфильтрация переднего средостения на всем протяжении, уменьшение размеров мягкотканного компонента на 40% (согласно критериям irRecist) (рис. 2). Далее назначена поддерживающая терапия атезолизумабом 1200 мг каждые три недели, которая продолжается в настоящее время. Завершено 20 циклов терапии. На фоне лечения сохраняется стабилизация опухолевого процесса. Контрольная МСКТ ОГК после 18 циклов продемонстрировала стойко сохраняющийся ответ на лечение (рис. 3). При этом качество жизни пациентки удовлетворительное, что в конечном итоге и является основной целью терапии.
Дискуссия
МКРЛ – особая форма рака легкого, характеризующаяся быстрым ростом первичной опухоли, ранним метастазированием, высокой чувствительностью к химиотерапии. Нередко МКРЛ осложняется развитием синдрома сдавления верхней полой вены стремительно растущей опухолью или увеличенными медиастинальными лимфоузлами. Кроме того, МКРЛ может сопровождаться паранеопластическими синдромами, в частности миастеническим синдромом Ламберта – Итона [10]. Клинические особенности МКРЛ обусловлены высокой мутационной нагрузкой (в том числе в системе репарации ДНК), высоким иммуногенным потенциалом. Это может приводить к активации иммунной системы против опухоли, что обеспечивает лучший прогноз [4].
На прогноз больных МКРЛ также влияет состав популяции инфильтрирующих опухоль лимфоцитов. Количество эффекторных CD4+ T-лимфоцитов, продуцирующих интерлейкин 17, который в свою очередь обладает прямым антипролиферативным эффектом и способностью вызывать апоптоз, у пациентов с локализованным МКРЛ и длительным безрецидивным периодом больше, чем у пациентов с распространенным МКРЛ и прогрессированием заболевания соответственно [4, 11].
Наконец, известно, что экспрессия PD-L1 свидетельствует об активации Т-клеточного иммунного ответа и ассоциируется с лучшим прогнозом у больных МКРЛ [11]. Таким образом, подтверждается возможность применения моноклональных антител, блокирующих взаимодействие рецепторов PD-1 на Т-лимфоцитах иммунной системы и лигандов PD-L1 и PD-L2 на опухолевой клетке, то есть ингибиторов контрольных точек.
Одно из первых исследований – рандомизированное исследование II фазы по оценке сравнительной эффективности ипилимумаба (моноклональное антитело к рецептору CTLA-4, блокирующему активацию цитотоксических Т-лимфоцитов при взаимодействии с опухолевой клеткой) в комбинации с паклитакселом и карбоплатином и комбинации паклитаксела и карбоплатина с плацебо у больных диссеминированным МКРЛ. В данном исследовании ВБП в группе ипилимумаба составила 6,4 месяца, что достоверно выше, чем в контрольной группе, – 5,3 месяца (отношение рисков 0,64; р = 0,03). Однако прирост показателя ОВ не достиг статистической достоверности: в группе ипилимумаба и химиотерапии – 12,9 месяца, в группе химиотерапии – 9,9 месяца [12].
Еще одна попытка оценить эффективность и переносимость ипилимумаба в комбинации с этопозидом и препаратами платины у больных диссеминированным МКРЛ была предпринята в многоцентровом рандомизированном исследовании III фазы СА184-156. Медиана ВБП составила 4,6 месяца в группе ипилимумаба и 4,4 месяца (95%-ный доверительный интервал (ДИ) 4,4–4,6) в группе плацебо. Медиана ОВ достигла 11 месяцев в группе ипилимумаба и 10,9 месяца (95% ДИ 10–11,5) в группе плацебо. Различия статистически не достоверны – исследование оказалось негативным [13].
В многоцентровом открытом исследовании I/II фазы CheckMate032 сравнивали эффективность и переносимость ниволумаба в монотерапии (в дозе 3 мг/кг) и ниволумаба в комбинации с ипилимумабом в различных дозовых режимах (1 + 3 и 3 + 1 мг/кг соответственно) у больных распространенным МКРЛ с прогрессированием после не менее одной платиносодержащей химиотерапии. Несмотря на небольшое количество объективных ответов (в группе монотерапии ниволумабом объективный ответ составил лишь 10% (10/98)) в группах комбинированной терапии – 23 и 19%, эффект от лечения оказался длительным [14]. На основании результатов данного исследования ниволумаб в монорежиме или комбинации с ипилимумабом был внесен в рекомендации NCCN у больных рецидивным МКРЛ, получивших не менее одной линии платиносодержащей химиотерапии. В 2018 г. ниволумаб был одобрен для применения и в России в качестве третьей линии терапии больных диссеминированным МКРЛ.
Еще одной возможной точкой приложения ниволумаба и ипилимумаба является поддерживающая иммунотерапия у пациентов с локализованным МКРЛ без прогрессирования после завершения химиолучевой терапии. В настоящее время возможность применения этих препаратов оценивается в исследовании II фазы STIMULI [15].
Атезолизумаб – моноклональное антитело к рецептору PD-L1. Препарат продемонстрировал активность у больных МКРЛ с прогрессированием после проведенной химиотерапии в исследовании Ia стадии (NCT01375842), в котором принимали участие пациенты с различными солидными опухолями [16]. В исследование было включено 17 больных распространенным МКРЛ, при этом 65% из них получили не менее трех линий химиотерапии. В соответствии с критериями RECIST, объективный ответ составил 6%, а в соответствии с критериями irRecist (критерии, специально разработанные для иммунотерапии) – 24%. Медиана ВБП достигла 1,5 месяца, а медиана ОВ – 5,9 месяца.
В рандомизированном исследовании II фазы IFCT-1603 атезолизумаб не показал эффективности во второй линии терапии по сравнению с химиотерапией топотеканом или реиндукцией этопозида и карбоплатина в зависимости от показаний. Медиана ВБП составила 1,4 месяца в группе атезолизумаба и 4,2 месяца в группе химиотерапии, причем различия были статистически достоверны (р = 0,004) [17].
Наконец, проведено исследование эффективности атезолизумаба в комбинации с химиотерапией у больных, ранее не получавших лечения. В рандомизированное двойное слепое исследование I/III фазы IMpower133 было включено 403 пациента с распространенным МКРЛ, не получавших химиотерапии. Пациентам одной группы назначали этопозид + карбоплатин + плацебо, пациентам другой – этопозид + карбоплатин + атезолизумаб. Атезолизумаб 1200 мг вводили внутривенно каждые три недели сначала вместе с каждым курсом химиотерапии, затем в качестве поддерживающей терапии до прогрессирования заболевания. Достоверное увеличение и ВБП, и ОВ было получено при первом промежуточном анализе [9]. После медианы наблюдения 13,9 месяца медиана ОВ в группе атезолизумаба составила 12,3 месяца (95% ДИ 10,8–15,9), а в группе плацебо – 10,3 месяца (95% ДИ 9,3–11,3; р = 0,0069). ВБП достигла 5,2 месяца (95% ДИ 4,4–5,6) в группе атезолизумаба и 4,3 месяца (95% ДИ 4,2–4,5) в группе плацебо (p = 0,017).
Одногодичная ВБП группе атезолизумаба в два раза превысила таковую в группе плацебо – 12,6 против 5,4%. И хотя частота объективных ответов в группах атезолизумаба и плацебо в целом была сопоставима – 60,2 vs 64,4%, доля продолжающихся ответов была значительно выше в группе атезолизумаба – 14,9 против 5,4%. При межгрупповом анализе установлено, что преимущество в ОВ в группе атезолизумаба в комбинации с химиотерапией не зависит от пола, возраста (≥ 65 или < 65 лет), состояния ECOG (0 или 1 балл) и наличия метастазов в печени. Увеличение ОВ в группе атезолизумаба оказалось недостоверным только у больных с метастатическим поражением головного мозга, несмотря на проведенное лечение (облучение всего головного мозга или стереотаксическая лучевая терапия). Токсичность терапии не отличалась от таковой химиотерапии и атезолизумаба. Наиболее частыми нежелательными явлениями 3–4-й степени были нейтропения (23%), анемия (14%) и тромбоцитопения (10%). Иммуноопосредованные нежелательные явления (сыпь (19%), гипотиреоидизм (13%) и гепатит (7%)) зарегистрированы у 40% больных группы атезолизумаба и 25% больных группы плацебо [4, 9].
Таким образом, IMpower133 – первое исследование III фазы за последние три десятилетия, показавшее достоверное увеличение ОВ у больных диссеминированным МКРЛ. Комбинация этопозида, карбоплатина и атезолизумаба – новый стандарт первой линии терапии распространенного МКРЛ. Данная схема лечения недавно официально разрешена для применения в России и на практике показывает высокую эффективность у пациентов с МКРЛ даже при таких прогностически неблагоприятных состояниях, как синдром сдавления верхней полой вены.
Выводы
МКРЛ – одна из самых высоко злокачественных опухолей, склонных к раннему метастазированию и поэтому выявляемых обычно уже в диссеминированной форме.
Впервые за последние 20 лет в лечении МКРЛ зарегистрирована новая эффективная комбинация атезолизумаба, этопозида и карбоплатина, ставшая новым стандартом первой линии терапии МКРЛ. В настоящее время проводятся клинические исследования различных ингибиторов контрольных точек, определяются новые точки и место приложения препаратов для увеличения эффективности терапии МКРЛ.
S.S. Sidorova, D.Yu. Yukalchuk, D.M. Ponomarenko, Ye.A. Rybkina, D.A. Bogomolov, I.D. Klimova, Ye.S. Tyumentseva, S.P. Sidorov
Irkutsk Regional Oncological Dispensary
Contact person: Svetlana S. Sidorova, s_koninina@mail.ru
The article presents the case of successful use of the combination of atezolizumab with etoposide and carboplatin in the first-line treatment of small cell lung cancer (SCLC) complicated by superior vena cava compression syndrome. Despite the fact that SCLC is one of the most prognostically unfavorable malignancies, over the past decades, SCLC therapy has not undergone any changes and included only cytostatics. Currently, immunotherapy is actively being used in the drug therapy of various types of tumors, including SCLC. For the first time in many years, the significant increase in the median overall survival and progression-free survival was achieved due to the addition of a PD-L1-antibody inhibitor to the standard SCLC chemotherapy.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.