Химиоиммунотерапия немелкоклеточного рака легкого. Cлучай длительного ответа, несмотря на отмену терапии
- Аннотация
- Статья
- Ссылки
- English


Ингибиторы контрольных точек иммунитета изменили парадигму лечения метастатического немелкоклеточного рака легкого с отсутствием драйверных мутаций. В первой линии терапии в случаях умеренной экспрессии PD-L1 наиболее эффективным подходом является использование комбинированной химиоиммунотерапии [1]. В зависимости от клинической ситуации могут быть использованы комбинации химиотерапии с пембролизумабом [2, 3] как при плоскоклеточном, так и неплоскоклеточном раке легкого, двойная иммунотерапия ниволумабом и ипилимумабом с двумя циклами химиотерапии [4], а также в случаях аденокарциномы легкого возможно применение комбинации атезолизумаба, химиотерапии и бевацизумаба [5].
Клинический случай
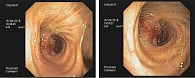
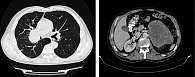
Пациент 1959 г. рождения, заядлый курильщик, обратился в Иркутский областной онкологический диспансер в сентябре 2019 г. с жалобами на нарастающую слабость, кашель, кровохарканье, снижение веса. При обследовании (рис. 1, 2) выявлена опухоль правого легкого с поражением промежуточного, верхнедолевого и правого главного бронхов с инвазией в ствол правой легочной артерии, метастазами в паренхиму легких, забрюшинные лимфоузлы и левый надпочечник, осложненная ателектазом средней доли и кровохарканьем. Морфологическое, цитологическое и гистологическое исследования установили плоскоклеточный рак без ороговения. Гистогенез опухоли был подтвержден иммуногистохимическим исследованием, которое также выявило умеренную позитивную экспрессию PD-L1 в 30% опухолевых клеток (клон DAKO 22C3). Установлен диагноз: центральный плоскоклеточный рак правого легкого Т3N2M1с IV стадии.
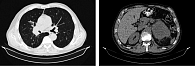
С 8 октября по 10 декабря 2019 г. проведено четыре курса химиоиммунотерапии пембролизумабом, паклитакселом и карбоплатином. На фоне лечения состояние пациента улучшилось, уменьшились слабость, кашель, исчезло кровохаркание, отмечено увеличение веса на 5 кг (7% от массы тела). При контрольном обследовании в декабре 2019 г., по данным мультиспиральной компьютерной томографии (МСКТ), достигнута частичная регрессия опухоли с уменьшением на 42% в соответствии с RECIST 1.1 (рис. 3).
После четырех курсов химиоиммунотерапии пациенту был назначен пембролизумаб в монорежиме 200 мг в/в один раз в три недели. Были выполнены введения 30 декабря 2019 г. и 21 января 2020 г. Одновременно отмечалось увеличение показателей аспартатаминотрансферазы (АСТ) и аланинаминотрансферазы (АЛТ) до 1-й степени токсичности по СТС AE v5.0 к четвертому курсу химиоиммунотерапии. После второго введения пембролизумаба в монорежиме при оценке лабораторных показателей 10 февраля 2020 г. зарегистрирована 3-я степень токсичности в соответствии с СТС AE v5.0. Показатели АЛТ и АСТ достигли 458,88 ед/л (норма 0,00–31,00 ед/л) и 294,63 ед/л (норма 0,00–32,00 ед/л) соответственно.
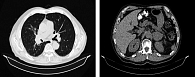
Наряду с этим произошло увеличение общего билирубина до 44,1 мкмоль/л (норма 6,6–28,2 мкмоль/л) – 2-я степень токсичности. Выполнены исследование маркеров гепатитов В и С и ультразвуковое исследование печени и желчных путей, не выявившие клинически значимых отклонений. Пациенту был установлен диагноз: иммуноопосредованный гепатит 3-й степени токсичности. Терапия пембролизумабом была отменена, пациент госпитализирован, назначены инфузионная терапия, адеметионин, преднизолон в дозе 150 мг (2 мг/кг) в сутки, омепразол, калия и магния аспарагинат перорально. Показатели АЛТ, АСТ и билирубина снизились до уровня, соответствующего 1-й степени токсичности, в течение двух недель терапии глюкокортикоидами и нормализовались на пятой неделе лечения. После нормализации показателей преднизолон был отменен с постепенным снижением дозы. Пациент продолжил активное наблюдение, и при контрольных обследованиях сохранялся ранее описанный положительный эффект (рис. 4, 5), хотя терапия пембролизумабом не возобновлялась.
Достигнутая в декабре 2019 г. частичная регрессия опухоли сохранялась до июля 2021 г., когда было выявлено прогрессирование опухоли (рис. 6) с увеличением первичной опухоли в корне правого легкого, ростом метастаза в левом надпочечнике и появлением метастазов в печени. Пациенту была назначена терапия второй линии доцетакселом, проведено три курса. Лучший ответ на лечение – стабилизация. Пациент погиб от прогрессирования опухолевого процесса в ноябре 2021 г.
Обсуждение
Лечение ингибиторами контрольных точек иммунитета может быть связано с рядом неблагоприятных иммуноопосредованных явлений: гипо- и гипертиреоз, общие симптомы, такие как усталость или миалгия, респираторные расстройства и кожные расстройства, расстройства желудочно-кишечного тракта, включая энтероколиты и гепатит [6]. В представленном нами случае пациент с плоскоклеточным раком легкого и умеренной экспрессией PD-L1 получал комбинированную химиоиммунотерапию. Терапия пембролизумабом была прекращена после шести введений (четыре месяца терапии) вследствие развившегося иммуноопосредованного гепатита 3-й степени тяжести. После коррекции возникшего осложнения, в соответствии с клиническими рекомендациями, терапия пембролизумабом не возобновлялась [6].
Однако достигнутый объективный ответ в виде частичной регрессии опухоли сохранялся после отмены терапии еще в течение полутора лет. Такой длительно сохраняющийся эффект от проведенного лечения после его отмены говорит об эффективности комбинированной химиоиммунотерапии с использованием пембролизумаба. Вероятно, пациенты, отвечающие на терапию ингибиторами контрольных точек иммунитета, имеют большую предрасположенность к развитию иммуноопосредованных побочных эффектов [7]. У нашего пациента общая продолжительность времени без прогрессирования с момента начала терапии пембролизумабом, карбоплатином и паклитакселом составила 21 месяц, а продолжительность жизни – 26 месяцев.
Заключение
Комбинация химиотерапии и пембролизумаба является эффективной опцией для лечения пациентов с метастатическим НМРЛ с умеренной экспрессией PD-L1 и может индуцировать длительные по продолжительности ответы на терапию, несмотря на прекращение лечения вследствие развившихся иммуноопосредованных побочных эффектов.
D.M. Ponomarenko, D.Yu. Yukalchuk, S.S. Sidorova, E.V. Snetkov, Yu.A. Chapygina
Irkutsk Regional Oncological Dispensary
Contact person: Dmitry M. Ponomarenko, dmitry@ood38.ru
The article presents a clinical case of achieving long-term remission in a patient with disseminated squamous non-small cell lung cancer on combination therapy with pembrolizumab, paclitaxel and carboplatin, despite the early cancellation of therapy after the development of immuno-mediated hepatitis.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.