Опыт применения дурвалумаба при нерезектабельном немелкоклеточном раке легкого третьей стадии: окончательные результаты
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. В исследовании приняли участие семь больных немелкоклеточным раком легкого, у которых не отмечалось прогрессирования заболевания по окончании химиолучевой терапии. Дурвалумаб назначали в дозе 10 мг/кг внутривенно один раз в две недели. Применение препарата в данном режиме продолжалось до прогрессирования процесса, или до тех пор, пока пациент получал клиническую пользу, или до появления непереносимой токсичности.
Результаты. Двое из семи пациентов получали терапию до прогрессирования заболевания в течение трех месяцев, двое – в течение шести месяцев, один – в течение девяти месяцев, один – в течение 13 месяцев и еще один – в течение 19 месяцев.
Тяжелых иммуноопосредованных нежелательных явлений не зафиксировано. Наблюдавшиеся гематологические и негематологические нежелательные реакции первой и второй степени не привели к отмене препарата.
Заключение. Монотерапия дурвалумабом характеризуется высокой эффективностью, приемлемым профилем токсичности и потенциально ассоциируется с высокой общей выживаемостью больных.
Материал и методы. В исследовании приняли участие семь больных немелкоклеточным раком легкого, у которых не отмечалось прогрессирования заболевания по окончании химиолучевой терапии. Дурвалумаб назначали в дозе 10 мг/кг внутривенно один раз в две недели. Применение препарата в данном режиме продолжалось до прогрессирования процесса, или до тех пор, пока пациент получал клиническую пользу, или до появления непереносимой токсичности.
Результаты. Двое из семи пациентов получали терапию до прогрессирования заболевания в течение трех месяцев, двое – в течение шести месяцев, один – в течение девяти месяцев, один – в течение 13 месяцев и еще один – в течение 19 месяцев.
Тяжелых иммуноопосредованных нежелательных явлений не зафиксировано. Наблюдавшиеся гематологические и негематологические нежелательные реакции первой и второй степени не привели к отмене препарата.
Заключение. Монотерапия дурвалумабом характеризуется высокой эффективностью, приемлемым профилем токсичности и потенциально ассоциируется с высокой общей выживаемостью больных.
Введение
Рак легкого является одним из самых распространенных видов рака. Кроме того, он занимает лидирующие позиции в структуре смертности онкологических больных.
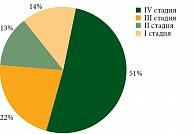
В Иркутской области в 2019 г. диагноз «немелкоклеточный рак легкого» (НМРЛ) поставлен 1152 пациентам, из них 893 (77,5%) мужчин и 259 (22,5%) женщин. Всего на диспансерном учете состояло 2807 человек, сняты с учета в связи со смертью – 702 [1]. Данные по стадиям впервые выявленного НМРЛ представлены на рис. 1.
Приблизительно у 30% при постановке диагноза обнаружена местнораспространенная нерезектабельная стадия [1]. Пациентам с местнораспространенным нерезектабельным НМРЛ и хорошим соматическим статусом показана одновременная химиолучевая терапия (ХЛТ) на основе препаратов платины. После проведения таковой медиана выживаемости без прогрессирования не превышает 13 месяцев [2]. До окончания пятилетнего периода наблюдения доживают не более 15% [2]. В отсутствие заметных достижений в области лечения местнораспространенного нерезектабельного НМРЛ [3–7] назрела необходимость в разработке новых терапевтических подходов для повышения выживаемости больных после одновременной ХЛТ.
Необходимо отметить, что современные стандарты по ведению пациентов после ХЛТ предполагают только динамическое наблюдение с целью выявления признаков рецидива или метастазирования [8, 9]. Так, согласно рекомендациям экспертов Европейского общества медицинской онкологии (European Society for Medical Oncology – ESMO), по завершении лечения местнораспространенного НМРЛ последующее наблюдение должно включать [8, 9]:
- изучение анамнеза и физикальное обследование каждые шесть месяцев в течение первых двух лет, затем ежегодно;
- проведение компьютерной томографии органов грудной клетки с контрастированием не реже одного раза в год;
- при возможности назначения противоопухолевой терапии проведение повторной компьютерной томографии каждые полгода в течение трех лет;
- консультирование о модификации образа жизни (отказ от курения) и фармакотерапии.
На сегодняшний день ни в одном исследовании по оценке консолидирующих курсов химиотерапии после ХЛТ положительных результатов не получено [3–7]. Именно поэтому эксперты ESMO не рекомендуют назначать консолидирующую химиотерапию после ХЛТ по радикальной программе. Они также ссылаются на отсутствие убедительных доказательств о какой-либо дополнительной пользе такого лечения для пациентов с местнораспространенным НМРЛ [9].
Первым рандомизированным исследованием фазы III ингибитора иммунных контрольных точек у больных местнораспространенным нерезектабельным НМРЛ III стадии без прогрессирования после одновременной ХЛТ на основе платиносодержащих препаратов стало исследование PACIFIC [10, 11]. В нем сравнивали эффективность и безопасность антитела к PD-L1 дурвалумаба в дозе 10 мг/кг один раз в две недели и плацебо. Пациентов включали в исследование через 1–42 дня по окончании одновременной ХЛТ при условии, что проведено не менее двух циклов химиотерапии на основе препаратов платины.
Дурвалумаб продемонстрировал статистически и клинически значимые преимущества перед плацебо как в отношении выживаемости без прогрессирования, так и в отношении общей выживаемости. Медиана выживаемости без прогрессирования по независимой заслепленной центральной оценке составила 17,2 месяца в группе дурвалумаба и 5,6 месяца в группе плацебо (относительный риск (ОР) 0,51; 95%-ный доверительный интервал (ДИ) 0,41–0,63). Таким образом, разница в медианах выживаемости без прогрессирования составила около года. Увеличение выживаемости без прогрессирования наблюдалось во всех предопределенных подгруппах пациентов, получавших дурвалумаб.
Результаты трехлетней общей выживаемости были представлены на конгрессе Американского общества клинической онкологии в 2019 г. [11]. Так, медиана общей выживаемости в группе дурвалумаба не была достигнута. В группе плацебо она составила 29,1 месяца. Стратифицированный ОР смерти – 0,69 (95% ДИ 0,55–0,86).
Дурвалумаб значительно превосходил плацебо по частоте ответа – 30,0 и 17,8% соответственно. Кроме того, медиана длительности ответа в группе дурвалумаба не была достигнута. В группе плацебо таковая составила 18,4 месяца [10].
Частота выявления новых очагов, включая метастазы в головном мозге, у получавших дурвалумаб оказалась ниже, чем у применявших плацебо [10].
Результаты исследования PACIFIC коренным образом изменили подход к тактике ведения пациентов после ХЛТ, что нашло отражение в клинических рекомендациях Национальной сети многопрофильных онкологических учреждений США [12]. В них предусмотрено, что терапия дурвалумабом показана после радикального курса одновременной ХЛТ у пациентов со всеми подстадиями III стадии нерезектабельного НМРЛ в качестве единственной лечебной опции.
По данному показанию дурвалумаб зарегистрирован в России в июле 2019 г. [13].
Цель исследования
В исследовании предполагалось оценить эффективность и безопасность дурвалумаба у пациентов с нерезектабельным немелкоклеточным раком легкого III стадии после химиолучевого лечения.
Материал и методы
Набор пациентов в рамках персонализированной программы использования незарегистрированного лекарственного препарата дурвалумаб (MEDI 4736) для терапии больных местнораспространенным нерезектабельным НМРЛ по окончании химиолучевой терапии проводился на базе областного онкологического диспансера г. Иркутска с октября 2018 г.
Основные критерии включения в исследование:
- возраст старше 18 лет;
- гистологически или цитологически подтвержденный местнораспространенный нерезектабельный НМРЛ III стадии (в соответствии с версией 7 IASLC Staging Manual in Thoracic Oncology);
- законченная платиносодержащая химиотерапия, проводимая одновременно или последовательно с лучевой терапией, без признаков прогрессирования заболевания;
- проведение режимов химиотерапии в соответствии со стандартами, в рамках химиолучевого лечения суммарная доза лучевой терапии 60 Гр ± 10% (54–66 Гр);
- начало лечения дурвалумабом менее чем через три месяца по окончании лучевой терапии.
В исследование не включали пациентов со смешанной гистологией рака легкого (мелкоклеточный и немелкоклеточный), ранее получавших любые антитела к PD/PD-L1, включая дурвалумаб, с активными или ранее документально подтвержденными аутоиммунными заболеваниями, тяжелой сопутствующей патологией.
Все участники исследования подписали информированное согласие на участие.
План лечения каждого пациента сформирован на общем мультидисциплинарном консилиуме диспансера и одобрен Министерством здравоохранения Российской Федерации.
Все пациенты после ХЛТ получали дурвалумаб в дозе 10 мг/кг один раз в две недели до прогрессирования заболевания, или до тех пор, пока отмечалась клиническая польза от данного вида лечения, или до появления непереносимой токсичности.
Оценка объективного ответа проводилась на основании данных мультиспиральной компьютерной томографии с внутривенным контрастированием согласно критериям RECIST v.1.1.
Анализ токсичности выполнен с помощью критериев СТС AE v.4.
Определяли также выживаемость без прогрессирования (время с момента регистрации до документального подтверждения прогрессирования) и общую выживаемость (время с момента регистрации до даты смерти от любой причины). Функцию выживаемости оценивали методом Каплана – Майера.
Результаты
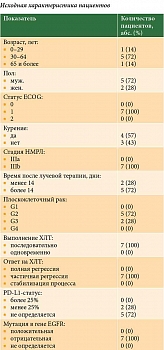
Всего в исследование было включено семь пациентов. Их исходные характеристики представлены в таблице [14].
Из семи больных двое получали терапию дурвалумабом до прогрессирования заболевания в течение трех месяцев, двое – в течение шести, один – в течение девяти месяцев, один – в течение 13, один пациент – в течение 19 месяцев.
Тяжелых иммуноопосредованных нежелательных явлений не зафиксировано. Наблюдавшиеся гематологические и негематологические нежелательные реакции 1-й и 2-й степени не привели к отмене препарата.
В качестве примера рассмотрим клинический случай.
Пациент М., 1966 года рождения. При прохождении профилактического осмотра на рентгенограмме органов грудной клетки обнаружена опухоль в средостении.
При дообследовании в апреле 2018 г., по результатам мультиспиральной компьютерной томографии (МСКТ) органов грудной клетки, выявлена медиастинальная форма рака правого легкого. Пациент направлен в областной онкологический диспансер.
Согласно данным фибробронхоскопии, рак правого главного бронха с ростом на карину.
Гистологическое заключение: плоскоклеточный рак G3.
При проведении магнитно-резонансной томографии головного мозга и МСКТ органов брюшной полости и малого таза метастазы не выявлены. Состояние по шкале Восточной объединенной группы онкологов (Eastern Cooperative Oncology Group – ECOG) соответствовало нулю.
EGFR отрицательный.
Диагноз: рак правого легкого T4N3M0 IIIb стадии 2-й клинической группы.
В апреле 2018 г. начата химиотерапия доцетакселом 75 мг/м2 и цисплатином 75 мг/м2. Проведено четыре курса полихимиотерапии. Дата окончания – 19 июня 2018 г.
Через четыре месяца в ходе контрольного обследования выявлено умеренное уменьшение метастатических лимфоузлов в средостении (стабилизация по RECIST 1.1).
Проведена лучевая терапия до суммарной очаговой дозы 60 Гр. Завершена 17 августа 2018 г. в Южной Корее.
После контрольной МСКТ в сентябре 2018 г. зафиксирована стабилизация процесса, прогрессирование отсутствовало.
Пациент включен в персонализированную программу использования незарегистрированного препарата дурвалумаб, который был назначен в качестве консолидирующей терапии по жизненным показаниям.
С октября 2018 г. начата иммунотерапия дурвалумабом в дозе 10 мг/кг внутривенно один раз в две недели. Контрольное обследование проводилось каждые три месяца.
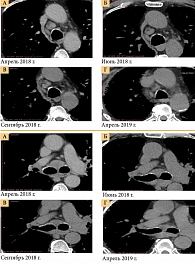
В апреле 2019 г., после шести месяцев терапии, рентгенологически подтверждена стабилизация процесса (рис. 2).
На контрольном обследовании в апреле 2020 г., согласно данным компьютерной томографии, при оценке опухоли по критериям RECIST 1.1 стабилизация процесса сохранялась. Масса тела стабильная, состояние по шкале ECOG – 1. Пациент вел активный образ жизни, продолжал работать.
За время терапии дурвалумабом нежелательных явлений не зарегистрировано.
В мае 2020 г. пациент погиб от травм в результате дорожно-транспортного происшествия. Патологоанатомическое заключение свидетельствовало об отсутствии прогрессирования злокачественной опухоли.
Обсуждение результатов
Существенный прогресс в терапии пациентов с местнораспространенным НМРЛ впервые был отмечен в исследовании PACIFIC. Установлено, что применение дурвалумаба по окончании ХЛТ может качественно изменить прогноз у данной категории больных. Речь, в частности, идет об увеличении продолжительности жизни.
В России для эффективного использования дурвалумаба в условиях реальной клинической практики необходимо пересмотреть ряд устоявшихся подходов. Так, в настоящее время в России ХЛТ при НМРЛ проводится не так часто. Некоторые пациенты получают ХЛТ в последовательном режиме (например, пациенты с ECOG 1 и 2). Эффект ХЛТ оценивается через один – три месяца после ее завершения, в то время как наиболее эффективным является максимально раннее начало применения дурвалумаба.
Согласно результатам нашего исследования, большинство пациентов получали последовательную ХЛТ и начинали вводить дурвалумаб более чем через две недели от последней дозы лучевой терапии (в приведенном клиническом случае спустя два месяца), что могло повлиять на результаты лечения.
В дальнейшем представляется важным оценить долгосрочные результаты применения данного препарата в условиях реальной практики.
Заключение
Монотерапия дурвалумабом характеризуется высокой эффективностью, приемлемым профилем токсичности и потенциально ассоциируется с высокой общей выживаемостью пациентов с нерезектабельным немелкоклеточным раком легкого III стадии после химиолучевого лечения [14].
D.Yu. Yukalchuk, D.M. Ponomarenko, T.N. Yukalchuk, A.M. Novopashin, G.N. Tepikina
Irkutsk Regional Oncological Dispensary
Contact person: Denis Yu. Yukalchuk, dyuyu558@mail.ru
Objective: to study the efficacy and safety of durvalumab in patients with unresectable non-small cell lung cancer of the third stage after chemoradiotherapy.
Material and methods. The study involved seven individuals with non-small cell lung cancer who did not show progression of the disease at the end of chemoradiotherapy. Durvalumab was administered at a dose of 10 mg/kg intravenously once every two weeks. The use of the drug in this mode continued until the progression of the process, or until the patient received clinical benefit, or until the appearance of intolerable toxicity.
Results. Two of seven patients received treatment before progression for three months, two – for six months, one – for nine months, one – for 13 months, and another – for 19 months.
No severe immune-mediated adverse events were recorded. The observed hematological and non-hematological adverse reactions of the first and second degree did not lead to the withdrawal of the drug.
Conclusion. Durvalumab monotherapy is highly effective, has an acceptable toxicity profile, and is potentially associated with a high overall survival rate in these patients.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.