Виферон против HCV. Опыт использования
- Аннотация
- Статья
- Ссылки



США хронический гепатит С является основной причиной, которая вызывает необходимость пересадки печени приблизительно у 200–300 тыс. человек в течение года. Каждая такая операция стоит порядка 100 тыс. долларов, а последующая иммуносупрессивная терапия на протяжении всей жизни обходится в 1–1,5 тыс. долларов ежемесячно. Данных по России о больных, которым необходима трансплантация печени, нет. Но если принять во внимание статистику США, то можно предположить, что таковых в нашей стране не меньше (33).
Правительство РФ предпринимает ряд мер, направленных на снижение угрозы заражения вирусными гепатитами и лечение таких больных. В России действует подпрограмма «Вирусные гепатиты» в рамках Федеральной целевой программы «Предупреждение и борьба с социальнозначимыми заболеваниями на 2007–2011 годы» (Минздравсоцразвития РФ, 2007).
Таким образом, проблема вирусных гепатитов заслуживает самого глубокого и комплексного изучения. Сложившаяся в настоящий момент обстановка: эпидемический характер заболевания, высокая стоимость и невозможность комплексной диагностики в регионах, дорогое и далеко не всегда эффективное специфическое лечение – предполагает поиск новых эффективных методов лечения такой непростой нозологической формы, как хронический вирусный гепатит С.
Современный подход к лечению вирусного гепатита С
Внедрение препаратов интерферона альфа (ифнα) в клиническую практику в середине 80-х годов открыло новую эру в лечении вирусных гепатитов, позволив проводить этиотропную терапию этих болезней. Эти препараты представляют собой сочетание пептидов, которые синтезируются лимфоцитами и макрофагами. Название «интерферон» происходит от слова «интерференция» (взаимное влияние). В настоящее время препараты ифнα – самые распространенные и наиболее изученные противовирусные агенты, применяемые в лечении вирусных гепатитов (3, 14, 37, 38, 42).
Среди более чем 20 подтипов ИФНα наиболее биологически значим альфа-2, рекомбинантными аналогами которого являются препараты Роферон (α2а), Интрон-А (α2b), а также отечественный Реаферон. Все вышеперечисленные препараты обладают высокой эффективностью. Однако препараты вводятся в организм больного парентеральным путем (внутривенно, внутримышечно, подкожно) и, как правило, в высоких дозах (30–10 млн ME в сутки). При этом наблюдаются побочные эффекты: гриппоподобный синдром, сильные головные боли, артралгия, депрессивное состояние, галлюцинации, выпадение волос, диарея (6, 14, 26, 34).
В результате фундаментальных исследований, проведенных в отделе интерферонов НИИ эпидемиологи и микробиологии им. Н.Ф. Гамалеи РАМН (Москва) под руководством профессора В.В. Малиновской, была найдена реальная возможность обойти сложности, возникающие при парентеральном применении препаратов интерферонов. В процессе углубленных исследований функционирования системы интерферона в онтогенезе (19, 22) был выявлен ряд закономерностей, позволивших решить стоявшие перед разработчиками задачи: снижение дозировки интерферона при однократном его введении; пролонгирование действия интерферона; устранение побочных эффектов, характерных для парентерального введения препаратов интерферона; обеспечение возможности применения препаратов интерферона не только для лечения взрослых, но и в педиатрической (неонатологической) и акушерской практике. Результатом проведенной работы стал препарат Виферон, производимый в зависимости от дозы интерферона (150 тыс. МЕ, 500 тыс. МЕ, 1 млн МЕ, 3 млн МЕ) (5, 24, 28, 47).
Выбранная лекарственная форма – суппозитории – обеспечивает простой, безопасный и безболезненный способ введения, что особенно актуально для педиатрии (неонатологии), а также при амбулаторном лечении и самостоятельном приеме препарата больными (28, 31, 32, 48).
В качестве действующего начала был выбран человеческий рекомбинантный ИФН-α2b, один из наиболее распространенных в клинической практике. Кроме того, в состав Виферона, помимо рекомбинантного ИФН-α2b, вошли мембрано-стабилизирующие препараты–антиоксиданты: α-токоферола ацетат (витамин Е) и аскорбиновая кислота (витамин С) в терапевтически эффективных дозах (2, 5, 10, 20, 21).
Комбинированная терапия (КТ) ИФН с Рибавирином в настоящее время является мировым стандартом в лечение HCV-инфекции (4, 8, 12, 25, 27, 29, 40, 43, 44).
Важно отметить, что свой противовирусный эффект при HCV Рибавирин оказывает только в присутствии ИФН (монотерапия рибавирином неэффективна) и препятствует формированию резистентности вируса гепатита C к терапии. Хотя у 20–25% больных на фоне монотерапии рибавирином уровень трансаминаз нормализуется, после отмены препарата происходит возврат повышенных показателей АЛаТ и АСаТ (3, 7).
Механизм действия Рибавирина остается до конца не выясненным, хотя известно, что он является конкурентным ингибитором инозинмонофосфатдегидрогеназы. Рибавирин уменьшает внутриклеточный пул гуанозина трифосфата, что опосредованно сопровождается снижением синтеза вирусной РНК. Рибавирин способен избирательно накапливаться в моноцитах, лимфоцитах и эритроцитах, воздействуя таким образом на внепеченочные очаги HCV-инфекции (3, 39).
Рандомизированное контролируемое исследование КТ Рибавирина и ИФН в качестве первичной терапии больных HCV показало увеличение устойчивого ответа в 2 раза. Причем у пациентов с высокой репликативной активностью – более 3 млн gE/мл – выявлено 10-кратное возрастание частоты постоянного ответа по сравнению с монотерапией ИФН (41 и 4% соответственно). У пациентов с низкой концентрацией вирусной РНК – менее 3 млн gE/мл – не наблюдали преобладания эффективности КТ по сравнению с монотерапией ИФН. Частота постоянного ответа составляла 29% и 25% соответственно (7, 37, 41, 45, 46).
У больных HCV с исходно высоким уровнем виремии удлинение сроков КТ с 24 до 48 недель увеличивает эффективность на 10%, тогда как у пациентов с низким уровнем виремии существенной разницы между эффективностью курсов выявлено не было (49).
При генотипе 1b КТ ИФН с Рибавирином в течение 24–48 недель в 2–3 раза более эффективна, чем монотерапия ИФН. У пациентов с генотипом 1b 24-недельного курса КТ может быть достаточно в случае исходно низкого уровня виремии (менее 2 млн gE/мл), а при уровне виремии более 2 млн gE/мл требуется 48-недельный курс КТ. При других генотипах бывает достаточно 24-недельного курса КТ независимо от уровня виремии (34, 49).
Немаловажным звеном в лечении HCV является применение озонотерапии (ОТ). При этом используется доказанный многими авторами выраженный антивирусный эффект (11), который проявляется как через непосредственное воздействие озона на вирус, так и опосредованно – через воздействие на вирус пероксидов, образующихся в результате взаимодействия озона с биологическими структурами организма, иммуномодулирующим действием озона (11). Важным оказывается и то, что озон стимулирует фагоцитоз, оказывает защитный эффект на здоровые клетки, в то же время повышая элиминацию клеток, пораженных вирусом.
Основным методом применения ОТ при гепатитах является внутривенное капельное введение 400 мл озонированного физиологического раствора в дозировке 4–6 мг/л, несколькими процедурами в зависимости от формы ВГ. Различие в дозах при остром и хроническом гепатите связано с тем, что при этом используются различные эффекты ОТ. При остром гепатите необходимо антивирусное воздействие, а при хроническом важны иммуномодулирующий, протективный эффект, стимуляция репарации (1, 11, 13, 17, 18, 23).
Цель работы
Целью проведенной работы было изучение эффективности различных схем лечения HCV с последующим сравнительным анализом.
Материалы и методы исследования
На базе медицинского отдела МНТО «Гранит» было проведено лечение 96 больных хроническим вирусным гепатитом С с высоким уровнем репликации (РНК HСV более 2 млн копий в 1 мл), из них 55 мужчин и 41 женщина, средний возраст больных 33±6 лет. При генотипировании HCV генотип 1b был выявлен у 83, 1а – у 5, 2а – у 1 и 3а – у 7 больных. Все больные были разделены на 3 группы. Длительность заболевания составила 5±2,5 года. Из всех обследованных HCV впервые выявлен был у 29 человек, 28 обследованных ранее получали противовирусную терапию в виде монотерапии α-интерферонами длительностью не более 6 месяцев, первичный ответ был у 12 из этих больных. Лица, получавшие лечение ранее, были равномерно распределены в 2-й и 3-й группах. В первую группу вошли больные с сопутствующей соматической патологией, а также 8 человек, ранее получавших лечение, у которых были отмечены выраженные побочные эффекты интерферонотерапии (в том числе у 5 больных наблюдалась лейко- и тромбопения, вследствие чего ранее полученное лечение было прервано). Больные с генотипами 1а, 2а и 3а HCV бы-ли равномерно распределены
в группах.
Первая группа (26 человек) получала лечение Вифероном в суточной дозировке 6 млн МЕ на двухкратный прием, в течение 3 месяцев, далее 3 раза в неделю, в течение 48 недель в комбинации с Рибаверином из расчета 15 мг/кг массы тела ежедневно на протяжении всего периода терапии.
Вторая группа (32 человека) получала стандартную базисную терапию: диету № 5, противовирусную терапию препаратами Реаферон (α2b интерферон) или Роферон А (α2a интерферон) по схеме: 6 млн МЕ внутримышечно или подкожно ежедневно в течение месяца, далее 3 раза в неделю в течение 48 недель в сочетании с постоянным приемом противовирусного препарата Рибаверин из расчета 15 мг/кг массы тела ежедневно на протяжении всего периода терапии.
Третья группа больных (38 человек) с их добровольного согласия получала комплексное лечение, включавшее диету № 5 с расширением рациона, содержащего пищевые волокна, витаминотерапию и ИФТ (Реаферон или Роферон А в дозе 6 млн МЕ внутримышечно или подкожно ежедневно в течение месяца, далее 3 раза в неделю в течение 48 недель) в сочетании с постоянным приемом противовирусного препарата Рибаверин из расчета 15 мг/кг массы тела ежедневно на протяжении всего периода терапии.
В дополнение к комбинированной противовирусной терапии все больные получали озонотерапию (ОТ), проводимую 2 курсами по 10 инфузий озонированного физиологического раствора с концентрацией озона 4–5 мг/л трижды в неделю на курс лечения в начале и спустя 3 месяца от начала интерферонотерапии.
Эффективность терапии оценивалась по степени выраженности побочных эффектов, биохимическому и вирусологическому (первичному и стойкому) ответу. Также через 3 месяца от начала курса терапии была оценена внешнесекреторная функция печени путем проведения этапного хроматического дуоденального зондирования (ЭХДЗ) (15, 16, 30, 36).
Статистическая обработка полученных результатов проводилась с использованием программы Primer of Biostatistics (v 4.03). Для анализа качественных признаков таблиц сопряженности использовался критерий хи-квадрат (χ2). Анализ эффективности лечения проводился с помощью критерия Стьюдента, используемого в непараметрической статистике при сравнении 2 статистических выборок.
Результаты исследования и их обсуждение
В ходе проведенного исследования все больные прошли полный курс терапии (48 недель), прерывания лечения в связи с выраженными побочными эффектами не было.
Оценка переносимости противовирусной терапии
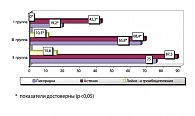
Все больные HCV прошли полные курсы противовирусной терапии. В начале лечения были отмечены некоторые побочные эффекты (см. рисунок 1).
Как видно из данных, представленных на рисунке 1, наиболее часто наблюдался астенический синдром, реже – лихорадка и в отдельных случаях – лейко- и тромбоцитопения. Во 2-й группе наблюдалась астения у 28 (87,5%), лихорадка – у 24 (75%) и лейко- и тромбоцитопения – у 5 (15,6%) больных HCV; в 3-й группе астения – у 26 (68,4%), лихорадка – у 25 (65,8%) и лейко- и тромбоцитопения – у 4 (10,5%) больных; в 1-й группе (получавшие Виферон) астения выявлена у 11 больных (42,3%), лихорадка – у 5 (19,2%), случаев лейко- и тромбоцитопении не наблюдалось.
Полученные результаты, безусловно, положительно характеризуют Виферон. Использование озонотерапии снижает частоту возможных побочных явлений, однако в группе, получавшей Виферон, уровень побочных эффектов достоверно ниже.
Оценка биохимического ответа
У всех больных HCV проводилось изучение основных биохимических показателей. Результаты основных из них приведены в таблице 1.
Из данных, приведенных в таблице 1, видно, что у всех групп больных HCV достоверно увеличены основные биохимические показатели печеночного метаболизма. После проведенного курса терапии у всех групп также достоверно улучшились все исследуемые критерии. В 1-й группе больных HCV результаты статистически сопоставимы с результатами во 2-й и 3-й группах, что положительно характеризует все использованные методы терапии.
Оценка вирусологического ответа при лечении вирусных гепатитов
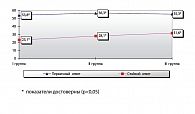
Оценка вирусологических показателей проводилась с учетом первичного ответа (исчезновение РНК HCV и ДНК HBV, зафиксированное не менее 2 раз с интервалом не менее 2 недель) и стойкого ответа (исчезновение РНК HCV и ДНК HBV, зафиксированное через 6 месяцев после окончания курса лечения). Результаты представлены на рисунке 2.
Как видно из данных, представленных на рисунке 2, у всех групп больных HCV получены достоверные результаты. Так, в 1-й группе первичный ответ наблюдался у 14 (53,8%), стойкий – у 6 (23,1%) больных; во 2-й группе первичный ответ – у 18 (56,3%), стойкий – у 9 (28,1%) больных; в 3-й группе первичный ответ был у 21 (55,3%) больного, стойкий – у 12 (31,6%) больных.
Результаты в 1-й группе, несмотря на более низкие показатели первичного и стойкого вирусологического ответа в лечении HCV, нежели в группах больных, получавших парентеральные интерфероны, сопоставимы с результатами во 2-й и 3-й группах, что заставляет признать приоритетное право использования Виферона у больных с сопутствующей соматической патологией и при тяжелых побочных эффектах лечения HCV.
Оценка внешнесекреторной функции печении у больных HCV
При оценке внешнесекреторной функции печени путем проведения ЭХДЗ учитывалось наличие билиарной недостаточности (БН) (уменьшение количества желчи и желчных кислот, поступающих в кишечник за 1 час после введения раздражителя меньше 1,2 ммоль/час (36, 16). Результаты представлены на рисунке 3.
Из данных, представленных на рисунке 3, видно, что у подавляющего большинства больных HCV присутствует синдром БН. При проведении противовирусной терапии отмечено достоверное купирование последнего. Так, в 1-й группе БН присутствовала до лечения у 25 (96,2%), после – у 19 (73,1%) больных; во 2-й группе – до лечения – у 30 (93,8%), после – у 24 (75%) больных; в 3-й группе до лечения БН присутствовала у 37 (97,4%) больных HCV, после – у 26 (68,4%).
Выводы
Виферонотерапия позволяет избежать основных проявлений побочных эффектов интерферонотерапии (лихорадки, астении, лейко- и тромбоцитопении).
Результативное использование препарата Виферон в комплексном лечении HCV предполагает его широкое применение у больных вирусным гепатитом С.
Несмотря на более низкие показатели биохимического и вирусологического ответа, Виферон является единственным альтернативным препаратом в лечении HCV инфекции у лиц с сопутствующей соматической патологией и тяжелыми побочными проявлениями лечения парентеральными препаратами интерферонов.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.