Аллергический и неаллергический ринит: эффективность барьерных методов
- Аннотация
- Статья
- Ссылки
- English

Окружающая среда может быть комфортной для жизни и деятельности человека и в то же время создавать серьезные проблемы для его здоровья.
Здоровье населения – интегральный медико-социальный и экономический показатель, отражающий уровень экономического и культурного развития, а также состояние медицинского обслуживания, природно-климатических и других условий проживания. Здоровье как социальный феномен характеризует не только качество жизнедеятельности, уровень физического развития, но также уровень заболеваемости и смертности. В любом цивилизованном государстве охрана здоровья и повышение качества жизни населения должны быть приоритетными задачами.
Взаимодействие организма с внешней средой (антигены, аллергены, микроорганизмы и др.) осуществляется через слизистые оболочки. Это основные зоны контакта макроорганизма с антигенами окружающей среды. Слизистые оболочки покрывают все полые органы, контактирующие с внешней средой (респираторный тракт, носоглотка, слуховые проходы, внутренняя поверхность век и др.). Поверхность слизистых тканей человека огромна (около 300–400 м2). На ее иммунное обеспечение требуется большое количество клеток и молекул. Слизистые оболочки служат барьером, защищающим организм от повреждающего воздействия агентов, способных проникать в организм через эпителий, вызывая развитие инфекционных и неинфекционных процессов, включая аллергические заболевания.
Здоровые слизистые оболочки надежно защищают организм от агрессивных воздействий. Поверхность поврежденной слизистой оболочки, как правило, заселяется микроорганизмами, что приводит к снижению защитных функций организма [1–5].
Барьерная функция слизистых оболочек реализуется и поддерживается за счет действия комплекса неспецифических факторов (перистальтические движения, движение ресничек эпителия, отделение слизи, выделение ферментов и др.), а также вовлечения специфических и неспецифических иммунных реакций, в частности местного, или мукозального, иммунитета.
Понятие местного (мукозального, от лат. mucosa – слизистая оболочка) иммунитета было сформулировано в 1930-х гг. А.М. Безредкой, который указал на важнейшую роль системы иммунитета, связанной со слизистыми оболочками.
Мукозальный иммунитет представляет собой совокупность реагирования всех клеток лимфоидного ряда, заселяющих слизистые оболочки, вместе с макрофагами, нейтрофильными и эозинофильными гранулоцитами, тучными клетками и другими клетками соединительной ткани и эпителия. Местный иммунитет – первый барьер иммунной защиты организма, предохраняющий его от проникновения микроорганизмов через слизистую оболочку и обезвреживающий их непосредственно в месте проникновения.
Оториноларингологи, иммунологи, аллергологи и другие специалисты особое внимание уделяют роли местного иммунитета в защите организма от воздействия повреждающих факторов внешней среды. Изучение данного вопроса требует проведения научно-исследовательских работ [3–10]. В настоящее время учение об иммунитете слизистых оболочек полностью не сформировано. Вместе с тем выделение отдельного подраздела «мукозальная иммунология» требует пересмотра ряда традиционных представлений о структуре и функционировании иммунной системы слизистых оболочек.
Мукозальная иммунная система (МИС) является автономной подсистемой интегральной иммунной системы. К мукозальному отделу иммунной системы относятся иммунологически значимые структуры: эпителиальный слой слизистых оболочек и субэпителиальное пространство, собственная пластина (lamina propria), в которой содержатся свободные лимфоциты и структурированная лимфоидная ткань, а также лимфатические узлы, дренирующие эти тканевые сегменты.
Главной составляющей МИС является мукозо-ассоциированная лимфоидная ткань (МАЛТ, MALT), представленная в разных органах:
- ТАЛТ (TALT) – лимфоидная ткань, ассоциированная с носоглоткой, евстахиевой трубой, ухом;
- НАЛТ (NALT) – лимфоидная ткань, ассоциированная с носовой полостью, ртом и ротоглоткой, конъюнктивой;
- БАЛТ (BALT) – лимфоидная ткань, ассоциированная с бронхами, трахеей, легкими, грудными железами (у женщин);
- КАЛТ (GALT) – лимфоидная ткань, ассоциированная:
- с гастроинтестинальной системой – пищеводом, желудком, тонким кишечником;
- толстым кишечником;
- проксимальными отделами урогенитального тракта, дистальными отделами урогенитального тракта;
- ДАЛТ (SALT) – лимфоидная ткань, ассоциированная с кожей (дерма).
Слизистая оболочка состоит из трех слоев:
- верхнего, или наружного, представленного эпителием. В эпителии нет кровеносных сосудов, а питание и обмен происходят за счет близлежащей соединительной ткани. Эпителий полости носа состоит из трех типов клеток: мерцательных, снабженных ресничками, способными двигаться, бокаловидных (одноклеточных), вырабатывающих слизь, являющуюся важнейшей составляющей назальной секреции, и вставочных эпителиоцитов (коротких и длинных), расположенных между клетками мерцательного эпителия. На верхушке эпителиоцитов также имеются микроворсинки;
- среднего, представленного соединительной тканью;
- внутреннего, состоящего из гладкомышечных волокон.
К основным функциям носовой полости относятся:
- дыхательная. Вдыхаемый через носовую полость воздух, проходя по дугообразному пути, очищается, нагревается и увлажняется;
- обонятельная. Обеспечивает восприятие запахов за счет обонятельного эпителия, расположенного в эпителиальной ткани носовой полости;
- резонаторная. Носовая полость с полостью рта, глоткой и околоносовыми пазухами служат резонатором для голоса;
- защитная. Например, чихание возникает вследствие раздражения окончаний тройничного нерва содержащимися в воздухе грубыми взвешенными частицами, что предохраняет слизистую оболочку от раздражения. Слезотечение способствует очищению при вдыхании вредных примесей воздуха, поскольку слеза стекает не только наружу, но и в полость носа через носослезный канал. Защитную функцию выполняют неспецифические и специфические иммунные механизмы.
Иммунная система слизистых оболочек носа, равно как и системный иммунитет, обеспечивает защиту с помощью факторов врожденного (неспецифического) и приобретенного (адаптивного) иммунитета.
Врожденный иммунитет слизистых оболочек реализуется за счет гуморального и клеточного звеньев иммунитета. Гуморальное звено слизистых оболочек представлено барьерными белками муцинами (мукус) (дефензины альфа и бета), кателицидинами, лектинами (коллектины А и Д), фиколинами (L, M, H, P), лизоцимом (антибактериальное вещество, разрушающее стенки патогенной бактерии), лактоферрином (белок для связывания солей железа), липокалинами, ингибиторами протеаз, альфа-2-макроглобулином, серпином, цистатином С, SLPI, SKALP/elafin, цитокинами и др.
Клеточное звено иммунной системы слизистых включает дендритные клетки, моноциты/макрофаги, интраэпителиальные Т-лимфоциты, нейтрофилы, тучные клетки, эозинофилы, естественные киллеры, которые являются также исполнительными клетками.
Адаптивный иммунитет мукозальной иммунной системы – структура, присутствующая уже при рождении. Но при рождении ее функциональная активность снижена, требуется активация, в частности за счет появления в лимфоидных фолликулах герминативных центров, где происходит активная пролиферация лимфоидных клеток (здесь же находится значительное количество В-лимфоцитов и плазматических клеток, продуцирующих иммуноглобулины различных классов).
Мукозальная иммунная система слизистой оболочки полости носа имеет две линии защиты организма:
- «иммунное исключение», или «иммунная охрана»;
- элиминация возбудителей инфекции, аллергенов и других антигенов, уже проникших в клетки.
Первая линия направлена на защиту организма от проникновения патогенных агентов внутрь клеток. Иммунное очищение предполагает распознавание, инактивацию, деструкцию, обезвреживание и удаление чужеродного антигенного материала, проникшего сквозь эпителий. Это осуществляется за счет:
- эпителиальных клеток на слизистой оболочке носа, способных вырабатывать неспецифические факторы защиты. В частности, продуцируются биологически активные вещества (БАВ) с бактерицидной, бактериостатической и противовирусной активностью, например лизоцим, лактоферрин, интерферон гамма, препятствующий проникновению вируса внутрь клетки;
- мукозальной функции, обеспечивающей местную защиту путем синтеза иммуноглобулинов (Ig) А и М и их секреторных компонентов. При контакте с внешней средой у человека с рождения начинают формироваться механизмы адаптивного иммунитета, представленные специальными иммунокомпетентными клетками, находящимися в слизистой оболочке. Именно взаимосвязь лимфоцитов и клеток эпителия обеспечивает функционирование мукозального иммунитета, основой которого является продукция секреторных IgA и IgM.
Дефицит местного иммунитета, прежде всего секреторного IgA, лежит в основе развития многих хронических инфекционно-воспалительных заболеваний слизистых оболочек и способствует формированию не только дисфункции мукозального иммунитета, но и аллергии.
Функция секреторных IgA и IgM заключается в снижении адгезии патогенных микроорганизмов и колонизации ими слизистой оболочки, а также в инактивации растворимых антигенов.
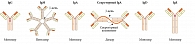
Секреторный IgA носового секрета отличается от сывороточных IgA тем, что:
- представлен димером с молекулярной массой около 390 кДа или различными полимерами (в сыворотке – мономерный IgA) (рис. 1);
- способен связываться с секреторным компонентом – гликопротеином с молекулярной массой 80 кДа;
- является продуктом эпителиальной клетки, которая «выставляет» его в качестве рецептора на своей базальной поверхности, где секретируется в полость носа и смешивается со слизью;
- его концентрация превышает таковую секреторного IgM в носовом секрете более чем в 100 раз.
Секреторный компонент защищает молекулу иммуноглобулина от бактериального протеолиза, в результате чего секреторные иммуноглобулины эффективно агглютинируют бактерии и связывают растворимые антигены.
Секреторный IgМ носового секрета представляет собой пентамер, способный связываться со своим секреторным компонентом (рис. 1).
Носовой секрет помимо секреторных содержит сывороточные иммуноглобулины, прежде всего IgG, а также следовые количества IgD и IgE. Эти иммуноглобулины попадают в назальный секрет с интерстициальной жидкостью, которая путем пассивной диффузии просачивается по межклеточным пространствам. Сывороточные иммуноглобулины вносят определенный вклад в иммунную систему слизистой оболочки, но в отсутствие секреторного компонента быстро подвергаются протеолизу [11, 12].
В реализации второй линии защиты также принимают участие факторы врожденного и адаптивного иммунитета:
- система комплемента участвует в каскадной иммунной реакции, обеспечивающей удаление повреждающих агентов из организма;
- цитокины влияют на регуляцию воспалительного процесса;
- естественные киллеры уничтожают поврежденные, опухолевые и другие клетки;
- эозинофилы и тучные клетки принимают активное участие в механизме аллергического воспаления;
- нейтрофилы и макрофаги поглощают и «переваривают» повреждающих агентов;
В-лимфоциты, продуцирующие IgG или иммуноглобулины «памяти», являются одними из главных участников второй линии защиты.
В отличие от слизистой оболочки желудочно-кишечного тракта (ЖКТ), где преобладают Т-клетки фенотипа CD8+, в слизистой оболочке полости носа доминирует Т-хелперная субпопуляция лимфоцитов с фенотипом CD4+. Не случайно реакция гиперчувствительности к аллергенам и микробным антигенам чаще развивается в слизистой оболочке респираторного тракта (слизистая оболочка носа и дыхательных путей), но не в слизистой ЖКТ.
В собственной пластинке (lamina propria) присутствует большое количество продуцирующих IgG плазматических клеток. Их количество возрастает в случае хронических воспалительных процессов в слизистой оболочке. IgG выполняет важнейшую роль в нейтрализации бактериальных токсинов и связывании микроорганизмов за счет опсонизации и их последующего уничтожения.
IgG не способен к активному транспорту через покровный эпителий (в отличие от секреторных IgA и IgM). Однако комплекс «антиген – IgG» связывает комплемент и взаимодействует с поверхностными рецепторами макрофагов и нейтрофилов в слизистой оболочке носа. Комплекс «антиген – IgG» активирует классический путь реакции связывания комплемента, в результате чего образуются БАВ, усиливающие проницаемость сосудистой стенки, хемотаксис нейтрофильных лейкоцитов, облегчается адгезия микроорганизмов к макрофагам. Последний участник этого каскада белковый фрагмент С9 образует так называемый мембрано-атакующий комплекс, который проникает в липидный слой клеточной мембраны и формирует трансмембранный канал, полностью проницаемый для электролитов и воды. Конечным этапом подобного каскада является уничтожение повреждающего агента, в частности инфекционного.
К наиболее частым причинам образования дефектов защитной системы слизистой оболочки носа относятся инфекционные (например, респираторные инфекции) и неинфекционные поражения слизистых
оболочек.
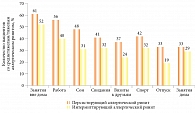
Из неинфекционных заболеваний слизистой оболочки носа часто встречается аллергический ринит, который во всем мире признан одним из самых распространенных аллергических заболеваний среди взрослого и детского населения. Последние 30 лет отмечается постоянный и повсеместный рост распространенности многих аллергических заболеваний, в том числе аллергического ринита, на долю которого в ряде стран приходится свыше 40% (таблица) [13].
Аллергический ринит является фактором риска развития бронхиальной астмы (насчитывается 200 млн пациентов с аллергическим ринитом и бронхиальной астмой), способствует развитию других заболеваний ЛОР-органов (синусита, отита, евстахиита, инфекций верхних дыхательных путей) (рис. 2), имеет высокую медико-социальную значимость (стоимость лечения около 2,5–3,5 млрд евро в год) [14].
Снижение функции мукозального иммунитета слизистой оболочки носа при аллергическом рините является одной из причин развития рецидивирующих острых респираторных инфекций у детей и взрослых и более продолжительного течения заболеваний.
Для восстановления эффективной функции МИС носа при аллергическом рините необходимо использовать как специфические, так и неспецифические методы защиты и контроля состояния слизистых оболочек и симптомов болезни.
К специфическим методам терапии аллергического ринита относятся элиминация (устранение) и аллергенспецифическая иммунотерапия (АСИТ) – наиболее эффективный, патогенетически обоснованный метод.
АСИТ – метод лечения IgE-опосредованных аллергических заболеваний, предусматривающий введение лечебных аллергенов в постепенно возрастающих концентрациях до достижения поддерживающей дозы с целью снижения чувствительности пациентов к повторному воздействию
аллергенов.
АСИТ вызывает развитие клинической и иммунологической толерантности к аллергенам, способствующей формированию длительного клинического эффекта, может предупреждать прогрессирование аллергических заболеваний и улучшать качество жизни больных [15].
К неспецифическим методам лечения аллергического ринита относятся фармакотерапия, барьерные методы лечения и профилактики и другие альтернативные способы контроля состояния слизистых оболочек и симптомов болезни.
Фармакотерапия, или симптоматическая терапия, направлена на устранение симптомов аллергического ринита и предполагает использование препаратов с различным механизмом действия, оказывающих влияние на разные звенья аллергического воспаления, развивающегося при манифестации или обострении заболевания.
При аллергическом рините применяются пероральные и топические антигистаминные средства, топические и системные глюкокортикостероиды, стабилизаторы мембран тучных клеток (интраназальные кромоны), интраназальные и пероральные деконгестанты, интраназальные антихолинергические средства, антилейкотриеновые препараты. Каждый препарат имеет свои показания и противопоказания, перечисленные в инструкции по применению. В частности, на фоне применения топических деконгестантов отмечается высокий риск развития возможных системных побочных эффектов (тахикардия, повышение артериального давления), что ограничивает частое использование данных препаратов в клинической практике.
Последние годы в силу высокой безопасности и достаточной клинической эффективности широкое распространение получили барьерные методы лечения аллергического ринита. Эти методы характеризуются способностью предупреждать или снижать проницаемость слизистых оболочек для аллергенов, препятствовать трансбарьерной сенсибилизации и развитию (обострению) аллергической реакции на действие аллергена.
В соответствии с принципом действия барьерные методы подразделяют:
- на механические: фильтры, ирригационная терапия (промывание носа) – персональная гигиена носа, позволяющая очистить полость носа и пазухи. Ирригационная терапия практиковалась на протяжении веков в Индии, Китае и других странах;
- химические: средства для смазывания полости носа в целях защиты от проникновения вирусов, бактерий и прочих возбудителей инфекции;
- методы сочетанного действия.
Несмотря на высокий профиль безопасности, некоторые барьерные методы противопоказаны для использования отдельными категориями пациентов.
Из недостатков механических барьерных методов следует отметить осторожное применение у детей и лиц с риском носового кровотечения, искривлением носовой перегородки, полипами, бронхиальной астмой. При ношении фильтра желательно меньше разговаривать и стараться дышать носом. Многие из барьерных методов имеют ограничения к применению в различные сезоны, особенно в зимний.
Особое внимание барьерным методам необходимо уделять в тех случаях, когда у пациентов имеются серьезные ограничения для приема лекарственных средств:
- беременность, лактация;
- детский возраст;
- спорт высших достижений;
- лекарственная аллергия и непереносимость.
К преимуществам барьерных методов относятся:
- простота применения;
- безопасность, в том числе в период гестации и лактации;
- сочетание с другими методами фармакотерапии;
- возможность использования в режиме «по требованию» (поездки, перелеты, нахождение в закрытых помещениях, где не исключен контакт с аллергенами и ирритантами);
- быстрый эффект, как при назначении назальных деконгестантов;
- отсутствие эффекта привыкания.
Накоплен большой опыт применения барьерных методов при аллергическом рините и получены убедительные данные о безопасности и клинической эффективности препарата Назаваль.
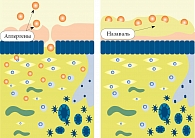
Назаваль – медицинское средство высокого класса безопасности, механизм действия которого заключается в защите слизистой оболочки полости носа от попадания в организм при дыхании разнообразных аэроаллергенов (пыльца растений, домашняя пыль, клещи домашней пыли, аллергены пуха, шерсть животных и птиц и др.), химических веществ, инфекционных агентов (бактерии, грибы, вирусы) и поллютантов (промышленные выбросы, выхлопы автотранспорта) (рис. 3).
Назаваль состоит из микронизированной целлюлозы растительного происхождения и вспомогательных веществ (экстракт натуральной мяты перечной).
Микронизированная целлюлоза – полисахарид (клетчатка), является частью клеточной оболочки растений, при соединении с водой набухает и образует гель, который и предотвращает контакт слизистой оболочки полости носа с внешними агрессивными агентами. Назаваль выпускается в виде назального порошкового спрея.
Вспомогательное вещество экстракт мяты перечной (3%), входящее в состав спрея Назаваль, делает его использование более комфортным, придает приятный мятный вкус и запах, а также служит индикатором адекватного применения (попадание в нос порошка целлюлозы).
При использовании назального спрея Назаваль предотвращается контакт слизистой оболочки полости носа с аэроаллергенами и поллютантами (пыльца растений, бытовые аллергены, клещи домашней пыли, домашняя пыль, грибковые аллергены, эпидермальные аллергены животных и птиц, инсектные аллергены, химические вещества и другие микрочастицы).
Назаваль применяют в тех случаях, когда необходимо обеспечить защиту слизистой оболочки полости носа от воздействия аллергенов, поллютантов, химических и инфекционных агентов, присутствующих в воздухе, и других негативных факторов внешней среды. Речь идет о лечении и профилактике обострений аллергического и неаллергического ринита. При легкой степени аллергического ринита Назаваль можно использовать в виде монотерапии, при средней степени – в составе комплексного лечения.
Назаваль, действуя как естественный барьер по отношению к аэроаллергенам, препятствует развитию аллергии и других поражений слизистой оболочки полости носа.
Клиническая эффективность спрея Назаваль подтверждена в многочисленных зарубежных и российских клинических исследованиях. Так, в открытом исследовании 30 пациентов обоего пола в возрасте 18–65 лет с аллергическим ринитом использовали препарат Назаваль. У 28 (99,6%) из них терапия оказалась высокоэффективной. На фоне применения Назаваля значительно уменьшилась выраженность симптомов (вплоть до их полного купирования) и статистически достоверно снизилась назальная реактивность после провокации на причинно-значимый аллерген [16]. У четырех пациентов симптомы аллергического ринита не развились даже при провокации аллергеном в максимальной концентрации.
Высокую клиническую эффективность Назаваль продемонстрировал и у детей. В исследовании, проведенном под руководством профессора Н.А. Геппе в 2010 г., препарат Назаваль статистически достоверно влиял на все симптомы аллергического ринита: ринорею, чихание, зуд и отек слизистой оболочки [17].
Для профилактики обострения аллергического ринита Назаваль целесообразно применять заблаговременно (за две недели до сезона пыления растений – предсезонная профилактика). При наличии других причин сенсибилизации (животные, птицы, аквариумные рыбки) препарат применяют до контакта с причинно-значимым аллергеном.
Безопасность спрея Назаваль относится к наивысшему классу по классификации средств медицинского назначения. Применение Назаваля не ограничено возрастом. Препарат разрешен к применению в период гестации и лактации, что характеризует его как барьерное средство, лишенное системного действия. Назаваль не вызывает сонливости, не влияет на способность к управлению транспортным средством.
Противопоказанием для применения Назаваля является индивидуальная непереносимость его компонентов.
L.V. Luss, N.V. Shartanova, Ye.V. Nazarova
Institute of Immunology of FMBA of Russia
Contact person: Lyudmila Vasilyevna Luss, lusslv@yandex.ru
Mucous membranes of the nose protect the organism from the negative effects of damaging environmental factors. The article analyzes the effectiveness of barrier methods of therapy in various forms of allergic and non-allergic rhinitis.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.