Анализ распространенности дифференцированного рака щитовидной железы (в рамках одного лечебного учреждения)
- Аннотация
- Статья
- Ссылки
- English




Введение
Наиболее распространенным и изученным эндокринным заболеванием считается узловой зоб. Несмотря на это, вопросы ведения таких пациентов не теряют своей актуальности. Прежде всего это связано с возрастанием распространенности дифференцированного рака щитовидной железы (ДРЩЖ) как среди взрослого, так и среди детского населения [1].
Увеличение количества таких больных может быть обусловлено, во-первых, повышением доступности визуализирующих методов обследования, таких как ультразвуковое исследование (УЗИ), компьютерная томография (КТ), магнитно-резонансная томография (МРТ). Обратной стороной улучшения качества диагностики стало увеличение количества необоснованных оперативных вмешательств на щитовидной железе [2]. Во-вторых, нельзя исключить истинный рост заболеваемости. К факторам, способствующим онкогенезу, относят неблагоприятную экологическую обстановку, увеличение количества обследований с использованием ионизирующего излучения (КТ, рентген, сцинтиграфия), распространение лучевых методов лечения, общее загрязнение среды токсическими веществами, обладающими канцерогенными свойствами [1, 3], изменение образа жизни, приводящее к ожирению. Установлено, что характерные для ожирения инсулинорезистентность и гиперинсулинемия ассоциируются с риском развития всех видов рака [4, 5].
Так, анализ заболеваемости ДРЩЖ среди россиян в 2007–2017 гг. свидетельствует о ее увеличении на 22,5%. При этом среди мужского населения прирост оказался выше, чем среди женского – 46,29 против 36,36%.
Именно поэтому в настоящее время усилия специалистов направлены на выявление причин заболеваемости, внедрение методов ранней диагностики злокачественных новообразований, создание систем стратификации риска, профилактику и своевременное лечение патологии.
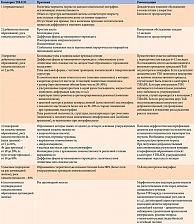
Необходимо отметить, что ключевая роль в диагностике рака щитовидной железы отводится УЗИ [6, 7], в силу большей доступности и дешевизны. В 2009 г. E. Horvarth и соавт., взяв за основу принципы разработки BIRADS (Breast Imaging Reporting and Data System), создали TIRADS (Thyroid Image Reporting and Data System) [8]. Это система интерпретации и протоколирования результатов визуализации очаговой патологии щитовидной железы для выработки тактики ведения пациента [7]. Предпосылками для создания данной системы послужили быстрый рост заболеваемости, стремительное улучшение выявляемости очаговой патологии щитовидной железы, значительное увеличение диагностических методов и технологий визуализации, прежде всего УЗИ, появление новейших технологий эхографии (цветокодированных режимов, трехмерной реконструкции, эластографии, контраст-усиленной ультразвуковой диагностики и т.д.), большое количество ошибок на всех этапах диагностического поиска, субъективность существующих критериев отбора пациентов для проведения тонкоигольной аспирационной биопсии (ТАБ), отсутствие преемственности специалистов, неверная или неполная интерпретация данных УЗИ врачами-диагностами, а также эндокринологами и хирургами, отсутствие стандартизированного подхода [9].
В 2011 г. J.Y. Kwak и соавт. модифицировали TIRADS. Использование системы позволило значительно улучшить интерпретацию выявляемой патологии щитовидной железы и стандартизировать лечебно-диагностический алгоритм [9]. В 2017 г. Европейская тиреоидологическая ассоциация выпустила рекомендации по ультразвуковой стратификации риска развития рака щитовидной железы – EU-TIRADS. Аналогичные рекомендации были приняты Американской тиреоидологической ассоциацией (ACR-TIRADS, 2017) и Корейским обществом радиационной тиреоидологии (K-TIRADS, 2016). В России TIRADS используют редко.
Целью нашего исследования стала оценка распространенности патологии щитовидной железы, включая ДРЩЖ, среди контингента, прикрепленного к ФГБУ «Поликлиника № 2» Управления делами Президента РФ, а также эффективности использования TIRADS в рутинной клинической практике.
Материал и методы
В исследование включены госслужащие, прикрепленные к ФГБУ «Поликлиника № 2» Управления делами Президента РФ, которым проводилось УЗИ щитовидной железы с января 2016 г. по декабрь 2018 г. Все пациенты прошли стандартное эндокринологическое обследование: сбор жалоб, анамнеза, физикальный осмотр, включая визуально-пальпаторную оценку щитовидной железы. При наличии жалоб, характерных для патологии щитовидной железы, определяли уровень тиреотропного гормона (ТТГ), свободного тироксина, свободного трийодтиронина, антител к тиреопероксидазе, тиреоглобулина и антител к рецепторам ТТГ. При подозрении на озлокачествление процесса проводили ТАБ с цитоморфологией пунктата. Гистологическое исследование удаленной тиреоидной ткани выполняли после тиреоидэктомии.
Для оптимизации работы врача-эндокринолога и улучшения контроля за узловыми образованиями щитовидной железы в ФГБУ «Поликлиника № 2» Управления делами Президента РФ была внедрена TIRADS. В зависимости от результатов анализа ультразвукового изображения щитовидной железы узловые образования относились к одной из категорий TIRADS (табл. 1).
Для более эффективного использования TIRADS была разработана внутренняя система реагирования при выявлении узлов щитовидной железы, относящихся к категориям 4 и 5: формирование статистического отчета «Впервые выявленная жизнеопасная патология», автоматическая передача информации о пациенте и выявленной патологии после соответствующего заполнения протокола УЗИ на компьютер заведующему отделением ультразвуковой диагностики, терапевтическим отделением, хирургическим отделением, а также врачу-эндокринологу (входящее письмо с отметкой «Срочно!») с последующим доступом к электронной истории болезни пациента и возможностью просмотра протокола УЗИ, результатов других инструментальных и лабораторных методов исследования, данных дневников врачей. Кроме того, были разработаны три статистических отчета по выявленным категориям TIRADS, позволяющих отслеживать количество проведенных УЗИ, присвоение категорий, положительную и отрицательную динамику, переход пациента в другую категорию риска.
Для удобства использования отчетов созданы дополнительные фильтры. С их помощью можно было выбирать участок прикрепления пациента, лечащего врача, отслеживать и сравнивать результаты лабораторных анализов (рис. 1–3).
Результаты
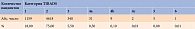
Проведено 6156 УЗИ щитовидной железы.
Возраст пациентов варьировался от 24 до 76 лет, в среднем – 53 года.
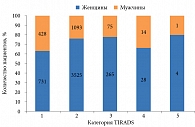
Количество женщин – 4545 (74%), мужчин – 1611 (26%).
Уровень ТТГ определен у 3672 пациентов.
Распределение пациентов в зависимости от категории TIRADS представлено в табл. 2 и на рис. 4.
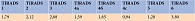
Средний уровень ТТГ у пациентов с разными категориями TIRADS представлен в табл. 3.
При проведении повторного УЗИ у 79 (1,2%) больных выявлена положительная динамика. Они были переведены в категории с более низким риском развития рака щитовидной железы, преимущественно во вторую и третью.
У 55 (0,9%) пациентов при проведении повторного УЗИ наблюдалась отрицательная динамика процесса, поэтому им была присвоена более высокая категория TIRADS.
За время наблюдения ТАБ проведена 102 пациентам, пунктированы 132 узла.
По результатам цитологического исследования у восьми пациентов (трое мужчин и пять женщин) обнаружены признаки папиллярного рака, у десяти больных (женщины) – цитограмма фолликулярной аденомы. Проведено 12 тиреоидэктомий.
Четыре пациента с фолликулярными аденомами и два пациента с подозрением на папиллярный рак отказались от оперативного лечения и находятся под наблюдением эндокринолога.
Послеоперационное гистологическое исследование ткани узлов щитовидной железы подтвердило цитологический диагноз в 100% случаев.
Показатель впервые выявленных злокачественных новообразований в 2016 г. составил 10,7 на 100 тыс. человек (8,10 в среднем по России и 7,28 по г. Москве), в 2017 г. – 28,80 на 100 тыс. человек. Это значительно превышает среднее значение по России.
Проведен также анализ экономической эффективности применения TIRADS. Согласно полученным результатам, количество проведенных УЗИ щитовидной железы снизилось на 35% (в 2014 г. – 4136, в 2018 г. – 2688), ТАБ – на 42,5% (в 2014 г. – 106, в 2018 г. – 58). Кроме того, сократилась частота выявления рака щитовидной железы (в 2014 г. – четыре случая, в 2018 г. – пять). В итоге было сэкономлено 3 188 264 руб.
В ходе исследования установлена прямая связь между риском развития рака щитовидной железы и возрастом пациентов. Так, доля пациентов моложе 30 лет и старше 60 лет в категориях TIRADS c высоким риском развития рака щитовидной железы увеличивалась. Однако при анализе результатов ТАБ и послеоперационного гистологического исследования тканей щитовидной железы наибольший риск рака щитовидной железы выявлен у лиц от 45 до 60 лет.
Кроме того, обнаружена зависимость степени риска развития рака щитовидной железы от уровня ТТГ. Более высокий уровень ТТГ ассоциировался с более высокими категориями Bethesda – категориями IV и V (рис. 5).
Вывод
Полученные результаты позволяют сделать следующие выводы:
- данные TIRADS коррелируют с результатами цитологического и гистологического исследований узловых образований щитовидной железы;
- TIRADS является эффективным методом диагностики и наблюдения за узловыми образованиями щитовидной железы в условиях поликлиники;
- благодаря внедрению TIRADS выявляемость рака щитовидной железы среди контингента ФГБУ «Поликлиника № 2» УДП РФ сохраняется на высоком уровне, одновременно снижается частота необоснованного проведения УЗИ и ТАБ;
- дополнительными предикторами риска развития рака щитовидной железы служат мужской пол, возраст от 45 до 60 лет, уровень ТТГ более 2,5 мкМЕ/мл.
S.V. Novosad, N.S. Martirosyan, PhD, I.G. Novichkova, PhD, N.A. Petunina, MD, PhD, Prof.
I.M. Sechenov First Moscow State Medical University
Polyclinic № 2 of the Administration of the RF President
Contact person: Sofya V. Novosad, sophia.novosad@gmail.com
The analysis of the differentiated thyroid cancer prevalence among patients attached to the FSBI ‘Polyclinic № 2’ of the RF President Office, as well as the effectiveness of TIRADS use for this aim. Presented data on the correlation between the results of TIRADS and Bethesda. Estimated such independent risk factors for thyroid cancer as sex, age, thyroid-stimulating hormone levels.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.