Антагонисты лейкотриеновых рецепторов в терапии бронхиальной астмы: кому, когда, как долго*
- Аннотация
- Статья
- Ссылки
- English
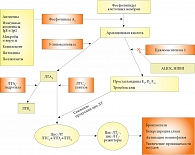


Важными медиаторами, участвующими в патогенезе бронхиальной астмы (БА), являются цистеиниловые лейкотриены (цис-ЛТ) ЛТC4, ЛTD4, ЛTE4, обладающие выраженными провоспалительными и бронхоконстрикторными свойствами и образующиеся в результате обмена арахидоновой кислоты по 5-липоксигеназному (5-ЛО) пути из фосфолипидов клеточной мембраны под действием фосфолипазы А2 (рис. 1). Цис-ЛТ генерируются эозинофилами, базофилами, тучными клетками, макрофагами и миелоидными дендритными клетками. Ацетилсалициловая кислота (АЦСК) и нестероидные противовоспалительные препараты (НПВП) являются ингибиторами циклооксигеназы 1 – фермента, наряду с 5-ЛО участвующего в обмене арахидоновой кислоты и контролирующего образование простагландинов и тромбоксанов (рис. 1). Не случайно при аспириновой БА, сопровождающейся непереносимостью АЦСК и НПВП, особенно значим уровень цис-ЛТ. Цис-ЛТ активируют по крайней мере два типа рецепторов на гладкомышечных клетках, индуцируя их сокращение, и на эндотелиальных клетках, увеличивая проницаемость сосудов. При этом в отношении влияния на сосудистую проницаемость они в 100 раз эффективнее гистамина. Кроме того, указанные медиаторы усиливают приток эозинофилов и других воспалительных клеток, стимулируют пролиферацию и дифференцировку миофибробластов, способствуя тем самым развитию субэпителиального фиброза. Подавляющее большинство фармакологических эффектов цис-ЛТ, относящихся к патофизиологии БА и аллергического ринита (АР), осуществляются через активацию специфических цис-ЛТ1-рецепторов, расположенных на тучных клетках, моноцитах и макрофагах, эозинофилах, базофилах, нейтрофилах, Т- и В-лимфоцитах, гладкомышечных клетках, бронхиальных фибробластах и эндотелиальных клетках. Поэтому фармакологические препараты – антагонисты цис-ЛТ1-рецепторов (монтелукаст, зафирлукаст и пранлукаст), применение которых давно одобрено во многих странах мира, хорошо зарекомендовали себя в качестве фармакотерапии БА и АР у взрослых и детей.
Монтелукаст – наиболее часто применяемый в Европе и Северной Америке препарат из названной группы. Пранлукаст используется преимущественно в Японии и других странах Азии. Зафирлукаст – первый зарегистрированный в европейских странах, в том числе в России, препарат – антагонист цис-ЛТ. Двукратный прием (для сравнения: монтелукаст применяется один раз в день) и возможное взаимодействие с пищей и другими лекарственными препаратами делают зафирлукаст менее востребованным. Препарат зилеутон – ингибитор 5-ЛО в нашей стране не зарегистрирован.
Солидная доказательная база, основанная на результатах рандомизированных клинических исследований и исследований в реальной практике, свидетельствует об эффективности монтелукаста и других препаратов – антагонистов лейкотриеновых рецепторов в улучшении симптомов и легочной функции при БА, уменьшении частоты обострений и потребности в бета-2-агонистах короткого действия (КДБА), редукции эозинофилии крови и мокроты у взрослых и детей с БА различной степени тяжести. У пациентов с персистирующими симптомами БА, получающих только симптоматическую терапию КДБА, монтелукаст улучшает контроль БА. Результаты нашего исследования, проведенного несколько лет назад, убедительно показали клинико-функциональную эффективность монотерапии монтелукастом у взрослых пациентов с легкой персистирующей БА в отношении достижения контроля заболевания. После 12-недельной монотерапии монтелукастом отмечалась достоверная положительная динамика дневных симптомов БА, снижалась потребность в КДБА, улучшалась функция легких [1].
Каким пациентам с астмой целесообразно назначать монтелукаст
Монотерапия антагонистами лейкотриеновых рецепторов, в частности монтелукастом, может быть альтернативой ингаляционным глюкокортикостероидам (ИГКС) у пациентов с легкой персистирующей БА, не желающих или по каким-либо причинам не могущих принимать ИГКС. На это указано в федеральных и основных международных руководствах по БА (рис. 2) [2] и АР GINA и ARIA. Более того, у детей младшего возраста с непродолжительным стажем болезни и высоким уровнем ЛТЕ4 в моче монотерапия монтелукастом эффективнее, чем терапия флутиказона фуроатом [3].
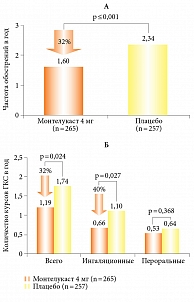
Для многих пациентов с БА характерны вирус-индуцированные обострения или ухудшения заболевания, развивающиеся несмотря на базисную терапию ИГКС. Как показали результаты исследований, уровень цис-ЛТ повышается при вирус-индуцированном обострении БА. ГКС практически не влияют на их продукцию, что делает обоснованным назначение монтелукаста пациентам с частыми вирус-индуцированными обострениями или ухудшением течения БА. Убедительные доказательства эффективности монтелукаста в отношении вирус-индуцированных обострений БА у детей в возрасте от двух до пяти лет получены в исследовании H. Bisgaard и соавт. [4]. В 12-месячном двойном слепом плацебоконтролируемом исследовании на фоне терапии монтелукастом отмечалось значимое (на 31,9% по сравнению с плацебо) редуцирование числа обострений БА. Средняя частота обострений БА на одного пациента составила 1,60 эпизода в группе монтелукаста и 2,34 эпизода в группе плацебо. Терапия монтелукастом способствовала увеличению периода до первого обострения БА в среднем на два месяца (р = 0,024) и снижению потребности в ингаляционных и системных ГКС (р = 0,027) по сравнению с плацебо (рис. 3) [4]. Результаты этого исследования приобретают особую актуальность в сезон вирусных инфекций, поскольку 85% обострений БА у детей и 60% обострений БА у взрослых индуцированы респираторными вирусными инфекциями, вызванными преимущественно риновирусом. Как известно, из-за большого числа серологических вариантов вакцин против данного возбудителя не существует.
Метаанализ клинических исследований влияния монтелукаста на бронхообструктивный синдром, развивающийся в результате РС-вирусного бронхиолита у маленьких детей, показал, что препарат способен снижать частоту этого синдрома в отсутствие значимых побочных эффектов [5].
Распространенность курения среди лиц, страдающих БА, не отличается от распространенности курения в популяции в целом. Считается, что по крайней мере треть пациентов с БА курильщики. Курение отрицательно влияет на течение БА. В отличие от некурящих у курящих больных значительно чаще имеют место неконтролируемая БА, обострения, нарушение и потеря функции легких. Причем на течение БА влияет не только активное, но и пассивное курение. Курение родителей приводит к более частым обострениям БА у детей, потребности в неотложной помощи и интубации [6, 7].
Цис-ЛТ участвуют в формировании воспаления у курящих больных БА. В исследовании K. Kontogianni и соавт. [8] показано, что в идуцированной мокроте курильщиков, страдающих астмой, уровень цис-ЛТ значительно выше, чем у некурящих, и коррелирует с уровнем эозинофилов. У некурящих такой взаимосвязи не зафиксировано. По сравнению с некурящими у курящих больных БА повышенный уровень цис-ЛТ может быть следствием дополнительной активации 5-ЛО никотином, что косвенно подтверждают данные о повышенном уровне цис-ЛТ в моче у активных или пассивных курильщиков независимо от наличия БА [9]. Монтелукаст может быть вариантом лечения у курящих больных БА, особенно при сниженном ответе на ИГКС.
В восьминедельном двойном слепом исследовании с перекрестным дизайном (все участники получали оба вида терапии) [10] оценивали влияние низкой дозы ИГКС (160 мкг беклометазона дипропионата (БДП) дважды в день) или монтелукаста (10 мг однократно вечером) на клинико-функциональные параметры (объем форсированного выдоха за первую секунду (ОФВ1) и пиковая скорость выдоха (ПСВ)) и маркеры воспаления (бронхиальная гиперреактивность и эозинофилы индуцированной мокроты) у курящих и некурящих пациентов с легкой персистирующей БА. У курящих больных зафиксирован лучший функциональный ответ на терапию монтелукастом. Увеличение утренней ПСВ у них существенно превышало таковое в ответ на БДП. Прирост ОФВ1 был одинаков, хотя противовоспалительный эффект, оцениваемый по редукции эозинофилов и эозинофильного катионного протеина в мокроте, был сильнее выражен на фоне применения БДП как у некурящих, так и курящих пациентов. Тем не менее приоритетный функциональный ответ курящих пациентов на монтелукаст свидетельствует об участии цис-ЛТ в воспалении и последующих функциональных нарушениях при БА у этой категории пациентов.
В более обширном двойном слепом рандомизированном клиническом исследовании сравнивали эффективность монтелукаста (10 мг однократно вечером), флутиказона пропионата (ФП) 250 мкг в день и плацебо у курящих пациентов (18–55 лет) с персистирующей БА [11]. Первичным критерием эффективности служил процент дней контролируемой БА на протяжении шестимесячного исследования. 347, 336 и 336 курящих пациентов с БА получали монтелукаст, ФП и плацебо соответственно. Разница в проценте дней контролируемой БА при использовании монтелукаста или ФП оказалась незначимой (р = 5,14). Это говорит об отсутствии существенной разницы в отношении контроля БА на фоне терапии монтелукастом и ФП у курящих больных БА. В ходе исследования отмечалась важная тенденция: больные с индексом курения ≤ 11 пачко-лет демонстрировали лучший ответ на ФП, пациенты с индексом курения > 11 пачко-лет – на монтелукаст. Сказанное позволяет предположить, что более длительное и интенсивное курение приводит к преимущественно нейтрофильному воспалению в слизистой оболочке бронхов и снижению ответа на ИГКС. В связи с этим терапия антагонистами лейкотриеновых рецепторов может иметь определенные преимущества у данной группы больных.
Таким образом, в отношении улучшения функции легких и достижения контроля терапия монтелукастом приоритетна у курящих больных астмой. Препарат может применяться в качестве монотерапии при легкой персистирующей БА у курящих подростков, отличающихся особенно низкой приверженностью ИГКС, и дополнительной терапии, усиливающей влияние ИГКС у курящих пациентов со среднетяжелой персистирующей бронхиальной астмой.
Аспириновая БА относится к группе респираторных заболеваний, обостряющихся после приема аспирина и других НПВП. Этот фенотип астмы встречается у взрослых, чаще у женщин, и связан с хроническим гиперпластическим риносинуситом, назальными полипами и приступами БА после приема аспирина и других неселективных ингибиторов циклооксигеназы, блокирующих циклооксигеназу 1. Распространенность данного фенотипа среди взрослых пациентов с БА около 10–25% [12]. В большинстве случаев данный фенотип характеризуется тяжелым течением. Респираторное заболевание (Aspirin Еxacerbated Respiratory Disease, AERD), вызванное аспирином, частично объясняется повышенной экспрессией 5-ЛО и ЛТC4-синтазы, что приводит к конститутивному гиперсинтезу цис-ЛТ, особенно усиливающемуся после приема аспирина и НПВП. Кроме того, AERD характеризуются избыточной экспрессией рецепторов цис-ЛT. У пациентов с аспириновой БА более высокий базовый уровень цис-ЛТ в слюне, мокроте, крови и моче, чем у пациентов с обычной неаспириновой БА [13]. Это подтверждает роль цис-ЛТ в патогенезе аспириновой БА. Больные с указанным фенотипом БА, как правило, недостаточно эффективно реагируют на ИГКС и имеют ощутимую пользу от дополнительного назначения антилейкотриеновых препаратов.
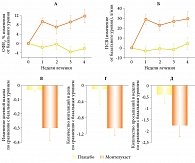
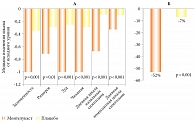
В плацебоконтролируемом исследовании у 80 взрослых пациентов с аспириновой БА изучали эффективность монтелукаста, добавленного к ИГКС (средние и высокие дозы), которые назначались ранее [14]. В группе монтелукаста наблюдалось значительное улучшение симптомов БА, тогда как в группе плацебо изменения отсутствовали (рис. 4) [14]. Улучшенная легочная функция на фоне применения монтелукаста была связана с меньшим количеством симптомов и обострений БА.
L. Mastalerz и соавт. [15] сравнили клинический ответ на монтелукаст у больных с аспириновой БА и аспирин-толерантных пациентов с БА. После трехнедельного приема монтелукаста 10 мг в день обе группы пациентов продемонстрировали аналогичное значительное улучшение контроля БА, утренней и вечерней ПСВ и качества жизни по сравнению с принимавшими плацебо.
Недавно были проанализированы восприятие и качество жизни пациентов с AERD, а также их оценка эффективности лечения [16]. Результаты показали неудовлетворенность пациентов текущими вариантами лечения, о чем свидетельствовали стойкие симптомы, неблагоприятное воздействие на качество жизни и стремление к различным альтернативным способам терапии. Из всех методов лечения наиболее эффективна десенситизация аспирином, за ней следует терапия антилейкотриеновыми препаратами и комбинация разных лекарств. Половина респондентов отметила эффективность антилейкотриеновых препаратов.
Таким образом, избыточное образование и патогенетическая роль цис-ЛТ при аспириновой БА, а также результаты клинических исследований свидетельствуют, что лечение монтелукастом, как правило в качестве дополнительной терапии к ИГКС, может улучшить контроль БА и назальные симптомы у пациентов с AERD.
Избыточный вес и ожирение, имеющие те же тенденции эпидемического распространения, что и БА, нередко у одного и того же пациента, в основном женского пола, формируют особый фенотип БА, характеризующийся поздним дебютом, среднетяжелым или тяжелым течением БА, умеренным снижением функции легких с некоторой обратимостью, зачастую неэозинофильным воспалением слизистой оболочки бронхов и менее частой атопией. Уровень цис-ЛТЕ4 в моче положительно коррелирует с индексом массы тела (ИМТ) пациентов с БА, что, вероятно, является результатом действия лептина. Как показали результаты исследования M. Peters-Golden и соавт. [17], фенотипу «БА у больных с ожирением» присуща неоднозначность ответа на контролирующую фармакотерапию. Ученые провели ретроспективный анализ четырех двойных слепых плацебоконтролируемых рандомизированных исследований с участием 3073 взрослых пациентов с персистирующей среднетяжелой БА, получавших монтелукаст (n = 1439), БДП (n = 894) и плацебо (n = 740). Первичной оценкой эффективности служил процент дней контролируемой БА. 52% больных, включенных в анализ, имели нормальный вес, 32% – повышенный ИМТ и 16% – ожирение. Согласно полученным результатам, повышенный ИМТ и ожирение влияют на возможность достижения контроля БА, приводя к снижению процента дней контролируемой БА. Ответ на ИГКС (БДП) также снижался с увеличением ИМТ, но не на монтелукаст. Различий в проценте дней контролируемой БА в ответ на терапию монтелукастом между пациентами с нормальным, повышенным ИМТ или пациентов с ожирением не установлено.
В двух других ретроспективных анализах сравнивали ИГКС или ИГКС/ДДБА (бета-2-агонисты длительного действия) с монтелукастом у пациентов с БА и избыточным весом и ожирением. ИГКС и ИГКС/ДДБА оказались последовательно более эффективны, чем монтелукаст, у больных всех категорий ИМТ [18]. Тем не менее, учитывая особенности фенотипа «БА у больных с ожирением», связанные с высокой коморбидностью (гипертензия, снижение толерантности к глюкозе, сердечно-сосудистые заболевания) и зачастую препятствующие назначению высоких доз ИГКС или комбинации ИГКС/ДДБА, а также нейтрофильный или смешанный профиль воспаления и вовлечение цис-ЛТ в его формирование, целесообразно рассматривать вопрос о назначении монтелукаста пациентам, не достигающим контроля на терапии ИГКС или ИГКС/ДДБА.
Еще одно важное свойство этой группы препаратов – выраженный бронхопротективный эффект в отношении бронхоспазма, вызванного физической нагрузкой (БВФН) у больных БА. БВФН отмечается у 70–80% больных с неконтролируемой астмой и персистирующими симптомами. Особенно БВФН характерен для детей и подростков, у которых он может быть единственным проявлением БА. Первые доказательства эффективности монтелукаста при БВФН появились еще в середине 1990-х гг., когда были опубликованы результаты исследований защитного действия препарата в отношении бронхоконстрикции, вызванной физической нагрузкой. В отличие от бета-2-агонистов эффективность монтелукаста при продолжительном лечении не уменьшается. Бронхопротективный эффект монтелукаста в отношении снижения ОФВ1 после физической нагрузки значительно превышает таковой плацебо. Кроме того, на фоне применения препарата не развивается тахифилаксия. Защитный эффект проявляется быстро – после приема первой дозы. Следовательно, у детей и подростков, страдающих БА с доминированием БВФН, а также у взрослых монтелукаст в качестве монотерапии при легкой БА или в комбинации с ИГКС при среднетяжелой БА может быть оптимальным выбором в целях достижения контроля и профилактики БВФН.
Как известно, для любой БА характерно поражение не только крупных и средних, но также мелких, дистальных бронхов. Постоянное неконтролируемое воспаление в периферических дыхательных путях может препятствовать достижению контроля и, напротив, способствовать увеличению бронхиальной гиперреактивности и числа обострений. Дистальные дыхательные пути служат важной мишенью при любой терапевтической стратегии БА. Монтелукаст назначают перорально. Препарат обладает системным эффектом, а значит, способен достигать как крупных, так и мелких бронхов. Лейкотриеновые рецепторы по-разному экспрессируются в фибробластах периферических дыхательных путей по сравнению с центральными [19], что может объяснить ремоделирование, вызванное цис-ЛТ, главным образом в периферических дыхательных путях, и, возможно, преобладающий эффект монтелукаста в дистальных отделах бронхов.
H. Nakaji и соавт. показали, что цис-ЛТ в мелких бронхах в 30 раз мощнее, чем в крупных бронхах. Кроме того, монтелукаст проявляет сильную антагонистическую активность против бронхоконстрикторного действия цис-ЛТ в изолированных мелких бронхиолах человека [20].
В нескольких исследованиях терапия монтелукастом способствовала небольшому, но значимому повышению плотности легочной ткани (уменьшение выраженности воздушных ловушек) по сравнению с плацебо и увеличению ряда функциональных показателей, в частности остаточного объема легких. Это косвенно подтверждает потенциальное влияние монтелукаста на воспаление в мелких бронхах у больных БА [21–23].
Таким образом, пациенты с неконтролируемой БА и признаками нарушения функции мелких бронхов (снижение форсированной жизненной емкости легких (ФЖЕЛ), уменьшение среднего экспираторного потока на уровне 25–75% ФЖЕЛ (МОС25–75), увеличение общей емкости легких и остаточного объема легких, увеличение сопротивления дыхательных путей) могут получить дополнительную пользу от приема монтелукаста в отношении функции легких и контроля заболевания.
Пероральные антагонисты ЛТ-рецепторов, обладающие системным эффектом на аллергическое воспаление, целесообразно назначать при сочетании БА и АР. Результаты множества исследований подтверждают эффективность этой терапии у больных изолированным АР и АР с сопутствующей БА, у которых эффективность антилейкотриеновых препаратов даже выше, чем у пациентов с изолированной БА.
В систематическом обзоре исследований эффективности монтелукаста при сезонном и круглогодичном АР с сопутствующей БА и в отсутствие таковой показано, что у пациентов с АР и БА на фоне приема монтелукаста по сравнению с плацебо значительно уменьшаются симптомы обоих заболеваний и снижается потребность в противоастматических лекарственных препаратах [24].
В клиническом исследовании монтелукаста в качестве дополнительной терапии к ИГКС больные БА с сопутствующим АР в отличие от пациентов без сопутствующего АР по-разному реагировали на комбинацию будесонида и монтелукаста с точки зрения контроля астмы (функция легких). В подгруппе пациентов с БА и АР комбинированный подход обеспечивал более высокую эффективность в улучшении функции легких по сравнению с удвоенной дозой будесонида (рис. 5) [25].
В ряде обсервационных исследований оценивали эффективность и безопасность монтелукаста у пациентов с БА и АР в реальной клинической практике. В 12-месячном исследовании участвовал 1681 пациент с легкой и среднетяжелой БА, недостаточно контролируемой ИГКС или ИГКС + ДДБА [26]. Пациентам назначали монтелукаст 10 мг/сут в качестве дополнительной терапии. Оценка контроля выполнялась через 3, 6, 9 и 12 месяцев. Показатель ACT (Asthma Control Test – тест по контролю над астмой) в общей популяции был основной конечной точкой исследования. Дополнительная терапия монтелукастом продемонстрировала значительное улучшение симптомов БА в течение 12 месяцев у всех пациентов. Однако у пациентов с АР уровень контроля по АСТ превышал таковой у пациентов без АР. Авторы пришли к выводу, что сопутствующий АР – значимый предиктор лучшего контроля БА в результате дополнительной терапии монтелукастом [26].
Монтелукаст эффективен и в терапии изолированного АР: на фоне его применения отмечается редукция всех симптомов заболевания, включая заложенность носа (рис. 6) [27]. Важный момент: препарат влияет на эозинофильное воспаление, что проявляется уменьшением эозинофилии крови и слизистой оболочки дыхательных путей (рис. 6) [27].
В ряде исследований монтелукаст продемонстрировал особенно высокую эффективность в комбинации с антигистаминными препаратами (АГП) второго поколения [28–30].
Назначение монтелукаста пациентам с астмой и/или аллергическим ринитом
Антагонисты лейкотриеновых рецепторов относятся к группе базисных противовоспалительных препаратов и применяются для достижения и поддержания контроля БА и АР. При легких симптомах сезонного и круглогодичного АР монтелукаст может служить альтернативой АГП второго поколения. При среднетяжелом/тяжелом АР монтелукаст может применяться в комбинации с АГП второго поколения или ИГКС (рис. 7) [31]. Безусловный приоритет в назначении монтелукаста имеют пациенты с АР и сопутствующей БА.
При БА монтелукаст можно использовать в монотерапии или комбинированной терапии у пациентов с неконтролируемыми симптомами. Результаты исследований, проведенных в реальной клинической практике, показали практически одинаковую эффективность монтелукаста и низких доз ИГКС у больных легкой персистирующей БА, монтелукаста и ДДБА в качестве дополнительной терапии к ИГКС у больных среднетяжелой неконтролируемой БА.
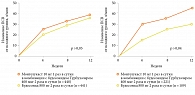
D. Price и соавт. [32] провели два двухлетних исследования в условиях реальной клинической практики. В первом сравнили эффективность антагонистов ЛТ-рецепторов (монтелукаст, зафирлукаст) и ИГКС в качестве начальной терапии БА у 326 пациентов, ранее не получавших лечения для контроля симптомов. Во втором сравнили антагонисты ЛТ-рецепторов (монтелукаст, зафирлукаст) и ДДБА в качестве дополнительной терапии у 361 пациента с БА, не контролируемой на монотерапии ИГКС. Основным критерием оценки служил мини-вопросник по качеству жизни с БА (Mini AQLQ), дополнительным – вопросник по контролю БА ACQ. Кроме того, оценивали частоту обострений БА (назначение пероральных ГКС или госпитализация). Использовали также мини-вопросник по качеству жизни с риноконъюнктивитом (Mini RQLQ). Эффективность антагонистов ЛТ-рецепторов оказалась эквивалентной эффективности ИГКС в качестве базисной терапии первой линии БА и ДДБА в качестве дополнительной терапии у пациентов, уже получавших ИГКС.
По крайней мере подобная эквивалентность была достоверно показана через два месяца терапии. Эквивалентность, оцененная через два года терапии, была недостоверной по главному критерию Mini AQLQ, но динамика второстепенных критериев (ACQ и ПСВ) была сопоставимой в группах сравнения. Поскольку исследования продолжались два года, их результаты отражают реальную клиническую практику со всеми ее преимуществами (разнообразие пациентов) и недостатками (отсутствие объективного плацебо-контроля). В исследованиях зафиксирована высокая приверженность больных лечению антилейкотриеновыми препаратами: в первом исследовании – 65%, по сравнению с ИГКС – 41%, во втором в качестве дополнительной терапии к ИГКС – 74%, к ДДБА – 46%.
Таким образом, неконтролируемые симптомы служат показанием для назначения монтелукаста в виде моно- или комбинированной терапии больным бронхиальной астмой и/или аллергическим ринитом.
Как долго пациенты с астмой и/или аллергическим ринитом могут применять монтелукаст
Монтелукаст считается безопасным лекарственным препаратом. Как правило, возникающие на фоне его применения незначительные побочные реакции по виду и частоте не отличаются от реакций, развивающихся при использовании плацебо. Общая распространенность нежелательных побочных реакций при использовании монтелукаста, согласно результатам клинических исследований, сопоставима с таковой на фоне приема плацебо. Монтелукаст в качестве дополнительной терапии не увеличивает частоту этих реакций по сравнению с терапией ИГКС и ДДБА.
В систематическом обзоре и метаанализе сравнивали эффективность и безопасность антагонистов лейкотриеновых рецепторов и плацебо у взрослых и подростков [33]. Пропорция пациентов с неблагоприятными событиями была одинакова среди больных, получавших монтелукаст и плацебо. Во всех клинических исследованиях, включенных в метаанализ, серьезных побочных эффектов при использовании монтелукаста не зарегистрировано. Авторы пришли к выводу, что частота нежелательных явлений, прекращения терапии из-за нежелательных явлений и ухудшений астмы схожи для антилейкотриеновых препаратов и плацебо, что отражает благоприятный профиль безопасности и переносимости антагонистов лейкотриеновых рецепторов.
Другой обзор клинических исследований обобщил информацию о безопасности и переносимости монтелукаста у детей и подростков – дошкольников и школьников (2751 пациент). Лечение монтелукастом в целом хорошо переносится. Наиболее частые нежелательные побочные реакции, отмеченные во всех клинических исследованиях, были связаны с инфекцией верхних дыхательных путей, ухудшением течения астмы, фарингитом и лихорадкой [34]. Исходя из результатов постмаркетинговых наблюдений было высказано предположение о возможном изменении поведения у лиц, принимающих монтелукаст. Речь, в частности, идет об увеличении беспокойства и агрессии, появлении бессонницы и суицидальных мыслей. Однако пересмотр и анализ 116 клинических исследований показал, что частота побочных эффектов, связанных с поведением, у пациентов, получающих монтелукаст, ничем не отличается от аналогичного показателя у пациентов контрольных групп [35, 36]. Важно, что хорошая переносимость и безопасный профиль монтелукаста сохраняются на протяжении его длительного (свыше 12 месяцев) применения [37]. В реальной клинической практике пациенты с БА принимают монтелукаст на протяжении многих лет с неизменным клиническим эффектом, хорошей переносимостью и безопасностью. Помимо этого монтелукаст является препаратом, на фоне применения которого при достижении и поддержании стойкого контроля БА можно снизить поддерживающую дозу ИГКС (step-down) [38].
Длительность применения монтелукаста при АР определяется продолжительностью симптомов: при сезонном АР препарат применяют в течение всего периода пыления и отменяют через две – четыре недели после его окончания. При круглогодичном АР препарат используют постоянно в течение всего года, длительность лечения зависит от эффективности элиминационных мероприятий или аллергенспецифической иммунотерапии.
Таким образом, у больных астмой и/или аллергическим ринитом монтелукаст, характеризующийся хорошей переносимостью и безопасностью и не вызывающий развития тахифилаксии, можно применять длительно, на протяжении месяцев и лет.
Известно множество дженерических форм монтелукаста. Монтелукаст компании «Сандоз» под торговым наименованием Монтелар® полностью соответствует требованиям, предъявляемым к качественным дженерикам. При более доступной цене препарат имеет высокий профиль эффективности и безопасности и обладает доказанной биологической и терапевтической эквивалентностью оригинальному препарату.
Заключение
Антагонисты лейкотриеновых рецепторов, в частности монтелукаст, имеют доказанную эффективность в отношении клинических и функциональных проявлений БА и АР и достижения контроля заболеваний.
Монтелукаст в качестве монотерапии может быть альтернативой низким дозам ИГКС, особенно у детей и подростков с легкой БА и АР, вирус-индуцированными обострениями БА, астмой, сопровождающейся сниженной толерантностью к физической нагрузке, а также в качестве step-down-терапии.
В качестве дополнительной терапии к ИГКС монтелукаст является альтернативой ДДБА. Этот вариант комбинированной терапии эффективен при аспириновой БА, БА с сопутствующим АР, БА у пациентов с ожирением, курящих больных БА, а также у больных астмой, имеющих противопоказания к назначению ДДБА.
Монтелукаст имеет хороший профиль безопасности. Частота побочных эффектов при его применении не отличается от таковой при использовании плацебо.
N.M. Nenasheva
Russian Medical Academy for Continuing Professional Education
Contact person: Natalya Mikhaylovna Nenasheva, 1444031@gmail.com
The goal of asthma therapy is to achieve and maintain control, but in real clinical practice about half of patients have an uncontrolled disease. The main drugs for long-term asthma control are inhaled corticosteroids, but there is a significant amount of evidence supporting the concept that some asthma phenotypes seem most sensitive to antileukotriene drugs used as mono or combined with inhaled corticosteroid therapy. Montelukast is the main representative of this class medication. This article discusses practical issues of using montelukast in patients with asthma and/or allergic rhinitis: which patients with asthma will benefit from its appointment, when and how long should the medicaton be used.

