Оценка использования ингаляционных устройств доставки препаратов у детей с бронхиальной астмой
- Аннотация
- Статья
- Ссылки
- English
Цель исследования – оценить технику выполнения ингаляции у детей с бронхиальной астмой.
Материал и методы. Проведено открытое проспективное сравнительное исследование, в которое были включены 89 детей с верифицированным диагнозом БА в возрасте от шести до 17 лет 11 месяцев, поступившие с обострением в городскую детскую клиническую больницу г. Уфы. В данной популяции с использованием клинико-анамнестического и функционального методов проанализированы структура, объем, способ и техника выполнения ингаляционной терапии, рекомендованной в амбулаторно-поликлинических условиях. Кроме того, все пациенты прошли инструктаж и обучение по применению ингаляторов.
Результаты. Все дети были госпитализированы в педиатрическое отделение с обострением патологии. Преимущественно это были пациенты со среднетяжелым (58,4%) и частично контролируемым (69,7%) течением БА, которые на амбулаторно-поликлиническом этапе получали терапию с использованием разных ингаляционных устройств доставки препаратов. Согласно результатам устного опроса, 77,5% наблюдаемых детей ранее обучались технике ингаляции. Их стаж применения одной формы ингаляционного устройства в среднем составлял 1,91 ± 1,02 года. В 35,9% случаев препарат доставлялся с помощью небулайзера, в 34,8% случаев – с помощью дозированных аэрозольных ингаляторов (ДАИ), в 29,3% случаев – с помощью дозированных порошковых ингаляторов (ДПИ). Участники исследования были разделены на две группы. В первую группу вошли пациенты в возрасте от шести до 11 лет 11 месяцев. Чаще всего (44,7%) им рекомендовали проведение ингаляционной терапии с помощью небулайзера. Вторую группу составили больные в возрасте от 12 до 17 лет 11 месяцев. Из них 47,6% применяли ДПИ.
При оценке техники выполнения ингаляции установлено, что у 47,2% детей имело место грубое ее нарушение, что могло привести к снижению поступления достаточного объема препарата в дыхательные пути и, как следствие, неконтролируемому течению и обострению заболевания. В 48,2% случаев ошибки совершались при использовании ДАИ. У 60,0% пациентов первой группы проблемы возникали при применении ДАИ, у 37,0% пациентов второй группы – при использовании ДПИ.
Анализ характера ошибок при выполнении ингаляции в зависимости от вида устройства и возраста больных БА показал, что при использовании ДАИ нарушалось координирование вдоха. Это препятствовало активации ингалятора. При использовании ДПИ ошибки были связаны с отсутствием адекватной координации ингаляционного маневра (вдоха с усилием), небулайзера – с выбором ингаляционной маски, а не мундштука.
Заключение. Для купирования аллергического воспаления при терапии БА у детей предпочтительным способом доставки лекарственных средств в дыхательные пути является ингаляционный. Ингаляционное устройство выбирается с учетом не только возраста, но и индивидуальных особенностей пациентов.
Согласно рекомендациям общепринятых клинических руководств, все молекулы ингаляционных глюкокортикостероидов и все формы ингаляционных устройств при соблюдении инструкции по их применению обеспечивают высокий противовоспалительный эффект. Чтобы избежать ошибок при проведении ингаляции, назначение ингаляционных устройств на амбулаторно-поликлиническом этапе должно проводиться только после обучения пациентов. Помимо этого при каждом очном визите к врачу показана оценка правильности техники выполнения процедуры.
Цель исследования – оценить технику выполнения ингаляции у детей с бронхиальной астмой.
Материал и методы. Проведено открытое проспективное сравнительное исследование, в которое были включены 89 детей с верифицированным диагнозом БА в возрасте от шести до 17 лет 11 месяцев, поступившие с обострением в городскую детскую клиническую больницу г. Уфы. В данной популяции с использованием клинико-анамнестического и функционального методов проанализированы структура, объем, способ и техника выполнения ингаляционной терапии, рекомендованной в амбулаторно-поликлинических условиях. Кроме того, все пациенты прошли инструктаж и обучение по применению ингаляторов.
Результаты. Все дети были госпитализированы в педиатрическое отделение с обострением патологии. Преимущественно это были пациенты со среднетяжелым (58,4%) и частично контролируемым (69,7%) течением БА, которые на амбулаторно-поликлиническом этапе получали терапию с использованием разных ингаляционных устройств доставки препаратов. Согласно результатам устного опроса, 77,5% наблюдаемых детей ранее обучались технике ингаляции. Их стаж применения одной формы ингаляционного устройства в среднем составлял 1,91 ± 1,02 года. В 35,9% случаев препарат доставлялся с помощью небулайзера, в 34,8% случаев – с помощью дозированных аэрозольных ингаляторов (ДАИ), в 29,3% случаев – с помощью дозированных порошковых ингаляторов (ДПИ). Участники исследования были разделены на две группы. В первую группу вошли пациенты в возрасте от шести до 11 лет 11 месяцев. Чаще всего (44,7%) им рекомендовали проведение ингаляционной терапии с помощью небулайзера. Вторую группу составили больные в возрасте от 12 до 17 лет 11 месяцев. Из них 47,6% применяли ДПИ.
При оценке техники выполнения ингаляции установлено, что у 47,2% детей имело место грубое ее нарушение, что могло привести к снижению поступления достаточного объема препарата в дыхательные пути и, как следствие, неконтролируемому течению и обострению заболевания. В 48,2% случаев ошибки совершались при использовании ДАИ. У 60,0% пациентов первой группы проблемы возникали при применении ДАИ, у 37,0% пациентов второй группы – при использовании ДПИ.
Анализ характера ошибок при выполнении ингаляции в зависимости от вида устройства и возраста больных БА показал, что при использовании ДАИ нарушалось координирование вдоха. Это препятствовало активации ингалятора. При использовании ДПИ ошибки были связаны с отсутствием адекватной координации ингаляционного маневра (вдоха с усилием), небулайзера – с выбором ингаляционной маски, а не мундштука.
Заключение. Для купирования аллергического воспаления при терапии БА у детей предпочтительным способом доставки лекарственных средств в дыхательные пути является ингаляционный. Ингаляционное устройство выбирается с учетом не только возраста, но и индивидуальных особенностей пациентов.
Согласно рекомендациям общепринятых клинических руководств, все молекулы ингаляционных глюкокортикостероидов и все формы ингаляционных устройств при соблюдении инструкции по их применению обеспечивают высокий противовоспалительный эффект. Чтобы избежать ошибок при проведении ингаляции, назначение ингаляционных устройств на амбулаторно-поликлиническом этапе должно проводиться только после обучения пациентов. Помимо этого при каждом очном визите к врачу показана оценка правильности техники выполнения процедуры.

Введение
Ведущая роль в патогенезе бронхиальной астмы (БА) отводится хроническому аллергическому воспалению дыхательных путей, которое выявляется не только при обострении, но и при ремиссии. Это обосновывает необходимость длительного применения препаратов базисной терапии для достижения контроля над симптомами заболевания и профилактики обострений [1].
Еще в первой версии программного документа Глобальной инициативы по лечению и профилактике БА была предложена ступенчатая терапия заболевания, которой придерживаются в России (национальная программа «Бронхиальная астма у детей» и клинические рекомендации «Бронхиальная астма») [2]. Ступенчатый подход к терапии БА предусматривает подбор безопасной и эффективной дозы препаратов, в первую очередь ингаляционных глюкокортикостероидов (ИГКС), а также способа их доставки в дыхательные пути в соответствии с текущей степенью контроля, тяжестью течения и наличием факторов риска обострения заболевания [3–5].
В настоящее время наиболее предпочтительным способом доставки лекарственных средств для лечения хронических заболеваний респираторной системы, в том числе БА, в педиатрической практике является ингаляционный [6]. Ингаляционный способ доставки препаратов позволяет довольно быстро получить положительный эффект благодаря непосредственному поступлению их в орган-мишень – трахеобронхиальное дерево. Ингаляционный путь доставки в отличие от парентерального или перорального обеспечивает высокую концентрацию лекарственного средства в респираторном тракте при снижении его общей дозы, тем самым минимизируется риск системного побочного воздействия [7].
Основными средствами доставки препаратов в дыхательные пути признаны небулайзеры, дозированные аэрозольные ингаляторы (ДАИ), ДАИ со спейсером или активируемые вдохом (ДАИ-АВ), дозированные порошковые ингаляторы (ДПИ), ингаляторы, индуцирующие мягкие аэрозоли (Soft Mist) [3, 4, 8, 9].
Помимо свойств препарата и вида ингаляционного устройства эффективность ингаляционной терапии БА у детей во многом зависит от корректной техники выполнения ингаляции с соблюдением терапевтического режима. Некорректно выполненная ингаляция приводит к существенному уменьшению дозы препарата, попадающего в дыхательные пути. Как следствие, снижается эффективность лечения, повышается потребность в больших дозах препарата или системной терапии глюкокортикостероидами, дополнительной медицинской помощи вследствие обострения патологии, что в свою очередь увеличивает расходы системы здравоохранения [10].
Цель исследования – проанализировать правильность использования устройств ингаляционной терапии для доставки препаратов у детей с диагнозом «бронхиальная астма», госпитализированных в связи с обострением заболевания.
Материал и методы
В период с октября 2021 г. по декабрь 2023 г. на базе педиатрического отделения городской детской клинической больницы г. Уфы (клиника) проведено открытое проспективное сравнительное исследование с участием 89 детей с верифицированным диагнозом БА в возрасте от шести до 17 лет 11 месяцев. Все пациенты поступили на стационарное лечение в клинику в связи с обострением заболевания.
Детей с БА в возрасте от шести до 11 лет 11 месяцев было 47 (52,8%) (средний возраст – 7,22 ± 1,14 года), от 12 до 17 лет 11 месяцев – 42 (47,2%) (средний возраст – 12,7 ± 1,34 года).
Для формирования выборки были разработаны критерии включения/исключения из исследования.
Критерии включения:
- возраст от шести до 17 лет включительно;
- верифицированный в соответствии с критериями согласительных документов аллергический фенотип БА;
- отсутствие сопутствующих хронических соматических заболеваний;
- наличие опыта использования ингаляционных средств доставки препаратов базисной противовоспалительной терапии более чем за три месяца до включения в исследование;
- наличие добровольного информированного согласия на участие в исследовании.
Критерии невключения:
- возраст до шести лет и старше 17 лет 11 месяцев 29 дней на момент включения в исследование;
- верифицированный в соответствии с критериями согласительных документов неаллергический фенотип БА;
- наличие сопутствующих хронических соматических заболеваний;
- отсутствие опыта использования ингаляционных средств доставки препаратов базисной противовоспалительной терапии;
- отсутствие добровольного информированного согласия на участие в исследовании.
У всех детей оценены клинико-анамнестические и лабораторно-инструментальные показатели, степень тяжести течения патологии, а также уровень контроля над симптомами.
В соответствии с российскими клиническими рекомендациями тяжесть БА устанавливали ретроспективно, исходя из объема базисной противовоспалительной терапии. Оценка уровня контроля симптомов БА осуществлялась в зависимости от возраста пациентов с помощью адаптированных и стандартизированных тестов. Речь, в частности, идет о тесте по контролю над астмой у детей (Childhood Asthma Control Test, С-ACT), рекомендованном для детей от четырех до 11 лет, и тесте по контролю над астмой (Asthma Control Test, ACTТМ), используемом у детей старше 12 лет.
С целью получения ретроспективных данных изучена первичная медицинская документация («История развития ребенка» (учетная форма 112/у)). Проанализированы структура, объем и способ ингаляционной доставки препаратов базисной противовоспалительной терапии, рекомендованной в амбулаторно-поликлинических условиях.
Оценка техники ингаляции проводилась после купирования приступа БА и зависела от вида ингаляционного устройства, назначенного на амбулаторном этапе.
Анализ техники ингаляции осуществлялся в соответствии с общепринятыми критериями согласно официальной инструкции по применению для каждого ингалятора в отдельности c использованием специально разработанной системы. Соблюдение всех требований к технике ингаляции и ингаляционного маневра оценивалось в два балла, частичное выполнение требований – в один балл, несоблюдение техники ингаляции и связанное с этим непоступление препарата в дыхательные пути – в ноль баллов. Демонстрация и присущая техника ингаляции осуществлялись на ингаляционных устройствах пользователей.
Оценку техники ингаляции с помощью небулайзера проводили на устройстве клиники.
Независимо от полученных результатов после демонстрации ингаляционного маневра все дети были проинструктированы в отношении использования рекомендованного ингаляционного устройства. Кроме того, были проведены мероприятия, направленные на обучение правильной технике ингаляции с последующим контролем усвоения полученных навыков.
Данные устного опроса пациентов и медицинской документации были внесены в сформированную базу данных в программе Microsoft Office Excel (2016 г.) с дальнейшей статистической обработкой. Их анализировали с применением методов описательной статистики. Качественные показатели представляли в виде долей. Межгрупповое сравнение полученных результатов проводилось с учетом объема выборки и распределения данных с применением непараметрических критериев (χ2).
Результаты и их обсуждение
Среди 89 (100%) детей с верифицированной БА преобладали мальчики. Так, мальчиков было 57 (64,1%), девочек – 32 (35,9%). Средний возраст пациентов составлял 9,21 ± 1,12 года.
Детей в возрасте от шести до 11 лет 11 месяцев насчитывалось 47 (52,8%) (первая группа), от 12 до 17 лет 11 месяцев – 42 (47,2%) (вторая группа). Средний возраст пациентов первой группы составлял 7,22 ± 1,14 года, второй группы – 12,7 ± 1,34 года.
У всех детей имело место обострение БА разной степени тяжести с недостаточным контролем над симптомами. С легким или среднетяжелым обострением БА был 71 (79,8%) ребенок, с тяжелым обострением – 18 (20,2%). Согласно результатам тестирования (валидизированные С-ACT и ACTТМ), у 89 (100%) детей отмечался недостаточный уровень контроля над симптомами БА. Частично контролируемое течение БА отмечено в 62 (69,7%) случаях, неконтролируемое течение – в 27 (30,3%).
На основании анализа данных медицинской документации и устного опроса установлено, что все дети с БА получили предписание по приему средств базисной терапии и были проинформированы о дозах препаратов и длительности лечения. Характер рекомендованного до госпитализации объема базисной противовоспалительной терапии, необходимого для достижения контроля над симптомами БА и снижения риска обострения и соотнесенного с определенной ступенью лечения, в зависимости от возраста пациентов представлен в табл. 1.
При оценке объема противовоспалительной терапии с соотношением со степенью тяжести заболевания (ступенью терапии) выявлено, что 22 (24,8%) пациента получали низкие дозы ИГКС, что соответствовало второй ступени терапии и легкой степени патологии. У 52 (58,4%) детей с БА объем базисной терапии соответствовал третьей ступени. Они получали монотерапию ИГКС в средних (19 (21,3%)) и высоких (11 (12,5%)) дозах либо комбинацию низких доз ИГКС и длительно действующих агонистов β2 (ДДБА) (22 (24,8%)). Из наблюдаемых нами детей с БА 15 (16,6%) получали средние дозы комбинации ИГКС – ДДБА, или терапию четвертой ступени.
В первой группе в качестве базисной терапии чаще всего использовали монотерапию ИГКС в низких (18 (38,3%)) и средних (13 (27,7%)) дозах, во второй группе – комбинацию ИГКС – ДДБА в низких (14 (33,3%)) и средних (11 (26,2%)) дозах.
Таким образом, в наблюдаемой популяции преобладало среднетяжелое течение БА – 52 (58,4%) ребенка. Количество пациентов с легким течением болезни составило 22 (24,8%), с тяжелым течением – 15 (16,8%). Большая часть наблюдаемых нами детей получала монотерапию ИГКС в низких, средних и высоких дозах – 52 (58,4%), из них 17 (19,1%) были старше 11 лет. Проведенный нами анализ не исключает наличия связи между объемом рекомендованной в амбулаторно-поликлинических условиях базисной терапии и риском обострения. На наш взгляд, целесообразно пересмотреть объем терапии с акцентом на использование свободной или фиксированной комбинации ИГКС и ДДБА (в режиме единого ингалятора (SMART)). Комбинация ИГКС и ДДБА обеспечивает аддитивный эффект, что позволяет достигать контроля над симптомами БА без повышения дозы ИГКС [3–5].
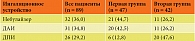
Анализ рекомендованной в амбулаторно-поликлинических условиях формы ингаляционного устройства для доставки препаратов в дыхательные пути у наблюдаемых детей с БА представлен в табл. 2.
Установлено, что для проведения ингаляционной терапии дети с БА чаще использовали небулайзеры (32 (36,0%)), чуть реже – ДАИ (31 (34,8%)) и ДПИ (26 (29,3%)).
Оценка рекомендованной формы ингаляционного устройства в зависимости от возраста пациентов выявила, что в первой группе терапия БА наиболее часто проводилась с использованием небулайзеров (21 (44,7%)), во второй группе – с использованием ДПИ (20 (47,6%)). При этом небулайзеры оставались актуальными средствами доставки препарата и у детей старшей возрастной группы (11 (26,2%)).
В настоящее время ингаляционная терапия с использованием небулайзера является наиболее широко применяемой в педиатрической практике как на стационарном, так и на амбулаторно-поликлиническом этапе [6, 9]. Согласно клиническим рекомендациям, выбор ингаляционного устройства для доставки препарата при стабильной БА должен основываться на предпочтениях пациентов [2]. У детей в качестве предпочтительного способа указываются ДАИ со спейсером. Последний позволяет повысить биодоступность и легочную депозицию препарата и тем самым достичь терапевтического эффекта [3–5].
С учетом того что все дети с БА на момент госпитализации в стационар получали противовоспалительную терапию и имели опыт использования ингалятора, нами была проведена оценка техники выполнения ингаляции. Согласно программным документам по диагностике и терапии БА у детей, неправильное выполнение процедуры может привести к неконтролируемому течению и обострению болезни [3–5]. Доказано, что независимо от вида ингаляционного устройства одна серьезная ошибка в технике проведения процедуры может утяжелить течение патологии.
В рассматриваемой популяции средний стаж применения одной формы ингаляционного устройства составлял 1,91 ± 1,02 года.
Согласно результатам устного опроса, владел информацией об ингаляционных устройствах и имел навыки выполнения ингаляции 61 (68,5%) ребенок. Ранее обучались технике ингаляции 69 (77,5%) детей. Следует отметить, что технические ошибки при проведении ингаляции возникают даже у пациентов с БА со стажем и длительным опытом использования ингаляционных устройств. Так, согласно данным литературы, при динамической оценке техники выполнения ингаляции выявлено, что до 76% применявших ДАИ и до 94% использовавших ДПИ допускали по крайней мере одну ошибку, 25% из них никогда не обучались проведению ингаляции [11].
У 89 (100%) детей была проанализирована правильность техники выполнения ингаляции (табл. 3). С этой целью использовали специально разработанную систему оценки, представленную ранее.
У 47 (52,8%) наблюдаемых нами детей с БА правильность техники выполнения ингаляции была оценена в два балла, у 15 (16,9%) – в один балл, у 27 (30,3%) – в ноль баллов. При этом между пациентами с плохой и хорошей техникой ингаляции выявлены статистически значимые различия (p < 0,05). Чаще выполняли процедуру без ошибок дети из второй группы – 27 (57,5%).
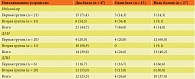
Анализ техники выполнения ингаляции у 89 (100%) детей показал, что большее количество ошибок совершалось при использовании ДАИ (13 (48,2%)). Таковых было меньше при применении ДПИ и небулайзеров – 10 (37,0%) и 4 (14,8%) соответственно.
При сравнении оценки техники выполнения ингаляции у детей с БА в зависимости от возраста установлено, что в первой группе чаще испытывали трудности при использовании ДАИ (12 (60,0%)), во второй группе – при применении ДПИ (10 (37,0%)).
Согласно результатам оценки техники выполнения ингаляции с помощью ДАИ, в обеих группах совершались одинаковые ошибки, которые были связаны с нарушением синхронизации старта ингаляции с началом вдоха, – 13 (48,2%). Таковое может быть скорректировано использованием спейсера. В случае его неэффективности показана замена на ДПИ, не требующие синхронизации респираторного маневра с активацией ингалятора [12].
В нашем исследовании спейсер был только у 7 (22,6%) детей с БА, использовавших ДАИ. Однако даже они испытывали различного рода трудности, связанные с применением этих устройств. Необходимо отметить, что 10 (37,0%) детей совершали грубые технические ошибки при использовании ДПИ.
Сравнительный анализ оценки техники выполнения ингаляции с помощью ДПИ у детей с БА показал, что в обеих группах совершалось одинаковое количество ошибок. Они были связаны с отсутствием адекватной координации ингаляционного маневра, что препятствовало попаданию достаточного объема препарата в дыхательные пути и являлось грубым нарушением терапии, так как легочная депозиция его частиц при использовании ДПИ может быть достигнута только в случае совершения вдоха с усилием [12]. Важно подчеркнуть, что в настоящее время разработаны тренажеры, которые позволяют пациентам с БА отрабатывать навыки корректной координации энергичного вдоха, необходимого для успешной депозиции препарата при использовании ДПИ.
Реже всего дети допускали ошибки при использовании небулайзеров. В обеих группах ошибались с выбором ингаляционной маски, а не мундштука, – 4 (14,8%). Использование лицевой маски увеличивает потерю препарата, из-за этого снижается его терапевтический эффект, а также повышается вероятность оседания на лице и попадания в глаза и носовую полость.
Заключение
В настоящее время сохраняется актуальность рационального применения противовоспалительных препаратов, влияющих на аллергическое воспаление при БА у детей.
Арсенал средств ингаляционной доставки препаратов в дыхательные пути довольно широкий. Однако при их использовании велика вероятность ошибок, способных снизить эффективность проводимой терапии.
При выборе ингаляционного устройства у детей с БА необходимо ориентироваться на их возраст, период патологии и способность выполнять инструкции по технике ингаляции.
Наиболее оптимальным средством ингаляционной доставки препаратов у детей любого возраста со стабильной БА и БА в период обострения является небулайзер. К недостаткам данного устройства относят потерю лекарства во время ингаляционного маневра.
Согласно рекомендациям программных документов, после купирования приступа детей со стабильной БА рекомендуется перевести с небулайзера на портативную форму ингаляционного устройства (ДАИ, ДАИ со спейсером и ДПИ). Выбор конкретного устройства должен основываться на предпочтениях пациента, а также на типе преобладающего инспираторного маневра. В выборе предпочтительной индивидуальной формы ингаляционного устройства может помочь обучение навыкам проведения ингаляционной терапии, которое, как правило, коррелирует с хорошей техникой ингаляции. Обучение пациентов с БА использованию ингаляционных устройств должно проводиться регулярно с обязательной проверкой техники при каждом очном визите к врачу, что, к сожалению, не всегда бывает возможным в условиях реальной клинической практики. Поэтому требуется оптимизация образовательных программ, в том числе с применением современных информационных технологий [12].
R.M. Fayzullina, МD, PhD, Prof., R.R. Gafurova
Bashkir State Medical University
Contact person: Rita R. Gafurova, rita.gafurova2017@yandex.ru
Allergic inflammation of the respiratory tract in patients with bronchial asthma, which is observed both in the period of exacerbation and in the period of remission in the absence of achieving complete control over the course of the disease, justifies the expediency of topical use of anti-inflammatory drugs. Inhalation is the most preferred method of drug delivery for asthma in pediatric practice. However, improper inhalation technique can cause an uncontrolled course and exacerbation of the disease.
The aim of the study was to evaluate the technique of inhalation in children with bronchial asthma.
Material and methods. An open prospective comparative study was conducted, which included 89 children with a verified diagnosis of asthma aged six to 17 years and 11 months who were admitted with an exacerbation of the disease to the Ufa City Children's Clinical Hospital. In this population, the structure, volume, method and technique of inhalation therapy recommended in outpatient settings were analyzed using clinical, anamnestic and functional methods. In addition, all patients were trained in the use of inhalers.
Results. All children with asthma were hospitalized in the pediatric department with an exacerbation of pathology. These were mainly patients with moderate (58.4%) and partially controlled (69.7%) course of asthma, who at the outpatient stage received therapy using various inhalation drug delivery devices. According to the results of an oral survey, 77.5% of the observed children had previously been trained in inhalation techniques. Their experience of using one form of inhalation device averaged 1.91 ± 1.02 years. In 35.9% of cases, the drug was delivered using a nebulizer, in 34.8% of cases – using metered-dose aerosol inhalers (DAI), in 29.3% of cases – using metered-dose powder inhalers (DPI).
The study participants were divided into two groups. The first group included patients aged six to 11 years and 11 months. Most often (44.7%) they were recommended to undergo inhalation therapy using a nebulizer. The second group consisted of patients aged 12 to 17 years and 11 months. Of these, 47.6% used DPI.
When evaluating the technique of inhalation, it was found that 47.2% of children had a gross violation of it, which could lead to a decrease in the intake of a sufficient amount of the drug into the respiratory tract and, as a result, uncontrolled course and exacerbation of pathology. In 48.2% of cases, mistakes were made when using DAI. In 60.0% of patients of the first group, problems arose when using DAI, in 37.0% of patients of the second group – when using DPI.
An analysis of the nature of errors during inhalation, depending on the type of device and the age of patients with asthma, showed that when using DAI, the coordination of inhalation was disrupted. This prevented the inhaler from being activated. When using DPI, errors were associated with the lack of adequate coordination of the inhalation maneuver (inhalation with effort), the nebulizer – with the choice of an inhalation mask rather than a mouthpiece.
Conclusion. For the relief of allergic inflammation in the treatment of asthma in children, the preferred method of drug delivery to the respiratory tract is inhalation. The inhalation device is selected taking into account not only the age, but also the individual characteristics of the patients.
According to the recommendations of generally accepted clinical guidelines, all forms of inhalation devices and all molecules of inhaled glucocorticosteroids, subject to the instructions for their use, provide a high anti-inflammatory effect. To avoid mistakes during inhalation, the appointment of inhalation devices at the outpatient stage should be carried out only after patient training. In addition, at each face-to-face visit to the doctor, an assessment of the correctness of the technique of performing the procedure is shown.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.