Эффективность и безопасность лапароскопического дриллинга яичников
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. В систематический обзор включены публикации на английском языке, посвященные оценке эффективности различных методов лапароскопического дриллинга яичников, за период 1992–2024 гг. Эффективность оценивали по результатам изменения уровня антимюллерова гормона, частоте наступления овуляции и клинической беременности. Обзор подготовлен по чек-листу PRISMA. В анализ включены рандомизированные и нерандомизированные оригинальные клинические исследования (проспективные контролируемые, проспективные когортные и т.д.), метаанализы, литературные и систематические обзоры.
Результаты. После поиска соответствующих исследований и исключения дубликатов синтезу подверглись 257 статей, 148 из которых были исключены из-за несоответствия названию и резюме. В качественный синтез вошли 34 исследования.
Выводы. В настоящее время невозможно определить, какой из существующих методов дриллинга яичников наиболее эффективен. Статистически значимой разницы в наступлении овуляции и беременности при использовании различных методов дриллинга не установлено, а вариабельность и разнородность оцениваемых критериев не позволяют выполнить метаанализ.
Материал и методы. В систематический обзор включены публикации на английском языке, посвященные оценке эффективности различных методов лапароскопического дриллинга яичников, за период 1992–2024 гг. Эффективность оценивали по результатам изменения уровня антимюллерова гормона, частоте наступления овуляции и клинической беременности. Обзор подготовлен по чек-листу PRISMA. В анализ включены рандомизированные и нерандомизированные оригинальные клинические исследования (проспективные контролируемые, проспективные когортные и т.д.), метаанализы, литературные и систематические обзоры.
Результаты. После поиска соответствующих исследований и исключения дубликатов синтезу подверглись 257 статей, 148 из которых были исключены из-за несоответствия названию и резюме. В качественный синтез вошли 34 исследования.
Выводы. В настоящее время невозможно определить, какой из существующих методов дриллинга яичников наиболее эффективен. Статистически значимой разницы в наступлении овуляции и беременности при использовании различных методов дриллинга не установлено, а вариабельность и разнородность оцениваемых критериев не позволяют выполнить метаанализ.

Введение
Согласно определению Всемирной организации здравоохранения (ВОЗ), бесплодие – это состояние мужской и/или женской репродуктивной системы, в связи с которым беременность не наступает после более чем 12 месяцев регулярного незащищенного полового акта [1]. Женское бесплодие обусловлено эндокринными заболеваниями, влияющими на процесс овуляции (35–40%), трубно-перитонеальным фактором (20–30%), органическими причинами бесплодия (15–25%) и иммунологической патологией (2%) [2, 3]. Нарушение овуляции занимает лидирующие позиции среди причин женского бесплодия. Эндокринное бесплодие связано в основном с синдромом поликистозных яичников (СПКЯ), характеризующимся наличием множественных мелких кист в яичниках, избытком андрогенов, нерегулярной овуляцией или ановуляцией [4]. По оценкам ВОЗ, СПКЯ наблюдается приблизительно у 8–13% женщин репродуктивного возраста. При этом до 70% случаев СПКЯ в мире остаются недиагностированными [5]. Согласно рекомендациям ESHRE (European Society of Human Reproduction and Embryology) и ASRM (American Society for Reproductive Medicine), для постановки диагноза СПКЯ используются обновленные в 2023 г. Роттердамские критерии СПКЯ. О СПКЯ говорят при наличии двух из трех следующих критериев после исключения других причин возникновения этих признаков:
- клиническая/биохимическая гиперандрогения;
- овуляторная дисфункция;
- поликистоз яичников при ультразвуковом исследовании [4, 6, 7].
К ультразвуковым критериям относится визуализация ≥ 20 фолликулов диаметром 2–9 мм в любом яичнике и/или увеличение объема любого яичника до значений ≥ 10 см3 (в отсутствие желтого тела, кист или доминантных фолликулов) [8].
В качестве терапии первой линии для преодоления ановуляторного бесплодия у пациенток с СПКЯ рекомендуется использовать летрозол или кломифена цитрат (кломифен) [8, 9]. При назначении кломифена необходимо учитывать индекс массы тела, возраст пациентки и исключить другие потенциальные факторы бесплодия. Текущая практика заключается в назначении кломифена с постепенным увеличением дозы до достижения подтвержденной овуляции. Эффективность стимуляции овуляции достигает 70–80%, частота зачатия – 22% на цикл [10]. Примерно у 85% пациенток с СПКЯ овуляция происходит в ответ на терапию кломифеном при максимальной используемой дозе 150 мг [10]. Как правило, лечение кломифеном предполагает не более шести циклов. Отсутствие овуляции в этом периоде расценивается как резистентность к кломифену. Она составляет 15–40% среди больных СПКЯ [11].
В качестве второй линии терапии при кломифен-резистентных формах СПКЯ показано добавление метформина к кломифену либо проведение стимуляции овуляции гонадотропинами [12]. Альтернативой при резистентности к лекарственной терапии является оперативное лечение – лапароскопический дриллинг яичников (ЛДЯ) [13].
ЛДЯ – хирургическое вмешательство, позволяющее восстановить овуляцию благодаря механическому разрушению утолщенной оболочки яичника. Данный метод сопоставим по эффективности с терапией гонадотропинами, но имеет меньшие риски гиперстимуляции яичников и многоплодной беременности [12]. ЛДЯ вызывает ряд морфологических и биохимических изменений в яичниках, включающих образование искусственных отверстий в капсуле яичников, разрушение фолликулов с последующим уменьшением количества теки и/или гранулезных клеток, разрушение стромальной ткани яичников. Эти факторы способствуют снижению продукции андрогенов, уменьшению периферического превращения андрогенов в эстрогены и возобновлению овуляторных циклов [12, 14].
Ранее для преодоления ановуляторного бесплодия выполняли клиновидную резекцию. В результате наступление беременности сопровождалось высоким риском развития спаечного процесса органов брюшной полости и органов малого таза в послеоперационном периоде. С введением минимально инвазивного подхода – ЛДЯ – хирургическое лечение кломифен-резистентных случаев СПКЯ стало более безопасным [15].
Существует несколько методов выполнения дриллинга, однако единого мнения о том, какой из них предпочтительнее, нет. Наиболее широко применяемой техникой считается использование монополярного электрода с выполнением четырех проколов яичника по 40 Вт каждый. Суммарная энергия, воздействующая на яичник, – 640 Дж [16, 17]. В отличие от монополярной биполярная электрокоагуляция вызывает обширное повреждение тканей яичника [18]. Лазерная вапоризация проводится с помощью лазера, позволяющего получить эффект локального испарения тканей яичника [19]. Ультразвуковой скальпель HARMONIC способен производить три типа воздействия: кавитацию, коагуляцию и пересечение с минимальным повреждением тканей. Принцип работы скальпеля основан на преобразовании электрической энергии в механическую [20]. Новым вариантом лечения является офисный микролапароскопический дриллинг яичников, который можно выполнять влагалищным доступом в амбулаторных условиях под местной анестезией. Это позволяет минимизировать болевые ощущения и сократить период госпитализации [21].
Цель – проанализировать частоту наступления беременности и овуляции при использовании различных вариантов ЛДЯ.
Материал и методы
В систематический обзор включены публикации, посвященные оценке эффективности различных методов ЛДЯ, за период 1992–2024 гг. При подготовке данной статьи был использован чек-лист PRISMA – минимальный набор элементов отчетности для написания систематических обзоров и метаанализов. Область применения PRISMA фокусируется на составлении отчетов об обзорах, оценивающих рандомизированные исследования.
В анализ включены рандомизированные и нерандомизированные оригинальные клинические исследования (проспективные контролируемые, проспективные когортные и т.д.), метаанализы, литературные и систематические обзоры. Рассматривались публикации только на английском языке. Поиск проводился в электронных базах данных PubMed, ClinicalTrials.gov и Cochrane Library по ключевым словам: laparoscopic ovarian drilling (лапароскопический дриллинг яичников), anovulatory infertility (ановуляторное бесплодие), polycystic ovary syndrome (синдром поликистозных яичников).
Три независимых исследователя выполнили электронный поиск публикаций по сформулированному запросу. Подходящие по названию исследования в дальнейшем оценивались по абстракту и полному тексту публикации. Дубликаты исключались. Полный текст оценивали три независимых исследователя для включения публикации в качественный анализ. Любые разногласия в процессе отбора статей для качественного синтеза устранялись путем консенсуса после совместного обсуждения с четвертым исследователем. Просматривались также списки литературы подходящих исследований с целью поиска дополнительной литературы.
Данные из включенных исследований собирались независимо тремя авторами с использованием стандартной процедуры; в отчет включали авторов, страну исследования, год публикации, характеристику пациентов, вмешательство и исходы.
Основной анализ данного систематического обзора направлен на сравнение методов ЛДЯ и выявление наиболее эффективного и безопасного из них. Критерии включения:
- репродуктивный возраст;
- наличие кломифен-резистентных форм СПКЯ;
- проведение лапароскопического дриллинга яичников в целях лечения бесплодия.
Статьи, в которых для индукции овуляции применялись медикаментозные методы лечения, исключались. Оценка предвзятости включенных в обзор исследований выполнена с использованием The Cochrane Handbook for Systematic Reviews of Interventions. Эту оценку независимо друг от друга проводили два исследователя с помощью шкал, рекомендованных обществом Cochrane. Разногласия в процессе оценки предвзятости устранялись путем консенсуса или с привлечением третьего автора. Для оценки риска систематической ошибки в рандомизированных контролируемых исследованиях применялась шкала RoB2.0, а в нерандомизированных исследованиях (проспективных контролируемых, проспективных когортных или ретроспективных исследованиях и др.) – шкала ROBINS-I.
Результаты
Отбор исследований
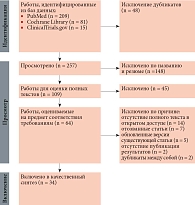
Поиск релевантных исследований в трех крупных базах данных выявил 305 статей (рис. 1): 209 в PubMed, 81 в Cochrane Library, 15 в ClinicalTrial.gov. Исключено 48 статей-дубликатов. Скринингу подверглись 257 статей, 148 из которых исключены по названию и резюме. Далее полнотекстовые версии 109 статей анализировали на предмет соответствия критериям включения и исключения. После оценки полнотекстовых статей исключено 45 работ.
Оставшиеся 64 статьи оценивались на предмет соответствия требованиям. Из них исключено 14 из-за отсутствия полного текста в открытом доступе, две – из-за отсутствия опубликованных результатов, семь отозванных статей, пять обновленных версий существующей статьи, два дубликата. Таким образом, 34 исследования использованы для качественного анализа: девять обзоров, восемь клинических испытаний, пять когортных исследований, пять рандомизированных контролируемых исследований, три метаанализа, два сравнительных исследования, одно кросс-секционное исследование, один систематический обзор.
Обобщение результатов
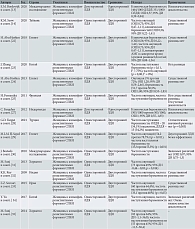
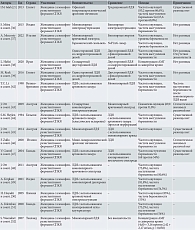
В 16 исследованиях выполнено сравнение одностороннего ЛДЯ с двусторонним (табл. 1) [13, 14, 22–35]. При этом только в одном из них выявлено статистически значимое преимущество методики как в отношении частоты свершившейся овуляции, так и частоты наступления беременности (p < 0,05) [36]. В свою очередь в восьми из ранее приведенных исследований статистически значимая разница не обнаружена [14, 22–25, 37–39]. Оценить результаты остальных исследований не представляется возможным из-за низкокачественных доказательств [13, 21, 26–29]. При сравнении эффективности использования электрокоагуляции и лазера в трех исследованиях также не выявлено статистически значимой разницы [14, 40, 41].
Преимущество использования монополярной электрокоагуляции по результатам частоты наступления беременности установлено только в одном исследовании [42]. Однако распределение пациенток по двум группам сравнения было неравномерным: 32 женщинам проводили дриллинг с использованием электрокоагуляции, 80 – с применением аргонового лазера (28 против 72%).
Существующие на данный момент методы дриллинга сравнивали в 10 исследованиях. Статистически значимая разница отсутствовала [21, 36–39, 43–47]. Сравнивались не только традиционные методы (монополярная и биполярная электрокоагуляция, лазерная вапоризация), но и относительно новые (использование гармонического скальпеля, неодимового (Nd:YAG) лазера. В трех исследованиях оценивали влияние дозы электрического тока при проведении дриллинга методом электрокоагуляции. Статистически значимой разницы между скорректированной и фиксированной не выявлено [37–39].
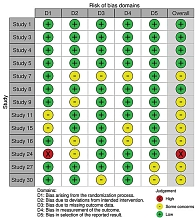
В соответствии с рекомендациями Cochrane Handbook, рецензенты оценили риск систематической ошибки в каждом из включенных исследований с использованием RoB2.0 для рандомизированных контролируемых исследований и ROBINS-I для нерандомизированных. Инструмент RoB2.0 включает риск систематической ошибки при процессе рандомизации, ошибку, связанную с отклонением от намеченного вмешательства, ошибку пропуска данных, ошибку измерения результатов и ошибку представления результатов.
Каждый пункт классифицирован как связанный с высоким риском, вызывающий сомнения или указывающий на низкий риск систематической ошибки.
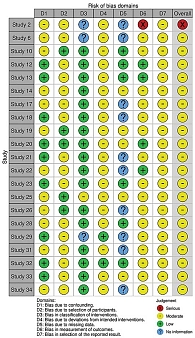
Инструмент ROBINS-I включает ошибку конфаудинга, ошибку отбора участников исследования, ошибку классификации воздействий, ошибку, связанную с отклонением от намеченного вмешательства, ошибку пропуска данных, ошибку измерения результатов, ошибку представления результатов. Каждый пункт классифицирован как указывающий на серьезный, умеренный или низкий риск систематической ошибки.
Любые разногласия разрешались путем обсуждения. Инструменты визуализации созданы приложением ROBVIS. Инструмент RoB2.0 показал в основном умеренный риск общей систематической ошибки для рандомизированных исследований (рис. 2). Согласно инструменту ROBINS-I, для нерандомизированных исследований общий риск систематической ошибки был умеренным, за исключением одного исследования, в котором риск ошибки оценили как серьезный (рис. 3).
Обсуждение
В рандомизированном клиническом исследовании M.L.M. El-Sayed и соавт. показано значительное увеличение частоты наступления клинической беременности и овуляции при двустороннем ЛДЯ (частота овуляций – 54,2 против 78,7%; p = 0,011; частота наступления беременности – 33,3 против 55,3%; p = 0,031) [29]. Однако в ретроспективном исследовании не выявлена статистически значимая разница в частоте наступления беременности в двух группах (частота наступления беременности: односторонний ЛДЯ – 20 (54,1%) пациенток, двусторонний ЛДЯ – 13 (34,2%)) [28]. В других исследованиях также не установлено статистически значимой разницы в частоте овуляций (отношение шансов (ОШ) 0,73; 95%-ный доверительный интервал (95% ДИ) 0,47–1,11) [14]; частота овуляции – 76 против 72% (ОШ 1,20; 95% ДИ 0,59–2,46) [24], частота беременности – 51,7 против 50,5% (ОШ 1,00; 95% ДИ 0,55 –1,83) [24].
J. Ott и соавт. в своем исследовании не отметили статистически значимых различий между двумя проводимыми методами дриллинга. Исследователи сравнивали ЛДЯ с использованием монополярной электрокоагуляции и ЛДЯ с применением монополярного крючкового электрода [43, 45]. В 2011 г. J. Ott и соавт. также показали, что оба метода одинаково эффективны для индукции спонтанной овуляции и беременности. Частота спонтанных овуляций у пациенток, которым проводился ЛДЯ с использованием монополярного крючкового электрода, составляет 75,8%, а частота спонтанной овуляции после электрокоагуляции находится в диапазоне 70–80% [48].
A. Kriplani и соавт. в проспективном исследовании установили, что ЛДЯ с использованием монополярной электрокоагуляции является эффективной хирургической процедурой у женщин с резистентным к кломифену СПКЯ. Данные наблюдений показали, что у 66 пациенток частота спонтанных овуляций составляет 81,8%, кумулятивная частота овуляций – 93,9%, частота наступления беременности – 54,5% [49].
K.M. Seow и соавт., C. Unlu и соавт. не обнаружили существенной разницы в показателях клинической беременности и овуляции (частота овуляции – 83 против 77,5%; ОШ 1,4; 95% ДИ 0,9–2,1, частота наступления беременности – 65% против 54,5%; ОШ = 1,5; 95% ДИ 1,1–2,1) у пациенток с кломифен-резистентными формами СПКЯ, у которых применялся ЛДЯ с использованием электрокоагуляции и лазера (табл. 2) [14, 40, 41]. Однако в приведенных исследованиях отражены значительно более высокие кумулятивные показатели частоты наступления беременности через год у женщин, подвергшихся ЛДЯ с использованием электрокоагуляции, в сравнении с использованием лазерной энергии (65 против 54,5%; ОШ 1,5; 95% ДИ 1,1–2,1). Кроме того, после повторной операции стало понятно, что использование лазерной энергии связано с увеличением частоты развития спаечного процесса в сравнении с электрокоагуляцией (41,5 против 31%) [41].
T.C. Li и соавт., S.M. Heylen и соавт., V. Gomel и соавт. оценивали эффективность ЛДЯ с использованием аргонового лазера у женщин с кломифен-резистентными формами СПКЯ (табл. 3) [21, 36–39, 42–52]. В ретроспективное исследование T.C. Li и соавт. было включено 118 женщин с СПКЯ, которым выполнялся ЛДЯ в целях преодоления ановуляторного бесплодия. Использовались два вида энергии: аргоновый лазер у 31 (28%) женщины и монополярная электрокоагуляция у 80 (72%). Показано, что при использовании электрической энергии (диатермии) процент наступления беременности выше, чем при использовании аргонового лазера [42]. В остальных проведенных исследованиях существенной разницы между двумя методами дриллинга не зафиксировано.
В исследовании H. Hayashi и соавт. были проанализированы данные 40 пациенток из Японии, у которых диагностировано бесплодие, ассоциированное с кломифен-резистентной формой СПКЯ. Эти пациентки получили лечение в объеме ЛДЯ с использованием аргонолучевой электрокоагуляции. После ЛДЯ овуляция произошла у 33 (83%) пациенток, беременность наступила у 22 (55%) [50].
Результаты рандомизированного клинического исследования L. Hafizi и соавт. продемонстрировали отсутствие различий в отношении установления регулярности цикла и овуляции между стандартным двусторонним ЛДЯ и двусторонним дриллингом с коррекцией дозы энергии. Уровень антимюллерова гормона (АМГ) (p = 0,73), тестостерона (p = 0,91) и дегидроэпиандростеронсульфата (p = 0,16) не различался в начале исследования и через месяц после выполнения дриллинга яичников (p = 0,94 для АМГ, p = 0,46 для тестостерона и p = 0,12 для дегидроэпиандростеронсульфата). Однако метод с корректировкой дозы повлиял на снижение уровня АМГ [38].
В ретроспективное исследование A. Felemban и соавт. было включено 112 женщин с бесплодием, ассоциированным с СПКЯ, резистентным к кломифена цитрату. В качестве лечения пациенткам выполняли ЛДЯ с использованием изолированной иглы-каутеризатора. После операции овуляция произошла спонтанно у 73,2% пациенток. Кумулятивная вероятность зачатия через 12, 18 и 24 месяца после операции составила 54, 68 и 72% соответственно. Использование изолированной иглы-каутеризатора связано с минимальной вероятностью образования послеоперационных спаек [51].
В итальянском проспективном рандомизированном исследовании 2000 г. участвовало 62 женщины. Они были разделены на две группы. Пациенткам группы А выполняли мини-лапароскопический дриллинг яичников с помощью местной анестезии и внутривенной седации. Пациенткам группы Б проводили традиционный ЛДЯ под общей анестезией. Уровень лютеинизирующего гормона значительно снизился после операции в обеих группах, а уровни фолликулостимулирующего гормона существенно не изменились ни после мини-лапароскопии, ни после лапароскопии. Число пациенток, выписанных в течение двух часов после операции, было достоверно выше в группе А. Потребность в послеоперационных анальгетиках была достоверно выше в группе Б. Частота овуляции составила 81,2% в группе А и 86,6% в группе Б [46].
I.M. Salah в контролируемом исследовании сравнивал эффекты офисного микролапароскопического дриллинга яичников под местной анестезией в качестве нового метода лечения с результатами, достигнутыми после традиционного ЛДЯ под общим наркозом. В группе из 60 женщин с ановуляторным СПКЯ проводился офисный микролапароскопический дриллинг яичников (основная группа), и 60 женщинам с ановуляторным СПКЯ был выполнен традиционный ЛДЯ. После оперативных вмешательств существенных различий в полученных результатах не зафиксировано: частота овуляций – 85,2 против 86,6%, частота наступления беременности – 65,6 против 60,0% соответственно [21].
A. Mercorio и соавт. в рандомизированном исследовании рассматривали различные методики дриллинга яичников – как традиционные, так и малоинвазивные. Установлено, что использование гармонического скальпеля так же эффективно, как и применение Nd:YAG-лазера, хотя последний с меньшей вероятностью приводил к спаечному процессу, поскольку конусообразные следы от лазера обеспечивали меньшее проникновение тепла в ткани [37].
L. Hafizi и соавт. оценивали малоинвазивную технологию – трансвагинальный дриллинг яичников под ультразвуковым контролем. Предварительные данные свидетельствуют о безопасности этой методики. Результаты в отношении частоты овуляции и беременности сопоставимы со стандартным биполярным лапароскопическим дриллингом без потенциального риска термического повреждения [38].
Выводы
В данном систематическом обзоре суммированы существующие клинические исследования, опубликованные на английском языке. Учитывая проанализированные данные различных авторов, можно сделать вывод, что на сегодняшний день невозможно определить, какой из методов дриллинга яичников наиболее эффективен. Статистически значимой разницы в наступлении овуляции и беременности при проведении одно- и двустороннего дриллинга не выявлено. Кроме того, не обнаружено различий в установлении регулярности цикла и овуляции между стандартным двусторонним ЛДЯ и двусторонним дриллингом с коррекцией дозы энергии.
Следует отметить, что исследования, включенные в данный систематический обзор, гетерогенны. Это не позволяет выполнить метаанализ. Ограничением настоящего обзора является также значительная вариабельность и разнородность оцениваемых критериев, применительно к которым сравнение нецелесообразно. Не во всех анализируемых исследованиях указано количество участниц, что также ограничивает систематический обзор.
Несмотря на то что используемые методы дриллинга яичников действительно приводят к увеличению частоты наступления овуляции и последующей беременности у женщин с диагностированным ановуляторным бесплодием, необходимо учитывать количество энергии, полученной тканями во время операции, и ее влияние на повреждение ткани яичника.
В дальнейших исследованиях необходимо оценивать не только непосредственно наступление беременности после оперативного вмешательства, но и влияние процедуры на течение беременности, а также акушерские, материнские и неонатальные риски.
Е.V. Sibirskaya, PhD, Prof., P.O. Nikiforova, A.S. Еgorova, O.S. Koryagina, A.M. Almyasheva, I.N. Kovshova
Russian Children’s Clinical Hospital – a Branch of N.I. Pirogov Russian National Research Medical University
N.I. Pirogov Russian National Research Medical University
Russian University of Medicine
Peoples' Friendship University of Russia
I.M. Sechenov First Moscow State Medical University
Contact person: Еlena V. Sibirskaya, elsibirskaya@yandex.ru
The aim is to analyze the frequency of pregnancy and ovulation when using various options for laparoscopic ovarian drilling.
Material and methods. This systematic review includes English language publications on studies comparing the efficacy of different laparoscopic ovarian drilling methods from 1992 to 2024. Efficacy was evaluated based on changes in AMH levels, ovulation frequency, and clinical pregnancy rates. The review was conducted following the PRISMA checklist. The analysis included randomized and non-randomized original clinical studies (prospective controlled, prospective cohort, etc.), meta-analyses, literature reviews, and systematic reviews.
Results. After searching for studies that matched the search criteria and excluding duplicates, 257 articles were identified, of which 148 were excluded due to title and abstract mismatches. A total of 34 studies were included in the qualitative synthesis.
Conclusions. Currently, it is impossible to determine which of the existing methods of ovarian drilling is the most effective. There is no statistically significant difference in the onset of ovulation and pregnancy when using different drilling techniques, and the significant variability and heterogeneity of the assessed criteria do not allow a meta-analysis.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.