Гепатоцеллюлярная карцинома
- Аннотация
- Статья
- Ссылки








Хронические вирусные инфекции как фон для развития гепатоцеллюлярной карциномы
Согласно данным проведенного в 2007 г. исследования, существует четкая тенденция к росту заболеваемости ГЦК. Здесь речь не идет об улучшении диагностики – по сути кардинальных прорывов в ранней диагностике этой опухоли в последние годы не произошло, а об истинном росте заболеваемости ГЦК. В России ежегодно регистрируется около 6000 пациентов с диагнозом «рак печени». Для роста заболеваемости ГЦК существуют следующие причины: увеличение числа больных циррозом печени (главным образом вследствие вирусных гепатитов В, С, а также алкогольной болезни печени, неалкогольного стеатогепатита и др.) и увеличение продолжительности жизни у больных циррозом печени в результате эффективной этиотропной и патогенетической терапии (еще 15 лет назад мы существенно реже наблюдали пациентов с ГЦК только потому, что пациенты до нее не доживали).
Хорошо изучены механизмы канцерогенеза, вызванного вирусом гепатита В. Вирус гепатита В (HBV) обладает тропностью к печеночной ткани, а хроническая инфекция этим вирусом приводит к прогрессирующему воспалению печени и развитию фиброза и цирроза печени и в конечном счете ГЦК.
Основные факторы риска развития ГЦК при HBV-инфекции (Kim, 2008; Lok, 2009) – это цирроз печени, мужской пол, возраст старше 50 лет, уровень HBV DNA > 104 копий/мл, положительный статус HBeAg+, генотип C HBV, мутации в области core promoter, повышенный уровень АЛТ, некровоспалительная активность в биоптате – и к ним с каждым годом добавляются новые по мере завершения различных исследований, помимо тех, что уже известны десятилетиями – курение сигарет, употребление алкоголя и пр.
Алкоголь сам по себе канцерогеном не является, но является ко-канцерогеном из-за вмешательства в клеточный цикл и реализации действия гепатотропных вирусов (активация протоонкогенов (c-myc, N-my2c, c-fos), угнетение функции генов-супрессоров опухолевого роста p53, подавление активности каспазы 3). Представлены последние данные о том, что у пациентов латентная инфекция анти-НВс при алкогольном циррозе является фактором канцерогенеза.
При HСV-инфекции ГЦК на стадии цирроза составляет до 8% в год, в отдельных случаях возможно развитие ГЦК на доцирротической стадии. Достоверной связи с генотипом вируса не установлено. Вероятные механизмы злокачественной трансформации: взаимодействие core-протеина вируса с геномом клетки (генами H-ras, p53) и повреждение генома в реакциях перекисного окисления.
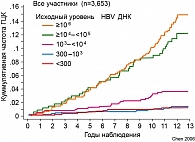
Факторы высокого риска развития ГЦК при HСV-инфекции те же, что и при HBV-инфекции (возраст > 50 лет, мужской пол, высокая гистологическая активность), по последним данным – выраженный фиброз (корреляция с количеством тромбоцитов, АСТ/АЛТ и другими неинвазивными показателями), высокий уровень сывороточного альфа-фетопротеина. Сочетание с HBV-инфекцией (даже отмечается корреляция с количеством HBV ДНК в печени в отсутствие HBsAg) (см. рисунок 1) и опять же злоупотребление алкоголем являются высокими канцерогенными факторами.
В исследовании Henderson (2009) из 32806 пациентов с хронической патологией почек на гемодиализе, инфицированных HCV, у 262 (0,8%) развилась ГЦК. В результате мультифакторного анализа выяснилось, что цирроз – в 12 раз (P < 0,001), злоупотребление алкоголем – в 3 раза (P < 0,001), сахарный диабет – в 1,3 раза (P = 0,04) увеличивает риск ГЦК. Ikeda (1993) отмечает корреляцию длительности HCV-цирроза и частоты развития ГЦК: 5 лет – 21,5%; 10 лет – 53,2%; 15 лет – 75,2%.
Скрининг за счет выявления ранних форм опухоли значительно повышает выживаемость при ГЦК. Больные с высоким риском развития рака (лица старше 40 лет, страдающие гепатитом В и С; больные циррозом печени) должны не менее одного раза в год проводить ультразвуковое исследование печени, а также определять в крови опухолевый маркер – альфа-фетопротеин.
Роль противовирусной терапии HBV-инфекции в различных исследованиях оценивается по-разному. Так, данные по лечению ИФН-a противоречивы, однако с перевесом в пользу снижения риска ГЦК у пациентов, где достигнут устойчивый ответ, нет данных по пегилированным ИФН; в исследовании Yuen (2001) лечение ламивудином больных HBV-циррозом не снижает риск ГЦК, однако в исследовании, проведенном Liaw (2004), лечение ламивудином больных HBV-циррозом снижает риск ГЦК вдвое (с 7,4 до 3,9%).
Роль нормализации трансаминаз исследовалась Ikeda (2006): чем выше биохимическая активность трансаминаз, тем выше частота развития ГЦК.
Результаты исследования Ishiguro (2009) (N = 19812, 1236 – инфицированы гепатотропными вирусами) демонстрируют зависимость уровня АЛТ и риска ГЦК. Если АЛТ < 30 ед/л, нет вируса – нет риска; АЛТ > 30 ед/л, нет вируса – риск ГЦК повышается в 9,4 раза; АЛТ < 30 ед/л, есть вирус – в 15,2 раза; АЛТ 30-69 ед/л, есть вирус – в 180,5 раза; АЛТ > 70 ед/л (2,5 нормы), есть вирус – в 454,2 раза (P для тренда < 0,001).
Последние исследования показывают связь хронических гепатитов В, С не только с ГЦК, но и с холангиокарциномой, что доказывает необходимость в противовирусной терапии для каждого больного, у которого даже может не развиться цирроз, но многократно повышен риск развития рака печени.
Особенности диагностики рака печени
Среди первичных злокачественных образований печени – ГЦК, холангиокарцинома, гемангиоэндотелиома, гемангиобластома, ангиосаркома, саркома – доля ГЦК составляет до 85%. В мире заболеваемость ГЦК (437000 случаев, или 5,4%) рассматривается на 5-м месте в общем количестве выявленных онкологических заболеваний (D. Parkin et al., 1999) и на 3-м месте (427000, или 8,2%) (Lancet, 2003) в значениях общей онкологической летальности. Так, в 2008 г. только в США зарегистрировано 21370 случаев ГЦК и 17000 случаев летальности у пациентов с таким диагнозом. Небольшое различие численных показателей заболеваемости и летальности отражает крайне неблагоприятный прогноз ГЦК. Критериями неблагоприятного прогноза ГЦК служат превышение размера опухоли > 5 см, инфильтративный опухолевый рост, мультилокулярная форма, метастатическое распространение. ГЦК обнаруживается слишком поздно, так как развивается без специфичных жалоб. Пациент может предъявлять жалобы на боль в верхнем отделе брюшной полости, тошноту, метеоризм, анорексию и потерю веса, слабость и утомляемость; при первичном обращении и физическом обследовании отмечаются повышение температуры тела, эктеричность склер и кожных покровов, асцит, латентно протекающая энцефалопатия, болезненность при пальпации увеличенной печени.
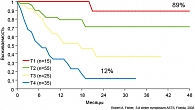
В то же время существует прямая зависимость выживаемости пациентов от срока обращаемости и выявления опухоли. Данные одного из докладов по категории опухоли T по каким-либо причинам нелеченных больных, приведенные на рисунке2 , убедительно подтверждают это положение. Медиана выживаемости только 12% больных с опухолью Т4 достигала 18 мес. (см. рисунок 2).
Стадирование ГЦК рассматривается как фактор для определения тактики лечения пациентов. Критериями для определения стадии ГЦК являются свойства опухолевого образования, такие как размер (возможность оценить массу опухоли), количество очагов (солитарный узел или мультилокулярная форма), локализация в долях печени с отношением к объему паренхимы, инвазивный рост в сосудистые структуры (наличие тромбоза воротной вены) и экстраорганно; наличие метастазов, в том числе в лимфатические узлы; степень дисфункции печени (количественные значения биллирубина, альбумина, наличие асцита); уровень альфа-фетопротеина и статус активности пациента. Врач лучевой диагностики делает свое заключение на основании полученных изображений, и объемный протокол, выдаваемый врачом-диагностом, позволяет гепатологу и хирургу оценить стадийность опухоли, для каждой из которых предлагается своя тактика лечения. Бремя ГЦК представляет серьезную проблему, и несмотря на появление препарата для системной терапии, улучшающего выживаемость больных ГЦК, – сорафениба (Нексавар), что является значительным достижением в лечении рака печени, ранняя диагностика, выявление и мониторинг популяции населения с высоким риском заболевания ГЦК должны оставаться в ряду первостепенных задач здравоохранения.
Для своевременной диагностики ГЦК проводят полное клинико-лабораторное обследование по обращению с высоким процентом специфичности исследований: определение уровня альфа-фетопротеина (повышение значений у 50-70% пациентов с первичным раком печени); ультразвуковое исследование органов брюшной полости; спиральная компьютерная томография органов брюшной полости с внутривенным болюсным введением контрастного вещества; магнитно-резонансная томография органов брюшной полости; радиоизотопные методы диагностики; чрескожная биопсия (сопутствует риск распространения опухолевых клеток при ранних опухолевых процессах, сложность попадания в небольшой узел); ангиография; лапароскопия. Статистика раннего выявления ГЦК по базе данных 1968-2004 гг. коллег из Ogaki Municipal Hospital (Japan) показывает, как вырос уровень диагностированных на ранних стадиях опухолевого процесса ГЦК даже у пациентов с циррозом печени в период наблюдения 2001-2004 гг. в сравнении с предшествующими периодами (см. таблицу), однако остается всего лишь на уровне 1/3 всех случаев с верифицированным диагнозом ГЦК.
К факторам риска развития ГЦК прежде всего относят HBV- и HCV-инфекции (вирусные гепатиты), алкоголизм и табакокурение, диффузные заболевания печени (гемохроматоз), ионизирующее радиационное излучение и пр.
Диагностика ГЦК у пациентов с циррозом печени вызывает трудности с идентификацией изображений у диагностической службы. Были выработаны определенные алгоритмы и практические рекомендации (EASL, AASLD & JSH Conference, Barcelona 2005; AASLD Practice Guidelines 2007; С.J. Zech, Workshop LIVER IMAGING, ESGAR, 2009) в связи с особенностями диагностики ГЦК у пациентов с циррозом. При размере опухоли, в диаметре превышающем 2 см, у пациентов с циррозом использование одного из методов визуализации (СКТ, МРТ, УЗИ) с в/в контрастированием для подтверждения гиперваскуляризации и оценки «вымывания» (wash-out) контрастного препарата или уровень альфа-фетопротеина более 200 нг/мл (ГЦК) позволяют диагностировать ГЦК.
Наличие опухоли (ГЦК?) в диаметре 1-2 см предполагает использование сочетания двух методов визуализации (СКТ или МРТ, МРТ или УЗИ) с в/в контрастированием для оценки ранней артериальной гиперваскуляризации и «вымывания» (wash-out) в венозную фазу контрастирования. В качестве рекомендации – МРТ органов брюшной полости минимум с двумя контрастными препаратами. Чрескожная биопсия может иметь место при подтверждении диагноза ГЦК, хотя возможны затруднения из-за размера подозрительного на ГЦК очага.
Подозрительный на опухоль очаг в диаметре менее 1 см требует динамического УЗИ-наблюдения каждые 3-4 месяца, так как в этом случае данные СКТ или МРТ об артериальной васкуляризации не позволяют точно дифференцировать узлы регенерации и ГЦК.
В последние годы в распоряжении врачей-диагностов появляется довольно много контрастных веществ для МРТ исследований (их многообразие можно сравнить с прилавком торговца специями), но только не в нашей стране. Среди Gd-содержащих препаратов гепатоцит-специфичным является Примовист®, год назад предоставленный для использования в России компанией Bayer Schering Pharma. Вводимый внутривенно Примовист® предназначен исключительно для диагностических целей и представляет собой парамагнитное контрастное средство на основе гадолиния. Повышая МР сигнал от опухоли, на динамических и отсроченных изображениях Примовист® улучшает выявление очаговых поражений печени (в т.ч. их количество, размер, сегментарное распределение и визуализацию) и позволяет получить дополнительные данные по их характеристике и классификации, увеличивая тем самым достоверность диагноза.
Кроме гепатоцит-специфичных контрастных препаратов, не менее важны для ранней диагностики ГЦК RES-специфичные, однако такие препараты в настоящее время нам недоступны.
Аспекты хирургического лечения гепатоцеллюлярной карциномы
В своем сообщении я представляю хирургический взгляд на такую сложную проблему, как ГЦК. Сложность и значимость ее определяются главным образом тем, что заболеваемость ГЦК растет, развитие болезни проходит на фоне уже скомпрометированной печени, как правило, низкая операбельность предопределена поздней диагностикой, а возможности лекарственного лечения еще более ограничены. Однако в настоящее время я вижу в решении этой проблемы значительные достижения, несмотря на ее драматизм, в том числе и появление первого препарата для системной химиотерапии – сорафениба (Нексавар®), улучшающего выживаемость больных с ГЦК.
Большинство случаев заболевания ГЦК относится к населению стран Азии и Африки – 30 на 100 тыс. населения, тогда как в Европе фиксируют 2 случая на 100 тыс. населения, и частота гепатоцеллюлярного рака растет быстрее, чем остальных опухолей. Причем повсеместно заболеваемость вирусными гепатитами С, В составляет 70% среди больных ГЦК. Из собственного опыта замечу, что еще в конце 1980-х гг. из 10 пациентов с ГЦК только 2-3 имели фоновый цирроз, у остальных была сохранная печень и можно было выполнять резекцию, сегодня ситуация выглядит с точностью до наоборот. Клиническая картина: соотношение мужчин и женщин с ГЦК составляет 3 : 1, это в основном пациенты в возрасте 50-70 лет, фоном ГЦК, как правило, является вирусный гепатит, цирроз, алкогольная болезнь печени. Симптомы – боль, слабость, лихорадка – все те же симптомы, что и при циррозе печени. Поэтому диагностический алгоритм предусматривает при обнаружении на УЗИ объемного очага в случае повышенных значений уровня альфа-фетопротеина предположение диагноза «карцинома», а при нормальном уровне альфа-фетопротеина сомнения должны последовательно разрешаться результатами компьютерной томографии, магнитно-резонансной томографии или ангиографии, затем биопсией.
Тактика лечения ГЦК определяется не только стадией опухоли, но и степенью поражения печени (цирроз) – функциональные показатели печени играют очень важную роль в выборе лечения ГЦК. Разработано несколько классификационных систем (Okuda, TNM, CLIP), но универсальной классификации пока не существует. Барселонская классификация (BCLC) при гепатоцеллюлярном раке в различных его стадиях предусматривает различные хирургические и нехирургические методы лечения, такие как резекция, трансплантация, локальная деструкция, трансартериальная химиоэмболизация, лучевая терапия и системная химиотерапия сорафенибом (Нексавар®).
На взгляд хирурга, можно внятно лечить всего 10-30% таких пациентов. Хирургическому лечению подлежат пациенты со следующими характеристиками: опухоль – 1 очаг до 5 см либо 3 очага до 3 см; функция печени должна быть относительно сохранна (Child-Pugh класс A). Нехирургическому лечению подвергаются пациенты, распространенность опухоли и низкие функциональные резервы печени (Child-Pugh классы В, С) которых не позволяют провести хирургическое вмешательство.
До начала лечения важна оценка функционального состояния печени по общеизвестным критериям (Child-Pugh, индоцианин зеленый (ICG), объемы печени). У 12-14% пациентов при опухоли справа природно имеется небольшой остаточный объем левой доли печени менее 20%, что ограничивает какие бы то ни было хирургические возможности, у этой группы больных сначала высокотехнологичными методами наращивают левую долю и путем двухэтапного лечения появляется возможность выполнить резекционное вмешательство.
Предоперационная химиоэмболизация (TACE) в неоадъювантном режиме ухудшает прогноз, об этом свидетельствуют результаты исследований (Wu C.C. et al., 1995, N = 52; Sasaki A. et al., 2006, N = 235), где 5-летняя выживаемость существенно различалась (%) при TACE «+»и TACE «–» (23 против 57 в первом исследовании и 28,6 против 50,6 во втором, р < 0,05).
Резекционные вмешательства при анатомической резекции печени дают достоверно большую 5-летнюю выживаемость, чем при неанатомической резекции, чем разрешают сомнения колеблющихся в выборе хирургов в пользу анатомической резекции.
По результатам резекций, проведенных лидерами хирургической гепатологии (Bismuth H. et al., 1993; Belghiti J. et al., 1994; Llovet J.M. et al., 2002; Lau H. et al., 1997; Wu С.С. et al., 1996; Makuuchi M., et al., 1993; Вишневский В.А. и соавт., 2008; Полуэктов В.Л. И соавт., 2008), рубеж 5-летней выживаемости преодолели от 30 до 53% пациентов. Однако если учесть, что всего 15-20% пациентов подлежат резекциям, такие результаты вовсе не кажутся радужно оптимистичными.
Внутрипеченочный рецидив: у 50-80% в течение 2 лет. Ранний рецидив возможен при сосудистой инвазии, высоком уровне альфа-фетопротеина, тип резекции также имеет значение (анатомическая или атипичная). Поздний, спустя годы после резекции (de novo?), зависит от активности гепатита и мультицентричности опухоли. Но возможны и правомочны повторные операции у селективной группы больных, отвечающих следующим критериям отбора: первично – солитарная опухоль, рецидив – солитарная опухоль, безрецидивный период не менее года, нет инвазии в воротную вену. 38% 5-летней выживаемости – это вполне достойный результат. Тщательный отбор пациентов является залогом хороших отдаленных результатов.
Радикальными методами лечения являются резекция и трансплантация печени.
Трансплантация печени стала сегодня очень перспективной и успешной технологией при ГЦК, когда тщательно проводится селекция кандидатов на ее проведение. Ее достоинства – удаление опухоли, устранение фонового заболевания и ликвидация портальной гипертензии. Недостатки также очевидны – проблема донорских органов, длительный период ожидания, иммуносупрессия, а значит, возможность рецидивного состояния.
Локальная деструкция ГЦК – современное, можно сказать, модное направление. Это несложная технология, осложнений дает относительно мало (10%, летальность – 0,3%). Показанием к ней являются небольшие (диаметром не более 3-5 см) нерезектабельные опухоли. Методы локальной деструкции – это внутриопухолевое введение этанола (PEI); наиболее часто и эффективно используемая радиочастотная абляция (РЧА), микроволновая коагуляция.
Следующая опция нехирургического лечения – трансартериальная химиоэмболизация. Предпосылкой к ней служит преимущественно артериальное кровоснабжение опухоли, принцип действия заключается в выключении артериального кровотока в опухоли (ишемия) и воздействии химиопрепарата (цитотоксический эффект). Результаты мета-анализа – вершины доказательной медицины – свидетельствуют в ее пользу (ответ 35%) в сравнении с контрольным наблюдением.
Перспективным направлением в лечении ГЦК также можно назвать метод трансартериальной лучевой терапии, использующий микросферы с иттрием.
В перспективе предстоит широкое внедрение вакцинации для профилактики вирусных гепатитов, разработка и внедрение специфической противоопухолевой вакцины, создание новых таргетных препаратов и использование комбинированного подхода к лечению (хирургия, лекарственная терапия, иммунотерапия), изучение роли клеточных технологий для увеличения функциональных резервов печени. Наша философия базируется на том, чтобы всевозможно улучшать лечение и побеждать в борьбе с гепатоцеллюлярным раком.
Современные подходы к терапии рака печени: прошлое, настоящее, будущее
Заболеваемость ГЦК колеблется в областях земного шара. В Юго-Восточной Азии, где высока распространенность вирусных гепатитов, заболеваемость ГЦК самая высокая, в России частота ГЦК у мужчин составляет около 4 случаев на 100000 населения.
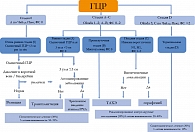
В Барселонской классификации (рисунок 3) отражены возможные способы терапии ГЦК, системная терапия сорафенибом (НексаварÒ) рассматривается на поздней стадии ГЦК, но при сохранности функциональных резервов печени, когда исчерпаны радикальные методы. Контингент больных, которых можно подвергнуть терапии сорафенибом значительно шире, чем тех, кому показаны радикальные методы лечения.
Для пациентов с метастатическим поражением лимфатических узлов и отдаленными метастазами системная химиотерапия является единственно возможным методом лечения. Однако при терапии одним средством частота объективного ответа достигает лишь 10-20%. Наиболее часто для химиотерапии используется доксорубицин. Часто в рамках исследований изучались эпирубицин и митоксантрон. Выживаемость на фоне монотерапии в среднем не превышает 4 месяцев. Кроме того, нужно помнить, что на фоне химиотерапии нередко наблюдается реактивация вируса гепатита В – распространенной причины цирроза печени у таких больных.
При сравнении монотерапевтических схем очевидно, что, зачастую не достигнув повышения медианы безрецидивной и общей выживаемости, достоверно повышалась частота тяжелых токсических эффектов.
Полихимиотерапия также не позволяет достигнуть стойкой стабилизации заболевания и повысить выживаемость, хотя некоторые комбинации химиотерапии привели к повышению частоты ответа по сравнению с монотерапией. Частота ответа при комбинированных режимах колеблется от 13 до 47%.
В исследовании III фазы (Yeo W. et al. JNCI), опубликованном в 2005 году, сравнивался режим монотерапии доксорубицином и комбинация PIAF, включающая цисплатин, 5-ФУ, доксорубицин, IFN-a2b (PIAF). При использовании комбинации частота ответа возросла до 20,9%, хотя достоверной разницы достигнуто не было, медиана общей выживаемости изменилась недостоверно, зато частота токсических реакций 3 и 4 степени достоверно выросла, увеличилось также число смертельных исходов, связанных с терапией.
Таким образом, мы «бросаем пациента из огня да в полымя» – пытаясь его спасти химиотерапевтическими препаратами, мы рискуем его потерять в связи с токсическими эффектами на химиотерапию.
С началом эры таргетных препаратов и до ее начала активно изучался молекулярный патогенез ГЦК. Как и предполагалось, механизмов много: цирроз печени с повреждением тканей и мутации онкогенов и генов-супрессоров. Кроме того, отмечены изменения клеточных сигнальных путей: ангиогенный, EGF-EGFR, Wnt/b-катенин, PI3K/AKT/mTOR, Raf/MEK/ERK. Эти пути являются целями молекулярной терапии.
На пути пролиферации и выживания клетки, управляемые через сигнальный путь Raf/MEK/ERK, направлены многие из созданных на сегодня таргетных препаратов. Подавляющее большинство действует на уровне рецепторов к различным стимулирующим молекулам. Сорафениб воздействует и на начало каскада, и на промежуточном этапе передачи сигнала.
Также было отмечено, что при ГЦК секретируется избыток проангиогенных факторов, в том числе сосудистый эндотелиальный фактор роста (VEGF), тромбоцитарный фактор роста (PDGF), плацентарный фактор роста, трансформирующие факторы роста a и b, базисный фактор роста фибробластов (FGF), эпидермальный фактор роста (EGF), фактор роста гепатоцитов, ангиопоэтины, ИЛ-4 и ИЛ-8. Логично было бы направить свои усилия и по этому пути.
Бевацизумаб непосредственно блокирует рецепторы к сосудистому эндотелиальному фактору роста, в то время как остальные молекулы, включая сорафениб, сунитиниб, талидомид, нарушают ниже расположенные пути каскада.
Бевацизумаб изучался в исследовании (Malka D. et al, ASCO, 2007) с участием 26 пациентов в дозе 5 мг/кг через каждые две недели. У половины больных удалось достигнуть стабилизации процесса (эффективность: 1 полный ответ, 12 стабилизация, 7 прогрессия). Однако в 3 случаях отмечались геморрагические осложнения, потребовавшие отмены лечения (кровотечения – 2, геморрагический асцит – 1).
Сочетание бевацизумаба с оксалиплатином и капецитабином позволило значительно улучшить результаты в отношении ответа на терапию (W. Sun et al. J Clin Oncol, 2007): более чем у 90% больных наблюдался частичный ответ или стабилизация, медиана времени до прогрессии составила лишь 4,5 месяца. Однако у 2/3 пациентов отмечались токсические реакции 3 и 4 степени.
Целью для таргетного препарата эрлотиниб является рецептор эпидермального фактора роста. Медиана выживаемости при его использовании в исследовании с участием 38 пациентов достигла 13 месяцев, хотя время до прогрессирования лишь 3,2 месяца, что позволило сделать авторам вывод о возможности стабилизации процесса (Philip P.A. et al. J Clin Oncol, 2005).
Исследование по сочетанию эрлотиниба и бевацизумаба с блокировкой обоих типов рецепторов дало очень обнадеживающие результаты (Thomas M.B. et al. J Clin Oncol 2007). Ответ наблюдался в 50% случаев, медиана выживаемости достигла 9 месяцев, а медиана общей выживаемости 19 месяцев. Токсические реакции 3 и 4 степени тяжести были связаны с общей слабостью, повышением артериального давления и развитием желудочно-кишечных кровотечений.
Сорафениб (Нексавар®), являясь ингибитором тирозинкиназ, подавляет и пролиферацию опухолевых клеток, и ангиогенез. Выживаемость на сорафенибе при гепатите В + 7,3 мес., гепатите С + 12,4 мес. (p = 0,29). По применению сорафениба при ГЦР проведены исследования и II, и III фазы. Международное, мультицентровое, рандомизированное, двойное-слепое, плацебо-контролируемое исследование III фазы SHARP включало 602 пациента. Критериями включения были гепатоцеллюлярная карцинома, гистологически подтвержденная, неоперабельная; минимум один измеримый очаг; ECOG 0-2; класс А по Чайлд-Пью; ранее системная терапия не проводилась. В данном исследовании было показано достоверное улучшение выживаемости в группе применения сорафениба. Причем сорафениб оказался эффективным и в подгруппе пациентов с инвазией и внепеченочным распространением опухоли. Увеличение выживаемости при приеме сорафениба доказано и в исследовании ASIA-PACIFIC STUDY III фаза.
Эффект сорафениба, по данным компьютерной томографии, отличался от классического уменьшения размеров опухоли на фоне химиотерапии. Был виден некроз опухоли. Через 4 месяца наблюдения на фоне лечения процент некроза опухоли оставался на уровне 50%.
Как правило, ГЦК развивается на фоне цирроза печени. Учитывая, что в исследовании SHARP участвовали только пациенты с циррозом печени по Чайлду-Пью класс А, интересны результаты назначения сорафениба у больных с более тяжелой стадией цирроза. По сравнению с классом А в группе цирроза В класса отмечалось более существенное повышение билирубина, нарастание энцефалопатии и усиление асцита. Фармакокинетика сорафениба была сходной у пациентов с обеими стадиями цирроза (Abou-Alfa G.K. et al., 2008).
Поиск оптимального режима химиотерапии продолжается, но на сегодня единственной опцией продления жизни у нерезектабельных больных ГЦК является сорафениб (Нексавар), продемонстрировавший достоверное увеличение выживаемости. Возможно, его эффективность будет повышена еще за счет комбинации таргетных и классических препаратов.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.