Ксалкори: новые возможности таргетной терапии ALK-позитивного немелкоклеточного рака легкого. XIX Российский онкологический конгресс. Сателлитный симпозиум компании Pfizer
- Аннотация
- Статья
- Ссылки



Значение мультидисциплинарного подхода в выборе тактики терапии пациентов с ALK-позитивным немелкоклеточным раком легкого
Выбору правильной тактики лечения препятствуют ошибки, допущенные при диагностике местно-распространенного и метастатического немелкоклеточного рака легкого (НМРЛ). По мнению заведующего отделением клинических биотехнологий Российского онкологического научного центра им. Н.Н. Блохина, д.м.н. Константина Константиновича ЛАКТИОНОВА, морфологическая верификация диагноза служит стратегической составляющей при определении наиболее оптимальной тактики ведения больных НМРЛ. Именно морфологический материал позволяет установить наличие у больного специфических молекулярно-генетических нарушений.
Роль морфологической верификации в диагностике рака легкого трудно переоценить. Вместе с тем в России только у 68% больных НМРЛ диагноз подтверждается морфологически. Лечение 32% пациентов основано на рентгенологических данных. Нередко за рак легкого принимают туберкулезный очаг, шаровидную пневмонию и назначают соответствующее лечение.
Бронхоскопия легких, трансбронхиальная и трансторакальная биопсия, признанная одним из основных методов получения опухолевого материала, позволяют установить морфологическую картину заболевания. В последние годы основной акцент делают на изучении цитологического материала – цитологические исследования плеврального экссудата, пунктата периферических лимфоузлов или отдаленных метастазов у больных НМРЛ. Цитологический материал вполне пригоден для полноценного генетического тестирования. Это подтверждают данные собственных исследований, проведенных К.К. Лактионовым. В частности, было проведено цитологическое исследование плевральной жидкости для последующей молекулярно-генетической диагностики опухоли. Специалисты проанализировали результаты исследований метастатических плевритов у 28 пациентов с НМРЛ. Во всех случаях материала было достаточно для всего спектра исследований. Речь идет об иммуноцитохимическом методе (ИЦХ), определении мутаций гена EGFR и анализе транслокации ALK. Согласно результатам молекулярно-генетической диагностики, у двух из 28 пациентов выявлена мутация EGFR, у одного – ALK-транслокация. «Это означает, что цитологический материал диагностически ценный, его можно использовать при индивидуализированном подходе к лечебной тактике», – констатировал докладчик.
Еще одним распространенным способом получения цитологического материала при НМРЛ является трансторакальная пункция. Она выполняется при периферических новообразованиях легкого, когда другие методы получения материала недоступны.
К.К. Лактионов ознакомил участников симпозиума с результатами тонкоигольной биопсии, проведенной под контролем компьютерной томографии (КТ)/ультразвукового исследования у 78 пациентов с выявленным периферическим новообразованием легкого с неясным морфологическим заключением.
Указанным больным была выполнена трансторакальная пункция. Верификацию диагноза удалось получить у 73 (93,6%) пациентов. У двух из 73 больных выявлен туберкулез, у одного – меланома, у четырех – мелкоклеточный рак легкого. Безусловно, подходы к лечению данных нозологий отличаются от подходов к лечению НМРЛ.
Вторичной задачей исследования стала оценка возможности использования опухолевого материала, полученного при трансторакальной пункции, для молекулярно-генетического анализа. У 32 (50%) из 64 пациентов материала было достаточно для проведения всего спектра исследований (ИЦХ, метод полимеразной цепной реакции (ПЦР) и флуоресцентная гибридизация in situ (FISH)). Согласно полученным данным, у четырех больных выявлена EGFR-мутация, у одного – транслокация ALK. Таким образом, полученного при трансторакальной пункции опухолевого материала было достаточно для генетического тестирования.
Существуют два основных морфологических типа НМРЛ – плоскоклеточный и неплоскоклеточный. В соответствии с европейскими рекомендациями, в частности NCCN (National Comprehensive Cancer Network – Национальная всеобщая онкологическая сеть) по стандарту молекулярной диагностики, неплоскоклеточный рак легкого следует тестировать на мутации EGFR и транслокации ALK. При плоскоклеточном раке легкого молекулярно-генетическое исследование проводится исключительно у некурящих и никогда не куривших пациентов при наличии небольшого биопсийного образца и смешанной гистологии1.
Уже выделены клинические характеристики, ассоциированные с транслокацией ALK. В ряде работ отмечается, что онкогенная перестройка EML4-ALK чаще регистрируется в аденокарциномах, у некурящих и молодых пациентов2–4. Доказано, что именно EML4-ALK является основным вариантом транслокации ALK при НМРЛ и главным онкогеном для рака легкого5.
В настоящее время в качестве таргетной терапии ALK-позитивного рака легкого назначают кризотиниб. По сравнению с химиотерапией препарат демонстрирует более высокие результаты в лечении данного заболевания. На основании рекомендаций Российского общества клинической онкологии (RUSSCO) кризотиниб используется в качестве первой линии терапии у больных НМРЛ с инверсией ALK. Если кризотиниб не назначают в первой линии терапии, его применяют во второй линии.
Кризотиниб (Ксалкори) – конкурентный ингибитор АТФ тирозинкиназ рецепторов ALK, MET и ROS1. В результате селективной ингибирующей активности кризотиниба (Ксалкори) прекращается патологическое деление и наступает апоптоз опухолевых клеток.
Кризотиниб, разработанный в 2005 г., уже в конце 2011 г. был рекомендован FDA (Food and Drug Administration – Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США) для лечения распространенного ALK-позитивного НМРЛ. В 2012 г. препарат был зарегистрирован в России. По словам К.К. Лактионова, история успеха кризотиниба (Ксалкори) – это история успеха таргетной терапии в целом. От момента создания препарата до его регистрации прошло всего шесть лет. Именно за этот период удалось провести качественные клинические исследования и получить убедительные результаты, послужившие основанием для ранней регистрации препарата Ксалкори.
Методы диагностики транслокаций ALK – FISH, ПЦР и иммуногистохимический (ИГХ) – имеют свои преимущества и недостатки. До недавнего времени стандартным способом выявления ALK-позитивного НМРЛ считался FISH. Однако результаты проведенных исследований подтверждают ИГХ-метод как самостоятельный для выявления транслокаций ALK. При подтверждении у пациента статуса ALK-позитивного НМРЛ следует рассмотреть вопрос о целесообразности назначения препарата Ксалкори.
К сожалению, полностью вылечить больных НМРЛ нельзя, но можно в два-три раза увеличить продолжительность их жизни. Конечно, со временем у большинства пациентов развивается резистентность к ингибиторам тирозинкиназы ALK. В таком случае можно провести ребиопсию из очага прогрессирования. Правда, ребиопсия – сложный технологический процесс и частота удачных ребиопсий не превышает 60–70%. «Можно провести повторное молекулярно-генетическое тестирование для выявления вторичных или дополнительных онкогенных мутаций, активации альтернативных обходных сигнальных путей, влияющих на способность кризотиниба достигать активного центра ALK. Повторное молекулярно-генетическое тестирование позволит выбрать наиболее оптимальную лечебную тактику», – отметил докладчик в заключение.
Программа RUSSCO: молекулярно-генетическая диагностика ALK в России
Как отметил исполнительный директор Российского общества клинической онкологии Илья Валерьевич ТИМОФЕЕВ, в ходе исследований доказано, что выявление транслокации с участием гена ALK при НМРЛ позволяет назначать высокоэффективное лечение ингибитором ALK. По данным крупного рандомизированного регистрационного исследования фазы III, частота объективных ответов у пациентов с ALK-позитивным НМРЛ на фоне терапии кризотинибом составила 74% по сравнению с 45% у пациентов из группы химиотерапии6. «Еще недавно такие результаты казались фантастическими. Сегодня практически все пациенты реагируют на лечение препаратом Ксалкори», – уточнил докладчик.
Не случайно в рекомендациях NCCN и обновленных рекомендациях ESMO (European Society for Medical Oncology – Европейское общество медицинской онкологии) 2016 г. с уровнем доказательности 1А сказано, что тестирование на предмет транслокации ALK предпочтительно у пациентов с НМРЛ. ESMO рекомендует проводить тестирование ALK у больных как с неплоскоклеточным, так и с плоскоклеточным НМРЛ методом FISH, а у некоторых пациентов – методом ИГХ.
«Специфичность и чувствительность ИГХ-метода сходны с таковыми метода FISH. Последний достаточно сложный, его используют только несколько лабораторий в нашей стране. ИГХ-метод имеет более широкое распространение», – пояснил И.В. Тимофеев. Российское общество клинической онкологии также рекомендует проведение молекулярно-генетической диагностики на наличие мутаций гена EGFR и транслокации гена ALK.
По инициативе RUSSCO и при поддержке компании Pfizer в нашей стране уже на протяжении трех лет реализуется программа по молекулярно-генетической диагностике транслокаций ALK у больных НМРЛ. Программа стартовала 1 января 2012 г. К ноябрю 2015 г. материал, полученный у 5864 пациентов, был направлен в лаборатории. За период с 1 января 2012 г. по 10 ноября 2015 г. протестировано 4573 пациента из 94 городов страны. Более половины образцов (57,6%) направлено из Центрального и Сибирского федеральных округов.
Мутация гена ALK выявлена у 7,13% пациентов, причем у женщин чаще, чем у мужчин, – 13,15 и 4,17% соответственно. По словам докладчика, общий показатель больных НМРЛ с транслокацией ALK достиг 400. Это несколько выше, чем в европейской популяции. Именно эти пациенты являются кандидатами на лечение кризотинибом.
«Мы решили проанализировать эффективность терапии ALK-позитивного НМРЛ в нашей стране. С этой целью мы начинаем крупное наблюдательное исследование, главной задачей которого является сравнение эффективности таргетной терапии кризотинибом у ALK-позитивных больных НМРЛ с эффективностью иного лечения, назначаемого в отсутствие кризотиниба ALK-позитивным пациентам с НМРЛ», – пояснил И.В. Тимофеев.
Дизайн исследования – по типу «случай – контроль». В нем предусмотрены две идентичные по основным прогностическим признакам когорты: ALK-позитивные больные НМРЛ, применяющие кризотиниб на основании результатов тестирования в программе, и пациенты с ALK-позитивным НМРЛ, получающие другое лечение и составляющие контрольную группу. Результаты, полученные в рамках наблюдательного исследования, позволят оценить эффективность лечения больных с ALK-позитивным раком легкого в России.
В завершение докладчик сформулировал основные выводы:
-
молекулярно-генетическое тестирование является стандартом диагностики местно-распространенного и метастатического НМРЛ;
-
тестирование проводится с целью существенного повышения эффективности таргетной терапии;
-
RUSSCO при поддержке компании Pfizer предоставляет возможность бесплатного тестирования ALK в России.
Выбор оптимальной терапии для ALK-позитивных пациентовс НМРЛ. Представление клинических случаев
По словам руководителя радиологического центра Главного военного клинического госпиталя им. Н.Н. Бурденко, к.м.н. Алексея Владимировича СМОЛИНА, наличие ключевых повреждений генома опухолевой клетки предполагает высокую эффективность молекулярно-направленной терапии и определяет подходы к выбору химиотерапии. Основание – собственный клинический опыт и результаты клинических исследований. А.В. Смолин привел случай из практики.
Поступившему несколько лет назад в госпиталь 30-летнему пациенту с НМРЛ назначили стандартный режим химиотерапии препаратом платины. Однако после курса лечения началось бурное прогрессирование заболевания. Потребовалась вторая линия химиотерапии пеметрекседом, позволившая на целых шесть месяцев стабилизировать процесс.
Спустя полгода болезнь вновь начала прогрессировать. Проведенная молекулярно-генетическая диагностика опухоли показала наличие транслокации ALK. К сожалению, в то время эффективная терапия ALK-позитивного НМРЛ отсутствовала, кризотиниб еще не был зарегистрирован в нашей стране. Третья линия химиотерапии оказалась неэффективной. Больной умер через 15 месяцев от начала лечения.
По мнению докладчика, внимания заслуживает тот факт, что больной ALK-позитивным НМРЛ ответил на терапию пеметрекседом. Анализ литературы демонстрирует, что медиана выживаемости без прогрессирования (ВБП) и частота объективных ответов на фоне стандартного режима химиотерапии пеметрекседом у пациентов с транслокацией ALK достоверно выше, чем у больных НМРЛ с мутацией гена KRAS.
Появление препарата Ксалкори позволило значительно улучшить показатели выживаемости у больных ALK-позитивным НМРЛ. Именно Ксалкори стал первым эффективным препаратом в лечении распространенного ALK-позитивного рака легкого. В подтверждение сказанного докладчик рассмотрел еще один клинический случай.
Больной К., 47 лет. Четыре курса химиотерапии по схеме «карбоплатин + паклитаксел», полученные пациентом с 27 августа по 2 ноября 2012 г., позволили достичь стабилизации заболевания. С 29 ноября 2012 г. была начата поддерживающая терапия пеметрекседом. На фоне стабилизации процесса отмечалась тенденция к росту опухоли.
По словам А.В. Смолина, в то время специалистам уже были известны результаты клинических исследований фаз I и II (PROFILE 1001 и PROFILE 1005), продемонстрировавшие высокую медиану ВБП и частоту объективных ответов у пациентов с ALK-позитивным НМРЛ на фоне применения кризотиниба и послужившие основанием для регистрации препарата и его одобрения к использованию в клинической практике7, 8. «Мы надеялись, что пациент сможет дожить до того момента, когда у нас появится кризотиниб, и приняли не вполне стандартное решение – выполнили больному позитронно-эмиссионную томографию и провели лобэктомию», – пояснил он.
Контрольная КТ от 12 марта 2014 г. показала отрицательную динамику. Однако позднее отмечалось прогрессирование заболевания: к трем имевшимся очаговым уплотнениям, размеры которых увеличились с 3,3 до 8,5 мм, добавились около 15 новых уплотнений диаметром от 2 до 6 мм. При выполнении FISH-теста в образце ткани опухоли выявлена перестройка в гене ALK, предполагавшая высокую чувствительность опухоли к терапии кризотинибом.
С 10 июля 2014 г. пациент начал получать таргетную терапию препаратом Ксалкори (кризотиниб) 500 мг/сут. Наблюдался положительный клинический эффект – полный ответ на лечение, подтвержденный 30 сентября 2015 г. данными КТ.
«Два клинических случая и две совершенно разных продолжительности жизни. Второй случай демонстрирует возможности препарата Ксалкори. Благодаря его включению в алгоритм лечения больной живет уже более трех с половиной лет», – отметил А.В. Смолин.
Докладчик ознакомил участников симпозиума с результатами исследования PROFILE 1014 (NCT01154140) – первого проспективного рандомизированного исследования фазы III, в котором сравнивали эффективность таргетной терапии кризотинибом (Ксалкори) с таковой стандартной химиотерапии в условиях первой линии лечения при распространенном ALK-позитивном НМРЛ6.
Пациенты с распространенным, рецидивирующим и метастатическим ALK-позитивным несквамозным НМРЛ, ранее не получавшие системного лечения, были случайным образом распределены на две группы – группу открытого лечения кризотинибом (n = 172) 250 мг внутрь два раза в сутки и группу химиотерапии (n = 171), получавшую внутривенно пеметрексед 500 мг/м2 и цисплатин 75 мг/м2 или карбоплатин, целевая AUC 5–6 мг/мл/мин каждые три недели до шести циклов. После прогресирования заболевания рандомизированным в группу кризотиниба пациентам разрешалось продолжать его прием, пациентам группы химиотерапии – перейти на лечение кризотинибом.
Первичной конечной точкой была ВБП по данным независимой радиологической экспертизы, вторичными – частичный и общий ответ, общая выживаемость, профиль безопасности.
Результаты исследования PROFILE 1014 показали статистически достоверное преимущество кризотиниба перед стандартными режимами химиотерапии по основным оцениваемым аспектам. Так, частота объективного ответа в группе кризотиниба составила 75% (95-процентный доверительный интервал (ДИ) 67–81), в группе химиотерапии – 45% (95% ДИ 37–53).
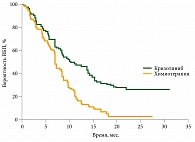
Важный момент: у больных ALK-позитивным НМРЛ в группе кризотиниба было достигнуто не только увеличение частоты объективного ответа почти в два раза, но и существенное улучшение ВБП по сравнению с группой химиотерапии (рис. 1).
Медиана ВБП в группе кризотиниба была на четыре месяца больше – 10,9 месяца. В группе стандартных режимов химиотерапии этот показатель составил 7 месяцев.
Поскольку на момент окончания сбора данных было зарегистрировано только 26% летальных исходов от всех причин, ни в одной группе не была достигнута общая выживаемость. Необходимо принимать во внимание и тот факт, что анализ не учитывал потенциальные искажающие эффекты перехода между группами. Между тем около 70% пациентов из группы химиотерапии получали кризотиниб после прогрессирования.
В отличие от группы химиотерапии в группе кризотиниба улучшение качества жизни и снижение симптоматики рака легкого были выражены более значительно. Нежелательные явления в группе кризотиниба наблюдались реже и имели легкую степень тяжести, а длительность лечения была больше, чем в группе химиотерапии (медиана 10,1 против 4,1 месяца). В целом профиль безопасности кризотиниба соответствовал описанному у пациентов с ALK-позитивным НМРЛ, ранее получавших лечение9.
Исследование PROFILE 1014 продемонстрировало преимущество кризотиниба перед химиотерапией в отношении увеличения ВБП и частоты объективного ответа у больных ALK-позитивным НМРЛ. Применение кризотиниба ассоциировалось с улучшением оцениваемых пациентами параметров физического функционирования, симптомов НМРЛ и качества жизни.
А.В. Смолин вновь обратился к собственному опыту применения кризотиниба и привел очередной пример.
Больной Ц., 35 лет. Стаж курения – 15 лет (20 сигарет в сутки). Зимой 2014 г. пациент впервые отметил болезненность в левой половине грудной клетки. Рентгенологически была выявлена инфильтрация верхней доли левого легкого, которую расценили как внебольничную пневмонию. От стационарного лечения пациент отказался, ему провели курс антибактериальной терапии с положительной динамикой.
В октябре 2014 г. возобновились боли в левой половине грудной клетки. При КТ с контрастированием выявлены большой левосторонний гидроторакс, патологическое образование верхней доли левого легкого до 2 см и множественные мелкие очаги до 0,6 см в верхней доле левого легкого, лимфаденопатия средостения, тромбоз S1 сегментарной вены и деструкция 8-го и 9-го ребер слева с наличием небольшого мягкотканного компонента.
В госпитале 18 ноября 2014 г. пациенту выполнили пункцию левой плевральной полости – эвакуировано 2300 мл жидкости. При цитологическом исследовании плевральной жидкости обнаружены клетки аденокарциномы. 24 ноября 2014 г. в ходе видеоторакоскопии слева диагностировано обширное метастатическое поражение плевры.
При гистологическом исследовании биоптата плевры выявлена морфологическая картина метастаза первичной аденокарциномы легкого. Магнитно-резонансная томография (МРТ) показала наличие солитарного метастаза 8 мм правой теменной доли головного мозга с зоной перифокального отека. Установлен диагноз: периферический рак (аденокарцинома) верхней доли левого легкого с метастазами в плевре слева, лимфатических узлах средостения, костях скелета, T2N2MIB, стадия IV.
Нараставший болевой синдром (8–9 баллов по шкале ВОЗ) потребовал назначения наркотических анальгетиков. Проведена лучевая терапия на зону болевого синдрома.
При FISH-анализе в образце ткани опухоли выявлена перестройка в гене ALK, предполагавшая высокую чувствительность опухоли к терапии препаратом Ксалкори. С 21 января 2015 г. пациент начал получать таргетную терапию этим препаратом. Спустя месяц от начала приема Ксалкори отмечался полный регресс болевого синдрома. Данные КТ от 17 марта 2015 г. показали частичный регресс экстракраниального опухолевого поражения, уменьшение метастазов в головном мозге.
Результаты контрольной КТ от 12 мая 2015 г. показали положительную динамику, которая сохранялась до июля 2015 г., когда с помощью КТ было констатировано увеличение очага в головном мозге. Причем вне головного мозга ситуация оставалась стабильной. Было принято решение об облучении головного мозга и продолжении терапии препаратом Ксалкори.
До 28 октября 2015 г. сохранялся частичный регресс метастазов в головном мозге. Данные КТ продемонстрировали тенденцию к прогрессированию процесса в легких. Таким образом, на фоне терапии препаратом Ксалкори время для интракраниального прогрессирования составило 5,5 месяца, для экстракраниального – 9 месяцев. Больной начал получать пеметрексед в качестве терапии второй линии.
Рандомизированное клиническое исследование PROFILE 1007 было посвящено сравнению эффективности кризотиниба с эффективностью химиотерапии во второй линии лечения ALK-позитивного НМРЛ. В исследовании участвовали 347 пациентов из стран Европы, Северной и Южной Америки, ряда стран Азиатско-Тихоокеанского региона. В соотношении 1:1 они были рандомизированы на группу кризотиниба (Ксалкори) (n = 172) и группу химиотерапии (n = 171) пеметрекседом (n = 99) или доцетакселом (n = 72). Группы были равнозначны по основным факторам прогноза.
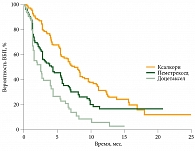
Согласно полученным данным, частота объективных ответов в группе кризотиниба составила 65% (95% ДИ 58–72), в группе химиотерапии – 20% (95% ДИ 14–26). Эффективность кризотиниба, отмечавшаяся в 66% случаев, была достоверно выше таковой пеметрекседа (29%) и доцетаксела (7%). Исследование показало преимущество кризотиниба (Ксалкори) перед однокомпонентной химиотерапией и по увеличению ВБП (рис. 2).
Медиана ВБП в группе препарата Ксалкори составила 7,7 месяца, в группе пеметрекседа – 4,2 месяца, в группе доцетаксела – 2,6 месяца. Анализ основных аспектов продемонстрировал, что наибольшей эффективностью во второй линии терапии больных ALK-позитивным НМРЛ обладает кризотиниб – препарат Ксалкори.
Результаты перечисленных исследований позволяют сделать вывод, что препарат Ксалкори является препаратом выбора в первой и второй линии терапии ALK-позитивного НМРЛ.
А.В. Смолин представил участникам симпозиума еще один клинический случай.
Больная К., 35 лет. С ноября 2013 г. ее беспокоили боли в межлопаточной области при движении и редкий сухой кашель. 21 ноября 2013 г. рентгенологически установлены полиморфные очаговые тени по всем легочным полям и усиление легочного рисунка. После обследования в туберкулезном госпитале туберкулез был исключен. 13 февраля 2013 г. выполнена трансторакальная игловая биопсия 3-го сегмента правого легкого. По результатам ИГХ-исследования от 26 марта 2014 г. сделано заключение, что морфологическое строение и иммунофенотип соответствуют папиллярной аденокарциноме легкого.
Основными жалобами пациентки при поступлении в клинику были нарастающая одышка при физической нагрузке, выраженная слабость, температура тела около 40 ºС. При проведении эхокардиографии выявлены уплотнение листков перикарда и феномен «поплавка». Была проведена пункция перикарда, эвакуировано 700 мл геморрагического выпота. Цитологическое исследование перикардиальной жидкости показало картину аденокарциномы. Диагностирован центральный рак верхней доли правого легкого T4N0M1 с массивным метастазированием в обоих легких, правосторонний гидроторакс, гидроперикард.
С 18 марта по 8 апреля 2014 г. больная получила два курса химиотерапии по схеме «карбоплатин + паклитаксел» на фоне стандартной премедикации и антиэметиков. Несмотря на проводимое лечение, состояние больной ухудшалось: нарастали симптомы опухолевой интоксикации, дыхательная недостаточность, имело место кровохаркание, рецидивировали плеврит и перикардит с угрозой тампонады. Это свидетельствовало о рефрактерности опухоли к платиносодержащей химиотерапии и прогрессировании процесса. Общий соматический статус ECOG снизился до 4.
При FISH-исследовании в образце ткани опухоли выявлена перестройка в гене ALK, предполагавшая высокую чувствительность опухоли к терапии препаратом Ксалкори (кризотиниб). По жизненным показаниям пациентке 22 апреля 2014 г. была начата терапия препаратом Ксалкори 500 мг (две капсулы) в сутки. На фоне лечения исчезла отдышка, прекратилось кровохаркание, нормализовалась температура тела. К 21 мая 2014 г. отмечался частичный регресс опухоли, а через три месяца от начала таргетной терапии – практически полный регресс опухоли. Длительность ответа составила 14 месяцев.
Несмотря на быстрый противоопухолевый эффект кризотиниба, со временем у больных ALK-позитивным раком легкого может развиться резистентность из-за недостаточного проникновения препарата в центральную нервную систему. Это может быть связано с вторичными мутациями ALK, которые, согласно данным исследований, развиваются у трети пациентов с ALK-резистентными опухолями. Причем опухоли, резистентные к кризотинибу, демонстрируют избирательную чувствительность и к другим ингибиторам тирозинкиназы ALK.
В большинстве случаев у больных ALK-позитивным НМРЛ злокачественный процесс распространяется в головной мозг.
В конце июня 2015 г. пациентке К. после жалоб на головные боли и снижение памяти была проведена МРТ, которая выявила множественное метастатическое поражение головного мозга. «В соответствии с современными рекомендациями, мы продолжили таргетную терапию кризотинибом и провели облучение головного мозга. В результате добились полного регресса метастазов в головном мозге», – уточнил А.В. Смолин.
Наука не стоит на месте, разрабатываются перспективные ALK-ингибиторы тирозинкиназы, которые находятся на разных стадиях клинических исследований. Безусловно, не все ингибиторы тирозинкиназы ALK одинаковы. У кризотиниба есть важное преимущество – он может применяться не только при транслокации гена ALK, но и при мутации генов ROS1 и MET.
Завершая выступление, А.В. Смолин констатировал, что существует несколько методов лечения больных с транслокацией ALK, среди которых все более значимое место занимает таргетная терапия препаратом Ксалкори. Сегодня этот препарат по праву считается стандартом лечения распространенного ALK-позитивного рака легкого в первой и последующих линиях терапии.
Заключение
Ксалкори (кризотиниб) – первый эффективный препарат, применяемый при распространенном ALK-позитивном немелкоклеточном раке легкого. Согласно данным клинических исследований, Ксалкори (кризотиниб) ассоциируется с достоверным увеличением медианы выживаемости без прогрессирования, частоты объективных ответов у больных ALK-позитивным НМРЛ, с улучшением оцениваемых пациентами параметров физического функционирования, симптомов НМРЛ и качества жизни по сравнению с химиотерапией.
Ксалкори (кризотиниб) признан стандартом как первой, так и второй линии терапии ALK-позитивного НМРЛ и включен по этим показаниям в рекомендации NCCN, ESMO, RUSSCO.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.