Опыт применения рамуцирумаба в комбинации с паклитакселом во второй линии терапии метастатического рака желудка
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. Пациенты получали рамуцирумаб 8 мг/кг внутривенно один раз в две недели в комбинации с паклитакселом 80 мг/м2 внутривенно в 1, 8 и 15-й дни 28-дневного цикла. Терапия в данном режиме продолжалась до прогрессирования заболевания или непереносимости препаратов.
Результаты. Как показали промежуточные результаты применения рамуцирумаба во второй линии терапии у больных метастатическим раком желудка, у одного пациента достигнут объективный ответ на терапию в виде частичного регрессирования, еще у десяти – стабилизация. Медиана выживаемости без прогрессирования и общей выживаемости не достигнута, поскольку большинство пациентов продолжают получать терапию, причем двое из них свыше восьми месяцев. Спектр нежелательных явлений незначителен. Зарегистрирована гематологическая и негематологическая токсичность 1–2-й степени. Серьезных нежелательных явлений не зафиксировано.
Заключение. Комбинация рамуцирумаба и паклитаксела характеризуется высокой эффективностью, приемлемым профилем токсичности и потенциально ассоциируется с высокой общей выживаемостью у пациентов с метастатическим раком желудка, прогрессирующим на фоне первой линии терапии.
Материал и методы. Пациенты получали рамуцирумаб 8 мг/кг внутривенно один раз в две недели в комбинации с паклитакселом 80 мг/м2 внутривенно в 1, 8 и 15-й дни 28-дневного цикла. Терапия в данном режиме продолжалась до прогрессирования заболевания или непереносимости препаратов.
Результаты. Как показали промежуточные результаты применения рамуцирумаба во второй линии терапии у больных метастатическим раком желудка, у одного пациента достигнут объективный ответ на терапию в виде частичного регрессирования, еще у десяти – стабилизация. Медиана выживаемости без прогрессирования и общей выживаемости не достигнута, поскольку большинство пациентов продолжают получать терапию, причем двое из них свыше восьми месяцев. Спектр нежелательных явлений незначителен. Зарегистрирована гематологическая и негематологическая токсичность 1–2-й степени. Серьезных нежелательных явлений не зафиксировано.
Заключение. Комбинация рамуцирумаба и паклитаксела характеризуется высокой эффективностью, приемлемым профилем токсичности и потенциально ассоциируется с высокой общей выживаемостью у пациентов с метастатическим раком желудка, прогрессирующим на фоне первой линии терапии.


Введение
Рак желудка в структуре заболеваемости занимает четвертое место среди злокачественных новообразований у мужчин (7,9%) и пятое место у женщин (5,2%), но в структуре смертности прочно удерживает вторую позицию (10,3%). У большинства пациентов (69,6%) на момент постановки диагноза имеет место поздняя стадия (III или IV) заболевания, когда методы лечения существенно ограничены. У 45% больных с локальной формой рака желудка, выявленной при первичной диагностике, в течение пяти лет диагностируются метастазы. У 85% пациентов регионарная форма прогрессирует и переходит в метастатическую [1, 2].
В отсутствие противоопухолевого лечения продолжительность жизни больных диссеминированным раком желудка колеблется от трех до пяти месяцев.
Целесообразность и эффективность лекарственной терапии при диссеминированном раке желудка, подтвержденные в рандомизированных исследованиях II–III фаз, сегодня не вызывают сомнения. По сравнению с оптимальной симптоматической терапией химиотерапия достоверно увеличивает продолжительность жизни больных.
Перечень противоопухолевых препаратов, эффективных при раке желудка, включает фторпиримидины как для перорального, так и для парентерального использования, производные платины, таксаны, антрациклины, ингибиторы топоизомеразы I, а также препараты таргетной терапии. Эффективность каждого препарата в монорежиме не превышает 30%. Увеличение эффективности лекарственной терапии связано с использованием комбинированных, достаточно токсичных режимов химиотерапии (DCXF, TOFL, FOLFORINOX и др.). Химиотерапия первой линии диссеминированного рака желудка носит паллиативный характер. Эффект отмечается у 35–40% больных с медианой общей выживаемости от восьми до десяти месяцев [3].
В настоящее время накоплены данные о молекулярно-генетических изменениях при раке желудка (экспрессия PDGF-альфа, HER2, TGF-бета, EGFR, c-met и др.), что позволяет рассчитывать на эффективность таргетной терапии.
HER2 – рецептор EGF гиперэкспрессирован у 13–22% больных раком желудка, чаще при кишечном типе рака. При НER2-позитивном раке желудка общий эффект от химиотерапии повышается на 12% при добавлении трастузумаба, а медиана выживаемости увеличивается до 13,8 месяца (в контрольной группе – 11,3 месяца). Иная ситуация при раке желудка с HER2-негативным статусом (78–87%). Например, в исследовании AVAGAST добавление бевацизумаба к химиотерапии способствовало увеличению частоты достижения объективного ответа и медианы выживаемости без прогрессирования болезни, но не влияло на медиану общей выживаемости.
В настоящее время режимы второй линии не зарегистрированы. Актуальной остается проблема разработки новых таргетных системных препаратов для повышения эффективности лечения на поздних стадиях заболевания [4].
Пациентам со статусом 0–2 по шкале ECOG (Eastern Cooperative Oncology Group – Восточная объединенная группа онкологов), не отягощенным тяжелыми сопутствующими заболеваниями, рекомендована химиотерапия второй линии. Сравнение таксанов и иринотекана во второй линии химиотерапии показало их сопоставимую эффективность.
Рамуцирумаб – первый биологический препарат, который применяли в режиме монотерапии. В исследовании REGARD рамуцирумаб увеличивал медиану выживаемости у пациентов с поздними стадиями аденокарциномы желудка и прогрессированием заболевания после первой линии химиотерапии [5]. Комбинация рамуцирумаба с паклитакселом, статистически значимо увеличивающая общую выживаемость по сравнению с режимом плацебо в комбинации с паклитакселом (исследование RAINBOW), может быть использована в качестве нового стандартного режима второй линии лечения при раке желудка поздних стадий [6].
Материал и методы исследования
Исследование было выполнено на базе Областного онкологического диспансера г. Иркутска. Набор пациентов проводился с 1 июня 2016 г. до 31 января 2017 г. в рамках Всероссийской программы безвозмездной передачи препарата рамуцирумаб для оказания помощи больным раком желудка поздних стадий с прогрессированием заболевания на фоне или после предшествующей химиотерапии на основе производных платины и/или фторпиримидинов по жизненным показаниям.
Главными критериями включения в исследование стали возраст старше 18 лет, гистологически подтвержденный метастатический рак желудка, прогрессирование заболевания после первой линии химиотерапии, состояние на момент исследования по ECOG 0–1, лабораторные показатели без клинически значимых отклонений от нормы. В исследование не включались пациенты с плоскоклеточным раком желудка, циррозом печени, желудочно-кишечной перфорацией, свищами, артериальной тромбоэмболией за последние шесть месяцев, любым значительным желудочно-кишечным кровотечением, значительной венозной тромбоэмболией за последние три месяца перед рандомизацией, плохо контролируемой артериальной гипертензией, метастатическим поражением центральной нервной системы.
Все участники исследования подписали информированное согласие.
Индивидуальные планы лечения были подготовлены на общем мультидисциплинарном консилиуме диспансера и одобрены Министерством здравоохранения Российской Федерации.
Больные получали лечение по схеме: рамуцирумаб 8 мг/кг в виде внутривенной инфузии в течение 60 минут один раз в две недели в комбинации с паклитакселом 80 мг/м2 внутривенно в 1, 8 и 15-й дни 28-дневного цикла. Лечение проводилось на фоне профилактической противорвотной и десенсибилизирующей терапии, инфузионной поддержки. Каждые две недели исследователи оценивали эффективность по результатам компьютерной томографии грудной клетки, брюшной полости и малого таза, а также по данным эзофагогастродуоденоскопии с биопсией и определению лечебного патоморфоза. Лечение продолжалось до прогрессирования заболевания или развития неприемлемой токсичности.
Объективный ответ оценивали на основании данных мультиспиральной компьютерной томографии с внутривенным контрастированием согласно критериям RECIST v.1.1 и данным эзофагогастроскопии с биопсией (фото в формате DICOM, определение лечебного патоморфоза в биопсийном материале). При анализе токсичности использовали критерии СТС AE v. 4. Определялись выживаемость без прогрессирования (время от регистрации до документального подтверждения прогрессирования) и общая выживаемость (время от регистрации до даты смерти от любой причины). Функцию выживаемости описывали методом Каплана – Майера.
Результаты
В исследование с 1 июня 2016 г. по 31 января 2017 г. было включено 12 пациентов. В ходе проспективного анализа промежуточных результатов применения рамуцирумаба и паклитаксела у больных неоперабельным распространенным раком желудка во второй линии терапии подтверждены эффективность и безопасность данной схемы лечения в наблюдаемой популяции. Одна пациентка прекратила терапию спустя десять недель от ее начала из-за ухудшения общего состояния. На контрольном обследовании по критериям RECIST констатировано прогрессирование заболевания. Больная умерла через две недели после обследования. У 11 пациентов на контрольном обследовании после двух месяцев терапии зарегистрирована стабилизация заболевания. Эти пациенты продолжили лечение.
Среди пациентов в возрасте от 32 до 68 лет (средний возраст – 50 лет) было восемь (67%) женщин и четверо (33%) мужчин. Во всех случаях при гистологическом исследовании выявлена аденокарцинома (G1 – 8%, G2 – 50%, G3 – 42%). Очаги, измеряемые по критериям RECIST v. 1.1, присутствовали у шести (50%) больных. У шести (50%) пациентов выявлены только неизмеряемые очаги. Время до прогрессирования заболевания на фоне первой линии терапии у девяти (75%) пациентов составило менее шести месяцев, у троих (25%) более полугода. Наличие мутации HER2/neu не выявлено. Общее состояние всех больных расценивалось как удовлетворительное – ECOG 0–1. У 11 (92%) пациентов число органов метастазирования не превышало двух. У большинства больных (92%), участвовавших в исследовании, диагностированы перитонеальные метастазы. Асцит обнаружен у пяти (42%) пациентов. В анамнезе перенесли гастрэктомию трое (25%). Девять (75%) пациентов не были оперированы (табл. 1).
Больные получили от шести до 16 введений рамуцирумаба и от девяти до 24 введений паклитаксела (12–32 недели лечения, в среднем 22 недели). Пять введений рамуцирумаба с последующим контрольным обследованием получили все участники исследования. Десять (83%) пациентов продолжают получать терапию в прежнем объеме без коррекции доз препаратов с соблюдением режима введения. По результатам компьютерной томографии и эзофагогастродуоденоскопии у одного пациента зафиксировано прогрессирование опухоли после пяти введений рамуцирумаба (десять недель терапии). 11 пациентов продолжили получать терапию в режиме: рамуцирумаб 8 мг/кг в виде внутривенной инфузии в течение 60 минут один раз в две недели в комбинации с паклитакселом 80 мг/м2 внутривенно в 1, 8 и 15-й дни 28-дневного цикла.
Объективный ответ на терапию, по данным мультиспиральной компьютерной томографии в соответствии с критериями RECIST v. 1.1 и эзофагогастродуоденоскопии, зарегистрирован у 11 пациентов. Частичное регрессирование достигнуто после 20 недель лечения рамуцирумабом и паклитакселом у одного (8%) больного. Еще у десяти (83%) наблюдалась стабилизация. У одного (8%) пациента при первом контрольном обследовании после десяти недель терапии отмечалось прогрессирование. Выживаемость без прогрессирования у одного (8%) пациента составила шесть месяцев, рост опухоли констатирован после 13 введений рамуцирумаба. Случаев полного регрессирования опухоли не установлено. Частичное регрессирование опухоли заключалась в выраженном улучшении эндоскопической картины первичной опухоли по результатам эзофагогастродуоденоскопии и патоморфозе опухоли 4-й степени в биопсийном материале (рисунок). Динамики по перитонеальным метастазам не наблюдалось.
Медиана выживаемости без прогрессирования и медиана общей выживаемости не были достигнуты, поскольку большинство пациентов продолжают участвовать в исследовании. На сегодняшний день можно констатировать, что у десяти (83%) пациентов, продолжающих получать терапию, контроль над опухолью сохраняется. У двоих (17%) продолжительность терапии превысила восемь месяцев.
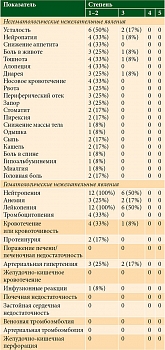
Одна пациентка умерла после 12 недель от начала терапии вследствие прогрессирования основного заболевания. Случаев гематологической и негематологической токсичности не зарегистрировано. Чаще имела место гематологическая токсичность. Нейтропения 1–2-й степени зафиксирована у 12 (100%) пациентов, что обусловлено применением паклитаксела. У трех (25%) больных наблюдалось развитие артериальной гипертензии, у четырех (33%) – носовые кровотечения, у двух (17%) – протеинурия. Полный спектр токсичности представлен в табл. 2.
Обсуждение
Согласно промежуточным результатам, показатели выживаемости без прогрессирования и общей выживаемости значительно превысили результаты, которые обычно имеют место при проведении стандартной терапии второй линии метастатического рака желудка. Несмотря на использование разных комбинаций, объективные ответы не превысили 20–25%, медиана продолжительности жизни – пять-шесть месяцев (от начала второй линии химиотерапии) [7]. Аналогичные результаты были получены при использовании паклитаксела в монорежиме или в комбинации с другими препаратами [8–13]. Еженедельное применение паклитаксела (60–80 мг/м2) характеризовалось меньшей токсичностью (нейтропения 3–4-й степени в 16–32% случаев) при одинаковом количестве объективных ответов (8–27%) по сравнению со стандартным трехнедельным режимом в серии японских исследований [9, 10]. На фоне применения паклитаксела в комбинации с цисплатином отмечалась высокая частота нейтропении 3–4-й степени (до 34%) и периферической нейропатии 2–3-й степени (до 38%) [12, 13].
По сравнению с другими нозологиями терапия рака желудка несколько отставала в плане внедрения в клиническую практику таргетных препаратов. Тем не менее сегодня рак желудка является одним из заболеваний, при которых испытывают новые варианты персонализированного лечения. В последнее время появляется все больше обнадеживающих результатов, связанных с лечением этой агрессивной и рефрактерной к стандартной химиотерапии опухоли [14]. Неудовлетворительные результаты исследования бевацизумаба не перечеркнули дальнейший интерес к изучению антиангиогенной терапии при раке желудка. Следующим препаратом этой серии стал рамуцирумаб, представляющий собой антагонист фактора роста эндотелия сосудов, который связывает рецептор VEGFR-2 и блокирует лиганды рецептора VEGF-A, VEGF-C и VEGF-D.
По сравнению с плацебо монотерапия рамуцирумабом статистически значимо улучшала показатели общей выживаемости в исследовании REGARD. Рамуцирумаб статистически значимо увеличивал общую выживаемость у пациентов с аденокарциномой желудка или желудочно-пищеводного соединения поздних стадий и прогрессированием заболевания после первой линии химиотерапии. Препарат снижал риск смерти от любой причины и риск прогрессирования заболевания вдвое. Преимущество рамуцирумаба по показателю выживаемости сохранялось практически во всех исследуемых группах. Влияние на общую выживаемость было несколько ниже у женщин, но расчетные значения выживаемости без прогрессирования заболевания у них были в пользу рамуцирумаба. После анализа влияния потенциальных расхождений в исходных характеристиках между лечебными группами преимущество рамуцирумаба по показателям общей выживаемости и выживаемости без прогрессирования заболевания после корректировки по другим прогностическим факторам оставалось неизменным. В данной популяции пациентов рамуцирумаб показал хорошую переносимость. При этом большинство нежелательных явлений отмечалось с одинаковой частотой в группах рамуцирумаба и плацебо. Гипертензия (нежелательное явление, ассоциируемое с большинством антиангиогенных препаратов) чаще отмечалась в группе рамуцирумаба, но гипертензия 3-й степени наблюдалась лишь у единичных пациентов, получавших рамуцирумаб. Данные о качестве жизни, согласно оценке пациентов, были скудными, однако эффект рамуцирумаба был не хуже эффекта плацебо. Кроме того, время до ухудшения оценки общего состояния оказалось статистически значимо более продолжительным у тех, кто получал рамуцирумаб [5]. Впоследствии положительными оказались результаты исследования фазы III по добавлению рамуцирумаба к паклитакселу во второй линии терапии рака желудка. Все это послужило основанием для регистрации в 2014 г. препарата для лечения больных метастатическим раком желудка [4, 15].
Рамуцирумаб в комбинации с еженедельным паклитакселом в отличие от других таргетных препаратов с антиангиогенным действием достоверно увеличивал число объективных ответов.
В клиническом исследовании III фазы RAINBOW эффективность и безопасность рамуцирумаба и паклитаксела сравнивали с таковыми паклитаксела и плацебо. Добавление к терапии паклитакселом рамуцирумаба позволило добиться увеличения показателя средней выживаемости пациентов до 9,6 месяца. У больных, получавших паклитаксел и плацебо, средняя выживаемость составила 7,4 месяца. Кроме того, на фоне терапии рамуцирумабом и паклитакселом риск прогрессирования заболевания или смерти снизился на 37% (по сравнению с использованием паклитаксела и плацебо), выживаемость без прогрессирования увеличилась на 52% [6].
В настоящее время планируется исследование фазы III RAINFALL по применению рамуцирумаба в первой линии терапии рака желудка.
При выборе и проведении второй линии терапии метастатического рака желудка следует учитывать, что заболевание на этой стадии неизлечимо. Именно поэтому основными задачами лечения являются увеличение продолжительности жизни больных, улучшение ее качества (облегчение симптомов заболевания, профилактика и лечение осложнений терапии), сбалансированность терапевтического эффекта (в том числе выживаемости) и качества жизни.
Полученные нами данные о переносимости комбинации рамуцирумаба и паклитаксела согласуются с данными исследования RAINBOW и свидетельствуют о хорошем профиле безопасности препаратов [6]. Планируется продолжить данное исследование. Это позволит получить более полные и подробные результаты применения рамуцирумаба и паклитаксела у больных неоперабельным распространенным раком желудка во второй линии терапии.
Заключение
На основании полученных данных можно сделать вывод, что рамуцирумаб является важной составляющей лечения при аденокарциноме желудка или желудочно-пищеводного соединения поздних стадий у пациентов с прогрессированием заболевания после химиотерапии первой линии. Показано, что по механизму действия и профилю токсичности рамуцирумаб существенно отличается от стандартных режимов химиотерапии при аденокарциноме пищевода и желудка.
Полученные результаты подтверждают роль сигнальной активности VEGFR-2 как важной терапевтической мишени при аденокарциноме желудка или желудочно-пищеводного соединения поздних стадий [5].
D.Yu. Yukalchuk, D.M. Ponomarenko, T.N. Yukalchuk, A.V. Shevchuk, Ye.A. Likhova
District Oncologic Dispensary (Irkutsk)
Contact person: Denis Yuryevich Yukalchuk, dyuyu558@mail.ru
Study objective: to examine efficacy and safety of ramucirumab and paclitaxel in patients with unresectable advanced gastric cancer in the second line therapy.
Material and methods. Patients were administered with 8 mg/kg ramucirumab via intravenous route, once a week, in combination with 80 mg/m2 paclitaxel via intravenous route on day 1, 8 and 15 of the 28-day protocol. Such therapy was continued until disease progression or drug intolerance.
Results. Intermediate results of using ramucirumab in the second line therapy in patients with metastatic gastric cancer demonstrated that objective therapy-related response such as partial regression in one patient and stabilization in ten patients was reached. Median progression-free survival and total survival were not achieved as the majority of patients still continue to receive therapy, among whom two patients – for more than eight months. Negligible range of adverse events was recorded. Hematological and non-hematological degree 1–2 toxicity was recorded. No serious adverse events were documented.
Conclusions. A combination of ramucirumab and paclitaxel is characterized with high efficacy, acceptable toxicity profile and potentially associated with high total survival of patients with metastatic gastric cancer exhibiting progression during the first line therapy.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.