Оценка качества жизни пациентов с распространенной/рецидивирующей меланомой кожи на фоне лечения ингибиторами контрольных точек иммунного ответа
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. В исследование включено 30 пациентов, получавших лечение ингибиторами контрольных точек по поводу распространенной/рецидивирующей меланомы в условиях Cанкт-Петербургского городского клинического онкологического диспансера с 2020 по 2023 г. Измерение показателей качества жизни по опроснику SF-36 и симптомов по шкале ESAS-R проводили до начала терапии, через один и три месяца.
Результаты. Возраст включенных пациентов варьировал от 30 до 87 лет (средний возраст – 64 ± 11 лет (95% ДИ 57,20–71,11)). Меланома кожи встречалась у 90% пациентов, меланома слизистой оболочки – у 10%. Функциональный статус у 40% пациентов по шкале ECOG был 2–3 балла. Пролголимаб получали 40% пациентов (n = 12), 26,7% (n = 8) – комбинацию «ниволумаб 1 мг/кг + ипилимумаб 3 мг/кг», 23,3% (n = 7) – ниволумаб в монорежиме, 6,7% (n = 2) – ипилимумаб, 3,3% (n = 1) – комбинацию «ниволумаб 3 мг/кг + ипилимумаб 1 мг/кг». Зарегистрировано значимое снижение интенсивности боли (до начала лечения – 2,29 ± 1,979, через три месяца – 1,29 ± 1,922 (р = 0,021)), улучшение общего профиля симптомов (до начала лечения – 15,79 ± 11,127, через месяц – 12,00 ± 8,899, через три месяца – 12,82 ± 12,157 (р = 0,006)) по опроснику ESAS-R. По большинству шкал анкеты SF-36 отмечено улучшение показателя в сравнении с исходным уровнем, статистически значимое изменение получено для физического функционирования (р = 0,05), боли (р = 0,01), социального функционирования (р = 0,013), психического здоровья (р = 0,01), общего показателя физического компонента здоровья (р = 0,001), общего показателя психического компонента здоровья (р = 0,042).
Выводы. Полученные результаты демонстрируют положительное влияние назначения ингибиторов контрольных точек иммунного ответа на качество жизни и профиль симптомов пациентов с диагнозом «распространенная/рецидивирующая меланома».
Материал и методы. В исследование включено 30 пациентов, получавших лечение ингибиторами контрольных точек по поводу распространенной/рецидивирующей меланомы в условиях Cанкт-Петербургского городского клинического онкологического диспансера с 2020 по 2023 г. Измерение показателей качества жизни по опроснику SF-36 и симптомов по шкале ESAS-R проводили до начала терапии, через один и три месяца.
Результаты. Возраст включенных пациентов варьировал от 30 до 87 лет (средний возраст – 64 ± 11 лет (95% ДИ 57,20–71,11)). Меланома кожи встречалась у 90% пациентов, меланома слизистой оболочки – у 10%. Функциональный статус у 40% пациентов по шкале ECOG был 2–3 балла. Пролголимаб получали 40% пациентов (n = 12), 26,7% (n = 8) – комбинацию «ниволумаб 1 мг/кг + ипилимумаб 3 мг/кг», 23,3% (n = 7) – ниволумаб в монорежиме, 6,7% (n = 2) – ипилимумаб, 3,3% (n = 1) – комбинацию «ниволумаб 3 мг/кг + ипилимумаб 1 мг/кг». Зарегистрировано значимое снижение интенсивности боли (до начала лечения – 2,29 ± 1,979, через три месяца – 1,29 ± 1,922 (р = 0,021)), улучшение общего профиля симптомов (до начала лечения – 15,79 ± 11,127, через месяц – 12,00 ± 8,899, через три месяца – 12,82 ± 12,157 (р = 0,006)) по опроснику ESAS-R. По большинству шкал анкеты SF-36 отмечено улучшение показателя в сравнении с исходным уровнем, статистически значимое изменение получено для физического функционирования (р = 0,05), боли (р = 0,01), социального функционирования (р = 0,013), психического здоровья (р = 0,01), общего показателя физического компонента здоровья (р = 0,001), общего показателя психического компонента здоровья (р = 0,042).
Выводы. Полученные результаты демонстрируют положительное влияние назначения ингибиторов контрольных точек иммунного ответа на качество жизни и профиль симптомов пациентов с диагнозом «распространенная/рецидивирующая меланома».

Введение
Увеличение продолжительности жизни принято считать главной целью лечения пациентов со злокачественными новообразованиями. Однако важно помнить, что современная стандартная терапия предполагает, кроме улучшения показателя общей выживаемости, также сохранение или улучшение качества жизни [1].
Качество жизни – это многомерная концепция, представляющая собой субъективное восприятие человеком уровня своего физического, психологического, эмоционального и социального функционирования [2]. Это единственный измеримый показатель, отражающий опыт самого пациента, который часто значительно отличается от представлений врача.
Основными функциями мониторинга качества жизни в онкологии являются:
- дополнение данных об эффективности и переносимости противоопухолевого препарата, необходимых для принятия решения о назначении терапевтической опции;
- раннее выявление симптомов заболевания и нежелательных явлений в процессе лечения;
- оценка прогноза течения онкологического заболевания [3].
Модуляторы иммунного синапса (анти-CTLA, анти-PD-1/PD-L1) – основные агенты лечения распространенной/рецидивирующей меланомы, демонстрирующие драматическое увеличение общей выживаемости и выживаемости без прогрессирования [4, 5]. Учитывая значительное бремя симптомов больных с метастатической меланомой, потенциально высокий риск развития нежелательных явлений при применении ингибиторов контрольных точек, нам представляется необходимым изучение качества жизни таких пациентов [6, 7].
Основной источник информации о качестве жизни – клинические испытания. В исследовании CheckMate 067 пациенты, получавшие иммунотерапию ниволумабом и ипилимумабом, несмотря на большую частоту осложнений 3–4-й степени (59% в группе комбинированной иммунотерапии, 22% в группе моноиммунотерапии), сообщали о стабильном уровне качества жизни, сопоставимым с таковым у пациентов, получавших ниволумаб [5, 8]. Введение пембролизумаба лучше переносится по показателю качества жизни в сравнении с химиотерапией (KEYNOTE-002) [9] и ипилимумабом (KEYNOTE-006) [10, 11]. Назначение ниволумаба также значимо улучшало качество жизни в сравнении с использованием дакарбазина (CheckMate 066) [9]. На сегодняшний день не опубликованы данные по качеству жизни на фоне терапии пролголимабом.
Исследования в условиях реальной клинической практики имеют большое значение [12], во все вышеперечисленные клинические испытания включали только пациентов с функциональным статусом ECOG 0–1, во всех проведенных исследованиях качество жизни являлось лишь эксплоративной конечной точкой.
Цель исследования – оценить качество жизни пациентов с распространенной/рецидивирующей меланомой на фоне лечения ингибиторами контрольных точек иммунного ответа.
Материал и методы
В анализ включено 30 пациентов с диагнозом метастатической или рецидивирующей меланомы, получавших лечение ингибиторами контрольных точек в условиях Санкт-Петербургского городского клинического онкологического диспансера с 2020 по 2023 г.
Для оценки уровня качества жизни использовались следующие инструменты: общий опросник SF-36 (The Short Form 36), специальный опросник ESAS-R (The Edmonton Symptom Assessment System Revised). Измерения проводились до начала лечения, через один и три месяца терапии.
Анкета SF-36 составлена из 36 вопросов, которые сгруппированы в восемь шкал:
- физическое функционирование;
- ролевое функционирование, обусловленное физическим состоянием;
- боль;
- общее здоровье;
- психическое здоровье;
- ролевое функционирование, обусловленное эмоциональным состоянием;
- социальное функционирование;
- жизненная активность.
Первые четыре шкалы объединяются в показатель физического компонента здоровья, последующие – в показатель психологического компонента здоровья. Результат рассчитывается по формуле, максимальное значение 100 баллов указывает на полное благополучие [13]. Клинически значимым является изменение баллов по шкалам опросника SF-36 на 5 и более пунктов [14].
Эдмонтонская шкала оценки симптомов (ESAS-R) содержит девять цифровых оценочных шкал для наиболее часто встречающихся симптомов у онкологических пациентов (боль, усталость, сонливость, тошнота, снижение аппетита, одышка, депрессия, тревога, ухудшение самочувствия) и одного симптома по выбору пациента. Выраженность каждого симптома оценивается в баллах от 0 до 10, где 0 – отсутствие симптома, 10 – сильно выраженный симптом. Результатом является сумма баллов всех симптомов. Чем он выше, тем ниже качество жизни [15].
Выживаемость без прогрессирования (ВБП) определялась как время от начала лечения до регистрации прогрессирования. Общая выживаемость (ОВ) рассчитывалась как время от начала лечения до летального исхода или последнего визита пациента, если событие не произошло. Оценка иммуноопосредованных нежелательных явлений (иНЯ) проводилась в соответствии с CTCAE v. 5.0 (Общие терминологические критерии нежелательных явлений). Ответ на лечение вычислялся по критериям iRECIST.
Статистический анализ. Применялась описательная статистика (для выборок с нормальным распределением – средние значения, стандартное отклонение, 95% доверительный интервал (ДИ); для выборок, распределение которых отличалось от нормального, – медиана и 25-й и 75-й квартили). ВБП и ОВ рассчитывались с помощью метода Каплана – Мейера. Характер распределения данных проанализирован тестом Шапиро – Уилка. Для оценки статистической значимости изменений качества жизни использовался критерий Фридмана. Взаимосвязь между количественными переменными с ненормальным распределением, количественными и качественными переменными оценивали с помощью коэффициента корреляции Спирмена.
Результаты
Характеристика пациентов
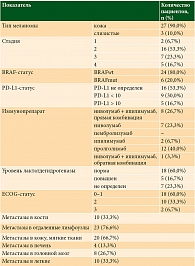
Возраст пациентов варьировал от 30 до 87 лет (средний возраст – 64 ± 11 лет (95% ДИ 57,20–71,11)). Половина (50%) исследуемой группы – женщины. Большую часть составляли пациенты с меланомой кожи, однако три пациента (10%) имели диагноз «меланома слизистых оболочек». BRAF-мутации встречались в 20% случаев (у шести пациентов). У 40% пациентов общесоматический статус по шкале ECOG составлял 2–3 балла. Диапазон предшествующих линий лечения – от 0 до 3. Пролголимаб получали 40% (n = 12) пациентов, 26,7% (n = 8) – комбинацию «ниволумаб 1 мг/кг + ипилимумаб 3 мг/кг», 23,3% (n = 7) – ниволумаб в монорежиме, 6,7% (n = 2) – ипилимумаб, 3,3% (n = 1) – комбинацию «ниволумаб
3 мг/кг + ипилимумаб 1 мг/кг». Медиана наблюдения за пациентами составила девять месяцев [4–14]. Полная клиническая характеристика пациентов представлена в табл. 1.
Безопасность лечения
У 50% больных на фоне лечения развились иммуноопосредованные нежелательные явления, частота осложнений 3–4-й степени составила 36,7%. Наиболее часто встречающимися нежелательными явлениями иммунотерапии были следующие: кожная токсичность (30%), гепатит (26,7%), тиреоидит (16,7%). Кроме того, были зафиксированы такие редкие иНЯ, как нейтропения 4-й степени (у одной пациентки), гиперкреатининемия 3-й степени (у одного пациента), миозит (у двух пациентов). Редкие осложнения разрешились после назначения глюкокортикостероидов, однако иммунотерапия была отменена. Полная информация о частоте нежелательных явлений представлена в табл. 2.
Результаты лечения
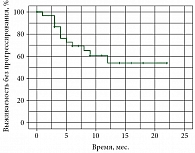
Медиана ВБП не достигнута, средняя ВБП составила 14,540 месяца (95% ДИ 11,317–17,763), через 22 месяца наблюдения прогрессирование произошло у 12 (40%) пациентов (рис. 1).
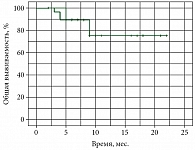
Медиана ОВ не достигнута, средняя ОВ составила 18,203 месяца (95% ДИ 15,538–20,868), через 22 месяца наблюдения 6 (20%) пациентов погибли (рис. 2).
Показатели качества жизни
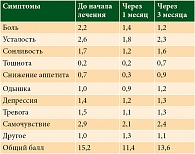
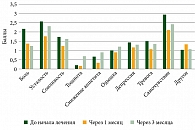
По результатам самооценки пациентов по опроснику ESAS-R, в процессе лечения отмечено значимое снижение интенсивности боли (до начала лечения – 2,29 ± 1,979, через один месяц – 1,46 ± 1,598, через три месяца – 1,29 ± 1,922 (р = 0,021)), улучшение общего профиля симптомов (до начала лечения – 15,79 ± 11,127, через один месяц – 12,00 ± 8,899, через три месяца – 12,82 ± 12,157 (р = 0,006)). Выраженность таких явлений, как тошнота, плохое самочувствие, сонливость, снижение аппетита, одышка, депрессия, тревога, оставалась без существенных изменений. Профиль симптомов по опроснику ESAS-R в динамике представлен в табл. 3.
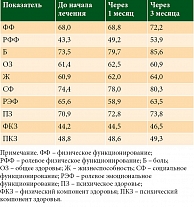
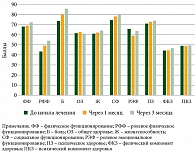
При анализе ответов пациентов на анкету SF-36 по большинству шкал выявлено улучшение показателя в сравнении с исходным уровнем. Значимое улучшение отмечено для физического функционирования (р = 0,05), боли (р = 0,01), социального функционирования (р = 0,013), психического здоровья (р = 0,01), общего показателя физического компонента здоровья (р = 0,001), общего показателя психического компонента здоровья (р = 0,042). Клинически значимые улучшения, влияющие на самочувствие пациента, зарегистрированы для шкал физического функционирования (изменение среднего балла на 6 пунктов), боли (изменение среднего балла на 14 пунктов), социального функционирования (изменение среднего балла на 8 пунктов). Качество жизни по опроснику SF-36 в динамике детализировано в табл. 4. Результаты по обоим опросникам представлены на рис. 3 и 4.
Не было выявлено статистически значимой связи между осложнениями и изменениями показателей качества жизни.
Оценена связь между объективным ответом на лечение и изменением компонентов качества жизни. Отмечена положительная умеренная взаимосвязь между ответом на лечение и улучшением по опроснику ESAS-R (коэффициент корреляции 0,434, р = 0,017), а также между ответом на лечение и улучшением физического компонента здоровья по опроснику SF-36 (коэффициент корреляции 0,371, р = 0,043).
Обсуждение и выводы
Полученные результаты демонстрируют положительное влияние назначения ингибиторов контрольных точек иммунного ответа на качество жизни и профиль симптомов пациентов с диагнозом «распространенная/рецидивирующая меланома». В процессе лечения зарегистрированы статистически значимое улучшение физического и социального функционирования, общих показателей физического и психического компонентов здоровья, снижение боли и общего бремени симптомов. Это влияние может быть обусловлено не только клинической эффективностью модуляторов иммунного синапса и хорошей переносимостью лечения, но и непосредственным положительным воздействием такого лечения на различные области функционирования пациента.
Основные ограничения данного наблюдательного исследования в условиях реальной клинической практики – это небольшой объем и разнородность изучаемой группы, а также отсутствие валидированного для иммунотерапии инструмента для оценки качества жизни.
Корреляционный анализ не выявил связи между развитием осложнений терапии и изменением качества жизни. Среди прочего объяснением может быть недостаточная чувствительность существующих опросников для исследуемой выборки или отсутствие влияния некоторых тяжелых иНЯ (гепатит, нейтропения) на самочувствие пациента.
Необходимо продолжить подобные исследования для лучшего понимания воздействия иммунотерапии на жизнь пациента в широком смысле.
A.S. Sarmatova, R.V. Orlova, PhD, N.V. Zhukova, PhD, S.I. Kutukova, PhD, N.P. Belyak, PhD
St. Petersburg State University
St. Petersburg City Clinical Oncology Center
I.P. Pavlov St. Petersburg State Medical University
Contact person: Alexandra S. Sarmatova, sashademchenkova@gmail.com
Objective. To evaluate the quality of life in patients with advanced/recurrent melanoma receiving immunotherapy with checkpoint inhibitors.
Material and methods. The study enrolled 30 patients with advanced/recurrent melanoma treated with checkpoint inhibitors in the City Clinical Oncology Center, Saint Petersburg from 2020 to 2023. Quality of life was measured by SF-36 questionnaire and ESAS-R scale thrice: before treatment, after one and three months.
Results. The age of the included patients ranged from 30 to 87 years (mean age is 64 ± 11 years, 95% CI 57.20–71.11). Cutaneous melanoma was present in 90% of the patients, while melanoma of mucosal origin was found in 10% of the patients. The functional status of 40% of the patients on the ECOG scale was 2–3 points. 40% (n = 12) of patients received Prolgolimab, 26.7% (n = 8) received the combination of Nivolumab 1 mg/kg + Ipilimumab 3 mg/kg, 23.3% (n = 7) received Nivolumab in mono regimen, 6.7% (n = 2) received Ipilimumab, and 3.3% (n = 1) received the combination Nivolumab 3 mg/kg + Ipilimumab 1 mg/kg. There was a significant decrease in pain (before treatment 2.29 ± 1.979, after 3 months 1.29 ± 1.922 (p = 0.021)), an improvement in the overall symptom profile (before treatment 15.79 ± 11.127, after 1 month – 12.00 ± 8.899, after 3 months – 12.82 ± 12.157 (p = 0.006)) on ESAS-R questionnaire was registered. Improvement was noted in most scales of the SF-36 questionnaire compared with baseline, with statistically significant changes obtained for physical functioning (p = 0.05), pain (p = 0.01), social functioning (p = 0.013), mental health (p = 0.01), overall index of physical health component (p = 0.001), overall index of mental health component (p = 0.042).
Conclusion. The results demonstrate a positive effect of treatment with checkpoint inhibitors on the quality of life and symptom profile of patients diagnosed with advanced/recurrent melanoma.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.