Патологии гепатобилиарной системы у больных псориазом
- Аннотация
- Статья
- Ссылки
- English



По разным оценкам, в мире псориазом страдают около 125 млн человек. При этом распространенность данного заболевания характеризуется широкой географической вариабельностью – от 0,91% в США до 8,5% в Норвегии [1]. Это обусловлено разной степенью влияния факторов окружающей среды в климатических зонах, а также разнообразием генотипа человеческой популяции.
В последние годы особое внимание врачей и исследователей приковано к проблеме высокой коморбидности псориаза с рядом заболеваний внутренних органов, в том числе печени. Например, наблюдается ассоциация псориаза с аутоиммунными заболеваниями печени, такими как нейтрофильный холангит, первичный билиарный цирроз. Кроме того, некоторые системные методы лечения псориаза, в частности метотрексатом и циклоспорином, связаны с потенциальной гепатотоксичностью, вызванной прямым повреждением печени, иммуносупрессией либо сочетанием этих двух факторов.
В научной литературе описаны случаи идиопатических нарушений биохимических показателей функции печени у больных псориазом. Так, при ретроспективном исследовании 518 таких больных в 4% случаев выявлено умеренное повышение активности печеночных ферментов. В 8% случаев зафиксированы очень высокие показатели печеночной функции [2].
Лекарственное поражение печени у пациентов с псориазом
Лекарственное поражение печени – одна из ведущих причин экстренной трансплантации органа. Проявления подобного поражения варьируются от бессимптомного повышения активности печеночных ферментов до развития острой печеночной недостаточности. Повышение активности печеночных ферментов у больных псориазом, как правило, обусловлено потреблением гепатотоксических веществ (57% случаев). Не менее важная причина – развитие неалкогольного жирового гепатоза (22% случаев) [2].
Часто повышение активности печеночных ферментов в крови больных псориазом вызвано приемом метотрексата и ацитретина. В большинстве случаев данный показатель увеличивается незначительно и не отражает истинную тяжесть патологического процесса.
В ретроспективном исследовании, проведенном с 2000 по 2009 г. в Малайзии, 66 (9,3%) из 710 больных псориазом получали метотрексат. У 57,6% из них изменялась активность трансаминаз, при этом шестерым потребовалась отмена препарата [3].
В другом ретроспективном когортном исследовании, проведенном в Израиле, у 119 пациентов с псориатическим артритом и 690 больных псориазом, получавших метотрексат, анализировали функции печени. В обеих группах пациентов наблюдалось повышение активности печеночных ферментов. Факторами, предрасполагающими к повреждению печени, были женский пол и более высокая кумулятивная доза метотрексата. Возраст больных, сопутствующие заболевания и тип псориаза не влияли на риск развития поражения печени [4].
Интересно, что гепатотоксичность метотрексата у пациентов с псориазом не связана с уровнем потребления ими алкоголя, но, по-видимому, обусловлена наличием метаболического синдрома и неалкогольного жирового гепатоза.
С учетом того что метотрексат признан препаратом выбора среди лекарственных средств для системной терапии псориаза, в настоящее время ведется поиск способов снижения гепатотоксичности на фоне применения этого лекарственного средства. Рассматривается сочетанное применение данного препарата с фолатами (без ущерба для терапевтической эффективности в отношении основного заболевания), преднизолоном, а также ингибиторами фактора некроза опухоли (ФНО) альфа.
Алкогольная болезнь печени
Чрезмерное употребление алкоголя повышает риск развития псориаза, особенно у мужчин. По данным исследования A.M. Tobin и соавт., у 15% обследованных пациентов с подтвержденным диагнозом алкогольной болезни печени выявлен псориаз [5]. В крупном американском исследовании с участием свыше 80 000 пациентов показано, что риск развития псориаза у женщин почти в два раза выше при употреблении алкогольных напитков два-три раза в неделю. Авторы отметили повышенный риск развития псориаза при употреблении нефильтрованного пива и предположили, что причиной могут быть глютеновые соединения [6]. Пациенты с псориазом имеют повышенные уровни антиглиадиновых антител и в отличие от лиц без псориаза могут характеризоваться так называемой чувствительностью латентного глютена.
H.Y. Ma и соавт. установили, что интерлейкин (ИЛ) 17 – критический медиатор фиброза печени различной этиологии, играющий роль и в псориатическом процессе. Во время индуцированного фиброза печени при алкогольной болезни печени активируется продукция ИЛ-6, поддерживающего пролиферацию кератиноцитов при псориазе [7].
Неалкогольная жировая дистрофия печени
Понятие неалкогольной жировой дистрофии печени включает широкий спектр ее патологических состояний – от простого стеатоза до стеатогепатита, что сопровождается высоким риском развития цирроза и гепатоцеллюлярной карциномы. Распространенность неалкогольной жировой дистрофии печени в общей популяции составляет 10–25%, но среди больных псориазом этот показатель возрастает до 17–65% [8]. При этом у пациентов со стеатозом или стеатогепатитом и сопутствующим псориазом регистрируются более высокие значения PASI (Psoriasis Area and Severity Index – индекс тяжести и площади поражения псориазом), а также уровня С-реактивного белка в крови, чем у пациентов с изолированным поражением кожи [8]. Кроме того, псориаз расценивается как важный предиктор прогрессирования фиброза печени.
С патогенетической точки зрения неалкогольная жировая дистрофия печени представляет собой локальное проявление метаболического синдрома. Общие для псориаза и неалкогольного стеатоза/стеатогепатита провоспалительные цитокины, такие как ИЛ-1-бета, ФНО-альфа, ИЛ-6, способны формировать и поддерживать основные звенья патогенеза указанных заболеваний: инсулинорезистентность, накопление липидов, воспаление.
Следует отметить, что ФНО-альфа и ИЛ-6 не только регулируют пролиферацию и дифференцировку кератиноцитов, но и увеличивают инсулинорезистентность, а также стимулируют дальнейшую выработку провоспалительных цитокинов. Микроциркуляторное ремоделирование в коже больных псориазом регулируется в основном ИЛ-17 и ФНО-альфа, повышение уровня которых может быть следствием стеатоза и фиброза печени. Изменение концентрации адипонектина, наблюдаемое при обоих патологических состояниях, поддерживает хронический воспалительный процесс. Таким образом, сочетание псориаза и неалкогольной жировой дистрофии печени способствует поддержанию и взаимному утяжелению этих заболеваний.
Первичный билиарный цирроз у больных псориазом
Первичный билиарный цирроз – медленно прогрессирующее аутоиммунное заболевание печени, встречающееся преимущественно у женщин в возрасте от 40 до 50 лет. Заболевание проявляется воспалением портальных трактов и аутоиммунным разрушением внутрипеченочных желчных протоков. Как следствие – нарушение оттока желчи, задержка токсических веществ в печени, нарушение ее функций, развитие фиброза, цирроза и печеночной недостаточности. У 90–95% пациентов с первичном билиарным циррозом появляются антимитохондриальные антитела, однако патологический процесс затрагивает только печень.
В настоящее время диагноз первичного билиарного цирроза устанавливают исходя из трех критериев: наличие антимитохондриальных антител в сыворотке крови, повышение активности печеночных ферментов (прежде всего щелочной фосфатазы) в течение более шести месяцев и характерные гистологические изменения в ткани печени. Для предварительного диагноза необходимо наличие двух из трех перечисленных изменений, для окончательного – трех [9].
Коморбидность первичного билиарного цирроза и псориаза – явление не редкое. Примерно у 13% больных циррозом развивается псориаз. В то же время у больных псориазом риск развития первичного билиарного цирроза достаточно высок [10].
Таким образом, сегодня имеются убедительные доказательства коморбидности заболеваний печени и кожи. Яркий пример – псориаз. При псориазе патология печени может быть либо первичной, либо обусловленной системной терапией основного заболевания.
Гепатопротекторы
Из сказанного следует, что комбинированная терапия псориаза предполагает применение гепатопротекторов. Обычно это эссенциальные фосфолипиды, история использования которых в качестве гепатопротекторов насчитывает 40 лет. Основное активное вещество – смесь фосфолипидов, выделяемая из соевых бобов, от 30 до 70% которой составляет фосфатидилхолин. Другие ингредиенты представлены фосфатидилэтаноламином, лизофосфатидилхолином, фосфатидилинозитом, триглицеридами. Один из основных механизмов действия фосфатидилхолина, упоминаемый в научной литературе, – восстановление структуры мембран клеток печени, которые примерно на 75% (мембраны митохондрий – на 92%) состоят из фосфатидилхолина, формирующего бислой. Фосфатидилхолин поддерживает нормальную текучесть и репарацию мембран, действует как антиоксидант, защищает митохондриальные и микросомальные ферменты от повреждения, замедляет синтез коллагена и повышает активность коллагеназы [11].
Учитывая проблему полипрагмазии, необходимо найти препарат, терапевтическими мишенями которого являются звенья патогенеза как псориаза, так и заболеваний печени. В этой связи интерес представляют препараты, в состав которых входят эссенциальные фосфолипиды и глицирризиновая кислота.
В проведенном нами биоинформационном исследовании обнаружен сигнальный путь, идущий от глицирризиновой кислоты через белок HMGB1 (High Mobility Group Box 1), гипотетически способный ингибировать псориатический процесс, подавляя продукцию основных провоспалительных цитокинов и клеточные процессы, влияющие на развитие псориаза [12]. Глицирризиновая кислота значительно снижает активность аминотрансфераз печени. Имеются данные, что длительный прием глицирризиновой кислоты препятствует развитию цирроза печени [13].
В экспериментальных исследованиях продемонстрирована способность глицирризиновой кислоты подавлять продукцию провоспалительных цитокинов ИЛ-1, ИЛ-6 и ФНО-альфа. Кроме того, глицирризиновая кислота характеризуется псевдоглюкокортикостероидной активностью, обусловленной ингибированием 11-бета-оксистероиддегидрогеназы, а топические глюкокортикостероиды – наиболее часто применяемые при псориазе препараты [12]. Эффективность и благоприятный профиль безопасности глицирризиновой кислоты (препарата Фосфоглив (глицирризиновая кислота + фосфолипиды)) продемонстрированы в рандомизированных клинических исследованиях при различных патологиях печени, а также в качестве патогенетической терапии у пациентов с хроническим гепатитом C [14]. На основании полученных результатов данная фиксированная комбинация была включена в клинические рекомендации и стандарты оказания медицинской помощи. Кроме того, было проведено несколько небольших исследований, результаты которых подтвердили положительное влияние Фосфоглива не только на состояние гепатобилиарной системы, но и на течение псориаза [15, 16].
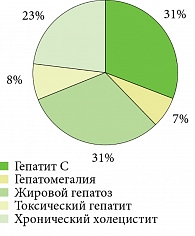
Под нашим наблюдением находилось 39 пациентов (семь женщин и 32 мужчины) с диагнозом распространенного псориаза, из них девять – с экссудативной формой, восемь – с псориатическим артритом. Средний возраст пациентов составил 43,55 ± 11,91 года, длительность заболевания – 14,47 ± 6,5 года. У 27% пациентов в анамнезе отсутствовали сопутствующие заболевания. В остальных случаях имели место различные сочетания патологий гепатобилиарной системы, сердечно-сосудистых заболеваний, метаболических нарушений (сахарный диабет, дислипидемия), венерические заболевания и т.д. Среди нарушений со стороны гепатобилиарной системы преобладали гепатит C (четыре пациента), жировой гепатоз и хронический холецистит (три пациента) (рис. 1).
Всем пациентам была назначена комплексная терапия, включавшая курс гепатопротекторов: Фосфоглив лиофилизат 5 г внутривенно струйно (ежедневно, однократно) десять дней, затем по две капсулы три раза в сутки до восьми недель. 21 больной получал также раствор метотрексата 20 мг № 2 один раз в день, восемь пациентов – ПУВА-терапию с аммифурином (пять таблеток за два часа до процедуры), десять пациентов – курс УФБ-терапии и медикаментозную терапию (раствор гемодеза 400,0 внутривенно капельно № 4, раствор глюконата кальция 10% – 10,0 внутримышечно № 10). Впоследствии десять пациентов выбыли из исследования из-за отказа наблюдаться после выписки из стационара. Те, кто остался под наблюдением, продолжили терапию метотрексатом 15 мг один раз в неделю (n = 21) и ПУВА-терапию до 25 сеансов (n = 8).
Результаты биохимического анализа крови 29 пациентов, проведенного до начала терапии, показали у 27,6% больных повышение уровней аланинаминотрансферазы (АлТ) и аспартатаминотрансферазы (АсТ), более чем у половины обследованных – увеличение уровней гамма-глутамилтранспептидазы (ГГТП) и щелочной фосфатазы (ЩФ) (55,1 и 51,7% соответственно). Уровни креатинина и общего билирубина в крови также превышали нормальные значения у 34,5% пациентов. В 72,4% случаев имел место повышенный уровень холестерина.
Повторный анализ крови на 11-й день лечения показал снижение целевых биохимических показателей крови, к 56-му дню терапии у всех пациентов (100%) с повышенным содержанием АлТ, АсТ, ГГТП, ЩФ, общего билирубина, холестерина и креатинина наблюдались нормальные значения или значения, в среднем превышающие норму не более чем на 10%. Несмотря на проводимую терапию, уровень креатинина не возрос. У всех пациентов (100%), у которых биохимические показатели крови изначально находились в пределах нормы, невзирая на гепатотоксичность проводимой терапии, отрицательная динамика отсутствовала. Более того, отмечалось снижение данных показателей (не более чем в 1,4 раза). Необходимо отметить, что у пациентов снизился уровень холестерина в крови, что могло быть связано с нормализацией функций печени.
Динамика биохимических показателей крови у пациентов с повышенными и нормальными значениями представлена в табл. 1 и 2 соответственно.
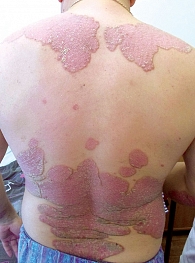
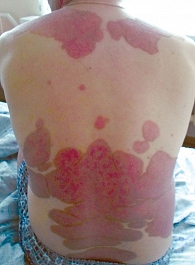
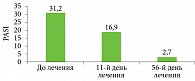
На фоне применения комплексной терапии с Фосфогливом (инъекции) отмечался интенсивный регресс высыпаний: уменьшение шелушения, инфильтрации (рис. 2 и 3). К 20-му дню высыпания полностью разрешились, оставив пигментные пятна. Наблюдение в течение восьми недель лечения показало отсутствие свежих высыпаний. Положительная динамика PASI также подтвердила эффективность комплексной терапии (рис. 4). Достоверность отличий между выборками (до и после лечения) составила p < 0,05.
Методом полимеразной цепной реакции в режиме реального времени нами был проведен сравнительный анализ уровней экспрессии генов MMP-1, MMP-9, S100A7, ИЛ-17 и ИЛ-6 в пораженной и визуально не пораженной псориазом коже, а также после лечения Фосфогливом. Анализ профилей экспрессии РНК проводился по 40 образцам кожи, взятым у десяти пациентов. На первом этапе анализировались биоптаты из участков кожи, пораженной псориатическим процессом, и непораженной кожи у одних и тех же пациентов. На втором этапе изучались образцы кожи пациентов, получавших курс гепатопротекторной терапии. После лечебного воздействия наблюдалось достоверное изменение экспрессии всех анализируемых генов. Достоверность отличий между выборками (до и после лечения) составила p < 0,01. Показано, что примененная схема лечения существенно изменяет уровень экспрессии изучаемых генов в пораженной коже (рис. 5).
Необходимо отметить, что только два пациента обратились повторно со свежими проявлениями псориаза через три месяца после окончания терапии, что можно объяснить сопутствующей патологией (гепатит C и дислипидемия). У остальных пациентов не зафиксировано обострения псориаза в течение шести месяцев по завершении лечения. Кроме того, за период наблюдения у всех пациентов не зарегистрировано нежелательных явлений на фоне приема Фосфоглива, в том числе повышения артериального давления и отеков.
Таким образом, Фосфоглив, включенный в комплексную терапию псориаза, продемонстрировал высокую эффективность в отношении кожных проявлений патологии (увеличение межрецидивного периода, улучшение динамики биохимических маркеров патологии печени), а также благоприятный профиль безопасности. Следует отметить удобство применения двух форм данного препарата. Парентеральное введение на этапе стационарного лечения позволяет добиться быстрого регресса высыпаний и нормализации биохимических показателей крови. Капсулированный Фосфоглив удобен для закрепления положительной динамики на амбулаторном этапе после выписки из стационара.
Ye.V. Denisova, Ye.V. Dvoryankova, K.T. Pliyeva, V.V. Sobolev, I.M. Korsunskaya
Moscow Scientific-Practical Center of Dermatovenerology and Cosmetology
Center for Physical and Chemical Pharmacology Theoretical Problems
Contact person: Irina Markovna Korsunskaya, marykor@bk.ru
In the article it is presented the modern view on the problem of combined pathologies of the hepatobiliary system and psoriasis, as well as the analysis of the possibility of hepatoprotectors use in complex therapy. Provided the results of our own studies of essential phospholipids and glycyrrhizic acid effectiveness in patients with psoriasis. It is shown that Phosphogliv shows the effectiveness in relieving the skin process and the normalization of biochemical indices of blood.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.