Роль смотровых кабинетов в улучшении показателей выживаемости больных со злокачественными новообразованиями шейки матки: данные по Челябинской области за 2005–2015 гг.
- Аннотация
- Статья
- Ссылки
- English

Введение
Злокачественные новообразования являются причиной почти каждой шестой смерти в мире. Ежегодно раком заболевает свыше 14 млн человек. По прогнозам экспертов, к 2030 г. эта цифра превысит 21 млн [1]. Всемирная организация здравоохранения сформулировала задачи по сокращению числа подобных преждевременных смертей на 25% к 2025 г. и на треть к 2030 г. [2].
Бесспорным лидером в структуре онкологической заболеваемости россиянок являются злокачественные новообразования органов репродуктивной системы. В России с 2005 по 2015 г. прирост абсолютного числа женщин со злокачественными опухолями репродуктивной системы составил 33% (29 881 пациентка). Наиболее социально значимыми как за рубежом, так и в России считаются злокачественные новообразования шейки матки: по данным проекта GLOBOCAN, в 2012 г. в мире зарегистрировано 527 600 новых случаев заболевания [3, 4].
Ежегодно в России регистрируется свыше 16 тыс. новых случаев злокачественных опухолей шейки матки. Прирост абсолютного числа заболевших за десять лет составил 28%. В возрастной группе 15–39 лет доля рака шейки матки была максимальной (22,3%), в возрастной группе 40–54 года – 10% (второе ранговое место после рака молочной железы). По прогнозам специалистов, к 2020 г. рост заболеваемости и распространенности злокачественных новообразований шейки матки составит 40%, в экономически развитых странах – 11% [5].
Совершенствование методов лечения больных раком шейки матки за последние 20 лет обошлось системе здравоохранения в 30–40 млрд долларов. Разрыв между эффективностью лечения и его стоимостью постоянно увеличивается.
Несмотря на то что профилактические осмотры играют существенную роль в диагностике опухолей шейки матки (в России активно выявляется 37,4% новых случаев), за последние десять лет доля больных, выявленных при проведении таких осмотров, увеличилась всего на 10%.
Злокачественные новообразования шейки матки в структуре онкологической заболеваемости, по данным популяционного ракового регистра (ПРР) Челябинской области за последние десять лет, стабильно занимают шестое ранговое место (в 2015 г. – 5,0%). Ежегодно в Челябинской области раком шейки матки в среднем заболевает свыше 370 женщин, умирает 175. С 2005 по 2015 г. прирост абсолютного числа заболевших злокачественными новообразованиями шейки матки достиг 28,1% и составил в 2015 г. 442 случая (в России 16 710 случаев, прирост показателя 29,3%). Пик заболеваемости пришелся на возрастную группу 40–44 года (56,6 на 100 тыс. населения). Для сравнения: в 2005 г. пик заболеваемости отмечался у пациенток менопаузального возраста – 50–54 года (36,5 на 100 тыс. населения). Иными словами, более чем за десятилетний период произошло заметное «омоложение» контингента заболевших на десять лет.
В 2005–2015 гг. в Челябинской области заболеваемость злокачественными новообразованиями шейки матки в возрастных группах 35–39, 40–44 и 55–59 лет увеличилась в 1,8 раза, а с 2012 г. единичные случаи заболеваемости регистрируются у девочек-подростков, что, несомненно, представляет потенциальную угрозу для трудоспособного и репродуктивного потенциала в будущем.
Смертность от злокачественных опухолей шейки матки в мире составляет около 270 тыс. случаев в год, из них более 85% приходится на страны с низким и средним уровнем доходов, к числу которых относится Россия [2].
В 2015 г. по уровню смертности от злокачественных опухолей шейки матки Челябинская область наряду с 85 субъектами РФ заняла 24-е место (стандартизованный показатель 6,46 на 100 тыс. населения).
Важным показателем качества ранней диагностики онкопатологии является доля злокачественных новообразований, обнаруженных на ранних стадиях, от общего числа выявленных случаев рака. Удельный вес больных с впервые установленным диагнозом злокачественных новообразований шейки матки, выявленных на I–II стадии опухолевого процесса, по Челябинской области не превышает 50% и равняется в среднем 46,1%. В то же время в России этот показатель в среднем достигает 60,4%.
В нашей стране до сих пор не разработана программа скрининга рака шейки матки, вакцинация против вируса папилломы человека не входит в национальный календарь прививок, возраст начала и окончания цитологического скрининга, его периодичность четко не оговорены и носят рекомендательный характер. Поэтому особая роль в предупреждении случаев злокачественных новообразований шейки матки отводится не врачам женских консультаций, а специалистам первичного звена здравоохранения – сотрудникам смотровых кабинетов.
Созданная в начале 1960-х гг. мощная сеть смотровых кабинетов не раз доказывала высокую результативность в активном выявлении злокачественных новообразований. В частности, удельный вес активно выявленных случаев злокачественных новообразований среди всех зарегистрированных больных в то время достигал 40% [6].
Основная задача работников смотровых кабинетов – проведение профилактического осмотра женщин старше 18 лет, обратившихся впервые в течение года в амбулаторно-поликлиническое учреждение в целях раннего выявления хронических, предопухолевых и опухолевых заболеваний.
Целью исследования стала оценка результативности работы смотровых кабинетов Челябинской области в улучшении показателей кумулятивной наблюдаемой и скорректированной выживаемости больных со злокачественными новообразованиями шейки матки за 2005–2015 гг.
Материал и методы
В настоящей работе представлены сведения ПРР Челябинской области за период 2005–2015 гг. о 784 случаях злокачественных новообразований шейки матки, из которых 389 случаев (основная группа) были выявлены активно в смотровых кабинетах Челябинской области, а оставшиеся 395 – при других обстоятельствах, таких как самообращение граждан, диспансеризация.
На основании базы данных ПРР Челябинской области впервые рассчитаны показатели кумулятивной наблюдаемой и скорректированной выживаемости пациенток со злокачественными новообразованиями шейки матки с учетом возраста, стадии заболевания, гистологической структуры опухоли и обстоятельств выявления.
Показатели выживаемости рассчитаны классическим методом анализа данных на популяционном уровне. Первичные материалы взяты из базы данных ПРР и отчетов о работе смотровых кабинетов учреждений здравоохранения муниципальных образований Челябинской области за 2005–2015 гг. Учреждения здравоохранения муниципальных образований Челябинской области предоставляют сводные отчеты (ежеквартальная, полугодовая, годовая форма) о работе смотровых кабинетов в Челябинский областной клинический центр онкологии и ядерной медицины на бумажном и электронном носителях по Форме отчета о работе смотровых кабинетов и показателям оценки работы смотровых кабинетов, утвержденной приказом Министерства здравоохранения Челябинской области от 27 августа 2010 г. № 1129 «Об организации работы смотровых кабинетов в учреждениях здравоохранения Челябинской области» (предыдущий приказ от 16 февраля 2005 г. № 61 «О мерах по совершенствованию работы смотровых кабинетов»).
В основную группу вошли 389 больных, у которых злокачественные новообразования были активно выявлены в смотровых кабинетах Челябинской области, в контрольную – 395 пациенток, у которых злокачественные новообразования диагностированы при иных обстоятельствах (в ходе диспансеризации взрослого населения, при самостоятельном обращении к врачу, в женской консультации).
Результаты и их обсуждение
Ежегодно смотровые кабинеты посещают около 450 тыс. женщин. При этом удельный вес лиц женского пола, посетивших смотровые кабинеты Челябинской области, от числа впервые обратившихся в поликлинику в 2010–2014 гг. в среднем составил 60,5%. Лишь в 2015 г. отмечался прирост данного показателя на 12% (то есть 72,5%). В 2010 г. цитологическое обследование в смотровых кабинетах прошли 85% женщин, в 2015 г. – 94,3%. Между тем охват цитологическим обследованием должен быть стопроцентным.
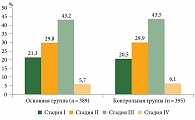
В основной и контрольной группах превалировали больные с локализованным опухолевым процессом (стадии I и II) – 199 (51,2%) и 199 (50,4%) пациенток соответственно (p > 0,05) (рис. 1).
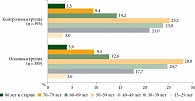
При статистическом анализе по возрастным периодам в исследуемых группах достоверных различий не выявлено (р > 0,05), что подтверждает однородность групп по данному прогностическому фактору. Рейтинговые места распределения больных с учетом возраста в группах были идентичны, максимальный удельный вес заболевших отмечался в возрастной группе 40–59 лет – 205 (52,7%) и 193 (48,9%) пациентки соответственно (то есть пре- и менопаузальный возраст) (рис. 2).
Важным прогностическим фактором, позволяющим оценить выживаемость онкологических больных, служит морфологический тип опухоли. При статистическом анализе по основным гистологическим типам опухолей достоверных различий в группах не установлено (р > 0,05). В большинстве своем опухоли имели строение плоскоклеточного рака (М8070–8073/3, 8076/3) – 335 (86,1%) больных основной и 337 (85,3%) пациенток контрольной группы. Опухоли шейки матки, имевшие строение аденокарциномы (М8140/3), встречались с одинаковой частотой – 37 (9,5%) случаев в основной и 40 (10,1%) в контрольной группе, железисто-плоскоклеточный рак (М8075/3,8560/3) – восемь (2,1%) и десять (2,5%) случаев соответственно. Сравнительно небольшую группу составляли такие гистологические варианты, как недифференцированный рак (М8020/3,8231/3) – по два (0,5%) случая в основной и контрольной группе. Иные гистологические варианты строения злокачественных новообразований шейки матки наблюдались у семи (1,8%) и шести (1,5%) пациенток соответственно (р > 0,05) (рис. 3).
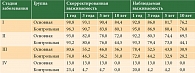
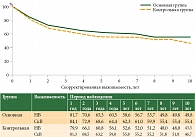
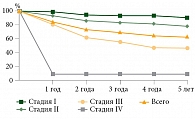
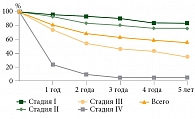
Важнейшим качественным критерием оценки эффективности противораковых мероприятий служит показатель выживаемости онкологических больных, отражающий адекватность стадирования всех выявленных случаев злокачественных новообразований [7]. Снижение показателей выживаемости с увеличением стадии злокачественного процесса вполне закономерно. В ходе исследования показатели пяти- и десятилетней кумулятивной скорректированной выживаемости больных со стадиями I и III основной группы превышали таковые пациенток контрольной группы – 90,4 и 84,4% против 83,8 и 80,1% соответственно для стадии I и 46,0 и 36,3% против 35,1 и 30,1% соответственно для стадии III (p < 0,05) (табл. 1, рис. 4–6).
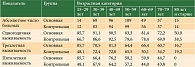
В таблице 2 приведены показатели выживаемости с учетом возраста пациенток. Четко прослеживается закономерность снижения показателей скорректированной выживаемости с увеличением возраста в обеих группах: у пациенток старше 60 лет группы контроля, больных старше 70 лет основной группы. Свыше 50% больных из общего числа, а также ни одна пациентка в возрасте 80 лет и старше из исследуемых групп не перешагнули пятилетний рубеж.
Обращают на себя внимание низкие показатели одногодичной, трех- и пятилетней выживаемости пациенток в возрасте 15–29 лет контрольной группы, у которых злокачественные новообразования диагностированы при самостоятельном обращении к врачам женской консультации, – 48,1 против 85,7% в основной группе, то есть более чем в 1,5 раза ниже по сравнению с основной группой (р < 0,05). Это свидетельствует о поздней обращаемости, местнораспространенном характере заболевания и агрессивном течении опухолевого процесса у молодых пациенток (табл. 2).
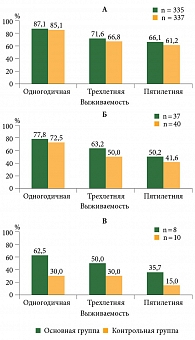
Анализ морфологически подтвержденных случаев злокачественных новообразований шейки матки показал, что гистологическая структура опухолей в основной и контрольной группах в большинстве случаев представлена плоскоклеточными новообразованиями (М8070/3–8073/3, 8076/3) – 335 (86,1%) и 337 (85,3%) больных соответственно. У этих пациенток показатели пятилетней выживаемости оказались достоверно выше (р < 0,05), чем у больных аденокарциномой и железисто-плоскоклеточным раком (основная группа – 66,1, 50,2 и 35,7% соответственно, контрольная – 61,2, 41,6 и 15% соответственно) (рис. 7).
Такая тенденция связана с тем, что аденокарцинома и железисто-плоскоклеточный рак в большей степени, чем опухоли плоскоклеточного строения, «ускользают» от профилактических мероприятий, поскольку поражение, как правило, затрагивает цервикальный канал и на преинвазивной стадии заболевание протекает бессимптомно. Это означает, что выявляемость на начальных стадиях относительно невелика – около 20% [8–11].
Кроме того, аденокарцинома шейки матки в отличие от плоскоклеточного рака характеризуется повышенным риском метастатического поражения яичников, что значительно ухудшает прогноз заболевания. Однако вопрос, является ли гистотип злокачественных новообразований шейки матки самостоятельным прогностическим фактором общей и безрецидивной выживаемости, остается открытым.
Заключение
Совершенствование системы ранней диагностики злокачественных новообразований направлено прежде всего на выявление опухолей визуальной локализации. Их диагностика не требует специального дорогостоящего оборудования и глубоких знаний медицинских работников первичного звена здравоохранения. Главная задача на этом этапе – заподозрить и вовремя направить пациентов к профильным специалистам для дообследования и верификации процесса.
Передовой опыт зарубежных коллег подтверждает эффективность и целесообразность скрининговых программ в отношении рака шейки матки. В связи с этим российское медицинское сообщество должно озаботиться поиском альтернативных, менее затратных, но не менее эффективных профилактических программ, которые способствовали бы снижению заболеваемости и смертности от злокачественных новообразований органов репродуктивной системы. Наглядный пример – деятельность смотровых кабинетов, результативность которой не вызывает сомнения: активная выявляемость злокачественных опухолей шейки матки как одной из лидирующих визуальных локализаций женских половых органов возросла на 5,6%, достигнув в 2015 г. 18,1% от числа впервые выявленных случаев злокачественных новообразований шейки матки. Стадийная структура выявленных случаев опухолей шейки матки (стадии I–II) в смотровых кабинетах Челябинской области превышает таковую в остальной популяции в целом – 50,6 против 42,3%.
Как показал анализ базы данных ПРР Челябинской области за десятилетний период, данные пяти- и десятилетней кумулятивной скорректированной выживаемости пациенток со злокачественными новообразованиями шейки матки, выявленными в смотровых кабинетах, достоверно выше, чем в остальной популяции (преимущественно в младших возрастных группах, с гистологическим вариантом строения злокачественных плоскоклеточных карцином шейки матки): 62,3 и 55,4% против 55,8 и 46,7% соответственно (p < 0,05).
Разработка программ, направленных на улучшение посещаемости смотровых кабинетов области, позволит повысить показатели выявляемости злокачественных новообразований на более ранних стадиях, минимизировать затраты на дальнейшее лечение и реабилитацию, а самое главное – улучшить показатели выживаемости для этой группы больных.
Авторы заявляют об отсутствии конфликта интересов.
A.G. Bochkova, A.S. Domozhirova, DM, Prof., I.A. Aksyonova, L.V. Kovalets
South Ural State Medical University
Chelyabinsk Regional Clinical Center of Oncology and Nuclear Medicine
Contact person: Anna Gennadyevna Bochkova, annabochkova7496@mail.ru
The article presents indicative data of women's examination rooms of the Chelyabinsk Region for 2005–2015, as well as indicators of observed and adjusted survival of patients with cervical cancer, calculated taking into account the stage of the disease, age of patients, histological forms and circumstances of tumor detection on the basis of the database of the population cancer register of the described area. The study of indicators of patient survival with malignant neoplasms allows to adjust the work of the cancer service, to orient the vector of preventive and therapeutic and diagnostic care, to use health care resources competently. During the study, the five- and ten-year survival rates of patients with cervical cancer, actively detected in the examination rooms, exceeded those ones in the rest of the population – 62.3 and 55.4% against 55.8 and 46.7%, respectively. Thus, the regional health care system of the Chelyabinsk Region has a specific task to increase the frequency of diagnosis of early forms of female genital organs malignant neoplasms. One of the ways to solve this problem is to optimize programs on improving the work of women's examination rooms.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.